NOP
http://www.oc-praktikum.de
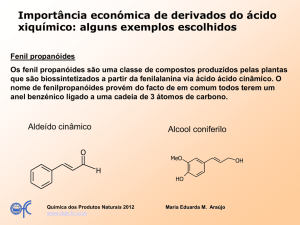
2017 Obtenção da amida do ácido cinâmico através da reação
do cloreto do ácido cinâmico com amônia
O
O
Cl
NH3
NH2
C9H7ClO
(166.6)
C9H9NO
(147.2)
(17.0)
Classificação
Tipos de reação e classes de substâncias
Reação do grupo carbonila em derivados do ácido carboxílico
Amida do ácido carboxílico
Cloreto do ácido carboxílico
Técnicas de Trabalho
Agitação magnética, adição gota a gota com funil volumétrico, agitação, extração, evaporação
com evaporador rotatório, recristalização, filtração, banho de gelo
Instruções (escala em batelada de 100 mmol)
Materiais
Frasco de 250 mL com 3 bocais, condensador de refluxo, funil de adição sem compensação
de pressão, agitador magnético, funil de separação de 500 mL, evaporador rotatório, banho de
gelo, bomba de vácuo
Substâncias de Partida
Cloreto do ácido trans-cinâmico (pf 32-35°C, pe 251-258°C
destilado; produto do experimento 2013)
Solução aquosa de amônia conc. (25%)
Éter metil terc-butílico (pe 55°C)
Acetato de etila (pe 77°C)
Sulfato de sódio para secagem
16,6 g (100 mmol)
80 mL (70 g, 1,0 mol)
80 mL
140 mL
cerca de 5 g
Reação
Adiciona-se a um frasco de 3 bocais de 250 mL com condensador de refluxo, agitação
magnética e funil de adição sem compensação de pressão, 80 mL de solução aquosa conc. de
amônia. O frasco de reação é resfriado em banho de gelo. Adiciona-se ao funil 16,6 g (100
mmol) de cloreto do ácido trans-cinâmico dissolvido em 80 mL de éter metil terc-butilico.
Esta solução é adicionada ao frasco sob agitação durante 30 minutos para evitar uma reação
1
March 2006
NOP
http://www.oc-praktikum.de
muito rápida. Após a adição a agitação é continuada por 30 minutos à temperatura ambiente.
Ocorre a precipitação de um sólido fino que não será segregado.
Etapa final
O conteúdo do frasco de reação é transferido para um funil de separação de 500 mL. O frasco
deve então ser lavado inicialmente com 50 mL de água e então com 50 mL de acetato de etila.
Estas soluções de lavagem são então transferidas para um funil de separação. O funil deve ser
então agitado vigorosamente e deixadas as fases se separarem. A fase aquosa deve ser
extraída 3 vezes com 30 mL de acetato de etila em cada vez e o extrato deve ser armazenado.
As fases orgânicas combinadas devem então ser secas com sulfato de sódio, o agente secante
deve ser filtrado e os solventes evaporados em um evaporador rotativo. A amida do ácido
cinâmico que surge é um sólido branco, que deve ser seco a vácuo até massa constante.
Rendimento: 12,0 g (81,5 mmol, 82%); PF146-148°C; pureza de 99% (CLAE)
O produto pode ser recristalizado a partir de solução aquosa, após isto ele deve ser seco a
vácuo até que toda água seja removida (massa constante).
Rendimento: 10,8 g (73,4 mmol, 73%); PF 147-148°C. As análise espectrofotométricas e
CLAE não apresentam diferenças para o produto recristalizado ou não.
A fase aquosa pode ser acidificada e então extraída 2 vezes com 50 mL de acetato de etila.
Após secagem da fase orgânica com sulfato de sódio e evaporação do solvente em evaporador
rotatório surgirá cerca de 200 mg de um resíduo sólido branco. Este resíduo consiste de 80%
de amida do ácido cinâmico e de 20% de ácido cinâmico (ver resultados analíticos). A fase
aquosa não contém substâncias que possam ser detectadas cromatograficamente com CLAE
nas condições de análise prescritas. Após a evaporação da água no evaporador rotativo surge
um resíduo sólido que consiste principalmente de cloreto de amônio.
Comentários
Quando na reação é utilizado como reagente o cloreto do ácido cinâmico bruto não destilado
(13,5 g, ver experimento 2013) é obtida a amida do ácido cinâmico (sem recristalização) com
um rendimento de 9,65 g (65,6 mmol, 66% em relação ao ácido cinâmico utilizado (14,8 g,
100 mmol)).
Quando se goteja o cloreto do ácido cinâmico à solução de amônia conc., não é permitido se
utilizar um funil de adição com balanço de pressão porque os vapores de amônia subirão até a
solução de cloreto ácido, onde reagirão formando a amida, que precipita e obstrui o funil de
adição. A solução de cloreto de ácido cinamico também pode ser adicionada da injeção com o
auxílio de uma seringa através de um septo.
Gerenciamento dos Resíduos
Reciclagem
Resíduo
Mistura de solventes destilados
Fase aquosa
Sulfato de sódio
Liquor mãe aquoso
Disposição
Solventes orgânicos não halogenados
Mistura de água e solventes halogenados
Resíduo sólido sem mercúrio
Mistura de água e solventes não halogenados
2
March 2006
NOP
http://www.oc-praktikum.de
Tempo
Cerca de 2 horas sem recristalização
Possível Intervalo
Antes e após a agitação
Grau de dificuldade
Fácil
Instruções (escala em batelada de 10 mmol)
Materiais
Frasco de 100 mL com 3 bocais, condensador de refluxo, funil de adição sem compensação
de pressão, agitador magnético, funil de separação de 100 mL, evaporador rotatório, banho de
gelo, bomba de vácuo
Substâncias de Partida
Cloreto do ácido trans-cinâmico (pf 32-35°C, pe 251-258°C
destilado; produto do experimento 2013)
Solução aquosa conc. de amônia (25%)
Éter metil terc-butílico (pe 55°C)
Acetato de etila (pe 77°C)
Sulfato de sódio para secagem
1,66 g (10,0 mmol)
10 mL (8,7 g, 125 mmol)
10 mL
40 mL
cerca de 1 g
Reação
Adiciona-se a um frasco de 3 bocais de 100 mL com condensador de refluxo, agitação
magnética e funil de adição sem compensação de pressão, 10 mL de solução aquosa conc. de
amônia. O frasco de reação é resfriado em banho de gelo. Adiciona-se ao funil 1,66 g (10,0
mmol) de cloreto do ácido trans-cinâmico dissolvido em 80 mL de éter metil terc-butílico.
Esta solução é adicionada ao frasco sob agitação durante 30 minutos para evitar uma reação
muito rápida. Após a adição a agitação é continuada por 30 minutos à temperatura ambiente.
Ocorre a precipitação de um sólido fino que não será segregado.
Etapa final
O conteúdo do frasco de reação é transferido para um funil de separação de 100 mL. O frasco
deve então ser lavado inicialmente com 10 mL de água e então com 10 mL de acetato de etila.
Estas soluções de lavagem são então transferidas para um funil de separação. O funil deve ser
então agitado vigorosamente e deixadas as fases se separarem. A fase aquosa deve ser
extraída 3 vezes com 10 mL de acetato de etila em cada vez e o extrato deve ser armazenado.
As fases orgânicas combinadas devem então ser secas com sulfato de sódio, o agente secante
deve ser filtrado e os solventes evaporados em um evaporador rotatório. A amida do ácido
cinâmico que surge é um sólido branco, que deve ser seco a vácuo até massa constante.
Rendimento: 1,15 g (7,81 mmol, 78%); PF146-148°C; pureza de 99% (CLAE)
3
March 2006
NOP
http://www.oc-praktikum.de
O produto pode ser recristalizado a partir de solução aquosa, após isto ele deve ser seco a
vácuo até que toda água seja removida (massa constante).
Rendimento: 900 mg (6,12 mmol, 61%); PF 147-148°C. As análise espectrofotométricas e
CLAE não apresentam diferenças para o produto recristalizado ou não.
A fase aquosa pode ser acidificada e então extraída 2 vezes com 50 mL de acetato de etila.
Após secagem da fase orgânica com sulfato de sódio e evaporação do solvente em evaporador
rotativo surgirá cerca de 200 mg de um resíduo sólido branco. Este resíduo consiste de 80%
de amida do ácido cinâmico e de 20% de ácido cinâmico (ver resultados analíticos). A fase
aquosa não contém substâncias que possam ser detectadas cromatograficamente com CLAE
nas condições de análise prescritas. Após a evaporação da água no evaporador rotatório surge
um resíduo sólido que consiste principalmente de cloreto de amônio.
Comentários
Quando na reação é utilizado como reagente o cloreto do ácido cinâmico bruto não destilado
(1,4 g, ver experimento 2013) é obtida a amida do ácido cinâmico (sem recristalização) com
um rendimento de 1,05 g (7,14 mmol, 71% em relação ao ácido cinâmico utilizado (1,4 g, 100
mmol)).
Quando se goteja o cloreto do ácido cinâmico à solução de amônia conc., não é permitido se
utilizar um funil de adição com balanço de pressão porque os vapores de amônia subirão até a
solução de cloreto ácido, onde reagirão formando a amida, que precipita e obstrui o funil de
adição. A solução de cloreto de ácido cinamico também pode ser adicionada da injeção com o
auxílio de uma seringa através de um septo.
Gerenciamento dos Resíduos
Reciclagem
Resíduo
Mistura de solventes destilados
Fase aquosa
Sulfato de sódio
Liquor mãe aquoso
Disposição
Solventes orgânicos não halogenados
Mistura de água e solventes halogenados
Resíduo sólido sem mercúrio
Mistura de água e solventes não halogenados
Tempo do experimento
Cerca de 1,5 horas sem recristalização
Possíveis Intervalo
Antes e após a agitação
Grau de dificuldade
Fácil
Caracterização
CLAE
Preparação da amostra: 0,1 mg da substância são dissolvidas em 1 mL de acetonitrila.
4
March 2006
NOP
http://www.oc-praktikum.de
Condições do CLAE:
Coluna:
Temperatura da coluna
Volume de injeção:
Gradiente:
Vazão
Comprimento de onda:
Phenomenex Luna C18; tamanho de partícula 3 μm, comprimento 150 mm, diâmetro
interno 4,6 mm
25°C
5,0 μL
0 min
5% acetonitrila + 95% água (+ 0,0059% ácido trifluoroacético)
40 min 95% acetonitrila + 5% água (+ 0,0059% ácido trifluoroacético)
50 min 95% acetonitrila + 5% água (+ 0,0059% ácido trifluoroacético)
1,0 mL/min
220 nm
Concentração porcentual foi calculada a partir das áreas dos picos.
CLAE I (Produto antes da recristalização)
mAU
13.073
800
700
600
500
400
300
200
100
0
0
5
10
15
20
25
30
35
40
45
min
25
30
35
40
45
min
CLAE II (Extrato da fase aquosa acidificada)
mAU
800
700
600
500
13.059
400
300
200
17.653
100
0
0
5
10
15
20
5
March 2006
NOP
http://www.oc-praktikum.de
Tempo de retenção
(min)
13,1
Área do pico (%)
CLAE I
CLAE II
100
80
Substância
Amida do ácido
cinâmico
Ácido cinâmico
17,7
20
7.6
7.4
7.2
7.0
6.8
6.6
(ppm)
12
11
10
9
8
7
6
5
4
3
2
1
0
(ppm)
Espectro de RMN 1H do produto puro (250 MHz, DMSO-D6)
(ppm)
6,61
7,13
7,2 – 7,6
Dentro do
multipleto:
7,42
Multiplicidade Constante de acoplamento
(Hz)
d
JAB = 15,9
wide s
m
d
JAB = 15,9
Número de H
1
1
7
1 of 7
Atribuição
HA
NH (apenas um)
NH + CH aromático
+HB
HB
Os sinais < 4 ppm correspondem ao DMSO, água e éter tert-butil metílico.
O
HB
NH2
HA
6
March 2006
NOP
http://www.oc-praktikum.de
Espectro de RMN 1H do ácido cinâmico (250 MHz, CDCl3) (para comparação)
O
HB
8.0
7.5
7.0
OH
6.5
HA
(ppm)
12
11
10
9
8
7
6
5
4
3
2
1
0
(ppm)
(ppm)
6,48
7,35 – 7,65
7,82
10,8
Multiplicidade Constante de acoplamento
(Hz)
d
JAB = 16,0
m
d
JAB = 16,0
Singleto largo
Número de
H
1
5
1
1
Atribuição
HA
CH areno
HB
OH
Espectro de RMN 1H do extrato da fase aquosa acidificada
7.6
7.2
6.8
6.4
(ppm)
12
11
10
9
8
7
6
5
4
3
2
1
0
(ppm)
(mistura da amida do ácido cinâmico e do ácido cinâmico) (250 MHz, DMSO-D6)
7
March 2006
NOP
http://www.oc-praktikum.de
Espectro deRMN 13C do produto puro (amida do ácido cinâmico) (250 MHz, DMSO-D6)
180
160
140
120
100
80
60
40
20
0
(ppm)
(ppm)
122,31
127,52
128,90
129,42
134,86
139,16
166,68
38,5-40,5
Atribuição
= CH – CONH2
CH areno
CH areno
CH areno
Cquart areno
– CH = CH – CONH2
– CONH2
solvente
Espectro de Infravermelho do produto puro (KBr)
Transmission [%]
80
60
40
20
0
4000
3500
3000
2500
2000
1500
1000
500
-1
-1 ]
Wellenzahl
[cm
Número
de onda [cm
]
(cm-1)
3375, 3175
3084
Atribuição
Estiramento N – H
Estiramento = C – H
8
March 2006
NOP
http://www.oc-praktikum.de
1665
1634
1610
1580, 1495
1450
Estiramento C = O, amida
Estiramento C = C, alceno
Estiramento C = C, areno
9
March 2006