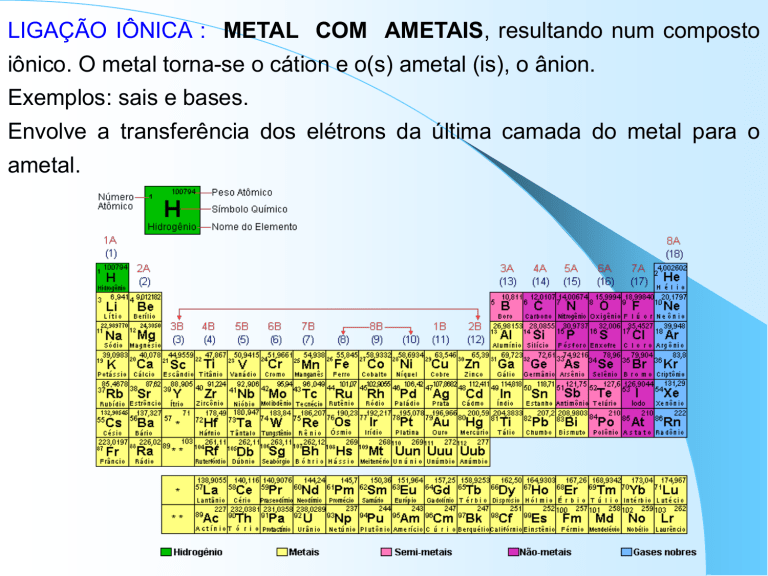
LIGAÇÃO IÔNICA : METAL COM AMETAIS, resultando num composto
iônico. O metal torna-se o cátion e o(s) ametal (is), o ânion.
Exemplos: sais e bases.
Envolve a transferência dos elétrons da última camada do metal para o
ametal.
LIGAÇÃO COVALENTE : ENTRE AMETAIS OU AMETAIS E
HIDROGÊNIO, resultando num composto molecular, ou seja numa
molécula.
Exemplos: ácidos e álcool.
Envolve o compartilhamento de pares eletrônicos da última camada.
Formulação de compostos iônicos
Íons: átomos ou grupo de átomos com carga.
Cátion: íon com carga positiva (perdeu elétrons), formado em geral
pelo metal.
Ânion: íon com carga negativa (recebeu elétrons), formado por
ametais.
Para formular e nomear compostos iônicos, siga os passos
•Coloque o cátion na frente do ânion, com suas respectivas cargas.
•Determinar os índices: quantos cátions e quantos ânions serão
utilizados na fórmula, de forma que o total de carga positivas se iguale
ao total de cargas negativas (se anulam).
•Escrever o cátion com seu índice e o ânion com seu índice, porém na
fórmula final não há cargas!!
•Para nomear o composto iônico, o nome do ânion vem primeiro,
portanto procure o nome do ânion na tabela de ânions, acrescente de, e
depois coloque o nome do cátion.
Fórmula geral de um composto iônico:
carga do cátion
carga do ânion
Cátion x+ Ânion y-
1o passo
OBS: Colocar sempre o cátion antes do ânion na fórmula!!
(Cátion )y (Ânion )x
índice do cátion
fórmula final
índice do ânion
Formular é definir os índices x e y!!
Nomenclatura: nome do ânion + de + nome do cátion
monovalentes
bivalentes
trivalentes
amônio
O amônio é um cátion que não é formado por metais!!
Não se esqueça de anotar o nome do cátion amônio na sua
tabela.
O nome dos ânions não oxigenados termina em ETO
Anote na sua tabela (tente escrever dentro de cada
quadrinho; o meu não coube).
cloreto iodeto
nitreto
fluoreto brometo sulfeto
carbeto
fosfeto
cianeto
O nome dos ânions muito oxigenados pode terminar em ATO
ou PER_ATO.
Anote na sua tabela (tente escrever dentro de cada quadrinho;
o meu não coube).
perclorato periodato
perbromato
tiossulfato
iodato
clorato
bromato
borato
fosfato
nitrato
carbonato
sulfato
permanganato
tiocianato
dicromato
manganato
ortossilicato
bicarbonato
cianato
cromato
Exercício exemplo: para cada ítem, dados os cátions e os ânions, forneça
a fórmula e o nome do composto iônico.
a) K+ Br–
c) Ag+ CN–
b) Na+ F–
d) Ca2+ I–
e) Zn2+ Cl–
g) Ca2+ CO32–
f) Al3+ F–
h) Al3+ PO43–
i) Na+ SO42–
j) K+ ClO3–
Exercício exemplo: para cada ítem, dados os cátions e os ânions, forneça
a fórmula e o nome do composto iônico.
a) K+ Br–
OBS: Como o total de cargas
positivas já é igual ao total de
cargas
negativas
(elas
se
anulam), vou usar 1 cátion K+ e 1
ânion Br–.
b) Na+ F–
OBS: Como o total de cargas
positivas já é igual ao total de
cargas negativas (elas se anulam),
vou usar 1 cátion Na+
e 1 ânion F–.
Resposta: KBr (os 2 índices são
1, e portanto não os coloco).
brometo de potássio
Resposta: NaF (os 2 índices são 1,
e portanto não os coloco).
fluoreto de sódio
Na fórmula final do composto iônico, as cargas não aparecem; somente
os índices aparecem!!
Exercício exemplo: para cada ítem, dados os cátions e os ânions, forneça
a fórmula e o nome do composto iônico.
c) Ag+ CN–
OBS: Como o total de cargas
positivas já é igual ao total de
cargas
negativas
(elas
se
anulam), vou usar 1 cátion Ag+ e
1 ânion CN–.
Resposta: AgCN (os 2 índices
são 1, e portanto não os coloco).
cianeto de prata
d) Ca2+ I–
OBS: Para anular o total de cargas
positivas, vou precisar de 2 I– na
fórmula.
Resposta: CaI2
iodeto de cálcio
Na fórmula final do composto iônico, as cargas não aparecem; somente
os índices aparecem!!
Exercício exemplo: para cada ítem, dados os cátions e os ânions, forneça
a fórmula e o nome do composto iônico.
e) Zn2+ Cl–
OBS: Para anular o total de
cargas positivas, vou precisar de
2 Cl– na fórmula.
f) Al3+ F–
OBS: Para anular o total de cargas
positivas, vou precisar de 3 F– na
fórmula.
Resposta: ZnCl2
cloreto de zinco
Resposta: AlF3
fluoreto de alumínio
Na fórmula final do composto iônico, as cargas não aparecem; somente
os índices aparecem!!
Exercício exemplo: para cada ítem, dados os cátions e os ânions, forneça
a fórmula e o nome do composto iônico.
g) Ca2+ CO32–
OBS: Como o total de cargas
positivas já é igual ao total de
cargas
negativas
(elas
se
anulam), vou usar 1 cátion Ca2+ e
1 ânion CO32–.
h) Al3+ PO43–
OBS: Como o total de cargas
positivas já é igual ao total de
cargas negativas (elas se anulam),
vou usar 1 cátion Al3+
e 1 ânion PO43–
Resposta: CaCO3
(os 2 índices são 1, e portanto
não os coloco).
carbonato de cálcio
Resposta: AlPO4
(os 2 índices são 1, e portanto não
os coloco).
fosfato de alumínio
Na fórmula final do composto iônico, as cargas não aparecem; somente
os índices aparecem!!
Exercício exemplo: para cada ítem, dados os cátions e os ânions, forneça
a fórmula e o nome do composto iônico.
i) Na+ SO42–
OBS: Para anular o total de
cargas negativas, vou precisar de
2 Na+ na fórmula.
Resposta: Na2SO4
sulfato de sódio
j) K+ ClO3–
OBS: Como o total de cargas
positivas já é igual ao total de cargas
negativas (elas se anulam), vou usar
1 cátion K+ e 1 ânion ClO3–.
Resposta: KClO3
(os 2 índices são 1, e portanto não
os coloco).
clorato de potássio
Na fórmula final do composto iônico, as cargas não aparecem; somente
os índices aparecem!!
Fazer o exercício 1 da página 11 da apostila
Exercícios: Nomenclatura e Formulação de Sais
1.Monte as fórmulas e dê os nomes dos sais.
cátion
ânion
Cl–
I–
S2–
NO3–
ClO4–
Na+
Ag+
Mg2+
Ba2+
Al3+
cátion
ânion
Cl–
I–
S2–
Na+
Ag+
Mg2+
Ba2+
NaCl
AgCl
MgCl2
BaCl2
cloreto cloreto cloreto de cloreto
de
de prata magnésio de bário
sódio
NaI
AgI
Mgl2
Bal2
iodeto iodeto iodeto de iodeto de
de
de prata magnésio
bário
sódio
Na2S
Ag2S
MgS
BaS
sulfeto sulfeto sulfeto de sulfeto de
de
de prata magnésio
bário
sódio
Al3+
AlCl3
cloreto de
alumínio
All3
iodeto de
alumínio
Al2S3
sulfeto de
alumínio
cátio
n
ânion
NO3–
ClO4–
Na+
Ag+
NaNO3
AgNO3
nitrato de nitrato de
sódio
prata
NaClO4
AgClO4
perclorato perclorato
de sódio
de prata
Mg2+
Ba2+
Al3+
Mg(NO3)2
nitrato de
magnésio
Mg(ClO4)2
perclorato
de
magnésio
Ba(NO3)2
nitrato de
bário
Ba(ClO4)2
perclorato
de bário
Al(NO3)3
nitrato de
alumínio
Al(ClO4)3
perclorato
de
alumínio
Cátions com carga variável:
carga menor: OSO
carga maior: ICO
Fe2+: ferroso
Fe3+: férrico
Cu+: cuproso
Cu2+: cúprico










