Índice
Resumo
pág. 2
Introdução
pág. 2 e 3
Procedimento Experimental
pág. 3 e 4
Resultados
pág. 5
Discussão/Conclusão
pág. 5
Questionário
pág. 6 e 7
Bibliografia
pág.7
1. Resumo:
Este trabalho laboratorial teve como objectivo a sintetização do éter trifenilmetil metílico a
partir do trifenilmetanol e de metanol. Para isso, utilizou-se meio ácido (H2SO4) para que a
reacção SN1 ocorresse e se formasse o produto desejado. Por fim, determinou-se o ponto de
fusão, de modo a estabelecer o grau de pureza do composto formado.
Obteve-se então 1,2g de produto, tendo a reacção um rendimento de 61%. Relativamente
ao ponto de fusão do composto sintetizado, este rondava o valor de 87ºC.
2.
Introdução:
Em termos reaccionais, a conversão do trifenilmetanol a éter
trifenilmetil metílico corresponde a uma substituição nucleófila unimolecular
(Sn1). Esta reacção dá-se sobretudo em dois passos fundamentais:
Primeiro o ácido sulfúrico vai protonar o grupo funcional OH do trifenilmetanol
formando um novo grupo O+H2.Como este novo grupo é um bom grupo de saída, tem muita
tendência a abandonar a molécula formando-se então o respectivo carbocatião.
Fig.1 - trifenilmetanol
O segundo passo consiste em reagir o metanol com este carbocatião. O metanol, de
fórmula molecular CH3OH, apresenta dois pares de electrões não ligantes no oxigénio desta
espécie, que podem ser utilizados para estabelecer uma ligação com o carbocatião. Surge,
então, uma nova molécula com os três grupos fenil e, em vez do grupo OH inicial, temos agora
o radical HO+CH3. Por último, e através de uma reacção ácido – base, o oxigénio perde o
hidrogénio que lhe está acoplado, obtendo-se assim o éter trifenilmetil metílico.
A nível cinético, o segundo passo dá-se mais rapidamente e é mais estável a nível
termodinâmico, porque contribui para a formação de um composto mais estável.
Para se poder obter o éter trifenilmetil metílico purificado, pelo método especificado no
protocolo experimental, recorre-se a uma recristalização dos cristais do éter. A recristalização
é basicamente um processo que consiste em readquirir cristais mais purificados de um
determinado composto já sólido. Para isso, o composto é dissolvido a quente e
posteriormente arrefecido, de forma lenta e gradual, para perder algumas das impurezas que
contém na sua matriz cristalina. A seguir a este arrefecimento procede-se a uma filtração a
vácuo e recupera-se o sólido [3].
O processo de recristalização requer portanto, inicialmente, a escolha de um solvente
adequado. O solvente ideal será aquele que dissolverá pouco o composto a frio e muito a
quente. Após o aquecimento, como existem impurezas que são insolúveis no solvente,
2
podemos proceder a uma filtração a quente para separar da mistura as impurezas que não
tenham solubilizado e ficar com o composto mais purificado [2].
A etapa seguinte da recristalização consiste em arrefecer a mistura do “solvente +
composto inicial” para que se dê a solidificação desse mesmo soluto. Se este arrefecimento for
suficientemente lento, ocorre a formação de cristais mais purificados. Se por outro lado, o
arrefecimento for rápido ocorre uma precipitação e as impurezas são arrastadas juntamente
com o precipitado, surgindo um composto impuro [2].
A presença de impurezas impede que o empacotamento das moléculas do composto seja
perfeito, diminuindo algumas das interacções intermoleculares e alterando algumas das
características desta substância, como por exemplo o seu ponto de fusão.
De uma forma geral, um composto impuro apresenta um ponto de fusão mais baixo e um
intervalo de fusão maior, comparativamente ao composto puro [3]. Por este motivo, o ponto de
fusão de um sólido permite avaliar o seu grau de pureza.
3. Procedimento:
Iniciar a experiência pesando 2,0g de trifenilmetanol num erlenmeyer de 50mL. Desfazer
estes cristais a pó com a ajuda de uma vareta e em seguida adicionar, lentamente, 20mL de
ácido sulfúrico sobre o trifenilmetanol. Ir-se-á formar uma solução acastanhada devido ao
aparecimento do carbocatião derivado do trifenilmetanol. À parte, colocar 80mL de metanol
dentro de um erlenmeyer de 250mL, introduzindo-o num recipiente com gelo até este
arrefecer.
Retirar do gelo o erlenmeyer com o metanol agora arrefecido e adicionar a este,
lentamente, a solução com o carbocatião. A solução vai ficar com uma coloração
esbranquiçada devido á formação do éter trifenilmetil metílico.
Devolver o erlenmeyer para o recipiente com gelo, agitando periodicamente até que se dê
a precipitação do éter. Assim que ele precipitar, transferir a solução para um funil de Buchner
acoplado a um kitasato para se proceder a uma filtração a vácuo.
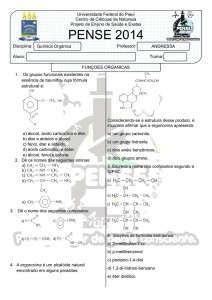
Antes de verter a solução para o funil, colocar neste um papel
absorvente humedecido com um pouco de água. No caso de existir
ainda algum éter no erlenmeyer inicial após a transferência para o
funil de Buchner, despejar o solvente que ficou no kitasato de novo
para o erlenmeyer, e voltar a verter para dentro do funil. De referir
que primeiro tem de se abrir a torneira da água para fazer vácuo e
só depois encaixar a mangueira no kitasato. Contudo quando acaba
Fig.2 - Filtração a vácuo
3
a filtração, faz-se o contrário, isto é, primeiro retira-se a mangueira e só depois se desliga a
torneira da água.
Diluir o filtrado que fica no kitasato com água e adicionar carbonato de sódio para haver
neutralização do ácido sulfúrico ainda em solução. De seguida eliminar pelo esgoto normal de
águas residuais.
Obtêm-se assim cristais sólidos de éter trifenilmetil metílico. Para se proceder a uma
recristalização deste composto colocar os cristais do éter num balão de vidro e acrescentar
metanol até preencher totalmente o sólido. Ligar ao balão de vidro, um condensador de
refluxo e aquecer a solução num banho de água quente. O condensador de refluxo vai impedir
que os vapores de metanol escapem do sistema.
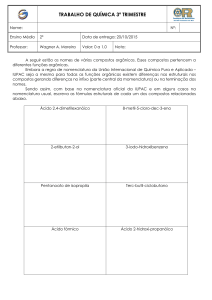
Quando o éter estiver completamente dissolvido no metanol proceder a uma
filtração a quente, tendo o cuidado de desligar todas as fontes próximas de calor já
que existem vapores de metanol (que é muito inflamável) a sair do balão de vidro.
Este tipo de filtração é utilizado de modo a evitar-se o arrefecimento da mistura
aquando do contacto directo desta com as paredes do funil. O papel de filtro é
geralmente dobrado em pregas a fim de aumentar a velocidade de reacção [4].
Seguidamente, transferir o filtrado para um novo erlenmeyer e arrefecer em
gelo. Realizar de seguida uma nova filtração a vácuo assim que o éter precipitar.
Fig.3 - Filtração a quente
Recolher o metanol que ficou no kitasato para um recipiente de recolha de solventes não
clorados e o éter trifenilmetil metílico para um frasco devidamente identificado. Passado uns
dias e assim que os cristais de éter estejam suficientemente secos medir o ponto de fusão e
retirar conclusões quanto á pureza do composto atingido.
4
4. Resultados:
Éter trifenilmetil
metílico
Ponto de fusão
tabelado
94ºC
Ponto de fusão
experimental
87ºC
Massa do frasco
vazio
21,6g
Massa do frasco +
composto
20,4g
Massa inicial
2g
Massa final
1,22g
Rendimento
61%
Massa do frasco vazio: 20,4g
Peso do frasco + composto: 21,6g
Massa do composto: 21,6 – 20,4 = 1,2g
Rendimento:
5. Discussão/Conclusão:
Ao longo desta actividade experimental são vários os passos necessários para a síntese do
Éter trifenilmetil metílico. Em cada um desses passos há sempre perda de compostos
intermédios, nomeadamente, no que diz respeito às filtrações à trompa e à transferência do
produto para o processo de refluxo, uma vez que é difícil retirar todos os resíduos dos
recipientes onde se encontravam, perdendo deste modo alguma da sua quantidade.
É de registar que existe a possibilidade, dado que estamos na presença de uma reacção de
substituição, de ocorrerem reacções paralelas (reacções de eliminação, por exemplo) que
influenciam de forma negativa o produto obtido.
O ponto de fusão, a uma dada pressão, por definição é um valor constante e característico
de uma substância pura, não se observando, durante a medição do ponto de fusão, variações
de temperatura significativas. No entanto, se a amostra for impura, a amplitude será maior,
sendo que a presença de impurezas contribui também para a variação do ponto de fusão.
Aquando da medição do ponto de fusão, verificou-se que este era de 87ºC, sendo o valor
do mesmo da substância pura 94 ºC. Com estes dados, conclui-se que o éter trifenilmetil
metílico apresentava muito provavelmente impurezas, dado o elevado valor obtido
experimentalmente.
5
Relativamente ao rendimento obtido, este foi de 61%, concluindo-se que foi sintetizada
uma quantidade apreciável de éter trifenilmetil metílico, o que é bastante bom, dado que se
verificou a existência de perdas de produto aquando da realização da experiência.
6. Questionário:
1 - Mostre o mecanismo da reacção de formação do éter trifenilmetil metílico
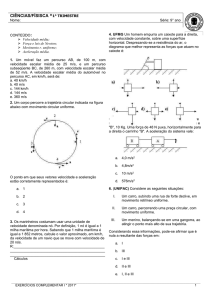
A síntese do éter trifenilmetil metílico tem como base a seguinte reacção
(C6H5)3COH
+ H2SO4
+
CH3OH
(C6H5)3COCH3
Fig.4- Difenilmetanol
2 – O Difenilmetanol reagiria mais devagar que o trifenilmetanol? Porquê?
O difenilmetanol tem menos um anel benzénico. Quando ficamos com o
carbocatião desta espécie (quando a molécula perde o grupo funcional OH) vão
existir menos híbridos de ressonância a estabilizar a carga positiva do
composto, o que torna a molécula menos estável.
Além disso, o carbono que fica com a carga positiva passa a ser menos substituído ao
apresentar menos um grupo fenil, o que também reduz a estabilidade do carbocatião. Como
tal, o primeiro passo da reacção do ácido sulfúrico com o difenilmetanol iria ser mais lento,
pois seria menos reactivo.
6
Por sua vez, o ataque do metanol (nucleófilo) ao carbocatião (electrófilo) dar-se-ia com
maior velocidade, já que este mesmo carbocatião é menos estável. Assim, formar-se-ia mais
rapidamente éter difenilmetil metílico a partir do carbocatião comparativamente com o
mesmo processo de formação do éter trifenilmetil metílico.
3 – É possível obter como produto secundário um alceno por eliminação E1? Porquê?
O grupo OH ao ser protonado pelo ácido sulfúrico converte-se em O+H2 que é um
bom grupo de saída. Ao sair este grupo, ficamos com um carbono com carga positiva
que podemos denominar de carbono alfa. Se um carbono beta, ou seja, um dos
carbonos ligados a este, apresentar um hidrogénio que possa ser removido por
reacção ácido-base, perde-se esse mesmo H+ e esse carbono beta fica com um par de
electrões disponível para estabelecer uma ligação dupla com o carbono alfa.
Ficaríamos portanto assim com um alceno.
No caso do carbocatião proveniente do trifenilmetanol, não seria de todo possível
obter um alceno como produto secundário, pois nenhum dos carbonos beta apresenta
um hidrogénio que possa ser captado.
7.
Bibliografia:
[1]-Protocolo – Química Orgânica Laboratório, Departamento de Engenharia Química e
Biológica ,IST, 2008/2009
[2]-http://www.pucrs.br/quimica/professores/arigony/praticas/acetanilida/recristalizacao.htm
[3]-http://www.dq.fct.unl.pt/cadeiras/tls/main/7%C2%AA%20Aula%20-%2014-11-2006%20%20Sublima%C3%A7%C3%A3o%20e%20Recristaliza%C3%A7%C3%A3o.pdf
[4]- http://www.fc.up.pt/gisocb/pdfs/QBiol2001_2002secure.pdf
7