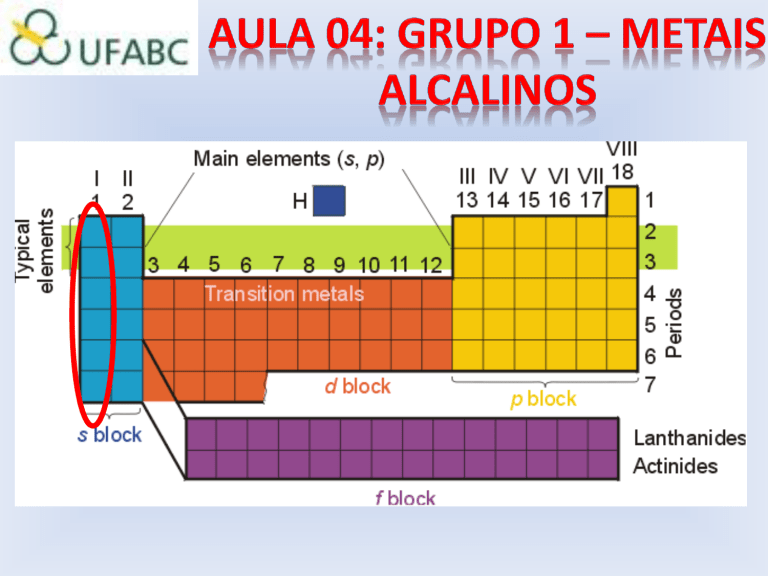
1
Li
Na
K
Rb
Cs
Fr
Abundância na crosta dos elementos do Grupo 1
As abundâncias são dadas na forma logarítmica (base 10) em gramas de
metal por 1000 Kg de amostra.
Como a escala vertical e logartímica, as diferenças são muito maiores o
que aparentam.
Log Li = 1,30 Li = 101,30 19 g de Li / 1000 Kg
Log Na = 4,36 Na= 104,36 23000 g de Na / 1000 Kg
Propriedades físicas dos metais
• maleáveis, dúcteis, bons condutores, frios ao tato e altamente
reativos.
• A maioria dos metais é sólido com átomos em um empacotamento
cúbico de corpo centrado (no de coordenação 8)
• pouco denso.
• Raios grandes e portanto energia de ionização baixa.
• Estrutura cristalina
Cúbica de corpo centrado
Energia de Ionização
• A primeira energia de ionização, I1, é a quantidade de energia
necessária para remover um elétron de um átomo gasoso:
Na(g) → Na+(g) + e- I1 = 495,7 kJ mol-1
• A segunda energia de ionização, I2, é a energia necessária para
remover um elétron de um íon gasoso:
Na+(g) → Na2+(g) + eI2 = 4563 kJ mol-1
• Quanto maior a energia de ionização, maior é a dificuldade para
se remover o elétron.
Propriedades Atômicas
G.E. Rodgers, J. Chem. Educ. 2014, 91, 216-224.
Propriedades Gerais
extremamente reativos (agentes redutores fortes).
(utilizados para obter metais puros: TiCl4 (g) + 4Na(l) 4NaCl(s) + Ti(s))
elétrons da última camada estão distantes do núcleo, a força de
atração entre núcleo e elétron é fraca; a energia necessária para
remover um elétron externo é
pequena, tão pequena que:
i) podem ser removidos pela irradiação com luz (Cs e K: cátodo em
células fotoelétricas)
ii) podem ser promovidos para orbitais mais externos pela energia
de uma chama.
Propriedades Gerais
Emissão sob a chama:
o elétron absorve um “quanta” de energia e é excitado
é promovido para um orbital mais externo
sua nova posição é instável
ele emite a energia absorvida na forma de luz
A intensidade da cor produzida na chama é proporcional
a concentração de íons ou átomos presentes
atração fraca entre os átomos na ligação metálica
Energia de
Coesão (kJ mol-1)
Li
161
Na
108
K
90
Rb
82
Cs
78
Baixa coesão
baixa resistência mecânica
Propriedades Gerais
Valores baixos para metais (comparados aos metais de transição)
Li, Na e K são menos densos
que a água
Devido ao raio
Propriedades Químicas
Eored são muito negativos
Reação com água
2 Li
+
H2O
2 Na + H2O
2 K + H2O
G = -nFEo
2 LiOH
2 NaOH + H2
2 KOH + H2
+
H2
Oxidam em
presença da
água
G < 0 termodinamicamente favorável
Para a reação com o Li o G é negativo e o mais elevado do grupo,
ou seja, maior liberação de energia
Propriedades Químicas
Reatividade com água
Conforme descemos o grupo o PF diminui e a energia
liberada provoca a fusão do metal deixando exposta uma
maior superfície do metal para o contato com a água.
http://www.youtube.com/watch?v=QSZ-3wScePM
Propriedades Químicas
Reação com gases do ar
Quando expostos ao ar perdem rapidamente o brilho devido a formação de
óxidos. O Li é o único que forma mistura com nitreto ( 6Li (s) + N2 (g) 2Li3N (s))
Li+, cátion pequeno, forma preferencialmente o óxido (O2-)
2 Li(s)
1
2
O2(g) Li2O(s)
Na+, um pouco maior, forma peróxidos (O2-2)
2 Na(s) O2(g) Na2O2(s)
K+, ainda maior, forma superóxidos (O2-1)
K(s) O2(g) KO2(s)
Propriedades Químicas
Tipos de ligação em compostos
Metais alcalinos apresentam valores relativamente pequenos de Eletronegatividade
Ao reagirem com outros elementos formam compostos com grande diferença de
eletronegatividade, portanto tendem a fazer ligação iônica:
Eletronegativade do Na
0,9
Eletronegatividade do Cl
3,0
Diferença de eletronegatividade
2,1
Valor 2,1 implica em uma ligação predominantemente iônica no NaCl.
Para KBr: 2,0; LiF: 3,0
Diferença de eletronegatividade ~1,7 corresponde a uma
ligação com aproximadamente 50% de caráter iônico
Estrutura dos Sólidos Iônicos
Metais: maleáveis
Sólidos iônicos: quebradiços
Estrutura dos Sólidos Iônicos
Em compostos iônicos, apresentam configuração eletrônica de
gás nobre, com todos os elétrons emparelhados.
Grande quantidade de energia para
excitar o elétron
Transição eletrônica na região do
ultravioleta
Compostos iônicos: brancos
Compostos iônicos contendo metais alcalinos coloridos:
Na2(CrO4) (amarelo)
Quem são os responsáveis pela coloração?
K2(Cr2O7) (alaranjado)
K(MnO4) (violeta intenso)
Os ânions com metais de transição,
não o metal alcalino!!
Entalpia de rede, HRo e o ciclo de Born-Haber
É a variação de entalpia molar
padrão que acompanha a
formação de íons gasosos a partir
do sólido:
MX(s) M+(g) + X-(g)
Hf = Hs + I + ½ Hd + E + U
Hs, I e Hd são positivas
E e U são geralmente negativas
Hf < 0
+ ½ Entalpia de
dissociação (Hd)
- Afinidade Eletrônica (E)
+ Entalpia de
sublimação (Hs)
+ Energia de
ionização (I)
- Energia Reticular (U)
Entalpia de
formação (Hf)
Ciclo de Born-Haber
+ ½ Entalpia de
dissociação (Hd)
- Afinidade
Eletrônica (E)
+ Entalpia de
sublimação (Hs)
- Energia Reticular (U)
+ Energia de
ionização (I)
- Entalpia de
Hidratação
Entalpia de
formação (Hf)
P/ formação do NaCl
P/ hidratação do NaCl
Para que uma substância se dissolva, a energia
liberada quando os íons se hidratam (energia de
hidratação) deve ser maior que a energia necessária
p/ romper o retículo cristalino (energia reticular - U).
Sólido se dissolve
Sólido é insolúvel
Todos os sais simples dos metais alcalinos são solúveis em água.
A energia reticular diminui ligeiramente enquanto a energia de
hidratação varia mais acentuadamente de cima p/ baixo.
A solubilidade em água da maioria dos sais do Grupo 1 decresce de
cima p/ baixo.
SEMELHANTE DISSOLVE
SEMELHANTE
Depende:
Se a energia liberada quando os íons se hidratam (energia
de hidratação) for maior que a energia necessária p/
romper o retículo cristalino (energia reticular - U).
Dissolve
Métodos de Obtenção
Obtenção dos alcalinos na forma metálica
são os agentes redutores mais fortes que se conhecem não
podendo ser obtidos por redução dos seus óxidos
são tão eletropositivos que reagem com água. Não podem ser
deslocados por outro elemento mais eletropositivo.
COMO FAZER?
Métodos de Obtenção
Eletrólise de cloretos fundidos
2 NaCl(l) 2 Na(l) + Cl2(g)
Eo = -2,71 - 1,36 = - 4,07 V
2 Cl- (aq) Cl2 (g) + 2 e2 Na+ (l) + 2 e- 2 Na (s)
Escala industrial
Célula de Downs
REAÇÃO GLOBAL:
NaCl Na(l) + ½Cl2(g)
Métodos de Obtenção
Rubídio e césio são obtidos como subprodutos do processamento do
lítio
Frâncio é radioativo com meia vida de apenas 21 min não
ocorre na natureza de maneira significativa
Principais Compostos
• Liga com Li (14%), Al (1%) e Mg (84%): estrutura de aeornaves
• Baterias
• LiOH: empregado na fabricação de graxas para motores (Resistente a altas
ltemperaturas)
• LiH: empregado na geração de H2 para uso militar
• Li2CO3: emprego recente em tratamento de disturbios como o transtorno
bipolar
• Li[AlH4]: poderoso agente redutor utilizado em química orgânica p/ reduzir
compostos carbonílicos a álcoois
Relação diagonal
Semelhança entre o 1º elemento de cada grupo com o elemento
abaixo à direita
Lítio e tratamento de transtorno bipolar
John Emsley, Vaidade, Vitalidade, Virilidade, Jorge Zahar Editor, 2006, Rio de Janeiro
Principais Compostos
• NaOH: obtido por eletrólise de solução salina
(NaCl)
Sólido branco, gorduroso, mole e corrosivo.
O mais importante composto de sódio para a
industria.
10o produto químico industrial em termos de
produção
2 Cl- (aq) Cl2 (g) + 2 e2 H2O (l) + 2 e- H2 (g) + 2 OH- (aq)
Escala industrial
Esquema de uma moderna célula
cloroálcali usando uma membrana
catiônica (troca de cátions), a qual
tem alta permeabilidade para íons
Na+ e baixa para íons OH- e Cl-.
REAÇÃO GLOBAL:
NaCl + H2O NaOH + ½H2 + ½Cl2
Principais Compostos
Principais Compostos
• NaCl: sal de cozinha
• NaHCO3: empregado como fermento, antiácido estomacal,
extintor de incêndio
.brando
NaHCO3 aquec
Na2CO3 H 2O CO2 ( g )
NaHCO3 ( aq) HA( aq) Na ( aq) A -(aq) H2O(l ) CO2 ( g )
• Na2O2: empregado como alvejante em polpa de madeira,
papel, algodão e linho
Na2O2 ( s ) H2O(l ) 2 NaOH( aq) H2O2 (l )
• Na2S: empregado para fabricar corantes orgânicos sulfurados e nos curtumes
para remover os pelos do couro
• Na2CO3: empregado para remover cátions Ca2+ e Mg2+ de águas duras
Ca2 ( aq) CO3
2
( aq)
CaCO3 ( s )
Na2CO3: empregado para remover cátions Ca2+ e Mg2+ de águas duras
Ca2 ( aq) CO3
2
( aq)
CaCO3 ( s )
Geralmente chamado de barrilha
Obtido pelo método Solvey (1861 - por Ernest Solvay)
2NaCl(aq) + CaCO3(s)
Na2CO3(s) + CaCl2(aq)
O equilíbrio está deslocado p/ a esquerda devido à alta energia de
rede (entalpia de rede)
REAÇÕES
CaCO3 CaO + CO2
H = +43,4 Kcal
C(amorfo) + O2 CO2
H = -96,5 Kcal
CaO + H2O Ca(OH)2
H = -15,9 Kcal
NH3 + H2O NH4OH
H = -8,4 Kcal
2NH4OH + CO2 (NH4)2CO3 + H2O
(NH4)2CO3 + CO2 + H2O 2NH4HCO3
NH4HCO3 + NaCl NH4Cl + NaHCO3
2NaHCO Na CO + CO + H O
H = -22,1 Kcal
H = +30,7 Kcal
REAÇÃO GLOBAL:
CaCO3 + NaCl Na2CO3 + CaCl2
Principais Compostos
• KOH: utilizado para fabricar sabão líquido
• KCl: Sal “light”
• KNO3: ocorre na natureza como mineral salitre, utilizado em
armas (pólvora)
4 KNO3(s) + 7 C(s) + S(s) 3CO2(g) + 3CO(g) + 2N2(g) + 2K2CO3(s) + K2S(s)
• KBr: utilizado em fotografia e como antiafrodisíaco
• KO2: máscara de respiração (usado em minas, submarinos e
veículos espaciais)
4 KO2 + 2 CO2 2K2CO3 + 3O2
4 KO2 + 4 CO2 + 2 H2O 4 KHCO3 + 3O2
Mercado especializado e pequeno.
Aplicações:
• vidros para aplicação em fibras ópticas;
•Indústria de telecomunicações;
•Equipamentos de visão noturna
•Células fotoelétricas
•Relógio de Césio (relógio atômico)
John Emsley, Moléculas em exposição
Na+ é ativamente expulso das células enquanto o K+ não (Bomba
de sódio)!
A diferença de concentração entre Na+ e K+ gera um gradiente de
potencial elétrico através da membrana celular, essencial p/ o
funcionamento de células nervosas e musculares.
Bibliografia
•
Atkins, P., Jones, L., Princípios de Química - Questionando a Vida Moderna e o Meio
Ambiente, 3 ed., Porto Alegre: Bookman, 2006.
•
Shriver, D. F., Atkins, P., Química Inorgânica, Ed Artmed, 2003 .
•
Lee, J. D., Química Inorgânica Não Tão Concisa. Edgard Blucher Ltda, 3a ed., São
Paulo, 1980
•
Brent, R., The Golden book of Chemistry Experiments, Golden Press, New
York,1960