1º
Química A
Jaqueline/Lailson
Aval. Trimestral
EM
27/06/13
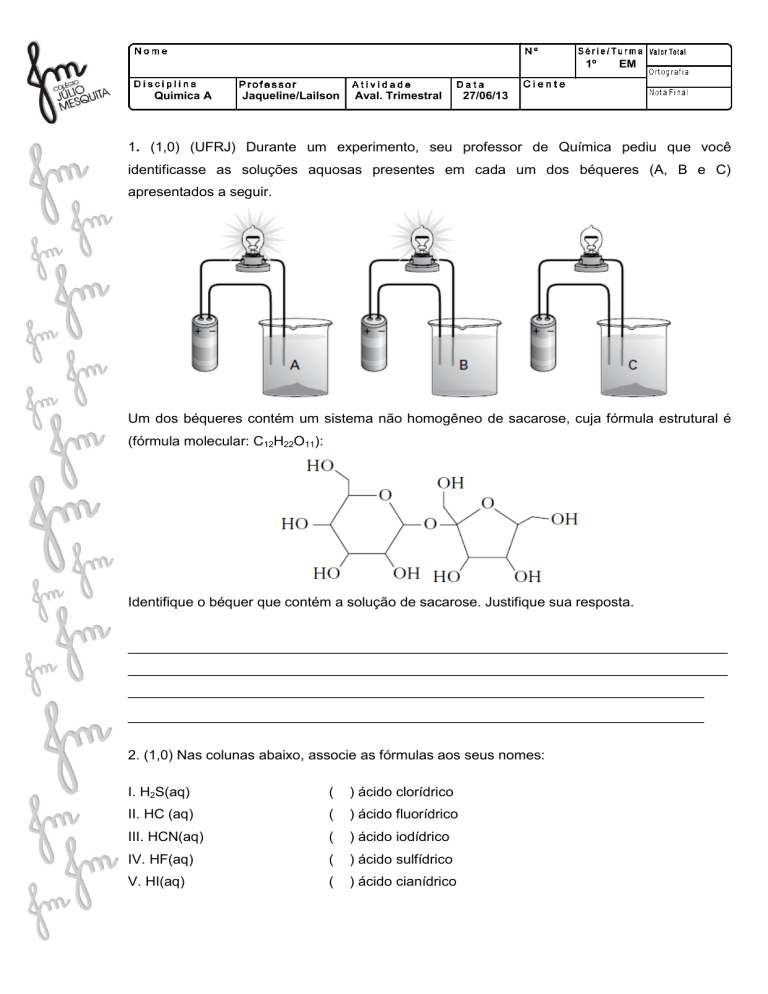
1. (1,0) (UFRJ) Durante um experimento, seu professor de Química pediu que você
identificasse as soluções aquosas presentes em cada um dos béqueres (A, B e C)
apresentados a seguir.
Um dos béqueres contém um sistema não homogêneo de sacarose, cuja fórmula estrutural é
(fórmula molecular: C12H22O11):
Identifique o béquer que contém a solução de sacarose. Justifique sua resposta.
____________________________________________________________________________
____________________________________________________________________________
_________________________________________________________________________
_________________________________________________________________________
2. (1,0) Nas colunas abaixo, associe as fórmulas aos seus nomes:
I. H2S(aq)
(
) ácido clorídrico
II. HC (aq)
(
) ácido fluorídrico
III. HCN(aq)
(
) ácido iodídrico
IV. HF(aq)
(
) ácido sulfídrico
V. HI(aq)
(
) ácido cianídrico
3. (1,0) Classifique os ácidos em fortes, semifortes e fracos.
a) H3BO3
b) HMnO4
c) H2CrO4
d) H3PO4
e) H4SiO4
4. (1,4) Escreva a equação que representa a dissociação das seguintes bases, seguindo o
Exemplo: Ba(OH)2 → Ba2+ + 2OH–
a) LiOH
b) Aℓ(OH)3
5. (2,0) Escreva o nome e a fórmula das bases dos seguintes cátions:
Cátion
Li+
NH4+
Ba2+
Aℓ3+
Na+
Fórmula da base
Nome da base
6. (1,6) Considere os seguintes cátions e ânions:
+
+
2+
2+
2+
+
• cátions: Na , K , Ca , Mg , Ba , NH4 .
–
–
–
–
2–
–
2–
• ânions: Cl , F , I , NO3 , CO3 , HCO3 , SO4 , ClO
-
Escreva a fórmula dos seguintes sais:
a) cloreto de cálcio:
b) iodeto de magnésio:
c) carbonato de potássio:
d) nitrato de amônio:
7. (1,0) Sobre os compostos HCl, H2SO4, H3BO3 e H2CO3 classifique as afirmações como
verdadeiras ou falsas:
(
(
) Todos sofrem ionização quando em meio aquoso, originando íons livres.
) Segundo Arrhenius, todos são ácidos porque, quando em meio aquoso, originam como
cátions íons H+.
(
) Todos são compostos moleculares.
(
) De acordo com o grau de ionização, HCl e H2SO4 são ácidos fortes.
(
) Os compostos H3BO3 e H2CO3 formam soluções aquosas com alta condutividade
elétrica.
8. (1,0) (UEL-PR) Considere as soluções aquosas abaixo:
Solução
Cor
CuSO4
azul
KNO3
incolor
Na2SO4
incolor
K2CrO4
amarela
A partir dessa tabela, é possível concluir que os íons responsáveis pelas cores azul e amarela
são: Sua resposta será considerada somente se corretamente justificada no espaço
abaixo.
a) Cu2+ e SO42–
d) Na+ e NO3 –
b) K+ e CrO42–
e) Cu2+ e CrO42–
c) K+ e SO42–
____________________________________________________________________________
____________________________________________________________________________
____________________________________________________________________________
__________________________________________________________________________