COLÉGIO ESTADUAL DR. REBOUÇAS – ENSINO FUNDAMENTAL E MÉDIO
RIO BOM – PR
PROFESSORA: ILDA FRACASSI BATISTA
Proposta disciplinar- Química
Química embutida
Conteúdo estruturante: Biogeoquímica
Conteúdos básicos: Reações químicas
Conteúdo especifico: Velocidade das reações;
Fatores que influenciam na velocidade da reação
Quantidade de aulas: 4 aulas
Etapa: Ensino Médio
Recursos a serem utilizados:
rótulos de embalagens de alimentos de enlatados e embutidos
Livro didático
quadro de giz
laboratório de informática
laboratório de química
Encaminhamento metodológico
O desenvolvimento da proposta será divida em quatro aulas. Em um primeiro
momento será apresentado um texto para despertar a atenção dos alunos e os envolver
no assunto proposto. No segundo momento será realizada pesquisas e analise de
embalagens
de
embutidos,
onde
serão
retirados
dados
necessários
para
o
encaminhamento da aula, e no terceiro e quarto momento serão trabalhados conteúdos
da cinética química.
Aula 1
Nesse primeiro momento será apresentado um texto introdutório sobre alimentos
embutidos, seus componentes e efeitos maléficos para a saúde com intuito de possibilitar
aos alunos uma aproximação entre o conhecimento do dia- a- dia e o conhecimento
cientifico, onde será realizado um momento de discussões.
Você se alimenta ou come?
Você já parou para pensar na diferença entre se alimentar e comer? É simples.
Quando você se serve de um prato colorido, rico em fibras, minerais e vitaminas, está se
alimentando. Por outro lado, se você monta um prato cheio de produtos enlatados e
embutidos, está apenas matando a fome.
Claro que a praticidade dos produtos enlatados é tentadora, mas é preciso muito
cuidado. Não descuide da nutrição. Evite consumir enlatados e embutidos muitas vezes
na semana. Para conservar estes tipos de alimentos, as indústrias abusam aditivos
químicos.
Para tornar estes alimentos mais atraentes, duráveis e práticos, os fabricantes
usam inúmeros aditivos químicos. Os mais comuns são os aromatizantes, corantes,
antioxidantes, estabilizantes, conservantes e acidulantes. São eles os responsáveis pelo
sabor, cheiro e aspecto naturais dos alimentos industrializados.
Estes tipos de alimentos trazem riscos à saúde. Podem causar alergias e doenças
cardiovasculares. Quando consumidos em excesso, podem levar ao desenvolvimento de
tipos específicos de câncer.
Evite ceder à praticidade, porém se não tiver outra opção tenha muito cuidado ao
escolher a lata. Alimentos enlatados e embalados à vácuo são mais suscetíveis a
bactéria Clostridium Botulinum, isso porque o micro-organismo se desenvolve em locais
sem oxigênio. Latas estufadas é sinal da presença da bactéria, o “inchaço” acontece
pelos gases produzidos pela Clostridium Botulinum.
Você já ouviu falar em nitritos e nitratos? Estas substâncias são usadas para
conservação de alimentos como picles, salsichas, outros embutidos e alguns tipos de
enlatados. Acontece que, no estômago, nitritos e nitratos se transformam em
nitrosaminas, composição cientificamente cancerígena se consumida de forma continua
e abundante.
Lembre-se: alimentação saudável exige a ingestão de alimentos naturais e
frescos, já os produtos industrializados, ricos em gordura saturada, sal e açúcar, devem
passar longe do prato.
Para prevenir doenças cardiovasculares, obesidade, diabetes e outros problemas
de saúde, tenha uma alimentação adequada. Frutas, verduras, legumes e cereais
integrais são ricos em vitaminas, minerais e fibras. Faças destes alimentos sua principal
fonte de alimentação. Para a que a saúde não seja comprometida, lave os vegetais com
atenção e produtos adequados.
No final da aula será pedido aos alunos que tragam embalagens diversas de
alimentos embutidos de casa para a próxima aula.
Aula 2
Nesse momento os alunos serão divididos em grupos e orientados a analisar e em
seguida anotar os componentes químicos e as quantidades presentes em cada alimento
embutido e enlatado. Logo após realizarão pesquisas no laboratório de informática sobre
as quantidades aceitáveis para consumo diário e será realizado uma comparação com os
dados obtidos em sala de aula, sendo apresentados aos demais. Os alunos serão
orientados a pesquisar os valores aceitáveis
de componentes químicos no site da
ANVISA (Agência Nacional de Vigilância Sanitária).
Aula 3
Nessa aula será explicado o conteúdo: tipos de reações químicas.
A aula será ministrada oralmente, utilizando como apoio o quadro de giz, o livro
didático do aluno e o texto abaixo, que é um resumo que será entregue impresso a cada
aluno.
Tipos de reações químicas
O que evidencia uma reação é a transformação que ocorre nas substâncias em
relação ao seu estado inicial, essas modificações dependem do tipo de reação que os
reagentes irão passar.
Existem vários critérios para classificar reações químicas, um deles relaciona o
número de substâncias que reagem (reagentes) e o número de substâncias produzidas
(produtos). Para melhor exemplificar iremos utilizar as letras: A, B, C, X, Y.
Reação de síntese ou adição: são aquelas que duas ou mais substâncias originam um
único produto.
A+ B → C
Exemplo dessa reação: quando o magnésio reage com o oxigênio do ar:
2Mg(s) + 1 O2(g) → 2MgO(s)
Essa reação se faz presente em flashes fotográficos descartáveis e foguetes
sinalizadores.
Reação de análise ou decomposição: nessa reação uma única substância gera dois
ou mais produtos.
A→ B + C
Algumas
reações
recebem
nomes
especiais:
Eletrólise: as substâncias se decompõem pela passagem de corrente elétrica.
Fotólise:
Pirólise:
decomposição
decomposição
da
pela
substância
ação
do
química
calor
e
pela
luz.
do
fogo.
Exemplo: Os airbags são dispositivos de segurança presentes em vários
automóveis. Quando acionamos esse dispositivo, a rápida decomposição do composto
de sódio NaN3(s) origina N2(g) que faz inflar os airbags.
Veja a reação:
2 NaN3(s) → 3 N2(g) + 2 Na(s)
Reação de simples troca ou deslocamento: ocorre quando uma substância simples
reage com uma composta originando novas substâncias: uma simples e outra composta.
A + XY → AY + X
Exemplo: Quando uma lâmina de zinco é introduzida em uma solução aquosa de
ácido clorídrico, vai ocorrer a formação de cloreto de zinco e o gás hidrogênio vai ser
Zn (s) + 2 HCl (aq) → ZnCl2(aq) + H2 (g)
Observe que o Zinco deslocou o Hidrogênio, daí o porque do nome “reação de
deslocamento”.
Reação de dupla troca: dois reagentes reagem formando dois produtos, ou seja, se
duas substâncias compostas reagirem dando origem a novas substâncias compostas
recebem essa denominação.
AB + XY → AY + XB
Exemplo: a reação entre o ácido sulfúrico com hidróxido de bário produz água e sulfato
de bário.
H2SO4 (aq) + Ba(OH)2(aq) → 2 H2O(l) + BaSO4(s)
O produto sulfato de bário: BaSO4(s) é um sal branco insolúvel.
Por Líria Alves (Graduada em Química)
Logo após será entregue aos alunos uma folha de atividades complementares.
Colégio Estadual Dr Rebouças- Ensino Fundamental e Médio.
Aluno (a) : __________________________________________ nº: ________
Atividades
1) A reação que representa a formação do cromato de chumbo II, que
é um pigmento amarelo usado em tintas, é representada pela equação:
Pb(CH3COO)2 + Na2CrO4 → PbCrO4 + 2 NaCH3COO
Que é uma reação de:
a) oxirredução
b) dupla troca
c) síntese
d) deslocamento
e) decomposição
2) O fermento de pão pode ser obtido através da seguinte reação química:
CO2 + NaCl + NH3 + H2O → NaHCO3 + NH4Cl
Reagentes para a obtenção do fermento (NaHCO3): gás carbônico (CO2), cloreto de
sódio(NaCl), amônia (NH3) e água (H2O).
Fermento para pães
A equação acima demonstra a formação dos produtos:
a) carbonato de sódio e cloreto de amônio
b) bicarbonato de sódio hidrogenado e cloreto de amônio
c) bicarbonato de sódio e cloreto de amônio
d) tricarbonato de sódio e cloreto de amônio
3) No filme fotográfico, quando exposto à luz,ocorre a reação:
2 AgBr →2 Ag + Br2
Essa reação pode ser classificada como:
a) pirólise.
b) eletrólise.
c) fotólise.
d) síntese.
e) simples troca.
4) O consumo de ácido sulfúrico pode ser utilizado como um indicador do
desenvolvimento de um país. Industrialmente, esse ácido pode ser obtido a partir da
pirita de ferro, que consiste basicamente em sulfeto ferroso (FeS). Classifique as
equações de obtenção industrial do ácido sulfúrico mostradas a seguir:
I. FeS + O2 → Fe + SO2
II. 2 SO2 + 2 O2 → 2 SO3
III. SO3 + H2O → H2SO4
a) Dupla troca, síntese, síntese.
b) Dupla troca, análise, análise.
c) Síntese, simples troca, dupla troca.
d) Simples troca, análise, análise.
e) Simples troca, síntese, síntese.
Aula 4:
Nessa aula será explicado o conteúdo velocidade das reações e quais são os
fatores que implicam na velocidade da reação .
Como na aula 3, o conteúdo será explicado oralmente , utilizando como apoio o
quadro de giz e livro didático do aluno, textos e atividades impressas.
Velocidade das reações químicas
A Cinética Química é um campo que estuda os fatores que influenciam a taxa de
desenvolvimento das reações químicas, isto é, a velocidade com que se processam. Há
cada vez mais pesquisas em torno desta área, visto que muitas vezes queremos acelerar
algumas reações ou diminuir a rapidez de outras. Isso é especialmente importante para
as indústrias e essas pesquisas têm importantes consequências tecnológicas.
Mas, visto que a velocidade de uma reação pode variar em cada intervalo de tempo
e de uma substância para outra, costuma-se calcular a velocidade média das reações.
Considere a reação genérica a seguir, em que os coeficientes são as letras minúsculas e
os reagentes e produtos estão representados pelas letras maiúsculas:
aA+bB→cC+dD
A velocidade média dessa reação será dada dividindo-se a velocidade média de
reação de qualquer uma das substâncias reagentes ou a velocidade média de formação
de qualquer um dos produtos pelo seu respectivo coeficiente na equação química. Isto é
dado por:
FATORES QUE ALTERAM A VELOCIDADE DAS REAÇÕES QUÍMICAS
Alguns fatores podem aumentar ou diminuir a velocidade de uma reação química.
São eles:
- temperatura
- superfície de contato
- pressão
- concentração
- presença de luz
- catalisador
- inibidores
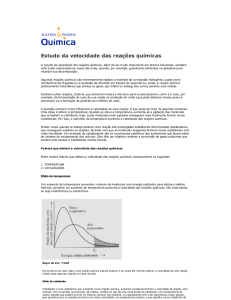
Temperatura
A temperatura está ligada à agitação das moléculas. Quanto mais calor, mais
agitadas ficam as moléculas. Se aumenta a temperatura, aumenta a energia cinética das
moléculas (movimento). Se as moléculas se movimentam mais, elas se chocam mais e
com mais energia, diminuindo a energia de ativação e em consequência, aumenta o
número de colisões efetivas e portanto a velocidade da reação também aumenta.
Por este motivo, aumentamos a chama do fogão para cozinhar e utilizamos a
geladeira para evitar a deterioração dos alimentos.
Superfície de Contato
A área de contato entre os reagentes também interfere na velocidade das reações
químicas. Quanto maior a superfície de contato, maior o número de moléculas reagindo,
maior o número de colisões eficazes e portanto, aumenta a velocidade da reação.
Isto explica porque devemos tomar um comprimido de aspirina, por exemplo,
inteiro do que em pó. O comprimido em pó reage mais rapidamente, causando lesões no
nosso estômago. Se ele for ingerido inteiro, levará mais tempo para reagir, evitando
lesões.
Uma substância em pó reage mais rápido do que uma substância inteira porque
possui maior superfície de contato.
Veja outros exemplos:
- a carne é digerida mais facilmente quando mastigada do que inteira;
- gravetos queimas mais rápido do que um pedaço de madeira de mesma massa;
- palha de aço queima mais rápido do que um pedaço de ferro de mesma massa.
Pressão
Pressão é a razão entre força e área, ou seja, fazer força sobre uma determinada
área. Com o aumento da pressão em um recipiente, diminui o volume e desta forma
aumenta a concentração dos reagentes. As moléculas se chocam mais, aumentando o
número de colísões e portanto, aumenta a velocidade da reação.
Concentração está relacionado à quantidade de soluto e de solvente de uma
substância. Se aumenta a concentração de reagentes , aumenta o número de moléculas
dos reagentes, aumentando o número de colísões e aumentando também a velocidade
da
reação.
Está
associada
à
Lei
Cinética
(Lei
de
Guldber-Waage).
Quando se aumenta a concentração de oxigênio numa queima, a combustão
acontece mais rápido.
Presença de Luz
Algumas reações químicas ocorrem com maior velocidade quando estão na
presença de luz. A luz influencia na velocidade das reações porque é uma energia em
forma de onda eletromagnética que ajuda a quebrar a barreira da energia de ativação.
A água oxigenada, por exemplo, se decompõe mais facilmente quando está exposta à
luz, por isso devemos deixá-la guardada em local escuro. A fotossíntese realizada pelas
plantas é um tipo de reação que é influenciada pela presença da luz. Outra reação onde
é muito utilizada a luz é a decomposição do AgBr que dá origem aos filmes fotográficos.
Catalisador
Catalisador é uma substância química que não participa da reação química.
Diminui a energia de ativação e aumenta a velocidade da reação.
O catalisador acelera a reação mas não altera a composição química dos
reagentes e produtos envolvidos. A quantidade de substância produzida na reação não
se
altera
com
o
uso
de
catalisadores.
Se a reação for reversível, a reação inversa também será acelerada, pois sua
energia
de
ativação
também
O catalisador não altera a variação de entalpia.
terá
um
valor
menor.
Gráficos com e sem catalisadores:
Catálise é o aumento de velocidade da reação, provocado pelo catalisador.
A palavra catálise, do grego katálysis, foi introduzida, em 1835, por Berzeliu.
No nosso organismo existem muitos catalisadores, que são chamados de
enzimas. A saliva e o suco gástrico (que contém ácido clorídrico) são exemplos de
enzimas
que
aumentam
a
velocidade
da
reação,
no
caso,
a
digestão.
Nas indústrias químicas, principalmente a petroquímica, os catalisadores são
muito utilizados para acelerar as reações, deixando o processo mais barato.
Uma forma de ver a ação dos catalisadores é adicionando açúcar ao refrigerante.
Os refrigerantes carbonatados contém dióxido de carbono (gás carbônico) e pode
ser eliminado mais facilmente com adição de açúcar. A reação de eliminação do gás
acontece com mais velocidade e percebe-se a formação de bolhas do gás deixando a
solução.
Na equação química, coloca-se o catalisador em cima da seta que representa a
reação
química.
Em função dos estados físicos dos reagentes e produtos, a catálise pode ser
homogênea ou heterogênea.
- catálise homogênea: quando reagentes e catalisador estão no mesmo estado físico
formando
um
sistema
monofásico.
- catálise heterogênea: quando reagentes e catalisador não estão no mesmo estado
físico formando um sistema heterogêneo.
Não existe um tipo ideal de catalisador. Para cada reação química existe um tipo
diferente de catalisador. Os catalisadors mais comuns são:
- metais - principalmente os de transição: Co, Ni, Pt, Pd
- ácidos - que catalisam muitas reações orgânicas: H2SO4
- óxidos metálicos – Al2O3, Fe2O3
- bases - NaOH
- enzimas – produzidas pelos organismos vivos: lipase, suco gástrico.
Inibidores
São substâncias, que ao contrário dos catalisadores, aumentam a energia de
ativação e como consequência diminuem a velocidade da reação química. Pode ser
chamado também de veneno de catalisador ou anticatalisador. Antigamente era
chamado de catalisador negativo.
Velocidade Instantânea
Nas reações químicas a velocidade a cada instante é diferente da velocidade
média. As velocidades instantâneas nunca são as mesmas, possuindo valores diferentes
durante a reação. Se os intervalos de tempo utilizados nas medidas da velocidade média
forem ficando cada vez menores, a velocidade média tenderá a assumir valores cada
vez mais próximos da velocidade em um certo instante.
Velocidade Instantânea é o valor para o qual tende a velocidade média quando os
intervalos de tempo vão se tornando cada vez menores.
Após a explicação do conteúdo,será realizados experimentos para melhor fixação.
Experimento 1:
Influência da temperatura na velocidade da reação
Esse experimento será observado o que ocorre com a velocidade das reações
quando se varia a temperatura. Para isto, serão medidos os tempos de reação para três
sistemas formados pelos mesmos componentes , mas sob temperaturas diferentes.
Materiais e reagentes
3 copos de 250 mL
cronômetro
água gelada e água quente
termômetro até 100 ° C.
3 comprimidos de anti – ácido efervescente
Procedimento:
1. Encha um copo com água gelada, anote sua temperatura.
2. Coloque um comprimido efervescente no béquer e anote o tempo que decorre até
dissolução completa.
3. Repita as mesmas operações com água à temperatura ambiente (25 ° C) e água a
50° C.
Experimento 2:
Influencia da superfície de contato na velocidade da reação
Nesse experimento será verificado o que ocorre com a velocidade das reações
quando existe uma maior ou menor superfície de contato.
Materiais e reagentes
2 copos com 250 mL de água
2 comprimidos anti – ácido efervescente
Procedimento:
1. Coloque um comprimido efervescente inteiro em um copo com água e no outro copo
um comprimido triturado. Observe.
Após os experimentos, os alunos farão um relatório explicando o observado.
Perspectiva de abordagem interdisciplinar:
Biologia- Fungos e bactérias: ação dos mesmos sobre os alimentos.
Matemática- Porcentagem, gráficos e tabelas: interpretação de informações
contidas nos rótulos, e criação e leitura de gráficos e tabelas.
Material complementar
Alimentos enlatados e embutidos causam danos à saúde . Disponível em:
http://saude.consultaclick.com.br/6591/
alimentacao/alimentos-enlatados-eembutidos-causam-danos-a-saude.
Acesso
em: 29/out./2014.
Cinética
química.
Disponível
em:
http://www.soq.com.br/conteudos/em/cineticaquimica/p5.php. Acesso em: 30/out./2014.
Tipos de reações químicas. Disponível em: www.brasilescola.com/quimica/tiposreacoes-quimicas.htm. Acesso em: 30/out.//2014.
Velocidades
das
reações.
Disponível
em:
http://www.brasilescola.com/quimica/velocidade-das-reacoes-quimicas.htm. Acesso em:
30/out./2014.
Referencias
Diretrizes Curricular do Ensino Médio