Resumo ATIVIDADE DE QUÍMICA – Dia 14/02/2017.
O que a Química estuda? A química estuda as propriedades, transformações e reações que
acontecem DENTRO da matéria.
CONSTITUIÇÃO DA MATÉRIA:
Átomo: Menor parte da matéria.
Molécula: Um conjunto de átomos, forma uma molécula. Exemplo: H2O (Dois átomos de
hidrogênio e um átomo de oxigênio, ou seja, o conjunto de 3 átomos, formou a molécula da
água).
Matéria: Conjunto de moléculas. Pode ser calculada em MASSA (quilogramas, gramas, etc.) e
VOLUME (Quilolitros, litros, etc.).
1. Uma parte da matéria é chamada de CORPO.
2. Quando uma matéria é modificada a fim de se tornar algo pronto, é chamado de
OBJETO.
EM TUDO HÁ QUÍMICA, não há exceções.
Gravidade: É a força que os corpos exercem uns sobre os outros. Exemplo: Gravidade da Terra
é 9,8.
Diferença de PESO e MASSA: Quando você vai medir seu “peso”, na verdade, você estará
medindo sua MASSA. O peso é o valor da massa multiplicado pela força gravitacional
(gravidade).
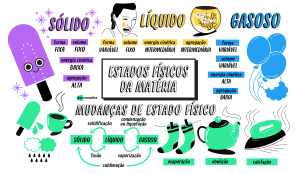
ESTADOS DA MATÉRIA: (Tentei fazer um esquema, mas não consegui, mals)
Sólido (moléculas extremamente juntas)
Possui uma forma, já que as moléculas estão
juntas
Líquido (moléculas separadas)
Gasoso (moléculas extremamente separadas)
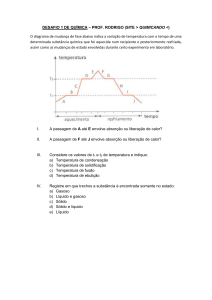
Transformações:
SETA AZUL: FUSÃO: Passagem do estado sólido para o líquido (exemplo: gelo se
descongelando).
SETA ROXA: VAPORIZAÇÃO (Passagem do estado líquido para gasoso). Há três etapas:
Evaporação: Primeira etapa: Baixa energia – Água vai esquentando.
Ebulição: Segunda etapa: Mais energia – Água se evapora.
Calefação: Terceira etapa: MUITA energia – Água se evapora MUITO rápido.
SETA AMARELA: CONDENSAÇÃO (ou liquefação): Água no estado gasoso, se esfria e se torna
líquida.
SETA VERMELHA: SOLIDIFAÇÃO: Água no estado líquido vai congelando.
SETA PRETA: SUBLIMAÇÃO: Água no estado sólido se transforma em estado gasoso, SEM
PASSAGEM PRO ESTADO LÍQUIDO, muita energia (calor).
SETA VERDE: RESSUBLIMAÇÃO (ou sublimação): Passagem do estado gasoso para sólido, sem
passagem pro estado líquido.
PROPRIEDADES DA MATÉRIA:
Propriedades gerais:
INÉRCIA: Capacidade do corpo em permanecer em movimento ou em repouso
conforme a situação.
MASSA: Está ligada à inércia. Mede a resistência que tem um corpo.
IMPENETRABILIDADE: Duas matérias não podem ocupar o mesmo espaço ao
mesmo tempo.
DIVISIBILIDADE: Toda matéria pode ser dividida até chegar em um átomo,
porção menor de uma matéria.
COMPRESSIBILIDADE: Propriedade em que, sob outras forças, esta matéria
pode diminuir. (Ver na apostila, é complicado).
ELASTICIDADE: Propriedade em que um corpo pode se esticar ou comprimir e
depois ele voltará na sua forma original.
INDESTRUTIBILIDADE: Matéria não pode ser destruída, e sim, transformada.
(Exemplo: Transformação de madeira em cinzas, vai estar queimando a
madeira e formará outra matéria, que é a cinza).
Propriedades funcionais: Cada matéria se enquadra em um grupo com suas
características. (Não é importante, acho).
Propriedades específicas: DIVIDE-SE em 3 ramificações (Propriedades organolépticas,
físicas e químicas).
Propriedades organolépticas: Propriedades relacionadas aos SENTIDOS DO CORPO.
COR (visão), SABOR (paladar), ODOR (olfato), TEXTURA (tato).
Propriedades físicas: TRANFORMAÇÕES (físicas, “por fora”):
DUREZA: Resiste ao corte, ou seja, somente uma matéria mais dura pode “cortar”
outra. (Exemplo da apostila: Para que um piso não seja riscado por areia, é preciso que
ele tenha uma DUREZA SUPERIOR do que a areia).
DENSIDADE: Relação de massa e volume de uma matéria.
TENACIDADE: Resistência a um choque (impacto). Quanto mais tenaz, mais resistente.
BRILHO: Propriedade que reflete a LUZ em uma matéria. Quando uma matéria não há
brilho, não é necessariamente que ela seja opaca. (Ver na apostila se não entenderam,
é complicado).
Propriedades químicas: TRANFORMAÇÕES (químicas, “por dentro”): Reação de uma
matéria quando “se relaciona” com outra.