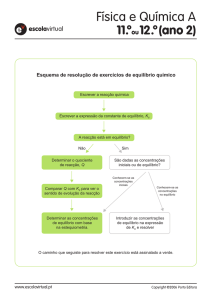
Atividade 2.2 – Sistematizando o que foi trabalhado
Vimos anteriormente que, quando um sistema atinge o estado de equilíbrio
químico, as concentrações das espécies presentes não variam, mesmo que as
reações direta e inversa continuem ocorrendo. Isso ocorre, pois as velocidades das
reações direta e inversa são iguais. É possível, porém, alterarmos algumas condições
do sistema para que estados de equilíbrios químicos diferentes sejam atingidos. Ou
seja, continuará havendo uma constância nas concentrações das espécies presentes,
porém, seus valores serão diferentes para cada estado de equilíbrio diferente.
Na atividade que realizamos com o “Cinetiqueitor/Equilibreitor” vimos que há
uma relação constante entre as concentrações das espécies A e B. Essa relação se
mantém, mesmo quando variamos a concentração inicial de A, ou seja, mesmo
quando estabelecemos um novo estado de equilíbrio químico ao alterarmos as
condições do sistema pela mudança nas concentrações das espécies. Essa relação
define a constante de equilíbrio químico (K).
A forma de se encontrar a constante de equilíbrio através das concentrações
das espécies irá variar de acordo com o tipo de sistema. No sistema que observamos
pelo “Cinetiqueitor/Equilibreitor”, a constante poderia ser achada pelo quociente do
valor da concentração de B pelo valor da concentração de A. Mas essa relação não
será sempre assim. Na verdade, para determiná-la devemos estabelecer o seguinte
quociente (entre 1 e 2):
1. O resultado da multiplicação das concentrações dos produtos elevadas aos
respectivos coeficientes estequiométricos.
2. O resultado da multiplicação das concentrações dos reagentes elevadas aos
respectivos coeficientes estequiométricos.
O quadro 2 apresenta as expressões da constante de equilíbrio para alguns tipos de
sistemas em equilíbrio químico mais comuns.
A constante de equilíbrio químico pode ser encontrada, também, através do
quociente entre as constantes de velocidade, k (não confunda com K, que em letra
maiúscula, significa constante de equilíbrio) das reações direta e inversa. Uma
constante de velocidade define a taxa de variação da concentração de uma espécie
Quadro 2 – Expressões matemáticas para o cálculo da constante de equilíbrio
(K) de alguns sistemas em equilíbrio químico
Tipo de sistema
Expressão da constante de equilíbrio (K)
[B]
A⇌B
[A]
[B]2
A ⇌ 2B
[A]
[C]
A+B ⇌C
[A]∙[B]
[C]2
A + 3B ⇌ 2C
[A]∙[B]3
[C]∙[D]
A+B ⇌C+D
[A]∙[B]
Fonte: Elaborado pelo autor
em uma reação química. Ela nos diz quantos mols/L variam ao longo do tempo.
Variações nas constantes de velocidade causam mudanças na constante de equilíbrio
e, para qualquer sistema, a constante de equilíbrio será dada pelo quociente entre as
constantes de velocidade.
Na aba “Cinetiqueitor”, a concentração inicial de A, ou seja, a concentração de
A no tempo 0 era a maior possível para A. Após o início da reação, esse valor
começou a diminuir enquanto a concentração de B aumentava e, como a reação
inversa não podia acontecer, não foi estabelecido um estado de equilíbrio químico.
Por outro lado, a aba “Equilibreitor” mostra um sistema no qual é possível
atingir um estado de equilíbrio químico. Da mesma forma que na situação anterior, a
concentração de A diminui e a concentração de B aumenta a partir do início da reação,
mas ocorre, também, a reação inversa. Isso permite que a reação atinja um estado de
equilíbrio sem que as concentrações de A e B se tornem iguais a zero. É importante
relembrar, porém, que as reações não param, elas apenas continuam ocorrendo a
velocidades iguais e, por isso, é possível estabelecer uma constante de equilíbrio para
o sistema.
Depois de atingido o estado de equilíbrio químico, as concentrações das
espécies não variam mais, a não ser que alteremos alguma condição do sistema. Isso
não quer dizer, porém, que a concentração de A seja igual a concentração de B. Isso
até é possível, se as condições do sistema permitirem, como ocorreu quando a
constante de velocidade da reação direta era igual à constante de velocidade da
reação inversa. Porém, em outras condições, qualquer uma das concentrações no
equilíbrio pode ser maior que a outra.
Em cada sistema diferente, podemos inferir a respeito de algumas condições do
sistema a partir do valor da constante de equilíbrio. Essas inferências dependerão do
tipo de sistema. No nosso caso, estamos discutindo uma reação do tipo A ⇌ B.
Portanto, podemos afirmar que se a constante de equilíbrio for maior que 1, a reção
direta ocorre em maior extensão que a reação inversa e a concentração de B, no
equilíbrio, é maior que a concentração de A. Mas, se for menor que 1, a extensão da
reação inversa é maior, assim como a concentração de A no equilíbrio será maior que
a concentração de A.
Este material foi desenvolvido por Gabriel Matos Vieira, em parceria com a equipe do
portal pontociência (http://pontociencia.org.br), como parte do projeto Portal do
Professor e Banco Internacional de Recursos Multimídia. O portal pontociência permite
copiar, distribuir, exibir e executar as obras, desde que mencionado o autor, sendo
proibido utilizar esta obra com finalidades comerciais. Para cada novo uso ou
distribuição, deve-se deixar claras as licenças de uso desta obra. Você pode adaptar
este material para finalidades educacionais sem fins comerciais.