Reatividade do grupo carbonila:
Construção do esqueleto carbônico
por condensações
Armin Isenmann
Parte I: os princípios da homocondensação e retro-síntese
Reatividade do grupo carbonila (incl. equilíbrio ceto-enol).
O alvo 1,3-difuncional, a partir dos componentes
pseudo-ácido e aceitador (incl. descarboxilações).
Manipulação das reatividades em condensações mistas:
1.
2.
3.
4.
5.
Utilização de um pseudo-ácido com baixa tendência de condensação
consigo mesmo e/ou um aceitador sem α-H. (incl. Aminometilação de
Mannich)
Desativação do pseudo-ácido por formação de uma imina.
Ativação do pseudo-ácido pela estabilização da forma enólica.
Emprego de um pseudo-ácido duplamente ativado (condensações de
Knoevenagel).
Com bases muito fortes se consegue desprotonar o pseudo-acido
quantitativamente em uma etapa preliminar.
Reatividade do grupo carbonila
Definição:
Condensação é a unificação de dois compostos
orgânicos sob formação de uma nova ligação
carbono-carbono.
Ampliação do esqueleto carbônico a partir
de um substrato A com carbono eletrofílico
e um substrato B com carbono nucleofílico.
Caso A = B : “Homocondensação” ou “autocondensação”
A ≠ B : “Condensação mista” ou “condensação cruzada”
Um carbono positivado (= eletrófilo) reage com um carbono carbanóide (= nucleófilo).
O grupo carbonila pode providenciar os dois componentes:
Carbono nucleofílico
em posição α
ao grupo carbonila
Tautomeria
CH
C
O
Enol
Base, - H+
O
C δ+
Carbono positivado:
Efeito do oxigênio –I >> +M
OH
Mesomeria
C
C
O-
O
Enolato
Tautomeria
Deslocamento reversível de um próton e uma ligação π ao
mesmo tempo.
Não é uma mesomeria, mas sim, um verdadeiro equilíbrio
entre dois compostos isoméricos.
Tautomerias são bastante comuns na química orgânica
•ceto - enol
•azometina (= imina = base de Schiff) – enamina
•amida (ou lactama) – ácido imido carboxílico
•endiol - α-hidroxicetona (na vitamina C)
•nitro - aci
•nitroso – oxima (aldoxima ou cetoxima)
•ácido hidroxâmico – carbiminodiol
Formas da catálise da tautomeria ceto-enólica
E
Base
Nu
-
H+(ou E+)
δ−
H
δ+
O
R CH C
forma ceto
R CH C
R CH C
+ H+
- H+
+
E+
O
O
H+
OH
- H+
Ânion enolato
R CH C
Base
+ H+
OH
OH
- H+
R CH2
C
- H+
R CH2 C
Cátion carbênio (oxônio)
+ H+
forma enol
O enolato e também o enol são carbanóides em posição α ao
grupo C=O. São sujeitos de ataque por eletrófilos.
O equilíbrio ceto-enol é acelerado por ácidos e por bases.
Em qualquer caso a tautomeria passa por uma forma
intermediária carregada. Portanto, a polaridade do ambiente
(solvente, teor de água, presença de sais) acelera esta reação.
Em compostos carbonilados simples a forma ceto é
dominante. Acetona: apenas 0,00025% em propenol.
Comprovantes para a forma enólica:
A espectroscopia r.m.n. revela uma posição especial dos sinais 1H (δ de até
17ppm)
Deslocamento das bandas de absorção no espectro infra vermelho
O composto carbonilado troca H por D em posição α, ao colocá-lo em D2O ou
C2H5OD
Pode-se adicionar bromo na dupla ligação da forma enólica
A velocidade da troca de hidrogênio, entre oxigênio e carbono α é bastante baixa.
Titulação com Br2:
A reprodução do enol pelo equilíbrio dinâmico dentro do tempo experimental é
desprezível, desde que se trabalha abaixo da temperatura ambiente.
forma enólica:
O H
CH C
O H
- Br-
CH C
Br
Br Br
- H+
Titulação
forma ceto:
O
CH2 C
O
+ Br2
CH C
Br
Observação: no ácido carboxílico também pode-se discutir uma
tautomeria. Porém, a adição de bromo não funciona por que a
densidade eletrônica deste “enol” é muito baixa. Portanto, a αbromação precisa da presença de um catalisador.
(Reação de Hell-Volhard-Zelinsky)
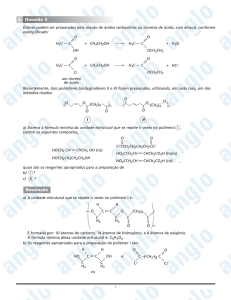
O que estes três compostos têm em
comum?
OH
1
OH
2
3
O
OAc
1
2
3
NH2
2
1
O
Grupos funcionais nos carbonos 1 e 3.
3
O alvo 1,3-difuncional
Retro-síntese (símbolo ⇒):
1. Analisar o esqueleto carbônico da molécula alvo (TM = Target Molecule)
2. Transformar todos grupos funcionais em oxigênios de NOX certo usando
transformações entre grupos funcionais (FGI = Functional Group
Interconversion) ou desconexões C-X.
3. Desconectar dois carbonos do esqueleto, geralmente os mais ramificados e
mais centralizados, usando uma reação de condensação.
•1,3-bifuncionais e compostos carbonilados α,β-insaturados
(= sistema de Michael)
•1,5-bifuncionais
•1,2-bifuncionais
•1,4-bifuncionais
•1,6-bifuncionais
1,3 e 1,5 podem ser feitos a partir de sintons com polaridade natural.
O
R1
OH
OH
O
R2
+
R1
CH2
Alvo 1,3-bifuncional
Aldol
R2
Aldeído (protonado) =
sinton eletrófilo
O
R1
CH2
Enolato =
sinton nucleófilo
Sintons naturais e reagentes para condensações
Nucleófilo: enolato ou enol
Reagente
Sinton
O
R
X
O
R
X
X = H, OEt, Alq, Ar
Eletrófilo:
Reagente
Sinton
R
OH
O
CH
CH
R
R1
R1
OH
R2
R2
O
R
O
O
C
R
C
X
X = Cl, OEt
Reagente
Sinton
O
O
⇐ Alvo 1,5-difuncional
R
R
Sistema conjugado
(sistema Michael)
Sintons não-naturais que levam aos alvos 1,2 e 1,4-difuncionais:
O
R
O
R
O
R
Nucleófilo:
Enolato, ou mais em geral, um carbono desprotonado.
Segue: Tabela de ácidos C-H e as bases necessárias
para sua desprotonação
Fonte: S. Warren, Organic Synthesis - The Disconnection Approach,
Wiley & Sons, Chinchester 1982, p. 143
Compostos 1,3-difuncionais:
1,3-dicarbonila
β-hidroxicarbonila (= aldol)
Carbonila α,β-insaturada
Nucleófilo em todos: enolato
1,3-Dicarbonilas
vêm da acilação do enolato
→ Condensação de Claisen
Catalisador = base (muitas vezes EtO-);
Reagente acilante (= eletrófilo): éster ou cloreto do ácido carboxílico
Exemplos
• Como fazer
O
O
OEt
?
O
O
O
b
C
a
O
a
OEt
+
Alvo
EtO
C
OEt
ruim: separou dois fragmentos desiguais
b
O
O
OEt
C
Base
OEt
O
O
C
C
EtO
OEt
Éster adípico
bom: só uma molécula de partida, simétrica = limpo
ciclização, intramolecular = fácil, rápido
Exemplo 2: inclui decomposição do composto 1,3-dicarbonila
O
2x R
C
O
OEt
EtO-
C
OEt
R
hidrólise
H2O / OHR
O
descarboxilação
H+, ∆
Rota padrão para cetonas simétricas.
Excurso:
Como funciona a descarboxilação térmica?
1) Liberar o ácido carboxílico livre (= hidrólise do éster)
2) Aquecer e desprender o gás carbônico.
R
R
O
H
O
O
C
C
C
∆
- CO2
O
OH
O
C C
C C
Enol
Regra geral:
Um ciclo de 5 ou 6 membros é uma conformação favorável.
Caso o estado de transição pode ser formulado assim,
A energia de ativação é baixa, então a reação é fácil e rápida!
H
β-hidroxicarbonila
eletrófilo = aldeído ou cetona
Mais reativo é o aldeído (Porquê? Duas respostas certas.)
Exemplo:
• Como fazer
O
OH
?
O
O HO
1
2
O
3
+
Alvo
O
Síntese: 2
Base
Alvo
Base: Ba(OH)2 = insolúvel; retirada imediata do alvo da zona reativa
A condensação é realizada favoravelmente no extrator Soxhlet:
Remoção de um dos produtos = Técnica mais importante
de levar reações equilibradas até altos rendimentos!
Controle termodinâmico
Em condensações:
1. Tirar H2O (subproduto de enonas,
feitas por condensação aldólica, cat. ácida ou por condensação de Knoevenagel)
2. Desprender CO2 , a partir de intermediários β-cetoácidos e 1,3-diácidos
3. Depositar o produto 1,3-dicarbonila em forma de complexo num cátion duro:
O
O
O
O
Base
Sal, insolúvel
Composto carbonilado α,β-insaturado
É muito fácil a desidratação da β-hidroxicarbonila (= aldol):
1) o próton a ser removido em posição α é enólico
2) o produto é estabilizado por conjugação
(∆H (conjugação) ≈ 15 - 17 kJ⋅mol-1)
OH
O
H+
CH
H
R
OH2
CH
H
O
O
R
- H2 O
- H+
CH
R
Reação anterior, esta vez sob catálise ácida:
não pára na β-hidroxicarbonila
O
2 H3C
+
[H ]
C CH3
- H2O
H3C
CH3
C
CH C
O
CH3
"Óxido de mesitila"
Análise:
O
O
+
O
Outro exemplo:
O
O
O
Onde quebrar?
O
O
O +
O
Condensações mistas
Nucleófilo (= componente metilênico = pseudo-ácido) é diferente
do eletrófilo (= carbonílico = aceitador).
Objetivo principal é direcionar as reatividades, isto é, marcar o papel
do eletrófilo em um composto carbonilado e do nucleófilo,
seletivamente, em outro composto carbonilado.
Assim se forma somente um produto.
Problema:
Os dois compostos carbonilados têm reatividades muito
semelhantes!
Ph
O
Ph
O
+
CHO
CH3
Síntese não funciona bem!
Alvo problema
1. Quem enoliza?
2. No caso da cetona, em que lado enoliza?
3. Quem é eletrófilo?
(Esses problemas se anulam ao usar dois componentes simétricos e/ou idênticos.)
As reatividades como nucleófilo e eletrófilo
não se opõem, mas geralmente aumentam juntos:
Enolizabilidade
Eletrofilia
Amida
Éster
Cetona
Anidrido
Aldeído
Cloreto de acila
Régio-seletividade em cetonas assimétricas
Controle cinético
vs.
Ambiente básico
Via única
Temperatura baixa
Produto mais rápido
Controle termodinâmico
Ambiente ácido
Sistema equilibrado
Temperatura alta
Produto mais estável
Exemplo: autocondensação da etilmetilcetona
O
O
O
OH
O
Base
O
Ácido
OH
OH
O
Porém:
A escolha das condições
certas é delicada!
Melhor usar uma das...
Técnicas de manipulação das
reatividades em
Condensações Mistas
Reatividade do grupo carbonila:
Construção do esqueleto carbônico
por condensações
Parte II
Técnicas de manipulação das
reatividades em condensações mistas
1. Utilização de um pseudo-ácido com baixa tendência de condensação consigo
mesmo e/ou um aceitador sem α-H.
2. Desativação do pseudo-ácido por formação de uma imina.
3. Ativação do pseudo-ácido pela estabilização da forma enólica (enoléter / enamina).
4. Uso de um pseudo-ácido duplamente ativado (= condensações de Knoevenagel).
5. Com bases muito fortes se consegue desprotonar o pseudo-acido
quantitativamente em uma etapa preliminar.
Nitroalcanos são bastante usados em condensações mistas: só podem ter o papel do
pseudo-ácido.
Técnica 1: usar compostos carbonilados não-enolizáveis
O
R1
R1,2 = H, OEt, Cl, Ar, Bu-t, COOEt
R2
Exemplos:
O
O
H
EtO
O
Cl
EtO
O
OEt
Condensação de Claisen-Schmidt
Cetona + aldeído aromático
O-
O
H3C
C CH2
Ar
H
O
- H2O
C
+
H3C
C
H3 C
C
O
CH2 CH Ar
H
OH
+
H3C
C
CH2 CH Ar
O
CH CH Ar
O
Cetona α,β− insaturada
Estratégia principal para os derivados do ácido cinâmico.
Síntese do ácido cinâmico segundo Perkin
Anidrido + benzaldeído
Base: Acetato
Sem solvente adicional o acetato age como base forte!
(em soluções aquosas, por outro lado, os sais de ácidos carboxílicos são bases
fracas, devido a camada de solvente em volta dos ânions.)
O
C C6H5
-
H3C
C O C CH3
O
O
+ AcO
- AcOH
H3C
C O C CH2
O
H
O
H3C
O
-
C6H5 CH
O
C
O
C
CH2
O
H3C
C
O
H
O
C6H5 CH CH C
O
-
∆
- AcOH
β-Eliminação
C6H5 CH CH COOSal do ácido cinamômico
O
Condensação com o éster do ácido fórmico
O
Ph C CH3
O
+
H C
-
O
+
[ C 2H5O Na ]
Ph
C CH2 CH
OC2H5
Acetofenona
= pseudo-ácido
OOC2H5
Aceitador
O
Ph C CH2 CH O
+
HOC2H5
Condensação com o éster do ácido oxálico
O éster do ácido oxálico, além de não ter um grupo metileno em posição α, é um
aceitador mais forte do que o éster simples. Isto se deve à presença do segundo
grupo acila em posição vizinha = retirador de elétrons. Assim o carbono do grupo
carboxílico fica mais positivado (= mais eletrofílico) ainda. Portanto, ele pode ser
usado em condensações mistas com cetonas ou outros ésteres – o produto sempre
fica definido.
O O
O
H3C
CH2 C
+
C2H5O C C OC2H5
OC2H5
Pseudo-ácido
Aceitador
+ C 2H5O- Na+
- C 2H5OH
O O
H3C
CH C
C OC2H5
COOC2H5
O O
H3C
CH C C OC2H5
COOC2H5
120 °C
- CO
O
H5C2O C
Ao aquecer o produto primário desta síntese
acima de 100 °C acontece uma
descarbonilação
(essa degradação é típica somente para os
compostos 1,2-dicarbonilados).
Produto:
Derivado do ácido malônico 2-substituído
O
CH C OC2H5
CH3
Éster 2-metilmalóico
Esta estratégia serve para produzir β-oxoéster
e ésteres malônicos mono-substituídos - que
não podem ser obtidos de maneira
satisfatória via alquilação do próprio éster
malônico. (Porquê?)
Condensação com o éster do ácido carbônico
Com cetonas para β-oxoésteres, com nitrilas para ésteres do ácido cianoacético.
Atenção: os ésteres do ácido carbônico são cancerígenos!
O
O
O
α + C2H5O
C
δ+
OC2H5
Dietilcarbonato
+ C 2H5O- Na+
- C 2H5OH
H
C
O
OC2H5
Outras condensações mistas com ésteres
Mais sensível às condições reacionais (solvente, temperatura, base),
mas também viável é a maioria das condensações mistas entre ésteres e
cetonas e entre ésteres e nitrilas.
Nestes casos, o éster tem predileção de ser o componente carbonílico:
R3
O
O
3
1
R CH2
R C
C
R1
4
R
C
CH
O
OR2
R4
C
+
R2OH
+
R2OH
O
β -dicetona
R3
O
3
1
R CH2 C N
R C
OR
2
R1
C
O
CH
C
N
β -oxocarbonitril
Restrições:
Rendimentos típicos em todas essas condensações: cerca de 50%.
Porquê?
O produto da condensação é quase sempre um composto
duplamente ativado (= 1,3-dicarbonilado)
⇒ reagem com muita facilidade como pseudo-ácidos.
Consequência: desprotonação, condensação com mais um
componente carbonílico, “supercarbonilação”.
Para reprimir esta reação paralela deve-se usar:
1) pequena quantidade de base (no exemplo acima: etóxido)
2) evitar um excesso do componente carbonílico na mistura
Além disso:
Todos os compostos 1,3-dicarbonilas podem sofrer
“clivagem de ácido”
(= reversa da condensação; ocorre sob catálise básica)
e
“clivagem de cetona”
(= descarboxilação de ácidos carboxílicos β-substituidos),
especialmente durante um tratamento prolongado a temperaturas altas
e sob influência de uma base (que é essencial na condensação de
Claisen).
Caso especial: Formaldeído
• F. é reativo demais
• podem ligar-se mais de um F. (= aceitador) ao componente metilênico
• F. polimeriza
• F. disproporciona aos poucos (Cannizzaro)
Muitas desvantagens, mas existe uma condensação mista
que aproveita da reatividade do formaldeído:
HO
Síntese do pentaeritritol
OH
HO
OH
Síntese de pentaeritritol
Acetaldeído + formaldeído + base
O
H3C
[ Base ]
+ H2C O
C
HO
CH2
O
CH2 C
H
Pseudo-ácido
+ B- HB
HO
CH2
O
CH C
H
H
O
CH2OH
Aceitador
(excesso)
H2C O
H2C O
Base
(HO CH2)3C
C
H
- HCOOH
Redox
HOCH2
C
CH2OH
CH2OH
Pentaeritrita
Existe um N-derivado do F. ainda mais reativo!
Aminometilação de Mannich
O
OH
+
R C CH3
H
δ−
R C CH2
O H
CH3
R C CH CH2 N
H3C
NH
H3C
+ H2C O
+
+ H
- H2O
Ciclo catalítico
H3C
δ+
N CH2
H3C
"Imônio"
CH3
Base de Mannich
β -Eliminação
- (CH3)2NH
∆
+ Base
O
R C CH CH2
Além dos pseudo-ácidos mencionados podem também ser usados
compostos aromáticos que são ativados no sentido substituição
eletrofílica. Isto podem ser fenóis ou hompostos heterocíclicos. Um
exemplo seja a síntese da gramina, por aminoalquilação de indol:
CH2 N(CH3)2
+ HCHO + HN(CH3)2
N
Indol
H
- H2O
N
H
Gramina
Todas as etapas reacionais ocorrem sob condições extremamente
brandas.
Algumas condensações de Mannich funcionam sob condições “in vivo”!
• A base de Mannich pode ser isolada e armazenada, especialmente
em forma do seu hidrocloreto.
• Quando for preciso, a base de Mannich pode ser degradada formando
cetona α,β-insaturada com grupo metileno final que é
• muito reativa e instável; difícil preparar por outro método (Wittig)
(= eletrófilo em uma adição de Michael ou dienófilo em ciclizações
de Diels-Alder,...)
• A degradação é bastante facilitada pela quaternização do N da base
de Mannich. Assim sai uma amina terciária.
(= variação da eliminação de Cope).
O
NR2
O MeNR2
CH2
CH2
H
MeI
Quaternização
H
O
CH2
- MeNR2
Grupo metileno
exocíclico
Técnica 2: Desativação do componente metilênico por aminas primárias
(Wittig 1964)
Aldeído + amina primária + base forte + cetona
A transformação do aldeído em uma base de Schiff reduz drasticamente a sua
capacidade como componente carbonílico. Esta função agora pode ser preenchida
por uma cetona que em si não é tão eletrofílica.
Etapa 1: desprotonar a base de Schiff = ativar o componente metilênico.
Etapa 2: adição do eletrófilo (que pode ser fraco).
H3C
CHO
+
H2N
1) (C6H5)2CO
2) H2O
- LiOH
H3C
C6H5
C6H5
C
OH
CH2 CH N
+ LDA
CH N
- LDAH+
+ H+ / H2O
- C6H11 NH2
- H2O
(C6H5)2C
H2C
CH N
CH CHO
Técnica 3: Estabilização da forma enólica / enolato
Princípio:
Estabilizar o enol = fortelecer o papel metilênico do composto
Enolálcool = instável ⇒ Transformação do componente nucleofílico
em enamina ou (silil)-enoléter
Papel da amina secundária / do cloreto de silila: Ativadores!
O
Nucleófilo ruim!
Enamina
NR2
Amina sec.
O
Me3SiCl
SiMe3
Silil-enoléter
Exemplo 1:
Componente metilênico: cetona;
componente carbonílico: aldeído.
O
O
N
N
O
O
N
H
CHO
H+
Morfolina
= amina sec.
Hidrólise
O
Exemplo 2:
Silil-enoléteres reagem com alta regiosseletividade e sob condições
brandas, na presença de ácidos de Lewis (neste exemplo: TiCl4).
O
δ+
O
C6H5 CH2 C
H
+ δ−
Si(CH3)3
+ TiCl4
- (CH3)3SiCl
O
C6H5 CH2 CH
TiCl3
O
H2O
OH
C6H5 CH2 CH
68%
(Segundo efeito do grupo trimetilsilil: hidrofobização.)
O
Técnica 4: Pseudo-ácidos com grupo metileno
duplamente ativado (Condensação de Knoevenagel)
retirador 1
H2C
retirador 2
Dois vizinhos retiradores de elétrons
⇒ elevada acidez C-H, pois a carga
negativa da base conjugada pode ser
distribuída, através de mesomeria, em
cima dos dois vizinhos.
Três efeitos contribuem à reatividade elevada deste grupo metileno:
1) O grupo –CH2 – torna-se muito mais ácido:
pKa(carbonila simples) ≈ pKa(1,3-dicarbonila) - 10.
2) A troca entre a forma ceto e enólica é acelerada.
3) Mais estabilidade termodinâmica do enol,
então mais enol no equilíbrio.
Ponto 1 e 2: Acidez C-H e rapidez da enolização
R3C
H
k1
k -1
R3C
+ H
k1
Ka =
k -1
+
Composto duplamente ativado
pKa
k1 (s-1)
4
8,3 ⋅ 10-1
H2C(NO2)2
Dinitrometano
H2C(COCH3)2
Acetilacetona
8,8
1,7 ⋅ 10-2
H3C-NO2
Nitrometano
10,2
4,3 ⋅ 10-8
10,7
1,2 ⋅ 10-3
12
1,5 ⋅ 10-2
13,3
2,5 ⋅ 10-5
20
4,7 ⋅ 10-10
H3CCO-CH2-COOC2H5 Acetoacetato de etila
H2C(CN)2
Dinitrila do ácido malóico
H2C(COOC2H5)2
Dietilmaloato
Em comparação:
H3C-CO-CH3
Acetona
Todos esses compostos (menos a acetona) podem ser desprotonados, quase
quantitativamente, por NaOH. (pKa da água (ácido do OH-) ≅ 15).
Possíveis retiradores ao lado do grupo –CH2 – :
carbonila
carboxila (ácido, éster, amida)
ciano
nitro
também apóiam o carbânion: sistemas aromáticos
3a Explicação da alta reatividade como pseudo-ácido:
A forma enólica é estabilizada, podendo até prevalecer no equilíbrio com a forma ceto.
H
Isso se deve à ponte de hidrogênio intramolecular:
O
O
O
O
C
C
C
C
CH
Forma enólica do
composto dicarbonila
CH2
Composto
% enol (na fase líquida,
ausência de solventes)
H3C-CO-CH3
Acetona
1,5 ⋅ 10-4
H2C(COOC2H5)2
Dietilmalonato
7,7 ⋅ 10-3
NC-CH2-COOC2H5
Cianoacetato de etila
2,5 ⋅ 10-1
C6H10O
Ciclohexanona
1,2
H3CCO-CH2-COOC2H5 Acetoacetato de etila
8,0
H3CCO-CH(C6H5)-COOC2H5
30,0
H2C(COCH3)2
76,4
Acetilacetona
C6H5CO-CH2-COCH3 Fenilacetilacetona
89,2
O teor da forma enólica depende da temperatura e sensivelmente do
solvente. Observa-se a estabilização da forma enólica por solventes
apolares. (O efeito de desaceleração por estes solventes é desprezível)
Acetilacetona:
Solvente
% enol
H2O
15
CH3CN
58
sem solvente, em fase líquida
80
C6H14
92
sem solvente, em fase gasosa
92
Os seguintes compostos têm relevância na síntese:
N C CH2 C N
C6H5 CH2 C N
O
C2H5 O C CH2 C N
O
O
C 2H 5 O C
O
Dinitrila do ácido malônico
Nitriloacetato de etila
Dietilmaloato
CH2 C OC2H5 Cianeto de benzila
O
H 3C
C CH2 C CH3
O
O
H 3C
C CH2 C OC2H5 Acetoacetato de etila
O
O
(RO)2P
CH2 C OR
Acetilacetona
Éster do ácido fosfônico
O último composto tem importância na síntese de olefinos a partir de compostos
carbonila, segundo Horner e Emmons, variação da reação de Wittig.
Estes compostos usados em condensações, sempre representam o
componente pseudo-ácido.
Sempre ocorre uma dupla-condensação com o componente carbonílico,
seguindo o esquema:
retirador 1
C O
+
H2C
retirador 2
[Cat]
- H2O
retirador 1
C C
retirador 2
Em comparação:
Condensação aldólica verso condensação de Knoevenagel
1) A condensação de Knoevenagel é uma condensação mista, portanto o espectro de
produtos acessíveis é muito mais amplo.
2) A escolha do catalisador é mais sútil: enquanto na condensação aldólica qualquer
ácido ou base de Brønsted serve, a reação de Knoevenagel usa catalisadores brandas
e específicas, tais como acetato de amônio, β-alanina, piridina ou piperidina *.
* G. Jones, Org.Reactions 15 (1967) 204
Exemplo 1:
Condensação com éster malônico
Comp. metilênico: X = Y =
O
C
Comp. carbonílico: H5C2
CHO
OC2H5
COOC2H5
H5C2 CH C
COOC2H5
[ H+ ]
COOH
H5C2 CH C
COOH
∆
- CO2
H5C2 CH CH COOH
Shortcut!
Usar diretamente o ácido malônico, em vez do seu éster. A descarboxilação ocorre
automaticamente.
Catalisador: HOAc / NaOAc = 1 : 1; pouco DMSO ajuda solubilizar o sal
Não pode ser ácido forte nem base forte, mas o mais suave possível,
para promover a reação mais rápida (controle cinético)
Solvente: benzeno ⇒ remoção azeotrópica da água liberada. Dean Stark
Estratégia de síntese:
Um grupo éster (ácido carboxílico) somente tem o papel de ativador (= oposto de
protetor), para reforçar o papel do componente metilênico.
Exemplo 2:
Condensação com acetoacetato de etila
O
O
X =
Y =
C
CH3
OC2H5
COOC2H5
H3C
CH C
C
[ H+ ]
COOH
H3C
CH C
C CH3
C CH3
O
O
∆
- CO2
O
H3C
CH CH C CH3
Cetonas α,β− insaturadas
Exemplo 3:
Alvos 1,3-dicarbonilas, via acilação do éster malônico ou derivados
Base: Mg(OH)2 : Mg2+ complexa e bloquéia os centros duros (= oxigênios)!
Nu- duro
E+ duro
O-
O
R COCl
OEt
O
Na+ O-
O
R
COCl
R
O
Nu- macio
O
OEt
OEt
OH
O
Mg
O
O
R
OEt
O
O
COCl
OEt
Hidrólise
Descarboxilação
R
O
R
O
Técnica 5: Desprotonação quantitativa do pseudo-ácido
A desprotonação completa e rápida de um composto carbonilado impede sua
atividade como eletrófilo (= componente carbonílico)!
Na maioria dos casos: nucleófilo = composto com grupo metileno duplo-ativado
(discutidos no último item) a ser desprotonado com bases comuns (alcóxidos).
Em outros casos: base bastante forte (NaH ou Ph3C- Na+)
Formação quantitativa do enolato numa etapa prévia (controle mediante indicador!)
Depois acrescentar o componente carbonílico, aos poucos.
Aplicar os participantes, pseudo-ácido : base : eletrófilo = 1 : 1 : 1.
Rendimentos mais altos do que as condensações mistas “comuns”.
Atenção!
Falta de base ⇒ condensação do composto 1 entre si mesmo.
Isto é, uma parte funciona como componente metilênico, outra parte como componente
carbonílico.
Excesso de base ⇒ condensação do composto 2 entre si mesmo, pela mesma razão.
Condensação de Stobbe
Éster succínico + aldeído / cetona + base forte
COOEt
CH2
O
COOEt
-
+
(CH3)3CO K
R2C O
CH
CH2
CH2
COOEt
Base
EtO C
+
H / H2O
C
CR2
1)
+
H / H2O
CH2
COO-
O
CR2
CH2
2)
O
C
OEt
COOH
C
CR2
O-
H2C
1)
COOEt
H
CH CR2
COOEt
Enolato
quantitativo
COOEt
COOH
O
Lactona
R2 C
CH CH2 COOH
Ácidos β,γ− insaturados
∆
- CO2
2)
COOH
R2 C
C
CH3
Síntese do éster glicídico, segundo Darzens
Cloracetato + aldeído + alcóxido (base)
O
R C
-
Cl
+ CH3O
CH2 COOCH3
- CH3OH
Cl
CH COOCH3
H
C
H2O / OH-
CH COOCH3
C CH COOCH3
O-
R
H
O
Cl
R
H
R
- Cl-
H
H+
CH COO-
C
O
Éster glicídico
R
H
C CH
O
C O
H O
∆
- CO2
R
H
C
C
H
OH
O
R CH2 C
H
Enol
Resultado: prolongação da cadeia carbônica do aldeído por um grupo metileno.
Síntese de Reformatzky
Bromoacetato de alquila + composto carbonila + zinco
Br
CH2 COOCH3
+
Zn
[ Br Zn
CH2 COOCH3 ]
ZnBr + CH2 COOCH3
quantitativo!
Inversão da polarização no carbono α
O-
O
R C
H
+ CH2 COOCH3
R C CH2 COOCH3
H
[ H3O+ ]
OH
R C CH2 COOH
H
- H2O
R CH CH COOH
Outras sínteses que aproveitam deste efeito:
quase todas as reações organo-metálicas – especialmente aquelas com metais
muito eletropositivas (preparo do reagente de Grignard: R-X + Mg → R-MgX).
FIM !!!!
Leia mais, no capítulo 6: Condensações, do
livro "Princípios da Síntese Orgânica"