qualidade
Ferramentas para avaliação da
qualidade das matérias-primas
Parte 1
A
aplicação
de técnicas em
várias etapas do
desenvolvimento
de um produto
permite uma melhoria
na padronização
e na qualidade
dos produtos e
dos processos de
produção
Jamile Barbosa, Bruno G.
Pereira e Sílvia L. Fialho
Introdução
C o n t r o l e d e C o n t a m i n a ç ã o 11 8
A indústria farmacêutica utiliza a
caracterização das matérias-primas
para a sua especificação e também
na etapa de pré-formulação de um
medicamento. Ambos os processos
se cruzam na medida em que certas
análises não descritas na monografia
farmacopéica podem ser definidas
durante a pré-formulação como forma de garantir as características adequadas ao produto e ao processo.
No estudo de pré-formulação são
definidas as características físicoquímicas necessárias à matéria-prima
do princípio ativo e aos excipientes,
complementando os ensaios descritos
na monografia farmacopéica. Ela é
parte integrante do processo de desenvolvimento de uma formulação
e seu objetivo consiste em fornecer
informações no sentido de serem elaboradas formulações robustas para
que o produto tenha uma performan30
Fevereiro 2009
ce adequada tanto no processo produtivo, quanto na sua estabilidade e
eficácia terapêutica. Para isso, alguns
parâmetros são comumente analisados na etapa de pré-formulação: solubilidade, estabilidade, coeficiente
de partição, constante de ionização,
densidade e propriedades do estado
sólido tais como a forma do cristal,
polimorfismo, área superficial, tamanho e forma da partícula, adsorção de
água, entre outros (GIRON, 2003).
Alguns desses ensaios já se encontram descritos na farmacopéia americana (United States Pharmacopeia
- USP 31), em seu Capítulo Geral e
tem sido cada vez mais utilizados.
Dentre eles, destacam-se as seguintes técnicas: determinação de tamanho de partícula por difração a laser,
microscopia óptica, área superficial
específica, análises térmicas, difração de raio-X, infravermelho médio
e próximo, espectroscopia Raman,
dissolução intrínseca e densidade
compactada e aparente. A tabela 1
é um resumo dessas principais técnicas e suas aplicações. Além disso,
serão apresentadas nesse artigo algumas dessas técnicas com um pouco mais de detalhes.
Um parâmetro de grande impacto no
produto de uso oral é a solubilidade do
princípio ativo pois, juntamente com a
sua característica de permeabilidade,
será decisivo para a sua absorção no
trato gastroinstestinal. Nesse sentido,
Amidon e colaboradores (1995) propuseram a classificação dos fármacos
em função de sua solubilidade e permeabilidade gastrointestinal, que se
tornou conhecida como o Sistema de
Classificação Biofarmacêutico (SCB),
o qual foi reconhecido pela agência regulatória americana (Food and Drug
Association – FDA). De acordo com
essa classificação, fármacos pouco solúveis apresentam a solubilização do
ativo como uma etapa limitante na absorção. Para esse tipo de fármaco, características como o tamanho da partícula e a estrutura cristalina assumem
grande importância. Assim, atenção
especial deve ser despendida ao desenvolvimento da pré-formulação e de
métodos de dissolução para esses fármacos (BROWN et al., 2004a).
A especificação de uma matériaprima busca a manutenção das suas
características críticas, o que impacta
na qualidade do produto e na eficiência dos processos produtivos que
foram estabelecidos nas etapas de
desenvolvimento. Elas são descritas
detalhadamente nas monografias farmacopéicas e precisam ser revisadas
periodicamente para que sejam atualizadas conforme as edições mais recentes dos compêndios oficiais, sejam
eles nacionais ou internacionais. Além
das revisões de cunho farmacopéico,
é importante também a realização de
estudos periódicos, pela avaliação do
comportamento das matérias-primas
durante o processo produtivo e da
qualidade do produto final, frente às
variações nas características dos diferentes lotes de matérias-primas. Essa
etapa é importante porque torna-se
possível mostrar pontos que podem
não ter sido contemplados durante os
estudos de pré-formulação e que serão
constatados à medida que se tem um
histórico maior de produção.
qualidade
Tabela 1 - Principais
Técnica
técnicas de caracterização de matérias - primas e suas aplicações
Símbolo
Faixa
de
Fundamento
Aplicação
trabalho
DIDR
Determinação
de tamanho de
partícula por
difração a laser
---
Microscopia óptica
MO
Calorimetria
exploratória
diferencial
DSC
Análise térmica dife- DTA
rencial
Termogravimetria
TG
Infravermelho
próximo
NIR
~ 250mg da
matéria-prima
por pastilha
0,1mm a 3mm
Avaliação de cristalinidade
(polimorfismo), solubilidade,
determinação do meio de dissolução.
Determinação e manutenção das
características do produto (p.ex.
aspecto, dureza, uniformidade de
mistura, friabilidade, aderência aos
punções, perfil de dissolução).
>1mm
Baseia-se na visualização de partículas Estudo da morfologia das partículas,
através de lentes que proporcionam
polimorfismo, determinação
diferentes aumentos do material,
de distribuição de tamanho de
utilizando-se para isso de uma fonte de partícula, outros.
luz e um condensador.
-180ºC a 725ºC Variação do fluxo de calor entre a
Avaliação de interações sólido-sólido,
amostra e a substância de referência. pureza e identidade de substâncias,
estudos de polimorfismo, hidratação
de moléculas, entre outros.
-180ºC a 1600ºC Variação de temperatura entre a
Semelhante à DSC.
amostra e a substância de referência.
Temperatura
Variações de massa ocorridas na
Estudos de estabilidade térmica;
ambiente a
amostra.
perfil de decomposição; composição
1600ºC.
qualitativa e quantitativa das
amostras.
Identificação de compostos
750 a 2500 nm. A luz infravermelha próxima, ao
orgânicos, distribuição de tamanho
incidir sobre a amostra, promove
excitações moleculares de sobretons e de partícula, medição quantitativa
combinações de vibrações, as quais são de grupos funcionais orgânicos
muito mais fracas do que as ocorridas
no IV médio.
Um aspecto importante nos estudos de pré-formulação e na definição
da especificação das matérias-primas
sólidas é o polimorfismo, uma vez
que os polimorfos podem apresentar características físicas e químicas
diferentes. Essas variações podem
ser benéficas quando previamente
planejadas ao se escolher determinada forma de acordo com sua característica, mas também podem gerar
grandes transtornos se ocorrerem
inadvertidamente. Portanto, é necessário conhecer as possíveis formas,
como e quanto diferem entre si e se
as mesmas podem alterar a qualidade
dos medicamentos. Vários são os fármacos que apresentam polimorfismo,
entre eles podemos citar como exemplos a carbamazepina, o mebendazol,
a glibenclamida, o fenobarbital e a espironolactona (BRITTAIN, 1999).
A presença de um polimorfo ina-
Velocidade de dissolução da matériaprima sob condição de área superficial
constante.
Difração ocorrida com um feixe de laser
quando incidido sobre as partículas.
dequado pode comprometer a qualidade do medicamento, já que ele
pode apresentar solubilidade, estabilidade, forma e dureza do cristal e
temperatura de fusão diferente. Desta forma, as conseqüências do polimorfismo são encontradas em todas
as etapas da produção e estocagem
das matérias-primas e dos produtos
(GIRON, 2003).
Técnicas de análise
matérias - primas
de
Dissolução Intrínseca
A dissolução intrínseca é uma técnica que tem sido muito empregada
nos estudos de pré-formulação para
a caracterização de fármacos sólidos.
Ela é definida como a velocidade de
dissolução da substância pura em forma de pastilhas, em que a área superficial é constante. É executada em dis-
solutores tradicionais equipados com
uma aparelhagem de agitação especial
(Aparelhagem de Wood), que permite
a avaliação das características associadas à matéria-prima (YU et al, 2004).
A dissolução intrínseca assim como
a permeabilidade são fenômenos dinâmicos, enquanto a solubilidade é
um fenômeno de equilíbrio. Portanto,
acredita-se que este parâmetro deve
estar mais bem correlacionado com a
dissolução in vivo que a solubilidade.
A partir disso, YU e colaboradores
(2004), fazendo uma correlação entre
os resultados encontrados nos testes
de dissolução intrínseca de 15 fármacos com aqueles já descritos conforme
o SCB, sugeriram o uso da dissolução
intrínseca como forma de estimar a
solubilidade de fármacos.
Alguns exemplos de aplicação da
técnica de dissolução intrínseca incluem a determinação da velocidade
Fevereiro 2009
C o n t r o l e d e C o n t a m i n a ç ã o 11 8
Dissolução
intrínseca
31
qualidade
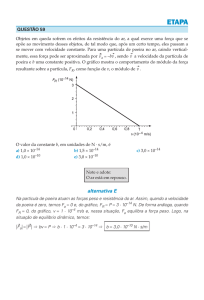
Figura 1 - Perfil de dissolução de pilotos de Glibenclamida
5mg, produzidos com diferentes lotes da matéria- prima (GLB 1 e
GLB 2). Condições de análise: meio de dissolução tampão fosfato pH 6,8 com surfactante 0,5%, 500 m L, aparelho 2, velocidade
de agitação 75rpm
100
Cedência %
80
60
Pi 1
Pi 2
40
20
0
0
10
20
30
40
50
Tempo de dissolução (min.)
60
70
Figura 2 - Perfil de distribuição de tamanho de partícula (µ m) da
matéria- prima glibenclamida , lotes GLB 1 (−) e GLB 2 (−). Para
GLB 1: d0,1=1,871; d0,5=7,732; d0,9 =17,13 e para GLB 2: d0,1=1,540;
d 0,5 =7,223; d 0,9 =27,341
C o n t r o l e d e C o n t a m i n a ç ã o 11 8
Volume %
Distribuição de tamanho de partícula
9,5
9
8,5
8
7,5
7
6,5
6
5,5
5
4,5
4
3,5
3
2,5
2
1,5
1
0,5
0
0,01
0,1
1
10
100
Tamanho de partícula (µm)
de dissolução de acordo com o pH, a
investigação de fenômenos de transferência de massa durante a dissolução,
o estudo dos efeitos de surfactantes e
do pH na solubilização de fármacos
pouco solúveis e o entendimento da relação entre a velocidade de dissolução
e a forma cristalina (YU et al, 2004).
32
Fevereiro 2009
1000 3000
O teste de dissolução intrínseca revela-se muito útil no desenvolvimento
da pré-formulação e da especificação
de um fármaco pouco solúvel (classes
II ou IV do SCB). Durante a realização dos estudos, diferentes lotes da
matéria-prima podem ser testados e
os resultados correlacionados com as
velocidades de dissolução. A maior
velocidade de dissolução intrínseca
muitas vezes é desejável para formas
farmacêuticas de liberação imediata.
Assim, as matérias-primas com resultados de dissolução intrínseca adequados devem ser selecionadas.
A dissolução intrínseca pode ser
utilizada nos testes de rotina de controle de qualidade, no entanto, por se
tratar de um teste geralmente demorado, outras técnicas podem ser preferidas. Para isso é importante buscar
correlações entre os resultados da
dissolução intrínseca e os resultados
das outras técnicas cuja aplicação
em rotina sejam mais facilmente implantadas (p.ex. microscopia óptica,
calorimetria exploratória diferencial,
infravermelho médio).
Determinação de Tamanho de
Partícula por Difração a Laser
Segundo a USP 31, a difração a laser
é uma das técnicas atualmente mais
usadas para a determinação do tamanho de partículas. O método é muito
rápido e fácil de ser executado, podendo ser adaptado para analisar amostras
presentes em diversas formas físicas.
A técnica se baseia no fenômeno de
difração ocorrido com um feixe de laser que é incidido sobre as partículas.
Como o padrão de difração é característico do tamanho de partícula, uma
análise matemática pode fornecer
com exatidão e repetibilidade o perfil
da distribuição de tamanho das partículas de determinada matéria-prima.
Os equipamentos atuais trabalham
com faixas que variam de 0,1µm a
3mm e os modelos ópticos para tratamento do sinal são baseados na teoria
de Mie em conjunto com a aproximação de Fraunhofer (USP 31). Alguns
equipamentos apresentam condições
diferenciadas que permitem análises
em faixas mais amplas, por exemplo,
de 0,02µm a 2mm.
Os equipamentos disponíveis para
a realização dos testes trabalham tanto com a matéria-prima na forma de
pó (“módulo seco”) quanto com ela
qualidade
em suspensão (“módulo úmido”) e o
melhor método a ser empregado deve
ser definido durante o desenvolvimento de cada análise, de acordo com as
características de cada uma. A distribuição de tamanho das partículas de
uma determinada matéria-prima é
apresentada pelo software na forma
de um gráfico e ainda pelos valores de
percentil (p. ex.: d0,1, d0,5 e d0,9). Esses
valores indicam a população de partículas que se encontra abaixo de determinado tamanho, por exemplo: d0,9
= 100µm indica que 90% do volume
total de partículas analisadas se apresentam com um tamanho igual ou inferior a 100µm. Da mesma forma d0,1,
d0,5 devem ser interpretados (USP 31).
A medida do tamanho de partícula
é um importante aspecto na caracterização da matéria-prima e de formulações, encontrando aplicabilidade
principalmente para apresentações
sólidas. Na indústria farmacêutica a
determinação de tamanho de partículas assume grande importância devido
a sua influência em várias etapas, desde a produção de um medicamento até
aos estudos de bioequivalência.
Assim temos que distribuições estreitas, ou seja, com pequena faixa
de tamanho de partícula minimizam
problemas de segregação que podem
ocorrer durante os processos de mistura das formulações. Além disso, o
tamanho da partícula pode influenciar na dureza de um comprimido,
fato de relevância principalmente
para os excipientes. Podemos citar
também a sua contribuição para a
obtenção de perfis de dissolução
adequados e, neste caso, tem-se o
exemplo da sua influência em formulações contendo o fármaco Glibenclamida (classe II do SCB), onde
a definição do tamanho de partícula
é essencial para que o produto consiga bons resultados de dissolução
(LACHMAN, LIEBERMAN, KANIG, 1986).
Para se avaliar o efeito da distribuição de tamanho de partícula no perfil
de dissolução de uma formulação contendo glibenclamida foram feitos dois
pilotos (Pi1 e Pi2) de Glibenclamida
5mg. Em cada piloto, Pi1 e Pi2, foram usados lotes diferentes do fármaco, GLB1 e GLB2, respectivamente.
Pode-se observar na Figura 1 que Pi1
apresenta maior cedência do fármaco
que Pi2. Avaliando-se a distribuição
de tamanho de partícula dos dois lotes de GLB (Figura 2), verifica-se que
GLB1 apresenta menor valor de d0,9
em relação a GLB2 e ambas apresentam os outros parâmetros (d0,1 e d0,5)
bem semelhantes. Considerando-se os
perfis de dissolução e a distribuição
de tamanho de partícula dos lotes de
GLB analisados, pode-se perceber
que o piloto (Pi1) produzido com o
menor tamanho de partícula apresen-
qualidade
Figura 3 - Microscopia óptica com luz polarizada da matériaprima A mido de M ilho dispersa em óleo, evidenciando o
fenômeno da cruz negra , aumento 200X
tou a maior cedência do fármaco e,
portanto, o valor de d0,9 de GLB1 é
mais adequado que o de GLB2.
Microscopia Óptica
C o n t r o l e d e C o n t a m i n a ç ã o 11 8
Como já mencionado anteriormente, as propriedades cristalinas
podem influenciar na velocidade de
dissolução de um fármaco, impactando em sua biodisponibilidade.
Já do ponto de vista tecnológico, o
hábito cristalino pode influenciar
na compressibilidade e nas propriedades de fluidez da matéria-prima
(FLORENCE, ATTWOOD, 2003).
Por hábito cristalino entendem-se
as diferentes formas que um cristal
pode apresentar, tais como as formas
aciculares, prismáticas, piramidais,
tabulares, colunares e lamelares. Assim, um cristal hexagonal pode apresentar, por exemplo, os seguintes
hábitos cristalinos: tabular, prismático ou acicular; já um cristal ortorrômbico pode apresentar os hábitos
tabular, prismático ou cúbico (FLORENCE, ATTWOOD, 2003).
Em se tratando da forma do cristal, as partículas esféricas são consideradas ideais para os processos de
mistura de pós secos, enquanto que
as formas aciculares dificultam esse
processo. A maioria dos compostos
34
Fevereiro 2009
farmacêuticos se encontra entre esses
dois extremos, sendo então importante, do ponto de vista farmacotécnico, uma avaliação microscópica
da forma da partícula nos estudos de
pré-formulação (AHMED, NAINI,
WADGAONKAR, 2005).
Além dos fatores já citados, a microscopia óptica apresenta também
aplicabilidade em estudos de polimorfismo. Entretanto, esta técnica
não é a mais empregada nesses casos,
dando-se preferência para aquelas que
apresentam resultados mais precisos,
como a difração de raio-X ou mesmo a
DSC. A pesquisa de polimorfos usando a microscopia é possível na medida
em que eles apresentam diferentes arranjos e/ou conformações das moléculas na estrutura do cristal, resultando
em hábitos cristalinos diferentes os
quais apresentam estruturas internas
diferentes. Essas diferenças na forma
do cristal podem, em muitos casos,
serem identificadas em análises de
microscopia. (LACHMAN, LIEBERMAN, KANIG, 1986). Pode-se ainda
utilizar um polarizador acoplado ao
microscópio óptico a fim de avaliar
a birrefringência e sua relação com a
estrutura cristalina do polimorfo. Por
outro lado, quando a matéria-prima
passa por processo de micronização
torna-se impossível avaliar o hábito
cristalino e sua aplicação na pesquisa
de polimorfos.
Uma outra aplicabilidade da microscopia óptica é a determinação da
distribuição de tamanho de partícula,
que pode ser feita manualmente ou de
forma automatizada. A primeira é realizada com o auxílio de um software
específico para fazer as medições, mas
dificilmente proporciona uma amostragem muito representativa, é demorada
e apresenta baixa resolução. Já a forma
automatizada conta com microscópios
que dispõem de acessórios para a realização desse tipo de análise, onde, ao invés de uma lâmina comum, é utilizada
uma cela bem maior, na qual é possível
a análise de até cerca de 1 milhão de
partículas. Como o processo é automatizado, ele proporciona resultados em
intervalos de tempo bem menores que
da forma manual. Entretanto, ainda
assim trabalha com uma amostragem
bem menor que a utilizada, por exemplo, na técnica de difração a laser.
É possível a introdução de análises
microscópicas na rotina dos laboratórios de controle de qualidade, podendo
ser empregada inclusive para a identificação das matérias-primas. O amido,
por exemplo, apresenta o chamado fenômeno da cruz negra, o qual fica evidenciado na microscopia com luz polarizada, mostrando em cada partícula
a formação de uma cruz negra em um
fundo azulado (Figura 3). Tal fenômeno se extingue quando o amido passa
pelo processo de pré-gelatinização.
Na próxima edição da revista Controle de Contaminação, a segunda e
última parte deste artigo falará sobre
outras duas ferramentas para análise
de matérias-primas: as análises térmicas e a técnica de espectroscopia
no infravermelho próximo.
Jamile Barbosa
Bruno G. Pereira
Sílvia L. Fialho
Divisão de Desenvolvimento
Farmacotécnico e Biotecnológico,
Fundação Ezequiel Dias/FUNED
[email protected]