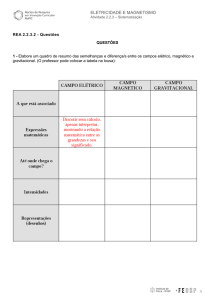
Princípio do Teste
P
Anti-HBs
Código: 60453002 Versão: 453/P7
O teste ImmunoComb® II Anti-HBs é um ensaio imunoenzimático
(EIA) em fase sólida, baseado no princípio de duplo
reconhecimento. A fase sólida é um pente com doze projeções
(“dentes”).
Cada dente é sensibilizado em duas posições:
Ponto superior – soro albumina bovina biotinilada (Controle
Interno).
Ponto inferior – HbsAg recombinante.
A Placa Reveladora tem 6 fileiras (A-F) de 12 cavidades, cada
fileira contendo reagentes prontos para uso em diferentes etapas
do ensaio. O teste é realizado por etapas, movendo-se o Pente de
fileira a fileira com incubação em cada etapa.
Para iniciar o teste, amostras de soro ou plasma são adicionadas
ao diluente nas cavidades da fileira A da Placa Reveladora. O
Pente é então colocado nas cavidades da fileira A. Os anticorpos
anti-HBs, se presentes na amostra, irão ligar-se ao HbsAg no
ponto inferior dos dentes do Pente (figura 1). Os componentes
não ligados são lavados na fileira B. Na fileira C, os anticorpos
anti-HBs capturados nos pontos Inferiores dos dentes reagirão
com o HbsAg biotinilado. Na fileira D, o complexo antígeno
biotinilado / anticorpo nos pontos inferiores dos dentes, e a soro
albumina bovina biotinilada nos pontos superiores (Controle
Interno), reagirão com estreptavidina marcada com fosfatase
alcalina (FA). Na fileira E, componentes não ligados serão
removidos por lavagem. Na fileira F, a fosfatase alcalina ligada irá
reagir com o substrato cromogênico. Os resultados são visíveis
como pontos cinza azulados na superfície dos dentes do Pente.
Formato: 3 x 12 testes
O kit ImmunoComb® II Anti-HBs é um teste para a detecção
quantitativa de anticorpos para o antígeno de superfície do vírus
da hepatite B (HbsAg) em soro ou plasma humano. Podem ser
realizados trinta e seis testes com um kit.
Introdução
O vírus da hepatite B (HBV) pertence a uma nova família de vírus
de DNA, chamada Hepadnaviridae. Ele apresenta um
hepatotropismo evidente e um único meio de replicação através
do mecanismo de transcrição reversa. O viríon completo ou
partícula de Dane, consiste em uma molécula de DNA circular
protegida por um capsídeo nuclear / antígeno de core (HBcAg), e
envolvido por uma lipoproteína de envelope, que é o antígeno de
superfície (HBsAg). O HBsAg também é encontrado no soro
como partículas ou filamentos esféricos, incompletos e não
infecciosos. Um pequeno componente do nucleocapsídeo do
HBV, o antígeno HBe (HBeAg), também é detectável no sangue
durante a fase replicativa do vírus.
O vírus da hepatite B é um vírus amplamente presente, com
distribuição global.
As principais vias de transmissão do vírus são: horizontal, através
de contaminação sexual ou parenteral; e vertical, com a
transmissão pré-natal da mãe infectada para o feto.
As conseqüências clínicas da infecção por HBV variam de
totalmente imperceptíveis (70% dos casos) a hepatite aguda com
icterícia. A maioria dos pacientes se recupera totalmente dentro
de seis meses após o início da doença. Uma pequena proporção
da população infectada (< 1,5%) pode desenvolver hepatite
fulminante, freqüentemente com resultado fatal. Em uma
proporção substancial (até 10%) dos pacientes adultos, o HBV
pode persistir, progredindo eventualmente para hepatite crônica
com desenvolvimento de cirrose e hepatocarcinoma.
Os portadores de hepatite B crônica (200 milhões ao redor do
mundo) formam o principal reservatório do vírus e contribuem
para a disseminação da doença.
Os anticorpos para HbsAg (anti-HBs) são os principais anticorpos
para neutralizar o HBV, que geralmente persistem pela vida
inteira e protegem contra reinfecção. O nível de anti-HBs,
entretanto, serve como indicador para avaliar a recuperação da
infecção por HBV, ou o sucesso da vacinação usando partículas
de HbsAg. Concentrações de anticorpos ≥ 10 UI/L indicam
imunidade ao HBV.
453/P7
Figura 1. Princípio do Teste
O kit inclui um Controle Positivo (anti-HBs) e um Controle
Negativo, para serem incluídos em cada ensaio. Ao término do
teste, o dente usado com o Controle Positivo deve mostrar 2
pontos cinza azulados. O dente utilizado com o Controle Negativo
deve mostrar o ponto superior e nenhum ponto inferior ou um
ponto bem claro. O ponto superior deve também aparecer em
todos os outros dentes, para confirmar se o kit está funcionando
adequadamente e se o teste foi realizado corretamente.
Materiais Fornecidos
Pentes
O kit contém 3 Pentes de plástico. Cada Pente tem 12 dentes, um
dente para cada teste (Figura 2).
Cada dente está sensibilizado com duas áreas reativas:
Ponto superior – soro albumina bovina biotinilada (Controle
Interno).
Ponto inferior – HbsAg recombinante.
Figura 2. Pente
Os pentes são fornecidos em embalagens de alumínio, contendo
dessecante.
1
Placas Reveladoras
O kit contém 3 Placas Reveladoras, cobertas por folhas de
alumínio.
Cada Placa Reveladora (Figura 3) contém todos os reagentes
necessários para o teste. A Placa Reveladora consiste de 6
fileiras (A-F) de 12 cavidades cada.
O conteúdo de cada fileira é:
Fileira A
Fileira B
Fileira C
Fileira D
Fileira E
Fileira F
Diluente de amostra
Solução de lavagem
HbsAg biotinilado
Estreptavidina marcada com fosfatase alcalina
Solução de lavagem
Solução substrato cromogênico contendo 5-bromo-4cloro-3-indolil fosfato (BCIP) e azul de nitrotetrazolium
(NBT)
Figura 3. Placa Reveladora
Controle Positivo – 1 frasco (tampa vermelha) de 1,5 mL de
plasma humano inativado pelo calor, diluído para um nível de
cutoff de 10 UI/mL para anti-HBs.
Controle Negativo – 1 frasco (tampa verde) de 1,5 mL de plasma
humano diluído, inativado pelo calor, negativo para anti-HBs.
Perfurador – para a perfuração da folha de alumínio que cobre as
cavidades da Placa Reveladora.
CombscaleTM – para leitura dos resultados.
Preparando a Placa Reveladora
1. Incubar a Placa Reveladora em uma incubadora a 37ºC por
45 minutos.
2. Cobrir a bancada de trabalho com papel absorvente para ser
descartado como resíduo bioinfectante no final do teste.
3. Misturar os reagentes agitando a Placa Reveladora.
Nota: Não remover a folha de alumínio da Placa Reveladora.
Furar a tampa de alumínio usando a ponteira descartável da
pipeta ou o perfurador, somente quando for indicado nas
instruções do Teste.
Preparando o Pente
Precaução: Para assegurar o funcionamento correto do teste,
não tocar nos dentes do pente.
1. Rasgar a embalagem de alumínio do Pente na extremidade
marcada. Remover o Pente.
2. O Pente e a Placa Reveladora podem ser utilizados total ou
parcialmente. Para usar parte de um pente:
a. Determinar quantos dentes são necessários para testar as
amostras e controles. Você precisa de um dente para cada
teste. Cada dente mostra o número “53” do código do kit,
para permitir a identificação dos dentes destacados.
b. Dobrar e quebrar o Pente verticalmente ou cortar com a
tesoura (veja Figura 4) para destacar o número necessário
de dentes (nº de testes incluindo 2 controles).
c. Retornar a parte do Pente não utilizada para o saco de
alumínio (com o dessecante). Fechar bem a embalagem,
por exemplo, com um clips, para manter seco. Armazenar o
Pente na caixa original do kit de 2 – 8ºC para uso posterior.
ImmunoComb® II
53
53
53
53
53
53
53
53
53
53
53
53
3
Segurança e Precauções
•
•
•
•
•
•
•
Este kit é somente para uso diagnóstico in vitro.
Todos os materiais de origem humana usados na
preparação do kit foram testados e considerados não
reativos para HbsAg, anticorpos para o vírus hepatite C e
anticorpos para HIV. Como nenhum teste pode garantir
completamente a ausência de contaminação viral, todas as
soluções de referência e amostras humanas devem ser
manipuladas como potencialmente infectantes.
Usar luvas cirúrgicas e avental. Seguir os procedimentos
aceitos para laboratório para trabalhar com soro ou plasma.
Não pipetar com a boca.
Descartar todas as amostras, Pentes, Placas Reveladoras e
outros materiais utilizados com o kit como resíduo
bioinfectante.
Não misturar reagentes de lotes diferentes.
Não usar o kit após o vencimento.
Armazemamento do Kit
Armazenar o kit em sua embalagem original de 2 – 8ºC. Nestas
condições, o kit permanecerá estável até a data de validade do
rótulo. Não congelar o kit.
Manipulação de Amostras
Tanto o soro como o plasma podem ser tesdados.
As amostras podem ser armazenadas por 7 dias de 2 – 8ºC antes
do teste. Para armazenar por mais de 7 dias, congelar as
amostras a –20 ºC ou inferior.
Centrifugar as amostras de soro após descongelamento.
Testar o sobrenadante.
Evitar ciclos repetidos de congelamento e descongelamento.
Procedimento do Teste
Material Necessário
•
Pipetas de precisão e ponteiras descartáveis para dispensar
100 µL.
•
Tesoura.
•
Cronômetro ou relógio de laboratório.
Preparando o Teste
Trazer todos os componentes, Placa Reveladora, pentes,
reagentes e amostras à temperatura ambiente e realizar o teste a
370C.
453/P7
Figura 4. Quebrando o Pente
Instruções do Teste
Nota: Realizar as incubações a 37ºC. As etapas de lavagem
devem ser realizadas à temperatura ambiente (22 – 26ºC).
Reação Antígeno-Anticorpo (Fileira A da Placa Reveladora)
1. Pipetar 100 µL de amostra. Perfurar a cobertura de alumínio
de uma cavidade da fileira A da Placa Reveladora com a
ponteira da pipeta ou com o perfurador e dispensar a
amostra no fundo da cavidade. Misturar enchendo e
esvaziando repetidamente a ponteira com a solução.
Descartar a ponteira da pipeta.
2. Repetir o passo 1 para as outras amostras, incluindo um
Controle Positivo e um Controle Negativo fornecidos no kit.
Usar uma nova cavidade da fileira A e trocar a ponteira para
cada amostra ou controle.
3. a) Inserir o Pente (o lado impresso de frente para você) nas
cavidades da fileira A contendo as amostras e controles.
Misturar: Inserir e retirar o Pente das cavidades várias
vezes.
b) Deixar o Pente na fileira A por 120 minutos a 37ºC .
Ajustar o cronômetro. Misturar um tempo adicional de 3
vezes (cada 30 minutos) durante a incubação. Próximo ao
final dos 120 minutos, perfurar a cobertura da fileira B
usando o perfurador. Não abrir mais cavidades que o
necessário.
c) Ao final dos 120 minutos, retirar o Pente da fileira A.
Absorver o líquido residual nas pontas dos dentes em
papel absorvente limpo. Não tocar a superfície frontal dos
dentes.
Primeira Lavagem (Fileira B)
4. Inserir o Pente nas cavidades da fileira B. Agitar: Retirar e
inserir vigorosamente o Pente nas cavidades e deixar pelo
menos 10 segundos para obter uma lavagem apropriada.
Repetir a agitação várias vezes no período de 2 minutos;
neste intervalo perfurar as coberturas da fileira C. Após 2
minutos, retirar o Pente e absorver o líquido residual como
no passo 3c.
Ligação do HbsAg biotinilado (fileira C)
5. Inserir o Pente nas cavidades da fileira C. Agitar como no
passo 3a. Incubar a Placa Reveladora com o pente por 30
2
minutos (ajustar o cronômetro) a 37ºC. Perfurar as
coberturas da fileira D. Misturar um tempo adicional durante
a incubação. Após 30 minutos, retirar o Pente e absorver o
líquido residual.
Ligação da Estreptavidina/ Fosfatase Alcalina (Fileira D)
6. Inserir o Pente nas cavidades da fileira D. Agitar. Incubar a
Placa Reveladora com o Pente por 20 minutos (ajustar o
cronômetro) a 37ºC. Perfurar as coberturas da fileira E.
Misturar um tempo adicional durante a incubação. Após 20
minutos, retirar o Pente a absorver o líquido residual.
Segunda Lavagem (Fileira E)
7. Inserir o Pente nas cavidades da fileira E. Agitar
repetidamente durante 2 minutos, como no passo 4. Neste
intervalo, perfurar as coberturas da fileira F. Após 2 minutos,
retirar o Pente e absorver o líquido residual.
Reação de Cor (Fileira F)
8. Inserir o Pente nas cavidades da fileira F. Agitar. Incubar a
Placa Reveladora com o Pente por 10 minutos exatos
(ajustar o cronômetro) a 37ºC. Após 10 minutos retirar o
Pente.
Reação de Parada (Fileira E)
9. Inserir o Pente novamente na fileira E. Após 1 minuto retirar
o Pente e deixar secar ao ar livre.
Descarte do lixo
Descartar as Placas Reveladoras, ponteiras, papel absorvente e
luvas usadas, como lixo bioinfectante.
≤
Resultado
Negativo
Controle
Positivo
Anti-HBs a um título de 10 UI/L
Figura 6. Resultado dos Testes
Interpretação Semi Quantitativa pela Leitura Visual
O nível de anti-HBs em cada amostra pode ser avaliado pela
comparação entre a intensidade da cor do ponto inferior de cada
dente, com a escala de cor do CombScale fornecida no kit.
Esta comparação se dá como a seguir: (Figura 7)
1. Calibrar o CombScale. Colocar o ponto inferior do dente de
Controle Positivo sob a intensidade de cor mais semelhante
ao da escala de cores. Ajustar a régua de modo que “10; C+”
apareça na janela acima da intensidade de cor selecionada.
2. Ler os resultados sem alterar a posição calibrada da régua.
Encontrar a intensidade de cor de cada ponto inferior com a
intensidade de cor similar da escala. Registrar o valor que
aparecer na janela acima desta intensidade como o título
aproximado de anti-HBs para a amostra correspondente.
Armazenamento da parte não utilizada do kit
Placa Reveladora
Se todas as cavidades da Placa Reveladora não foram utilizadas,
podem ser guardadas para uso posterior:
•
Selar as cavidades utilizadas com fita adesiva, de forma a
evitar respingos, mesmo que a Placa Reveladora tenha sido
esvaziada.
Outros materiais do kit:
•
Retornar o restante das Placas Reveladoras, Pentes,
perfurador, controles e instruções de uso ao kit.
Armazenar de 2 – 8ºC.
Amostra
Orgenics CombScale™
ANTI-HBs IU/L
5
10
C+
25
50
100
Calibrar o
CombScale
Resultados dos Testes
Validação
Para confirmar o funcionamento correto do teste e demonstrar
que os resultados são válidos, as três condições abaixo devem
ser cumpridas (veja figura 5):
1. O Controle Positivo deve produzir dois pontos no dente do
Pente.
2. O Controle Negativo deve produzir um ponto superior
(Controle interno). O ponto inferior não irá aparecer ou
aparecerá bem fraco, não afetando a interpretação dos
resultados.
3. Cada amostra testada deve produzir um ponto superior
(Controle interno).
Se alguma destas três condições não for cumprida, os resultados
são inválidos e as amostras e controles devem ser retestados.
Controle
Positivo
Controle
Negativo
Resultados
Inválidos
Figura 5. Validação dos testes
Leitura e Interpretação dos Resultados
Triagem
Comparar a intensidade do ponto inferior do dente de cada
amostra com o ponto inferior no dente do Controle Positivo
(Figura 6).
•
Um ponto com intensidade maior ou igual a do Controle
Positivo indica a presença de anti-HBs a um título ≥ 10 UI/L.
•
Um ponto com intensidade menor que a do controle positivo
é considerado como resultado negativo.
Figura 7. CombScale
Leitura no Equipamento
O refletômetro CombScanTM (ver o Manual do Usuário do
CombScan para instruções detalhadas) permite uma leitura
rápida e objetiva da intensidade da cor dos pontos do
ImmunoComb. Ler os resultados dos testes como absorbância
relativa usando o programa # 92 do CombScan, designando a
leitura do ponto inferior digitando “1” quando aparecer a
mensagem “pontos: 1,2,3” na tela. Converter as unidades de
absorbância relativas obtidas em valores de títulos para anti-HBs,
de acordo com a Tabela 1.
Tabela 1. Conversão de leituras de absorbância relativa para títulos.
Absorbância Relativa
Título (UI/L)*
< 693
<10
693 -1168
10
1169 -1723
25
1724 -2430
50
≥ 2431
≥ 100
* Baseado na calibração utilizando o soro padrão de referência
26/1/77 da OMS.
Interpretação
Títulos maiores ou iguais a 10 UI/L são considerados positivos,
representando os níveis mínimos de anticorpos necessários para
proteção imune contra infecção por HBV.
Documentação dos resultados
Como a cor desenvolvida no Pente é estável, os pentes podem
ser guardados para documentação posterior.
Limitações
Como em outros testes destinados para uso diagnóstico in vitro,
os resultados deste teste devem ser avaliados em conjunto com
todos os sintomas, histórico clínico e outros dados laboratoriais
realizados para o paciente.
453/P7
3
Características de Desempenho*
A sensibilidade e a especificidade do kit ImmunoComb II antiHBs foram avaliadas em um painel de 170 amostras de soro, em
comparação com dois ensaios EIA de referência.
Os resultados estão resumidos na Tabela 2.
Tabela 2. Resultados dos testes
Ensaio de
Referência
ImmunoComb II anti-HBs
Positivo
Positivo
50
Negativo
0
Negativo
2
118
P.O.Box 360 Yavne 70650, Israel
http://www.orgenics.com
Foram calculadas as seguintes características de desempenho:
•
Sensibilidade – 100%
•
Especificidade – 98.3%
* Informação detalhada disponível mediante solicitação.
Bibliografia
Follet EAC. 1998. Diagnosis of hepatitis B infection. In: Hugh Y
Mc Millan A, eds. Immunological diagnosis of sexually transmitted
diseases. Marcel Dekker, New York. Pgs 433-450.
Herrera FB. 1991. Hepatitis B vírus. In: Voral Hepatitis (Hollinger
FB, Percel RH, Robinsons WS, Gerin JL Ticehurst J, eds.) Raven
Press, New York, pp 73-138.
Kiyasu PK, Caldwell SH. 1993. Diagnosis and treatment of the
major hepatotropic viruses. Am J Méd Sci 306:248-261.
Krugman S. Overby LR, Mushavar IK, Ling C-M, Frosner GG,
Deinhart F. 1979. Viral hepatitis, type B: studies on natural history
and prevention re-examined. N Engl J. Méd 300:101-106.
Ogra PL, Beutner KR, 1981. Hepatitis viruses. In: Milgrom F.
Abeyounis CJ, Kano K. eds. Principles of immunological diagnosis
in medicine. Lea & Febiger, Philadelphia, pp. 247-259.
Robinson WS. 1991. Hepadnavindae and their replication. In:
Viral hepatitis (hollinger FB, Purcell, RHRobinson WS, Gerin JL.
Ticehurst J, eds.) Raven Press, New York, pp 39-71.
Swenson PD. 1991. Hepatitis viruses. In: Balows A . Hauster WJ.
Hemmann KL, Isenberg HD. Shadomy HJ, eds. Manual of Clinical
Microbiology, Fifth edition. American Society for Microbiology,
Washington, DC, pp. 959-983.
Produzido por:
ORGENICS LTD.
P.O.Box 360, Yavne
70650 - ISRAEL
Registro e Distribuição:
ORGENICS DO BRASIL LTDA
Alameda dos Ubiatans, 257 - Planalto Paulista
04070-030 São Paulo - SP
CNPJ : 01.767.606/0001-10
Atendimento ao consumidor
SAC: (11) 5589-4622
FAX: (11) 5581-3279
e-mail: [email protected]
Uso exclusivo para diagnóstico "in vitro"
Registro ANVISA nº 10348680027
Resp. Técnico : Wellington Staduto Braga da Silva
CRF-SP 13020
CONSERVAR ENTRE 2 - 8ºC
453/P7
4
Resumo dos Principais Procedimentos do Teste
Resumo do Procedimento de Teste
As instruções resumidas abaixo são para usuários experientes do kit ImmunoComb II anti-HBs.
(Para instruções detalhadas, por favor, veja o texto completo)
1. Incubar a Placa Reveladora em uma incubadora a 37ºC por 45 minutos.
2. Dispensar 100 µL de cada amostra e controle nas cavidades da fileira A da Placa Reveladora e
misturar.
3. Colocar o Pente na fileira A e continuar como descrito na Tabela 1.
Tabela 1. Resumo do Procedimento de Teste
Etapa
Reação antígeno-anticorpo
Fileira
A
Proceder como a seguir
Misturar; incubar por 2 horas a 37ºC; absorver.
Lavagem
B
Agitar; incubar por 2 minutos; absorver.
Ligação de HbsAg biotinilado
C
Misturar; incubar por 30 minutos a 37oC;
absorver.
Ligação de estreptavidina/
fosfatase alcalina
Lavagem
D
E
Misturar; incubar por 20 minutos a 37oC;
absorver.
Agitar; incubar por 2 minutos; absorver.
Reação de cor
F
Misturar; incubar por 10 minutos a 37ºC.
Reação de parada
E
Incubar por 1 minuto; secar ao ar livre.
453/P6
5