International Journal of Cardiovascular Sciences. 2016;29(6):492-499
492
ARTIGO DE REVISÃO
Treinamento de Força Moderado Atenua o Aumento da Pressão Arterial e Diminui o
Número de Núcleos em Cardiomiócitos de Ratos Hipertensos
Moderate Resistance Training Attenuates the Increase in Blood Pressure and Decreases the Cardiomyocyte Nuclei Number in Hypertensive Rats
Rodrigo Vanerson Passos Neves,1,3* Thiago Santos Rosa,1,3* Michel Kendy Souza,1 Clévia Santos Passos,2 Adriana
Aparecida Ferraz Carbonel,3 Cristiane Paula Teixeira,3 Francisco Navarro,4 Ricardo Santos Simões,5 Brande Ranter
Alves Soares,1 Maria Carmo Pinho Franco,3,5 Milton Rocha Moraes1,3*
Universidade Católica de Brasília,1 Brasília - DF; Instituto do Coração (InCor)2 – HCFMUSP; Universidade Federal de São Paulo (UNIFESP),3 SP;
Universidade Federal do Maranhão (UFMA),4 São Luís, MA; Universidade de São Paulo (USP),5 São Paulo, SP - Brasil
* Estes autores contribuíram igualmente para este estudo.
Resumo
Fundamentos: O treinamento de força (TF) é uma estratégia que diminui a pressão arterial (PA) em pacientes com
hipertensão arterial (HA) estágio 1 e atenua a progressão da PA em ratos hipertensos (estágio 3). A influência do TF
na remodelação cardíaca na HA não controlada ainda não está estabelecida.
Objetivo: O objetivo deste estudo foi avaliar os efeitos a longo prazo do TF em intensidade moderada na remodelação
cardíaca em ratos espontaneamente hipertensos (SHRs) sem tratamento.
Métodos: Dez SHRs machos com HA estágio 3 (PA sistólica ≥ 180 mmHg) e cinco ratos Wistar-Kyoto (WKY)
normotensos (PA sistólica < 120 mmHg) foram divididos em três grupos: sedentários normotensos (SED-WKY),
sedentários hipertensos (SED-SHR) e hipertensos TF (TF-SHR). O TF foi realizado em uma escada vertical (3 dias /
semana por 12 semanas, em dias não consecutivos) com 70% da carga máxima. A PA e a frequência cardíaca foram
registradas. Ao final do protocolo, os animais foram sacrificados e tiveram o ventrículo esquerdo seccionado para
análise histológica (hematoxilina e eosina e picrosirius red).
Resultados: O TF não atenuou o ganho de peso absoluto e relativo do coração e do ventrículo esquerdo no grupo
TF-SHR em comparação ao grupo SED-SHR. Não houve nenhuma diferença no volume nuclear nos cardiomiócitos
e conteúdo de colágeno entre os grupos. No entanto, o TF diminuiu o número de núcleos nos cardiomiócitos e
atenuou o aumento da PA sistólica no grupo TF-SHR em relação ao grupo SED-SHR. O Δ do duplo produto foi
menor no grupo TF-SHR em comparação aos grupos SED-WKY e SED-SHR.
Conclusões: Os dados obtidos demonstram que o TF não atenuou a hipertrofia cardíaca, mas reduziu a proliferação
nuclear nos cardiomiócitos e a progressão da PA em SHR com HA severa. (Int J Cardiovasc Sci. 2016;29(6):492-499)
Palavras-chave: Hipertensão, Ratos, Hipertrofia Ventricular Esquerda, Miócitos Cardíacos.
Abstract
Background: Resistance training (RT) is a strategy that decreases blood pressure (BP) in patients with stage 1 hypertension and attenuates
BP progression in hypertensive rats (stage 3). The influence of RT in cardiac remodeling in uncontrolled hypertension is not yet established.
Objective: The aim of this study was to evaluate the long-term effects of RT in moderate intensity in cardiac remodeling in spontaneously
hypertensive rats (SHRs) without treatment.
Methods: Ten male SHRs with stage 3 hypertension (systolic BP ≥ 180 mmHg) and five normotensive Wistar-Kyoto (WKY) rats (systolic
BP < 120 mmHg) were divided into three groups: sedentary normotensive (SED-WKY), sedentary hypertensive (SED-SHR), and RT
hypertensive (RT-SHR). The RT was conducted in a vertical ladder (3 days/week for 12 weeks, on nonconsecutive days) at 70% of the
maximum load. BP and heart rate were recorded. At the end of the protocol, the animals were euthanized and had their left ventricles sectioned
for histological analysis (hematoxylin and eosin and picrosirius red).
Correspondência: Milton Rocha Moraes
Programa de Pós-Graduação Stricto Sensu, Universidade Católica de Brasília – Campus I - QS 07 – Lote 01 – EPCT. CEP: 71966-700, Bloco G Sala G 119, Águas
Claras, Taguatinga, Distrito Federal, DF - Brasil
E-mail: [email protected]; [email protected]
DOI: 10.5935/2359-4802.20170008
Artigo recebido em 15/06/16; revisado em 08/07/16; aceito em 10/10/16.
Neves et al.
493
Int J Cardiovasc Sci. 2016;29(6):492-499
Artigo Original
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
Results: RT did not attenuate the absolute and relative weight gains of the heart and left ventricle in the RT-SHR group compared with the sedentary
group (SED-SHR). There was no difference in nuclear cardiomyocyte volume and collagen content between groups. However, RT decreased the
number of nuclei in the cardiomyocytes and attenuated the increase in systolic BP in the RT-SHR when compared with the SED-SHR group. The Δ
of the rate-pressure product was lower in the RT-SHR group compared with the groups SED-WKY and SED-SHR.
Conclusions: The data obtained demonstrate that RT did not attenuate the cardiac hypertrophy, but reduced the nuclear proliferation in
cardiomyocytes and the BP progression in SHRs with severe hypertension. (Int J Cardiovasc Sci. 2016;29(6):492-499)
Keywords: Hypertension; Rats; Hypertrophy, Left Ventricular; Myocytes, Cardiac
Full texts in English - http://www.onlineijcs.org
Introdução
O ventrículo esquerdo (VE) é órgão-alvo da
hipertensão e responde com hipertrofia à sobrecarga
constante de pressão no miocárdio. 1 Embora a
hipertensão arterial (HA) seja considerada um forte
determinante da hipertrofia do VE (HVE), a pressão
arterial (PA) explica apenas variações interindividuais
limitadas na massa do VE.1 Outras alterações estruturais
importantes no miocárdio, como a hipertrofia de
cardiomiócitos e aumento no conteúdo de fibroblastos e
elementos intersticiais, estão diretamente ligados à HVE
em ratos espontaneamente hipertensos (spontaneously
hypertensive rats, SHRs).2-4
Em roedores, a HVE é caracterizada por alterações
no volume e número de núcleos nos cardiomiócitos e
deposição de colágeno.5-8 Estas alterações induzem fibrose
cardíaca e rigidez, levando à redução da contratilidade
cardíaca, com progressão para insuficiência cardíaca.2,9
O treinamento aeróbio (TA) é uma intervenção
eficaz na proteção contra doenças cardiovasculares,
diminuindo a ocorrência de fatores de risco e dano ao
miocárdio e melhorando a função cardíaca em ratos
hipertensos.10 Pacientes com HA severa submetidos
ao TA mostraram um declínio na HVE e nos níveis
de PA. 11 Os mecanismos sugeridos entre o TA e
a HVE é uma redução na deposição de colágeno
intersticial, que impede a remodelação cardíaca
em humanos 11 e roedores. 12,13 Por outro lado, o
treinamento de força (TF) também tem sido relatado
como uma intervenção eficaz na redução de fatores
de risco cardíacos e PA em hipertensos,14 impedindo
a progressão da PA em SHRs com HA estágio 3 15
(níveis de PA ≥ 180 mmHg).16 Porém, pouco se sabe
ainda sobre os efeitos do TF sobre a HVE em pacientes
hipertensos. Apesar de estudos terem mostrado um
efeito hipotensor do TF em normotensos 17 e pacientes
hipertensos,14 bem como em roedores hipertensos,15
não há estudos investigando a associação do TF
com a diminuição ou controle da PA e a HVE na
HA sistólica. Além disso, não há um consenso sobre
as adaptações morfológicas cardíacas promovidas
pelo TF e seus possíveis efeitos sobre os fatores de
risco em pacientes hipertensos.18,19 Desta maneira, o
objetivo do presente estudo foi analisar as adaptações
morfológicas cardíacas em um modelo experimental
de HA submetido ao TF moderado. Nossa hipótese
foi de que o TF atenuaria o desenvolvimento de HVE
patológica induzida pela HA em SHRs não tratados.
Métodos
Animais
O estudo incluiu cinco ratos Wistar-Kyoto (WKY)
machos e 10 SHRs machos. Os animais apresentavam
17 semanas de idade e uma média de peso corporal
de 268,4 ± 32,1 g (WKY) e 327,0 ± 17,5 g (SHR).
A média dos níveis de PA sistólica dos animais
foi de 119,4 ± 3,6 mmHg e 205,8 ± 10,9 mmHg,
respectivamente. Os animais foram obtidos a partir
da Universidade Federal de São Paulo (UNIFESP).
O estudo foi aprovado pelo Comitê de Ética em
Pesquisa da inst it uição [n.922985/2014 omit ido
pela revisão].
Os animais foram mantidos em gaiolas plásticas
com cinco ratos em cada gaiola a uma temperatura
de 22 ± 2 °C e umidade relativa de 55 ± 10%, com
ração padrão para roedores (Nuvital ® CR1, São Paulo,
Brasil) e água ad libitum. Os ratos foram divididos
em três grupos de cinco animais em cada grupo:
WKY sedentários (SED-WKY), SHR sedentários
(SED‑SHR) e SHR submetidos ao TF (TF-SHR).
O número de roedores utilizados no presente estudo
foi pequeno e foi atingida uma boa reprodutibilidade
Int J Cardiovasc Sci. 2016;29(6):492-499
Neves et al.
Artigo Original
dos dados da PA, com coeficientes de variação de
2 ± 1% (SED‑WKY), 1 ± 1% (SED‑SHR) e 2 ± 1%
(TF‑SHR), demonstrando que a amostra tinha boa
homogeneidade e confiabilidade.
Condicionamento ao treinamento de força
Antes do TF, todos os animais foram condicionados
ao aparelho de TF (escada vertical), conforme descrito
anteriormente por Neves et al.15 Os animais foram
submetidos a três sessões de TF por semana em dias
não consecutivos por 2 semanas sem qualquer carga,
conforme descrito anteriormente.15 Todas as sessões
de treinamento ocorreram entre as 18:00 e 20:00 horas.
Os animais nos grupos sedentários foram mantidos
em uma caixa com mesmo tamanho da caixa do grupo
TF. Este procedimento foi realizado a fim de gerar as
mesmas condições de estresse em todos os animais.
Peso máximo transportado
Dois dias após o procedimento de condicionamento,
o peso máximo transportado (PMT) pelos animais do
grupo de treinamento foi determinado. Na subida
inicial, os animais transportavam 75% de seus pesos
corporais. Em seguida, adicionava-se 30 g de carga até
que a carga máxima tivesse sido atingida quando o rato
não conseguia mais subir toda a extensão da escada
em 4 – 9 tentativas. Foi definida como falha quando o
animal era incapaz de subir a escada após três ciclos
consecutivos de estímulos na cauda (com uso de pinça),
com um período de repouso de 60 s entre cada subida.
A carga mais pesada que o animal conseguia carregar
com sucesso ao longo de toda a extensão da escada foi
considerado como sendo o PMT para aquela sessão de
teste. Em seguida, a próxima sessão de teste consistiu
em subida na escada com 50%, 75%, 90% e 100% do
PMT prévio do animal, com um intervalo de descanso
de 60 s entre cada subida. Para as subidas subsequentes
na escada, uma carga de 30 g foi adicionada até que um
novo PMT foi determinado; o período de recuperação
entre cada subida foi de 120 s.20 Este procedimento foi
aplicado na primeira semana e repetido a cada 15 dias
durante as 12 semanas para ajustar a intensidade do
treinamento.15
Protocolo do treinamento de força
Após o PMT, os animais foram submetidos ao
protocolo do TF, no qual completaram 36 sessões
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
divididas em três sessões por semana em dias
não consecutivos, entre as 18:00 e 20:00 horas por
12 semanas, com cada uma das sessões consistindo de
6 – 8 séries de escaladas com 10 – 12 repetições, 1 min
de pausa entre cada série e uma duração média de
cada sessão de treinamento de ~10 – 12 min. A carga
de treinamento foi progressivamente ajustada (30 a 70%
do PMT), conforme descrito por Hornberger & Farrar,20
com utilização de tubos cônicos de 50 mL com pesos no
interior, fixos à parte proximal da cauda do animal com
uma trave de pressão com encaixe giratório e fita Scotch
de borracha (Scotch 3M, São Paulo, Brasil), conforme
descrito por Neves et al.15
Medida da pressão arterial
A PA sistólica (PAS) foi medida com o método
do manguito de cauda com PowerLab System
(ADInstruments Inc., Sydney, Austrália) com os
ratos conscientes. Para calcular a mudança na PA,
a PAS foi medida em todos os animais antes do
início do período de treinamento (T0) e ao final
das 12 semanas de TF, 48h após a última sessão de
exercício no mesmo horário a cada dia (entre 18:00 –
20:00) para permitir que os animais se adaptassem ao
procedimento. O duplo produto (DP) foi calculado
como o produto da frequência cardíaca e da PAS.
A PAS, a frequência cardíaca e o peso corporal foram
avaliados semanalmente por um mesmo examinador.15
Coleta de tecido
Os ratos foram sacrificados por decapitação 48 horas
após a última sessão de treinamento. Os corações foram
removidos e pesados imediatamente. O VE foi isolado
e pesado e depois seccionado transversalmente no
maior eixo e imerso em formaldeído a 10% (10 mM
de tampão PBS, pH 7,4) para posterior inclusão em
parafina. Durante o processamento histológico, cortes
com espessura de 5 µm foram obtidos e corados com
hematoxilina e eosina (H.E.) para a identificação do
volume e o número de núcleos por área, e corados com
picrosirius red para quantificação de colágeno.7
Análise morfológica e morfométrica
Fotomicrografias foram obtidas com utilização de um
microscópio de luz (Leica DM 1000, Wetzlar, Alemanha,
objetiva de 40X e ocular de 10X). Para análise do volume
nuclear dos cardiomiócitos, oito imagens foram obtidas
494
Neves et al.
495
Int J Cardiovasc Sci. 2016;29(6):492-499
Artigo Original
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
a partir de cada VE, totalizando 40 imagens por grupo.
Foi medido o diâmetro maior e menor de 12 núcleos
por imagem e avaliamos a atividade celular. Os valores
obtidos foram aplicados à fórmula: V = (A2 x B) / 1,91,
na qual o A é o menor diâmetro e B é o maior diâmetro do
núcleo e 1,91 é uma constante.7 O número de núcleos foi
avaliado nas mesmas fotomicrografias. Os núcleos foram
inicialmente delimitados em cada área da fotomicrografia
e o número de núcleos foi posteriormente calculado em
uma área de 0,016 mm2, como descrito por Cabanelas et al.7
Para analisar o volume e o número de núcleos por área,
utilizamos o programa AxioVision Rel, 4,8 (Carl Zeiss,
IL, EUA). Para quantificar a quantidade de colágeno no
VE, obtivemos oito imagens de cada animal, totalizando
40 imagens por grupo. Estas fotomicrografias foram
analisadas com o programa Image J® e a quantificação de
colágeno foi expressa em porcentagem por área.7
Análise estatística
Todos os dados estão expressos como mediana
(intervalo interquartil). Os testes de Shapiro-Wilk e
Levene foram utilizados para avaliar a normalidade
e homocedasticidade dos dados. Posteriormente, foi
utilizado o teste não paramétrico de Kruskal-Wallis
para comparar os dados morfológicos, morfométricos
e hemodinâmicos, enquanto o pós-teste de Dunn foi
utilizado para avaliar diferença entre os grupos. Valores
de p < 0,05 foram considerados significantes. As análises
estatísticas foram realizadas com o programa GraphPad
Prism, 6.0 (GraphPad Software, OH, EUA).
Resultados
Os grupos SED-SHR e TF-SHR apresentaram aumento
absoluto e relativo no peso do coração quando comparados
com o grupo SED-WKY. Um padrão de resultado
semelhante ocorreu em relação ao peso absoluto e
relativo do VE. Nenhuma diferença no volume nuclear
foi observada entre os grupos. O número de núcleos
por área se mostrou reduzido no grupo TF-SHR quando
comparado com o SED-SHR, mas nenhuma diferença foi
observada entre os grupos SED-WKY e TF-SHR em relação
a este parâmetro. Da mesma forma, não foi observada
diferença no volume de colágeno entre os grupos. O ganho
de peso corporal se mostrou reduzido no grupo TF-SHR
em comparação com o grupo SED-WKY, mas nenhuma
diferença significativa nesta variável foi observada entre
os grupos hipertensos (SED-SHR e TF-SHR). Todos os
resultados estão apresentados na Tabela 1.
O ΔPAS foi maior no grupo SED-SHR em
comparação com o grupo TF-SHR, mas nenhuma
diferença foi observada entre os grupos SED-WKY e
TF-SHR. Nenhuma alteração na frequência cardíaca foi
observada entre os grupos. O ΔDP no grupo TF-SHR se
mostrou reduzido quando comparado com o dos grupos
SED‑WKY e SED-SHR, conforme mostra a Tabela 2.
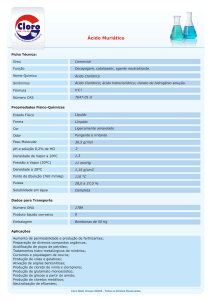
A PAS foi maior nos grupos hipertensos quando
comparados com o grupo normotenso tanto antes do
treinamento (SED-WKY: 122 mmHg [116 – 122 mmHg],
SED-SHR: 202 mmHg [198 – 2016 mmHg] e TF‑SHR:
208 mmHg [193 – 218 mmHg]) quanto após o
treinamento (SED-WKY: 127 mmHg [126 – 137 mmHg],
SED-SHR 222 mmHg [219 – 232 mmHg] e TF-SHR
202 mmHg [191 – 205 mmHg]). Como mostra a
Figura 1, a progressão da PAS após o treinamento foi
atenuada no grupo TF-SHR quando comparado com
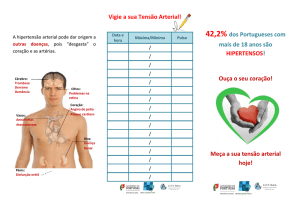
o grupo SED-SHR. A Figura 2 mostra fotomicrografias
representativas de cortes do VE corados com H.E. e
picrosirius red em todos os grupos.
Discussão
O presente estudo analisou as adaptações morfológicas
do miocárdio de SHRs com HA severa submetidos
a 12 semanas de TF. Nossa hipótese era de que o TF
poderia atenuar a HVE, diminuindo a progressão
de alterações morfológicas cardíacas induzidas pela
sobrecarga de pressão da HA. No entanto, nossos
resultados demonstraram que o TF foi incapaz de
reverter a HVE neste modelo experimental de HA
severa. Os níveis elevados de PA (≥ 180 mmHg) dos
animais e a ausência de tratamento farmacológico
podem ter influenciado estes resultados.
Sabemos que para alcançar as maiores reduções da
PA, é necessária uma combinação de exercício, dieta
e medicamentos anti-hipertensivos para diminuir a
pós-carga e alterar mecanismos bioquímicos, incluindo
redução da atividade do sistema renina-angiotensina,
levando a uma regressão da HVE na HA severa.21-23
Por outro lado, um resultado relevante do nosso estudo
foi o achado da análise histomorfométrica de redução no
número de núcleos nos cardiomiócitos (NNC) dos SHRs
submetidos ao TF (grupo TF-SHR) quando comparados com
os SHRs sedentários (grupo SED‑SHR). Esta diminuição
da proliferação de núcleos nos cardiomiócitos poderia
indicar um possível efeito benéfico do TF sobre a HA.
Curiosamente, ainda não existem estudos na literatura
analisando o NNC em roedores submetidos ao exercício.
Int J Cardiovasc Sci. 2016;29(6):492-499
Neves et al.
Artigo Original
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
Tabela 1 – Análise morfológica do coração dos animais após 12 semanas de treinamento de força
SED-WKY
SED-SHR
TF-SHR
Valor de P
54 (35 - 68)
25 (22 - 28)
23 (17 - 25) a
0,0031
Peso do Coração (g)
1,24 (1,14 - 1,29)
1,65 (1,54 - 1,83) a
1,83 (1,67 - 2,05) a
0,0019
PVE (g)
0,84 (0,79 - 0,85)
1,09 (1,06 - 1,18) a
1,13 (1,03 - 1,21) a
0,0089
PCar/PCor (mg/g)
3,80 (3,63 - 3,99)
4,70 (4,29 - 5,19) a
5,20 (5,04 - 5,77) a
0,0036
PVE/PCor (mg/g)
2,62 (2,47 - 2,67)
3,04 (2,95 - 3,39) a
3,24 (2,99 - 3,54) a
0,0018
34 (29 - 46)
46 (31 - 50)
41 (31 - 61)
0,6200
NN / 0,016 mm2
9,0 (7,1 - 10,8)
12,1 (11,2 - 14,3)
6,3 (5,6 – 8,9) b
0,0205
Volume de Colágeno (%)
8,0 (7,1 - 9,1)
8,7 (8,2 - 11,1)
10,6 (8,3 - 11,5)
0,1330
Δ Variáveis
Peso Corporal (g)
VN (µm3)
Os dados estão expressos como mediana (intervalo interquartil [percentis 25o - 75o]).Δ, Delta, pós-treinamento - pré-treinamento (12asemana - 1ª semana);
PCor, peso corporal; PCar, peso cardíaco; PVE, peso do ventrículo esquerdo; PCar/PCor, razão do peso cardíaco sobre o peso corporal; PVE/PCor, razão
do peso do ventrículo esquerdo sobre o peso corporal; VN, volume nuclear; NN / 0,016mm2, número de núcleos em uma área limitada de 0,016 mm2. a
Diferença versus SED-WKY; b diferença versus SED-SHR.
Tabela 2 – Parâmetros hemodinâmicos após 12 semanas de treinamento de força
SED-WKY
SED-SHR
TF-SHR
Valor de P
PA sistólica (mmHg)
9 (5 - 18)
20 (15 - 22)
-13 (-22 - 11) b
0,0115
Frequência Cardíaca
(bpm)
23 (5 - 68)
14 (-37 - 55)
-25 (-92 - 11)
0,0534
86 (61 - 175)
135 (-16 - 207)
-145 (-187 - -27) a,b
0,0111
ΔVariáveis
DP (mmHg•bpm)/100
Os dados estão expressos como mediana (intervalo interquartil [percentis 25o - 75o]). Δ, delta pós-treinamento - pré-treinamento (12a semana - 1ª semana);
PA, pressão arterial; DP, duplo produto. a Diferença versus SED-WKY; b diferença versus SED-SHR.
Ressaltamos que ainda há poucas evidências científicas
sobre a proliferação nuclear nos cardiomiócitos como um
índice de dano cardíaco.5,7 Dois estudos demonstraram que
um aumento no NNC é um possível marcador de piora
da cardiomiopatia em modelos experimentais, como ratas
ooforectomizadas7 e camundongos obesos,5 demonstrando
que doenças crônicas distintas poderiam alterar o NNC e
influenciar a apoptose celular e a fibrose.7 No entanto, nosso
496
Neves et al.
Int J Cardiovasc Sci. 2016;29(6):492-499
Artigo Original
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
275
Pressão Arterial Sistólica (mmHg)
497
a,b
250
b
225
b
b,c
SED-WKY
SED-SHR
200
TF-SHR
175
150
125
100
0
Após o treinamento
Antes do treinamento
Figura 1 – Monitorização da pressão arterial sistólica antes e após treinamento.
Os dados estão expressos como mediana (intervalo interquartil [percentis 25º – 75º]). Os valores foram comparados dentro de cada grupo e entre os
grupos. a Diferença versus pré-treinamento; b diferença versus SED-WKY; c diferença versus SED-SHR.
SED-WKY
SED-SHR
TF-SHR
B
A
200 µm
C
200 µm
E
D
200 µm
200 µm
F
200 µm
200 µm
Figura 2 – Fotomicrografias representativas de cortes do ventrículo esquerdo corados com hematoxilina e eosina (A, B e C) e picrosirius red (D, E e F).
As setas em A, B e C indicam os núcleos dos cardiomiócitos. As marcas vermelhas em D, E e F indicam colágeno. Amplificação de 400X.
grupo é o primeiro a ter estudado o NNC em SHRs com
HA severa submetidos ao TF.
de Pagan et al.,12 que submeteram SHRs ao TA em esteira
Quanto à ocorrência de fibrose, nossos resultados não
demonstraram alterações significativas no volume de
colágeno total nos animais SED-SHR e TF-SHR quando
comparados aos SED-WKY. Esses dados corroboram os
não observaram diminuição no volume total de colágeno
(12 m/min, 30 min/dia, 5 dias/semana) por 4 semanas e
I. Verificamos em nosso estudo que o TF não atenuou a
hipertrofia cardíaca avaliada pelo ganho em valor absoluto
e relativo do peso do coração em SHRs. No entanto, o TF
Int J Cardiovasc Sci. 2016;29(6):492-499
Neves et al.
Artigo Original
aplicado neste estudo pode ter atenuado a progressão
da PAS no TF-SHR (Δ = -7 mmHg) ao final das 12
semanas. Por outro lado, os animais sedentários
apresentaram um aumento na PAS: SED-SHR (Δ = +19
mmHg) e SED-WKY (Δ = +11 mmHg).
Embora alguns estudos apontem para uma
diminuição significativa nos níveis da PA
em associação ao TF em pacientes com HA estágio
1,14,19,24 bem como em animais,15,25 é possível que na HA
severa (≥ 180 mmHg), uma redução mais expressiva
da PA seja necessária para evitar a progressão da
HVE.1 Além disso, o tratamento farmacológico com
medicação anti-hipertensiva deve ser iniciado logo
após o diagnóstico da HA. 16 Seguindo esta linha,
um estudo recente em ratos com HA induzida por
nitro‑L-arginina metil éster (L-NAME) demonstrou
que o tratamento com betabloqueador (ex., nebivolol)
associado ao TA por 4 semanas foi mais eficaz em
reduzir o percentual de colágeno cardíaco do que cada
intervenção isolada.26
O presente estudo foi limitado pelo pequeno
tamanho da amostra em cada grupo (n = 5), o que pode
ter restringido a nossa capacidade de obter resultados
estatisticamente significantes. Além disso, poderíamos
ter utilizado ratos Wistar em vez de ratos WKY,
porque ao contrário do que ocorre em ratos Wistar, a
ocorrência de HVE em ratos WKY é independente dos
níveis pressóricos dos animais.27 Em estudos futuros,
será relevante investigar também a função cardíaca
e os parâmetros bioquímicos e moleculares, a fim de
elucidar o papel do TF no remodelamento ventricular
em SHRs tratados.
Além disso, o TF em intensidade moderada foi
eficaz na redução do DP em SHRs com HA estágio 3.
Este resultado tem um significado clínico importante,
uma vez que reflete uma diminuição do trabalho
cardíaco. O DP é considerado um bom marcador
para avaliar o consumo de oxigênio do miocárdio
durante o repouso ou esforço e é eficaz em estimar o
trabalho do miocárdio em resposta ao TF.28 Além disso,
não observamos alterações na frequência cardíaca;
portanto, a diminuição do DP pode ser atribuída à
significativa redução da PA observada.28
Conclusão
O TF moderado foi incapaz de reduzir a HVE em
um modelo experimental de HA severa sem tratamento
farmacológico, mas foi eficaz em atenuar o aumento nos
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
níveis da PA na HA e reduzir a proliferação nuclear em
cardiomiócitos de SHRs. Ainda assim, acreditamos que
a diminuição da PA é um fator importante para a HVE.
No futuro, será interessante analisar os efeitos do TF
com exercícios de leve a moderada intensidade como um
apoio ao tratamento farmacológico em seres humanos e
roedores com HA severa.
Agradecimentos
Agradecemos a Mauro Cardoso Pereira, da Divisão
de Nefrologia da Universidade Federal de São Paulo,
pela assistência com os animais durante o projeto.
Este trabalho foi apoiado pela Fundação de Amparo à
Pesquisa do Estado de São Paulo (FAPESP), o Conselho
Nacional de Desenvolvimento Científico e Tecnológico
(CNPq) e a Coordenação de Aperfeiçoamento de Nível
Superior (CAPES).
Agradecimentos também vão para o Dr Niels
Olsen, chefe do Laboratório de Imunologia Clínica e
Experimental-UNIFESP, por seu apoio entusiasmado
às nossas ideias.
Contribuição dos autores
Concepção e desenho da pesquisa e Redação
do manuscrito: Neves RVP, Rosa TS, Souza MK,
Passos CS, Carbonel AAF, Teixeira CP, Navarro
F, Simões RS, Moraes MR; Obtenção de dados,
Análise e interpretação dos dados e Revisão crítica
do manuscrito quanto ao conteúdo intelectual
importante: Neves RVP, Rosa TS, Souza MK, Passos
CS, Carbonel AAF, Teixeira CP, Navarro F, Simões
RS, Câmara NOS, Moraes MR; Análise estatística e
Obtenção de financiamento: Neves RVP, Rosa TS,
Moraes MR.
Potencial conflito de interesse
Declaro não haver conflito de interesses pertinentes.
Fontes de financiamento
O presente estudo foi financiado pela FAPESP, CNPq
e CAPES.
Vinculação acadêmica
Este artigo é parte de Dissertação de Mestrado de
Rodrigo Vanderson Passos Neves pela Universidade
Federal de São Paulo - UNIFESP.
498
Neves et al.
499
Exercício e Núcleos de Cardiomiócitos em Ratos SHR
Int J Cardiovasc Sci. 2016;29(6):492-499
Artigo Original
Referências
1.
Cramariuc D, Gerdts E. Epidemiology of left ventricular hypertrophy in
hypertension: implications for the clinic. Expert Rev Cardiovasc Ther.
2016;14(8):915-26.
15. Neves RV, Souza MK, Passos CS, Bacurau RF, Simoes HG, Prestes J,
et al. Resistance training in spontaneously hypertensive rats with
severe hypertension. Arq Bras Cardiol. 2016;106(3):201-9.
2.
Rossoni LV, Oliveira RA, Caffaro RR, Miana M, Sanz-Rosa D, Koike
MK, et al. Cardiac benefits of exercise training in aging spontaneously
hypertensive rats. J Hypertens. 2011;29(12):2349-58.
3.
Zhang J, Ren CX, Qi YF, Lou LX, Chen L, Zhang LK, et al. Exercise
training promotes expression of apelin and APJ of cardiovascular tissues
in spontaneously hypertensive rats. Life Sci. 2006;79(12):1153-9.
4.
Zamo FS, Barauna VG, Chiavegatto S, Irigoyen MC, Oliveira EM.
The renin-angiotensin system is modulated by swimming training
depending on the age of spontaneously hypertensive rats. Life Sci.
2011;89(3-4):93-9.
16. Mancia G, Fagard R, Narkiewicz K, Redon J, Zanchetti A, Böhm M,
et al; Task Force for the management of arterial hypertension of the
European Society of Hypertension; Task Force for the management
of arterial hypertension of the European Society of Cardiology. 2013
ESH/ESC guidelines for the management of arterial hypertension:
the Task Force for the Management of Arterial Hypertension of
the European Society of Hypertension (ESH) and of the European
Society of Cardiology (ESC). Blood Press. 2013;22(4):193-278.
5.
17. Moraes MR, Bacurau RF, Ramalho JD, Reis FC, Casarini DE, Chagas JR,
et al. Increase in kinins on post-exercise hypotension in normotensive
and hypertensive volunteers. Biol Chem. 2007;388(5):533-40.
Schipke J, Banmann E, Nikam S, Voswinckel R, Kohlstedt K, Loot
AE, et al. The number of cardiac myocytes in the hypertrophic and
hypotrophic left ventricle of the obese and calorie-restricted mouse
heart. J Anat. 2014;225(5):539-47.
18. Haykowsky MJ, Dressendorfer R, Taylor D, Mandic S, Humen D.
Resistance training and cardiac hypertrophy: unravelling the training
effect. Sports Med. 2002;32(13):837-49.
6. Pereira LM, Bezerra DG, Machado DL, Mandarim-de-Lacerda CA.
Enalapril attenuates cardiorenal damage in nitric-oxide-deficient
spontaneously hypertensive rats. Clin Sci (Lond). 2004;106(3):337-43.
19. Cornelissen VA, Fagard RH, Coeckelberghs E, Vanhees L. Impact of
resistance training on blood pressure and other cardiovascular risk
factors: a meta-analysis of randomized, controlled trials. Hypertension.
2011;58(5):950-8.
7. C a b a n e la s L A, C ar bonel AA, d os Santos MA , Si moes RS,
Liberatori‑Filho AW, Baracat EC, et al. [Cardiomyocytes
morphology and collagen quantification in the myocardium of
female rats treated with isoflavones or estrogens]. Rev Bras Ginecol
Obstet. 2012;34(10):447-52.
8. Noorafshan A, Khazraei H, Mirkhani H, Karbalay-Doust S.
Stereological study of the diabetic heart of male rats. Lab Anim Res.
2013;29(1):12-8.
9.
Ichiki T, Schirger JA, Huntley BK, Brozovich FV, Maleszewski JJ,
Sandberg SM, et al. Cardiac fibrosis in end-stage human heart failure
and the cardiac natriuretic peptide guanylyl cyclase system: regulation
and therapeutic implications. J Mol Cell Cardiol. 2014;75:199-205.
20. Hornberger TA Jr, Farrar RP. Physiological hypertrophy of the FHL
muscle following 8 weeks of progressive resistance exercise in the rat.
Can J Appl Physiol. 2004;29(1):16-31.
21. Sen S, Tarazi RC, Khairallah PA, Bumpus FM. Cardiac hypertrophy in
spontaneously hypertensive rats. Circ Res. 1974;35(5):775-81.
22. Phillips RA. Etiology, pathophysiology, and treatment of left ventricular
hypertrophy: focus on severe hypertension. J Cardiovasc Pharmacol.
1993;21 Suppl 2:S55-62.
23. Nishimura H, Kubota J, Okabe M, Ueyama M, Oka T, Kawamura K. Left
ventricular function of the heart regressed by nifedipine in spontaneously
hypertensive rats. Jpn Circ J. 1994;58(2):116-22.
10. Chicco AJ, McCune SA, Emter CA, Sparagna GC, Rees ML, Bolden DA,
et al. Low-intensity exercise training delays heart failure and improves
survival in female hypertensive heart failure rats. Hypertension.
2008;51(4):1096-102.
24. Moraes MR, Bacurau RF, Simoes HG, Campbell CS, Pudo MA, Wasinski
F, et al. Effect of 12 weeks of resistance exercise on post-exercise
hypotension in stage 1 hypertensive individuals. J Hum Hypertens.
2012;26(9):533-9.
11. Kokkinos PF, Narayan P, Colleran JA, Pittaras A, Notargiacomo
A, Reda D, et al. Effects of regular exercise on blood pressure and
left ventricular hypertrophy in African-American men with severe
hypertension. N Engl J Med. 1995;333(22):1462-7.
25. Araujo AJ, Santos AC, Souza Kdos S, Aires MB, Santana-Filho VJ,
Fioretto ET, et al. Resistance training controls arterial blood pressure
in rats with L-NAME- induced hypertension. Arq Bras Cardiol.
2013;100(4):339-46.
12. Pagan LU, Damatto RL, Cezar MD, Lima AR, Bonomo C, Campos DH,
et al. Long-term low intensity physical exercise attenuates heart failure
development in aging spontaneously hypertensive rats. Cell Physiol
Biochem. 2015;36(1):61-74.
26. Goessler KF, Martins-Pinge M, Veronez da Cunha N, Karlen-Amarante M,
de Andrade FG, Brum PC, et al. Treatment with nebivolol combined with
physical training promotes improvements in the cardiovascular responses
of hypertensive rats. Can J Physiol Pharmacol. 2014;92(3):234-42.
13. de Andrade LH, de Moraes WM, Matsuo Junior EH, de Orleans
Carvalho de Moura E, Antunes HK, Montemor J, et al. Aerobic exercise
training improves oxidative stress and ubiquitin proteasome system
activity in heart of spontaneously hypertensive rats. Mol Cell Biochem.
2015;402(1-2):193-202.
27. Aiello EA, Villa-Abrille MC, Escudero EM, Portiansky EL,
Perez NG, de Hurtado MC, et al. Myocardial hypertrophy of
normotensive Wistar‑Kyoto rats. Am J Physiol Heart Circ Physiol.
2004;286(4):H1229-35.
14. Moraes MR, Bacurau RF, Casarini DE, Jara ZP, Ronchi FA, Almeida SS,
et al. Chronic conventional resistance exercise reduces blood pressure
in stage 1 hypertensive men. J Strength Cond Res. 2012;26(4):1122-9.
28. Terra DF, Mota MR, Rabelo HT, Bezerra LM, Lima RM, Ribeiro AG,
et al. Reduction of arterial pressure and double product at rest after
resistance exercise training in elderly hypertensive women. Arq Bras
Cardiol. 2008;91(5):299-305.