Faculdade de Medicina da Universidade do Porto
Faculdade de Medicina Dentária da Universidade
do Porto
Diferenciação do
Tubo Neural
Ana Isabel Pereira de Azevedo
Ana Leonor Assunção Silva
Ana Nunes Vieira
Maria Inês Taboas Simões
Marta H.C. Nunes de Andrade
Biologia Celular e Molecular
Porto 2005
Índice
Pág.
1. Introdução
3
2. O desenvolvimento embrionário
3
3. Regulação molecular da indução neural
4
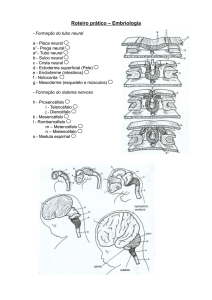
4. Neurulação
5
5. Diferenciação do tubo neural
7
5.1 Diferenciação céfalo-caudal
7
5.2 Diferenciação dorso-ventral
7
6. Malformações associadas ao desenvolvimento do tubo neural
9
6.1 Definição
9
6.2 Doenças
9
7. Investigação
10
8. Conclusão
12
9. Bibliografia
12
2
1. Introdução
A presente monografia, de carácter opcional, insere-se no âmbito da disciplina de Biologia
Celular e Molecular e, por meio dela, temos como objectivo alargar o nosso conhecimento, bem
como o de outros, acerca de uma etapa específica do desenvolvimento embrionário, a diferenciação
tubo neural e sua importância no desenvolvimento do sistema nervoso.
A nossa escolha recaiu neste tema tanto pela sua importância no contexto das matérias
abordadas em biologia do desenvolvimento, como pela relevância que tem na nossa futura
profissão. De facto, é nossa convicção que compreendendo os mecanismos que estão subjacentes a
uma normal diferenciação do tubo neural consigamos, mais facilmente, perceber o que está alterado
quando surgem malformações fetais associadas ao tubo neural.
Neste sentido, o nosso trabalho organiza-se de forma a darmos umas breves ideias sobre o
que se passa até o embrião chegar a ser tridérmico, focando-se, posteriormente, nos mecanismos
moleculares que regulam a indução neural e de que forma é que esta se processa. Reservaremos um
espaço para apresentação de algumas malformações conhecidas por défices de mecanismos que
explicitaremos. Optaremos, também, pela introdução de um capítulo no qual seleccionaremos
alguns dos trabalhos e avanços em investigações nesta área.
2. O desenvolvimento embrionário
O desenvolvimento embrionário começa após a fecundação, compreendendo todo o
processo desde a formação do zigoto até ao nascimento. Inicia-se com uma série de divisões
mitóticas do zigoto, originando a mórula que, ao ser implantada no útero, se modifica, havendo
diferenciação das células em dois grupos: a mais externa, o trofoblasto, que mais tarde, se diferencia
em citotrofoblasto e sinciotrofoblasto, enquanto que a mais interna, o embrioblasto, se diferencia
em hipoblasto e epiblasto, que originará posteriormente, na gastrulação, os três folhetos
embrionários: endoderme, mesoderme e ectoderme1,2.
Após a gastrulação, caracterizada por movimentos morfogénicos intensos, forma-se o
embrião tridérmico. Os três folhetos embrionários sofrem diferenciação celular, originando-se os
3
diferentes tecidos, os quais se inter-relacionam formando órgãos e sistemas de órgãos. Esta fase
denomina-se organogénese; é iniciada com a neurulação, que culmina na formação do tubo neural
(que originará o encéfalo e espinhal medula) e da crista neural (na base dos sistemas nervosos
periférico e autónomo), sendo induzida por um conjunto de interacções celulares. Segue-se a
diferenciação do tubo neural, num processo rápido, em que ocorre diferenciação a diversos níveis,
podendo distinguir-se diferenciação céfalo-caudal de dorso-ventral1,2.
3. Regulação molecular da indução neural
Os organismos são estruturas complexas compostas por diversos tipos de tecidos, os quais,
necessariamente, têm de comunicar entre si para que se possam desenvolver como um todo
estruturado. Também durante o desenvolvimento embrionário as células comunicam entre si e
transmitem sinais através de processos de indução. Por este mecanismo, um determinado tecido
produz um sinal que envia a outro, provocando uma resposta que, de alguma forma, altera o rumo
do seu desenvolvimento. Existem dois tipos principais de interacções entre as células: interacção
parácrina e justácrina. Em relação à primeira, podem agrupar-se os seus factores em quatro famílias:
o
Fibroblast Growth Factor (FGF): associados à angiogénese, desenvolvimento da
mesoderme e condução axonal, entre outros;
o
Hedgehog Family: sendo o mais conhecido desta família o Sonic Hedgehog, responsável
pela modelação do tubo neural em vertebrados e indução da formação de diversos tipos de
neurónios;
o
Wnt Family: importantes no estabelecimento da polaridade nos membros dos vertebrados;
o
TGF-β super Family: que inclui as famílias TGF-β, activina, BMP e Vg1, entre outras
proteínas. As proteínas BMP são capazes de controlar o ciclo celular de outras células, bem como a
sua migração e diferenciação2.
A BMP-4 assume um papel fundamental na indução neural. O seu bloqueio promove a
indução neural enquanto que, na sua presença, a ectoderme origina epiderme e a mesoderme forma
a mesoderme intermediária e a placa lateral. Quando ausente ou neutralizada a BMP-4, a ectoderme
4
dá origem ao tecido neural. Dada a importância da inactivação desta proteína, existem moléculas
que são segregadas com esse propósito, nomeadamente a noguina, a cordina e a folistatina,
presentes no nó primitivo, no notocórdio e na mesoderme pré-cordal. Elas induzem a mesoderme a
formar o notocórdio e a mesoderme paraxial (mesoderme desloca-se dorsalmente). Estes indutores
neurais apenas induzem os tecidos do encéfalo anterior e do mesencéfalo. As estruturas caudais da
placa neural (encéfalo posterior e medula espinhal) dependem da secreção de duas proteínas: a Wnt3 e FGF. O ácido retinóico também parece tomar parte na organização do eixo céfalo-caudal, uma
vez que pode fazer com que segmentos cefálicos sejam reespecificados para caudais, pela regulação
da expressão de genes homeobox3.
4. Neurulação
Subsequentemente à indução, a placa neural alongada expande-se, gradualmente, em
direcção à linha primitiva. Existem duas formas principais para converter a placa neural em tubo
neural: a neurulação primária e a secundária. Regra geral, a porção anterior do tubo neural provém
de uma neurulação primária, enquanto a posterior é secundária. O tubo neural completo é
constituído pela junção dos dois tubos formados separadamente3.
Na neurulação primária, as células que rodeiam a placa neural induzem-nas a proliferarem e
invaginar para formar uma estrutura tubular. Após a formação da placa neural, os seus bordos ficam
mais finos e ascendem para formar as pregas neurais, enquanto o sulco neural, em forma de U,
surge no centro da placa, dividindo os futuros lados esquerdo e direito do embrião. As pregas
neurais migram em direcção à linha média do embrião, fundindo-se para originar o tubo neural. A
neurulação primária pode ser dividida em quatro etapas distintas espacial e temporalmente:
1. e 2. formação e a modelação da placa neural. A partir da mesoderme dorsal são enviados sinais
para as células da ectoderme se alongarem e constituírem a placa neural. Estas células alongadas
diferenciam-se daquelas da epiderme. Os movimentos intrínsecos da epiderme e da placa neural dão
forma a esta, a qual se alonga ao longo do eixo antero-posterior e se torna mais estreita, para que se
possa dobrar e formar o tubo neural;
5
3. dobra da placa neural. Esta fase envolve a formação de
regiões onde a placa neural contacta com os tecidos
circundantes. Em mamíferos, as células da linha média da
placa neural são designadas de medial hinge point (MHP) e
tornam-se ancoradas ao notocórdio subjacente, o qual as
Fig. 1: Microscopia electrónica: sulco
neural e pregas neurais. Adaptado de 4.
induz a tornarem-se cuneiformes. Fica formado um canal na linha média dorsal. Pouco depois,
outros dois canais são formados perto do contacto da placa neural com a restante ectoderme, em
regiões designadas dorsolateral hinge points (DLHPs), ficando ancorados à superfície da ectoderme
das pregas neurais. Também estas células se tornam cuneiformes. Após a formação destes canais na
placa neural, ela acaba por se dobrar à volta deles, os quais funcionam como pivots. Forças
extrínsecas também actuam, puxando a epiderme para o centro do embrião. Estes eventos levam à
constituição das pregas neurais (fig.1);
4. fecho do tubo neural. À medida que as pregas neurais se
aproximam na linha média, aderem uma à outra e fundem-se.
Esta fusão não ocorre simultaneamente ao longo da ectoderme,
Fig. 2: Microscopia electrónica: tubo
neural. Adaptado de 4.
sendo que a neurulação cefálica é mais avançada que a caudal e que permanecem duas
extremidades abertas, uma anterior, o neuroporo anterior e uma posterior, o neuroporo posterior.
Em mamíferos, o fecho do tubo neural (fig. 2) é iniciado em vários locais ao longo do eixo anteroposterior3.
O processo da neurulação primária parece ser similar em
anfíbios, répteis, aves e mamíferos e divide a ectoderme em três
tipos de células: o tubo neural, posicionado internamente, que
dará origem ao encéfalo e espinhal medula, a epiderme,
localizada externamente e as células da crista neural (fig. 3)3.
Fig. 3: Microscopia electrónica: células da
crista neural. Adaptado de 4.
A crista neural constitui a região que põe em contacto o tubo neural e a epiderme. Forma-se
no local de elevação das pregas neurais, quando existem elevados níveis de BMP’s em contacto
6
com altos níveis de Wnt 6 da epiderme. As células da crista neural expressam os factores Fox D3 e
Slug. Este último inactiva moléculas adesivas entre as células da crista neural (N-caderinas),
permitindo que migrem ao longo do organismo. Esta estrutura irá, futuramente, originar os sistemas
nervosos periférico e autónomo3.
Na neurulação secundária, o tubo neural ascende a partir da coalescência das células
mesenquimatosas para formar uma estrutura sólida que, posteriormente, cavita e se converte em
tubular. O conhecimento da neurulação secundária é importante em medicina devido à prevalência
das malformações da medula espinhal posterior3.
5. Diferenciação do tubo neural
A diferenciação do tubo neural nas
diversas regiões do sistema nervoso central
(SNC) ocorre rapidamente e a vários níveis
simultaneamente:
Fig. 4: O tubo neural. Adaptado de 5.
o
diferenciação anatómica das diferentes estruturas do SNC;
o
diferenciação a nível tecidual para formar diferentes camadas quer na medula espinhal quer
no cérebro;
o
diferenciação a nível celular, com a formação de diferentes tipos de células nervosas
(neurónios) e de suporte (glia)2,3.
5.1 Diferenciação céfalo-caudal
A região cefálica do tubo neural experimenta um desenvolvimento muito acentuado,
ocorrendo formação das diferentes partes do cérebro e de estruturas cefálicas do SNC. Este
desenvolvimento é controlado por uma série de genes, incluindo os genes Hox2,3.
5.2 Diferenciação dorso-ventral
O tubo neural sofre uma polarização e diferenciação dorso-ventral, o que leva a que as
células de diferentes camadas ao longo deste eixo adquiram diferentes características e assumam
diferentes funções, como é o caso dos neurónios sensitivos e motores, os quais são formados nas
7
regiões dorsal e ventral do tubo, respectivamente. Os interneurónios formam-se nas regiões
intermédias3.
A polaridade é estabelecida por influência de tecidos vizinhos, nomeadamente o notocórdio,
ventralmente, e a epiderme, dorsalmente. A especificação do eixo dorso-ventral do tubo neural é
iniciada por dois grandes factores parácrinos. O notocórdio liberta Sonic Hedghog (shh) que vai
induzir a formação da placa ventral do tubo (floor plate); as células ventrais da placa passam,
também, a libertar shh. A epiderme (ectoderme dorsal) liberta proteínas da família TGF-β,
especialmente BMP 4, BMP 7, dorsalina e activina, as quais vão induzir a formação da placa dorsal
(roof plate), que passa, também, a libertar estas proteínas. Tais factores promovem um gradiente ao
longo das células vizinhas, difundindo-se a BMP 4 ventralmente e o shh dorsalmente3.
Os factores parácrinos interactuam para instruir a síntese de diferentes factores de
transcrição ao longo do eixo dorso-ventral do tubo neural. As células do tubo neural irão exprimir a
sua identidade de acordo com a influência que recebem das células vizinhas, uma vez que os
diferentes tipos de factores parácrinos activam ou inibem determinados factores de transcrição
celular, conduzindo a uma expressão genética diferencial ao longo das diversas camadas de células
do tubo neural. Assim, as células sujeitas a maior concentração de shh sintetizam os factores de
transcrição Nkx6.1 e Nkx2.2, tornando-se neurónios ventrais (V3). Os grupos celulares mais
dorsais, sujeitos a cada vez mais factores TGF-β e a menos shh produzem os factores de transcrição
Nkx6.1 e Pax6 e tornam-se neurónios motores. Os dois grupos celulares seguintes, que recebem
progressivamente menos shh, tornam-se os interneurónios V2 e V12,3.
A diferenciação dorso-ventral até aqui referida corresponde ao que se passa na metade
ventral da medula espinhal, da qual se originam os neurónios motores. Porém, da metade dorsal
originar-se-ão neurónios que terão por função a integração de informações sensoriais da periferia. A
organização da parte dorsal da medula espinhal definitiva resulta da migração e rearranjos
controlados das células, durante o desenvolvimento neural inicial. Todos os neurónios que farão
parte da medula espinhal dorsal originam-se no tubo neural dorsal. São quatro os domínios de
8
expressão de genes pró-neurais, que codificam para factores de transcrição da Basic Helix-LoopHelix (bHLH), os que definem as células progenitoras no tubo neural dorsal. Estes diferenciam-se,
originando seis tipos de interneurónios dorsais (dI1-dI6), os quais podem ser distinguidos através do
tipo de factores de transcrição que expressam. Os dados disponíveis até hoje indicam que os genes
pró-neurais são necessários para iniciar o desenvolvimento das diferentes classes de neurónios.
Alguns dos factores expressos são o Math1 (expresso pelas células localizadas dorsalmente,
adjacentes ao roof plate), neurogenina 1 (Ngn1) e Ngn2 (expressas em células localizadas mais
ventralmente) e Mash1 (expresso por precursores dos interneurónios dI3 e dI5). Claramente, muito
há ainda a investigar acerca das células do tubo neural, factores expressos e correlações entre
caracterização anatómica e funcionalidade, mas trata-se de uma área em franca evolução de
conhecimentos, actualmente 6.
6. Malformações associadas ao desenvolvimento do tubo neural
6.1 Definição
“Malformações congénitas do sistema nervoso central e estruturas adjacentes relacionadas
com uma formação anormal do tubo neural durante o primeiro trimestre de gravidez que
geralmente acontece entre dias 18 e 29 de gestação. Malformações da ectoderme e da mesoderme
(envolvendo o crânio e vértebras principalmente) podem acontecer como resultado de defeitos no
fecho do tubo neural. 7”
6.2 Doenças
A anencefalia é um defeito do tubo neural que acontece quando a extremidade cefálica do
tubo neural não fecha, normalmente entre o 23º e 26º dias de gravidez, resultando na ausência de
uma porção principal do encéfalo, crânio e couro cabeludo. Crianças com esta anomalia nascem
sem um encéfalo frontal. O tecido restante do encéfalo está, frequentemente, exposto 8, 9, 10.
A lisencefalia, que literalmente significa “cérebro liso”, é uma malformação de encéfalo rara
caracterizada por microcefalia e falta das circunvoluções normais do cérebro. É causado por uma
migração neuronal defeituosa 9.
9
A megalencefalia é uma condição na qual há um encéfalo anormalmente grande, pesado e
com mau funcionamento. Pensa-se que a megalencefalia está relacionada com uma perturbação na
regulação de reprodução de células ou com a sua proliferação 9.
A Malformação de Chiari é uma condição na qual há protrusão do cerebelo no canal
espinhal. Pode ser ou não aparente ao nascimento 9, 10.
A encéfaloceles é um conjunto de defeitos raros no tubo neural caracterizado por protrusões
do encéfalo e suas membranas nas aberturas no crânio. Estes defeitos são causados pelo insucesso
do tubo neural em se fechar completamente durante o desenvolvimento fetal 9, 10.
A espinha bífida é uma gama de malformações que são o resultado de fecho anormal ou
incompleto da porção caudal do tubo neural. É um defeito do tubo neural (uma desordem que
envolve desenvolvimento incompleto do encéfalo, espinha dorsal, e/ou as suas estruturas
protectoras) causado pela incapacidade da coluna do feto em se fechar correctamente durante o
primeiro mês de gravidez 8, 9.
7. Investigação
O conhecimento sobre como o sistema nervoso se desenvolve e qual o papel dos genes no
desenvolvimento fetal são as metas principais dos investigadores que estudam as doenças
neurológicas congénitas. Estão-se a concentrar esforços no sentido de entender os processos
complexos responsáveis no desenvolvimento normal do cérebro e sistema nervoso e como o seu
impedimento leva a doenças cefálicas. Entender como, por um lado, os genes controlam a migração
das células do cérebro, sua proliferação, diferenciação e morte e, por outro, como a radiação,
drogas, toxinas, infecções e outros factores influenciam estes processos, será um passo em frente na
prevenção10.
A existência de um gene variante, C677T, do gene da enzima 5,10-metilenotetrahidro-folato
redúctase, gene envolvido no processamento do folato, é suficiente para aumentar o risco de se
nascer com uma malformação associada ao tubo neural. Em homozigóticos para o alelo T, do gene
variante C677T, e os heterozigóticos CT estão associados a uma concentração baixa de folato,
10
concentrações altas de homocisteína e actividade enzimática mais baixa do que os homozigóticos
CC, sendo estes efeitos mais evidenciados para os homozigóticos. Estes são factores de risco para
as malformações do tubo neural. Tanto as concentrações baixas de folato como as altas de
homocisteína associadas aos genótipos do tipo CT e TT, podem ser corrigidos através de ácido
fólico. Realça-se a importância da entrada do ácido fólico nos programas de saúde social para todas
as mulheres em idade de engravidar para, assim, evitar as malformações associadas ao tubo neural.
Para além disso, o ácido fólico, previne, também, as doenças cardiovasculares 11.
Resultados obtidos em ensaios clínicos randomizados recolhidos mostraram que, pelo menos
metade dos casos de malformações associadas ao tubo neural podiam ter sido prevenidos se as mães
tivessem ingerido ácido fólico. Aconselha-se a ingestão de 0,4mg de ácido fólico no mês anterior à
concepção e nos três primeiros meses de gravidez. A título de prevenção e, para além da ingestão de
ácido fólico, podem referir-se as ultra-sonografias pré natais e o teste de risco fetal 12, 13.
Foram realizadas análises (SSCA) aos genes de 179 pacientes com espinha bífida com o
objectivo de analisar a BMP4 e o seu inibidor, NOG. A análise revelou quatro mutações para a
BMP4 e apenas uma para o NOG. Os investigadores acreditam que estas mutações, actuando com
outras variantes de genes, podem estar na base do aparecimento da espinha bífida. Em adição, um
estudo de casos e controlos trouxe evidências para um desequilíbrio no genótipo da BMP4 – a
existência da forma variante 455TC (V152A), no exão 5. A frequência de heterozigóticos 455TC é
mais baixa nos casos do que nos controlos, apesar da frequência dos alelos ser semelhante em
ambos os grupos. Uma explicação possível é que ser-se heterozigótico para o 455TC neste local é
um factor de protecção na população normal, apesar de até hoje ainda não ter sido provado 14.
Foi revelada a importância da FGF-1 e da FGF-2 para a proliferação e diferenciação das
células neuronais. Foi demonstrado que as células da zona sub-ventricular do cérebro adulto têm
características de percursores neuronais: elas podem responder à proliferação pela FGF-2 e à
indução da diferenciação pela FGF-1. Aparentemente, a exposição do embrião ao álcool diminui a
11
proliferação da camada ventricular e, consequentemente, reduz o número de neurónios formados, o
que sugere que o álcool é um inibidor da acção das FGF 15.
Neste momento está a ser levado a cabo nos EUA um estudo que tem como objectivo
descrever as condições genéticas que estão na origem da espinha bífida. Encontra-se ainda na fase
de recrutamento de pacientes 16.
8. Conclusão
O desenvolvimento do nosso trabalho permitiu-nos alcançar os objectivos a que nos
propusemos no início. Para nós, foi estimulante toda a abordagem de um tema tão interessante e
actual, particularmente no que se refere à pesquisa e selecção de artigos científicos subordinados a
novas descobertas nesta área.
As principais dificuldades com que nos debatemos foram, por um lado, o facto de sermos de
diferentes turmas e ser complexo conciliar os diferentes horários; por outro, conseguir reunir e
condensar tanta informação escrita e gráfica que existe disponível acerca desta temática num tão
curto limite de páginas.
Apesar de tudo, estamos satisfeitas com a tarefa que levámos a cabo e incentivámos a
continuação da realização deste tipo de trabalhos, uma excelente forma de interiorizar a matéria e de
procurar saber um pouco mais.
9. Agradecimentos
Por último, queremos deixar o nosso especial agradecimento à Drª Sandra Rebelo pela sua
disponibilidade e sugestões para melhorar este trabalho.
9. Bibliografia
1. Williams, P. L., Warwick, R., Dyson, M., Bannister; L. H. (1995) Gray Anatomia. 37ª Edição.
Londres. Editora Guanabra Koogan.
2. Alberts. Principles of Development. 2ª Edição. Wolpert.
3. Gilbert. Development Biology. 6ª Edição.
4. http://escuela.med.puc.d/.../atlas/cap3/priat3.html
5. http://www.forp.usp.br/mef/embriologia/geral.html
12
6. Anderson, T. C. (2003) Patterning cell types in the dorsal spinal cord: what the mouse mutants
say. Nature Publishing Group.
7. Joynt. (1992) Clinical Neurology. 55, pp. 31-41.
8. http://www.wrongdiagnosis.com/n/neural_tube_defect/intro.htm
9. http://www.ninds.nih.gov/disorders/disorder_index.htm
10. http://www.nlm.nih.gov/medlineplus/neuraltubedefects.htm
11. Kirke, P. N., et al. (2004) Impact of the MTHFR C677T polymorphism on risk of neural tube
defects: case-control study. British Medical Journal. 328, pp. 1535 – 1536.
12. Honein, M. A., et al. (2001) Impact of folic acid fortification of the US food supply on the
occurrence of neural tube defects. Journal of the American Medical Association. 285(23), pp. 29812986.
13. Berry, R. J., et al. (1999) Prevention of Neural-Tube Defects with Folic Acid in China. The New
England Journal of Medicine. 341, pp. 1485-1490.
14. Felder B., et al. (2002) Evaluation of BMP4 and its specific inhibitor NOG as candidates in
human neural tube defects (NTDs). [Pubmed]
15. Bartlett P. F., et al. (1994) Regulation of neurogenesis in the embryonic and adult brain by
fibroblast growth factors. [Pubmed]
16. http://www.clinicaltrials.gov/ct/show/NCT00031122?order=5
13