FUNDAÇÃO UNIVERSIDADE FEDERAL DE RONDÔNIA – UNIR
NÚCLEO DE CIÊNCIAS E TECNOLOGIA
DEPARTAMENTO DE QUÍMICA
MARIA CRISTINA NERY DO NASCIMENTO
Análise da Água Superficial e Subterrânea no Entorno do Depósito de
Resíduos Sólidos Urbanos de Porto Velho-RO.
Porto Velho-RO
2009
MARIA CRISTINA NERY DO NASCIMENTO
Análise da Água Superficial e Subterrânea no Entorno do Depósito de
Resíduos Sólidos Urbanos de Porto Velho-RO.
Monografia apresentada ao Departamento de
Química da Fundação Universidade Federal de
Rondônia, como parte dos requisitos para a
obtenção do grau de Licenciado em Química.
Área de Concentração: Meio Ambiente
Orientadora: Profª. Dra. Miyuki Yamashita
Porto Velho-RO
2009
ii
FICHA CATALOGRÁFICA
NASCIMENTO, M. C. N.
Análise da Água Superficial e Subterrânea no Entorno do
Depósito de Resíduos Sólidos Urbanos de Porto Velho-RO. /
Maria Cristina Nery do Nascimento.
Porto Velho/RO. 2009. 69p.
Área de Concentração: Meio Ambiente
Orientadora: Profª. Dra. Miyuki Yamashita
1. Resíduos Sólidos 2. Lixiviação 3. Metais Pesados 4. Água
iii
Análise da Água Superficial e Subterrânea no Entorno do Depósito de
Resíduos Sólidos Urbanos de Porto Velho-RO.
MARIA CRISTINA NERY DO NASCIMENTO
BANCA EXAMINADORA
__________________________________
(Dra. Miyuki Yamashita)
__________________________________
(Dra. Adaiane Spinelli)
__________________________________
(Ms. Elcimar Juarez Forte)
iv
Aos meus pais, Janete e Raimundo,
pelo amor, coragem e dedicação...
Ao meu esposo, Luiz,
pela compreensão e carinho...
Às minhas irmãs, Cláudia e Telma,
pelo apoio e cumplicidade...
Com todo meu amor,
a vocês dedico este trabalho.
v
AGRADECIMENTOS
Agradeço a Deus em primeiro lugar, por ter guiado os meus passos e me ajudado
a superar todos os obstáculos até este momento de minha vida.
À minha orientadora Prof. Dra. Miyuki Yamashita pela paciência, incentivo e
amizade, o que permitiu a elaboração coerente e didática deste trabalho.
À minha família, em especial minha mãe Janete e meu pai Raimundo, por tudo
que me ensinaram e ainda me ensinam no caminhar da vida, pela confiança, incentivo, e
principalmente pelo incondicional amor que me dedicam; ao meu esposo, Luiz, por todo
o amor, apoio, paciência, compreensão e carinho; e às minhas irmãs, Cláudia e Telma,
pelo apoio, cumplicidade e pelos momentos de descontração que me proporcionaram.
À minha família em geral, por sempre torcerem por mim.
À minha amiga Maria José, pela amizade, conselhos, apoio e carinho tão
valiosos.
Ao Prof. Dr. Wanderley Bastos, responsável pelo Laboratório Biogeoquímica
Ambiental, pela colaboração na cessão dos materiais e equipamentos necessários para a
realização deste trabalho.
À equipe do Laboratório de Biogeoquímica Ambiental, em especial a
Alessandra, que me ajudou na tarefa de proceder às análises bacteriológicas. Ao Dario,
que me ajudou na coleta em campo e nas análises de metais pesados. Ao Igor, que
colaborou na confecção de mapas. Pela paciência, ensinamentos e troca de experiências
de todos os membros do laboratório, que foram muito importantes para conclusão deste
trabalho.
Aos meus amigos de turma: Luís, Laerte, Márcia, Railane e Nilton, pelos
momentos de descontração e amizade. Desejo a todos vocês sucesso!
Aos professores, Mariza, Dilcélia, Charles, Aprígio, Avacir, Valdir, Mariângela,
Miyuki, Adaiane e Wiss, pelos conhecimentos transmitidos, além de todos os outros
professores do Departamento de Química, os quais contribuíram também para minha
formação acadêmica.
À associação de moradores da Vila Princesa, na pessoa de Seu Francisco e Seu
Bahia, pela autorização das coletas feitas na área da comunidade, pelas informações
fornecidas e pelo acompanhamento em campo.
vi
“O correr da vida embrulha tudo, a vida é assim:
esquenta e esfria, aperta e daí afrouxa,
sossega e depois desinquieta
O que ela quer da gente é coragem”
Grande Sertão, Veredas - João Guimarães Rosa
vii
SUMÁRIO
LISTAS DE TABELAS
ix
LISTAS DE FIGURAS
x
RESUMO
xi
ABSTRACT
xii
1. INTRODUÇÃO
01
2. REFERENCIAL TEÓRICO
02
2.1 Resíduos sólidos, definição e classificação
02
2.2 Resíduos gasosos e resíduos líquidos
04
2.3 Líquido lixiviado
05
2.4 Sistemas de destinação de resíduos sólidos
07
2.5 Resíduos sólidos no curso d’água
08
2.6 Resíduos sólidos urbanos e a contaminação por metais pesados
10
2.7 Efeitos tóxicos dos metais pesados no ser humano
12
2.8 Espectrometria de absorção atômica
15
2.9 Depósito de resíduos sólidos urbano de Porto Velho-RO
17
3. OBJETIVOS
21
3.1 Geral
21
3.2 Específicos
21
4. METODOLOGIA
22
4.1 Delineamento da pesquisa
22
4.2 Reagentes e soluções
22
4.3 Equipamentos
23
4.4 Pontos de amostragem
23
4.4.1 Mapa da área de estudo
24
viii
4.4.2 Descrição dos pontos amostrados
25
4.5 Coleta e conservação das amostras
28
4.6 Curva de calibração dos metais pesados
29
4.7 Extração química para a determinação de metais pesados
34
4.8 Análise bacteriológica
36
4.9 Análise dos dados
39
5. RESULTADOS E DISCUSSÃO
40
5.1 Parâmetros físico-químicos
40
5.1.1 Condutividade elétrica
40
5.1.2 Potencial Hidrogeniônico (pH)
41
5.1.3 Coliformes fecais e coliformes não fecais
42
5.1.4 Metais pesados
46
6. CONCLUSÕES
49
7. REFERÊNCIAS
50
ANEXO
55
ix
LISTA DE TABELAS
Tabela 01: Densidade dos principais metais pesados
11
Tabela 02: Localização geográfica de cada ponto
23
Tabela 03: Limites de Detecção da Técnica (LDT) para cada elemento
34
analisado.
Tabela 04: Padrões de balneabilidade através da resolução CONAMA nº.
43
274, de 29 de novembro de 2000.
Tabela 05: Padrões de potabilidade para águas subterrâneas, conforme
43
resolução nº. 518, de 25 de março de 2004.
Tabela 06: Resultados das análises físico-químicos e bacteriológicos das
45
amostras de água dos poços e igarapés, localizados no depósito de lixo de
Porto Velho-RO, 2009.
Tabela 07: Resultados das análises físico-químicos e bacteriológicos das
45
amostras de água dos poços e nascentes, localizados no depósito de lixo de
Porto Velho-RO, 2008.
Tabela 08: Valores máximos permitidos para os elementos químicos pela
46
resolução nº. 357, de 25 de março de 2005 (CONAMA).
Tabela 09: Concentração dos metais pesados do Lixão de Porto Velho-RO.
47
x
LISTA DE FIGURAS
Figura 01: Vista externa do lixão de Porto Velho-RO
17
Figura 02: Vista do lixão, obtida de uma estrada lateral de acesso.
19
Figura 03: Mapa com os pontos da amostragem
24
Figura 04: Igarapé Bica do Paulista.
25
Figura 05: Igarapé do Lixão.
26
Figura 06: Poço tubular.
26
Figura 07: Poço tipo amazonas.
27
Figura 08: Poço tipo amazonas.
27
Figura 09: Acondicionamento das amostras em garrafa de polietileno.
28
Figura 10: Amostras em frasco âmbar previamente esterilizado.
29
Figura 11: Curva de calibração do elemento químico Cádmio (Cd).
30
Figura 12: Curva de calibração do elemento químico Chumbo (Pb).
30
Figura 13: Curva de calibração do elemento químico Cobalto (Co).
31
Figura 14: Curva de calibração do elemento químico Cobre (Cu).
31
Figura 15: Curva de calibração do elemento químico Cromo (Cr).
32
Figura 16: Curva de calibração do elemento químico Manganês (Mn).
32
Figura 17: Curva de calibração do elemento químico Níquel (Ni).
33
Figura 18: Curva de calibração do elemento químico Zinco (Zn).
33
Figura 19: Extração química das amostras para a determinação de metais
35
pesados.
Figura 20: Acondicionamento das amostras em tubos de teflon.
35
Figura 21: Espectrofotômetro de absorção Atômica por chama.
36
Figura 22: Método de membrana filtrante.
37
Figura 23: Procedimento membrana filtrante.
38
Figura 24: Placa com colônias de coliformes fecais (E. coli) e coliformes e
38
não fecais.
Figura 25: Condutividade elétrica, nos pontos amostrados.
40
xi
Figura 26: Variação do pH entre os pontos amostrados.
41
Figura 27: Números de coliformes fecais (E. coli) das amostras.
42
Figura 28: Números de coliformes não fecais das amostras.
44
xii
RESUMO
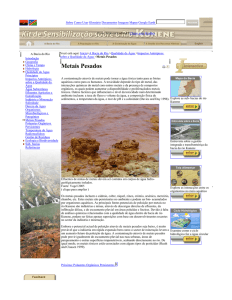
Atualmente, uma das grandes preocupações ambientais está relacionada aos resíduos
sólidos gerados pela sociedade moderna e consumista. Com a intensificação do
processo industrial, aliada ao crescimento da população e a conseqüente demanda por
bens de consumo, o homem tem produzido quantidades significativas de resíduos
sólidos, que acabam sendo constituídos de uma mistura muito complexa e de natureza
diversa. O município de Porto Velho-RO gera em torno de 220 toneladas de lixo urbano
por dia, o qual é disposto em uma área de lixão para resíduos sólidos urbanos desde
1993. O presente trabalho tem como objetivo avaliar as concentrações de metais
pesados (Cd, Cu, Co, Cr, Pb, Mn, Ni e Zn), quantidade de coliformes fecais e
coliformes não fecais, bem como o monitoramento dos parâmetros físico-químicos (pH
e condutividade elétrica) do lixão urbano de Porto Velho-RO. As amostras de água
foram coletadas em cinco pontos: dois igarapés e três poços (um poço tubular e dois
poços amazonas) no mês de abril de 2009. As análises de metais pesados foram
realizadas por espectrometria de absorção atômica por chama (GBC-Avanta). Os testes
bacteriológicos foram realizados pelo método membrana filtrante e o meio de cultura
choromocult. Os parâmetros físico-químicos foram realizados in loco. Os resultados
obtidos foram comparados com os valores máximos permitidos para metais, coliformes
fecais e pH em efluentes líquidos conforme a Resolução nº.357/2005 do Conselho
Nacional do Meio Ambiente (CONAMA) e pela Portaria nº.518/2004 do Ministério da
Saúde (MS). Os resultados obtidos nesse estudo mostram que a água superficial e a
água subterrânea no entorno do lixão municipal, estão com as suas qualidades
comprometidas.
PALAVRAS-CHAVE: 1. Resíduos Sólidos 2. Lixiviação 3. Metais Pesados 4. Água
xiii
ABSTRACT
Actually, a major environmental concern is related to solid waste generated by modern
consumerist society. With the intensification of the industrial process, coupled with
population growth and consequent demand for consumer goods, the man has produced
significant quantities of solid wastes that end up being made of a mixture of very
complex and diverse nature. The municipality of Porto Velho-RO generates around 220
tonnes of urban waste per day, which is provided in an area of landfill for municipal
solid waste since 1993. This study aims to evaluate the concentrations of heavy metals
(Cd, Cu, Co, Cr, Pb, Mn, Ni and Zn), amount of fecal coliform and total coliform
bacteria, as well as monitoring the physical and chemical parameters (pH and electrical
conductivity) of the landfill urban Porto Velho-RO. Water samples were collected at
five points: two streams and three wells (one tube well and two wells Amazon) in April
2009. The analysis of heavy metals was measured by spectrophotometer, atomic
absorption by flame (GBC-Avant). The bacteriological tests were performed by the
membrane filter method and the culture choromocult. The results were compared with
the maximum limits for metals, fecal coliform and pH in effluents in accordance with
Resolution No. 357/2005 of the National Council on the Environment (CONAMA) and
Ordinance No. 518/2004 the Ministry of Health ( MS). The results of this study show
that the surface water and groundwater in the vicinity of the municipal garbage dump,
are its qualities compromised.
KEYWORDS: 1. Solid Waste 2. leaching. 3. Heavy Metals 4. Water
xiv
1 INTRODUÇÃO
A população mundial supera os 6 bilhões de pessoas, enquanto no Brasil, a
população está em torno de 174 milhões de habitantes, a questão dos resíduos sólidos
urbanos (RSU) é preocupante, e cerca de 242 mil toneladas de RSU são produzidos
diariamente, dos quais aproximadamente 90 mil toneladas são resíduos sólidos domésticos.
A produção per capita de resíduos domésticos em áreas urbanas, no país, é em torno de 0,5
kg a 1,0 kg por dia, dependendo do porte da cidade (IPT, 2000).
Os resíduos sólidos são considerados a expressão mais visível e concreta dos riscos
ambientais, ocupando um importante papel na estrutura de saneamento de uma
comunidade urbana e, consequentemente, nos aspectos relacionados à saúde pública. Além
das conseqüências para a saúde comunitária, deve-se considerar ainda o impacto que a
disposição inadequada desses resíduos provoca no solo, na atmosfera, na vegetação e nos
recursos hídricos (MORITZ, 1995).
O gerenciamento dos resíduos sólidos urbanos não tem um manejo seguro e nem
um efetivo fluxo, pois existem muitos impactos sobre a saúde pública e o meio ambiente.
No levantamento realizado pelo IBGE, em agosto de 2000, a situação dos municípios
brasileiros referente à disposição final dos resíduos sólidos urbanos, é a seguinte: 63,6% na
forma de lixão (dispostos a céu aberto), 18,4% em lixão controlado (aterrado) e 13,8% em
aterro sanitário, do qual o percentual restante não foi informado para onde vão seus
resíduos (OLIVEIRA & PASCAL, 2004).
O município de Porto Velho-RO não é uma exceção da situação geral encontrada
no Brasil, e tem a disposição de seu lixo realizada à semelhança de vazadouro, onde o
mesmo é descartado de forma inadequada em depósito de resíduos sólidos urbanos,
“lixão”, sem qualquer técnica ou tratamento. Não foi realizado nenhum estudo técnico
prévio para a escolha daquela área e, tampouco montada, antes de sua instalação, uma infra
estrutura que fosse capaz de evitar os danos conseqüentes da disposição de grandes
quantidades diárias de lixo (NEUBAUER et al., 1999).
De acordo com a Secretária Municipal de Serviços Públicos (SEMUSP), este
depósito a céu aberto teve início em 1993. A disposição final dos resíduos sólidos urbanos
coletados em Porto Velho é feita em uma área de 51 ha. Desse total, aproximadamente
50% já está ocupado com os resíduos. A área restante corresponde a Vila Princesa, um vale
com nascentes e uma floresta parcialmente nativa (KREBS et al., 1999).
1
Estudos de poluição das águas desses locais mostram que todo lixão pesquisado
provoca algum tipo de poluição nas mesmas. Desta forma é de se presumir que lixões
poderão estar alterando a qualidade da água. Assim, preocupações com a contaminação dos
recursos hídricos, decorrente da presença de metais pesados provenientes da inadequada
disposição de resíduos sólidos, conduzem pesquisadores a direcionar seus objetivos de
pesquisa a estes problemas (OLIVEIRA & PASCAL, 2004).
Baseado nas informações citadas, é importante fazer um monitoramento da águas
superficiais e subterrâneas sobre os parâmetros: níveis de concentração de metais pesados
(Cd, Co, Pb, Mn, Ni, Cu, Zn e Cr), parâmetros físico – químicos (condutividade elétrica e
pH) e bacteriológicos (coliformes fecais e coliformes totais) na área do lixão de Porto
Velho – RO. Justifica – se a necessidade deste monitoramento, devido ao fato de o local do
depósito de resíduos sólidos estar a uma distância de, aproximadamente, 4 km da margem
do Rio Madeira e a preocupação pela saúde da comunidade que habita no entorno do
depósito.
2 Referencial Teórico
2.1 Resíduos sólidos, definição e classificação
Definem – se resíduos sólidos como o conjunto dos produtos não aproveitados das
atividades humanas (domésticas, comerciais, industriais, de serviço de saúde) ou aqueles
gerados pela natureza, como folhas, galhos, terra, areia, que são retirados das ruas e
logradouros pela operação de varrição e enviados para os locais de destinação ou
tratamento. Também podemos definir lixo como: os restos das atividades humanas,
considerados pelos geradores como inúteis, indesejáveis ou descartáveis. Normalmente,
apresentam – se sob estado sólido, semi – sólido ou semilíquido.
São várias formas possíveis de se classificar o lixo, por sua natureza física (seco e
molhado), por sua composição química (matéria orgânica e matéria inorgânica), pelos
riscos potenciais (perigosos e não–inertes). Normalmente, os resíduos são definidos
segundo sua origem e classificação de acordo com o seu risco em relação ao homem e ao
meio ambiente, em resíduos urbanos e resíduos especiais.
De acordo com Ambiente Brasil (2007) os resíduos sólidos são classificados em:
2
Os resíduos urbanos ou lixo doméstico: gerados nas residências, no comércio ou
em outras atividades desenvolvidas nas cidades. Incluem – se neles os resíduos dos
logradouros públicos, como ruas e praças, denominado lixo de varrição ou público. Nestes
resíduos encontram – se: papel, papelão, vidro, latas, plásticos, trapos, folhas, galhos e
terra, restos de alimentos, madeira e todos os outros detritos apresentados à coleta nas
portas das casas, pelos habitantes das cidades ou lançados nas ruas.
Domiciliar: originado da vida diária das residências, constituído por setores de
alimentos (tais como, casca de frutas, verduras, etc.), produtos deteriorados, jornais e
revistas, garrafas, embalagens em geral, papel higiênico, fraldas descartáveis e uma grande
diversidade e outros itens. Contém, ainda, alguns resíduos que podem ser tóxicos.
Comercial: originado dos diversos estabelecimentos comerciais e de serviços, tais
como, supermercados, estabelecimentos bancários, lojas, bares, restaurantes etc.
Público: originado dos serviços de limpeza urbana, incluindo todos os resíduos de
varrição das vias públicas, limpezas de praias, de galerias, de córregos e de terrenos, restos
de podas de árvores, limpeza de feiras livres, constituído de restos vegetais diversos,
embalagens, etc.
Os resíduos especiais: gerados em indústrias ou em serviços de saúde, como
hospitais, ambulatórios, farmácias, clínicas que, pelo perigo que representam à saúde
pública e ao meio ambiente, exigem maiores cuidados no seu acondicionamento,
transporte, tratamento e destino final. Também se incluem nesta categoria os materiais
radioativos, alimentos ou medicamentos com prazos de validade vencidos ou deteriorados,
resíduos de matadouros, inflamáveis, corrosivos, reativos, tóxicos e dos restos de
embalagem de inseticida e herbicida empregados na área rural.
Hospitalar: constitui-se dos resíduos sépticos, ou seja, que contêm ou
potencialmente podem conter germes patogênicos. São produzidos em serviços de saúde,
tais como: hospitais, clínicas, laboratórios, farmácias, clínicas veterinárias, postos de saúde
etc. São agulhas, seringas, gazes, bandagens, algodões, órgãos e tecidos removidos, meios
de culturas e animais usados em testes, sangue coagulado, luvas descartáveis, remédios
com prazos de validade vencidos, instrumentos de resina sintética, filmes fotográficos de
raios X etc. Em função de suas características, merece um cuidado especial em seu
3
acondicionamento, manipulação e disposição final. Deve ser incinerados e os resíduos
levados para aterro sanitário.
Portos, aeroportos, terminais rodoviários e ferroviários: constituem os resíduos
sépticos, ou seja, que contêm ou potencialmente podem conter germes patogênicos.
Basicamente originam-se de material de higiene pessoal e restos de alimentos, que podem
hospedar doenças provenientes de outras cidades, estados e países.
Industrial: originado nas atividades dos diversos ramos da indústria, tais como,
metalúrgica, química, petroquímica, papelaria, alimentícia etc. O lixo industrial pode ser
representado por cinzas, lodos, óleos, resíduos alcalinos ou ácidos, plásticos, papel,
madeira, fibras, borracha, metal, escórias, vidros, cerâmicas e etc.
Radioativos: resíduos provenientes da atividade nuclear (resíduos de atividades
com urânio, césio, tório, radônio, cobalto), que devem ser manuseados apenas com
equipamentos e técnicos adequados.
Agrícola: resíduos sólidos das atividades agrícolas e da pecuária, como as
embalagens de adubos, dos defensivos agrícolas, ração, resto de colheita etc. O lixo
proveniente de pesticidas é considerado tóxico e necessita de tratamento especial.
Entulhos: resíduos de construção civil, demolições e restos de obras, solos de
escavações. O entulho é, geralmente, um material inerte, passível de reaproveitamento.
2.2 Resíduos gasosos e resíduos líquidos
Os resíduos gasosos resultam das reações de fermentação aeróbia (desenvolvidos
na superfície) e anaeróbia (nas camadas mais profundas); a fermentação anaeróbia dá
origem a CO2 (dióxido de carbono) e a CH4(metano), o qual pode ser aproveitado para a
produção de biogás.
Os resíduos líquidos, também chamados lixiviados ou chorume variam de local
para local e dependem de: teor em água dos resíduos; isolamento dos sistemas de
drenagem; clima (temperatura, pluviosidade, evaporação); permeabilidade do substrato
geológico; grau de compactação dos resíduos; idade dos resíduos. Os lixiviados têm
4
elevada concentração de matéria orgânica, de materiais tóxicos, pelo que deve ser feita a
sua recolha e tratamento, de modo a impedir a sua infiltração no solo. Devido à grande
distância em que normalmente os aterros sanitários se encontram, tornam muitas vezes
inviável o acesso a esse tipo de destino final. A prática mais generalizada é o enterramento
de resíduos em terrenos adjacentes, muitas vezes sem preparação, em solos inadequados e
perto de espécies faunísticas e florística de elevada fragilidade, o que dá origem a focos de
poluição e de contaminação localizados. Uma forma de minimizar esses efeitos é a seleção
cuidadosa do local (tipo de solo, cobertura vegetal e regime hidrológico), sua
impermeabilização e seu recobrimento sistemático com terra (AMBIENTE BRASIL,
2007).
2.3 Líquido lixiviado
O lixo sofre um processo de liquefação ao ser decomposto, devido à digestão
praticada pelas bactérias, formando um caldo escuro e ácido denominado chorume
(lixiviado ou percolado).
Além disso, há naturalmente o problema do mau cheiro que se desprende sempre
que o lixo se decompõe por fermentação anaeróbia (BRANCO, 1997).
O líquido lixiviado (chorume ou percolado) é um líquido poluente originado da
decomposição do lixo. O chorume, ou líquido percolado, cuja composição é muito
variável, pode tanto escorrer e alcançar as coleções hídricas superficiais, como infiltrar no
solo e atingir as águas subterrâneas, comprometendo sua qualidade e, por conseguinte, seu
uso (SISINNO et al., 1997).
O chorume possui elevada carga de poluentes orgânicos e inorgânicos e, ao entrar
em contato com o solo, pode modificar, de forma intensa, suas características físicas,
químicas e biológicas, bem como as das águas subterrâneas, caso consiga alcançá-las.
A matéria orgânica presente no chorume tem importância na complexação e
transporte de metais pesados e na retenção de alguns contaminantes orgânicos. Aliado a
que a matéria orgânica natural presente no solo, além de participar desses processos, pode
aumentar a concentração de constituintes do chorume no solo e, consequentemente, nas
águas (LEITE et al., 2004).
5
O potencial de impacto deste efluente está relacionado com a alta concentração de
matéria orgânica, presença de metais pesados e de substâncias recalcitrantes.
A quantidade de líquido lixiviado produzido em um lixão depende de vários fatores
como: condições meteorológicas do local (umidade, precipitação, evaporação, temperatura
e ventos); geologia e geomorfologia (escoamento superficial e/ou infiltração subterrânea,
grau de compactação e capacidade do solo em reter umidade); condições de operação do
aterro (conformação e cobertura das células, grau de compactação dos resíduos, tipo de
equipamento, recirculação do percolado); idade e natureza dos resíduos sólidos (tipo,
umidade, nível de matéria orgânica, características); topografia (área e perfil do lixão);
qualidade e quantidade de recicláveis e hábitos da população. A composição do chorume
geralmente muda de um lixão para outro em função da qualidade e características dos RSU
(TORRES et al., 1997).
O volume de lixiviado é representado como os fenômenos físicos da percolação em
um maciço homogêneo constituído por um material poroso. Da água que precipita sobre o
aterro, parte é devolvida à atmosfera pela evapotranspiração, parte escoa superficialmente
e o restante se infiltra, podendo ficar retida na camada de cobertura ou produzir um fluxo
de percolação quando for atingida a saturação desta camada (ROCCA et al., 1993).
A infiltração da precipitação, através do solo, é um processo natural, e faz parte do
ciclo de recarga do lençol freático. A percolação é a infiltração de água através dos
resíduos sólidos, carreando com ela, as substâncias solúveis suspensas no mesmo; e a
lixiviação é a operação que separa certas substâncias, contidas nos resíduos sólidos, por
meio de lavagem ou de percolação (OLIVEIRA & PASCAL, 2004).
Os resíduos sólidos inicialmente agem como uma esponja e simplesmente
absorvem a água. Entretanto, o material atinge um teor de umidade conhecida como
capacidade de retenção. Qualquer acréscimo de água adicional resulta na percolação de
igual quantidade da massa. Alguma percolação poderá forma-se antes que a capacidade de
retenção tenha sido atingida, porque os resíduos, não sendo homogêneos, apresentam
canais, e alguns destes, também não absorvem a água prontamente. A absorção do
lixiviado irá variar em função do subsolo. Quando aumenta o nível de água no local do
lixão, surgem dois efeitos indesejáveis: primeiro, considerando o aumento da pressão do
percolado, irá aumentar a taxa de vazamento do líquido percolado no local, agravando o
risco de possível contaminação da água subterrânea; segundo, é que, em tais
circunstâncias, o nível de água contaminada, pode alcançar às fontes da superfície
(SCHALCH, 1984).
6
2.4 Sistemas de destinação de resíduos sólidos
Historicamente, existem três formas básicas adotadas pela sociedade urbana para a
disposição de resíduos sólidos: lixão ou vazadouro, aterro controlado e aterro sanitário
(CHARNOCK & WELLS, 1985).
Os lixões ou vazadouros resultam da simples descarga do lixo a céu aberto, sem
levar em consideração: a área em que está sendo feito à descarga, a percolação dos líquidos
derivados da decomposição do lixo, a liberação de gases para a atmosfera e a proliferação
de insetos, roedores e outros animais que podem transmitir doenças ao homem (SERRA et
al., 1998).
Aterro controlado diferencia-se dos lixões apenas pelo fato do lixo não ficar
exposto a céu aberto, por ser periodicamente coberto com terra. O solo não é
impermeabilizado e nem sempre possui sistema de drenagem dos líquidos percolados,
tampouco captação de gases formados pela decomposição da matéria orgânica.
Aterro sanitário refere-se a uma instalação previamente planejada para a posterior
disposição de resíduos sólidos, visando a não causar danos, nem perigo, ao meio ambiente
e à saúde pública (MUÑOZ, 2002).
Um aterro sanitário é a mais adequada forma de disposição de resíduos no solo.
Porém, apresenta os maiores custos de implantação. Uma vez que são aplicadas técnicas de
impermeabilização e contenção de líquidos percolados para impedir o contato direto dos
mesmos com o solo e os mananciais hídricos superficiais e subterrâneos. Estes líquidos
percolados, conhecidos como chorume, são também submetidos a tratamento, geralmente
em uma lagoa de estabilização, antes da sua introdução no sistema de drenagem superficial
(KREBS et al., 1999).
Segundo dados da PNSB – Pesquisa de saneamento 2000 (IBGE, 2002) somente
32,2% de todos os municípios destinam adequadamente seus resíduos sólidos (13,8% em
aterros sanitários e 18,4% em aterros controlados). Em 63,6% dos municípios, o lixo,
quando recolhido, é apenas transportado para os lixões. Estes não possuem nenhum tipo de
controle, quer quanto ao tipo de resíduos recebidos, quer em relação às medidas de
seguranças necessárias para minimizar ou evitar emissões de poluentes para o meio
ambiente.
A disposição inadequada dos resíduos sólidos promove a contaminação do solo, do
ar e das águas superficiais e subterrâneas, além da proliferação de vetores de doenças,
7
influenciando negativamente a qualidade ambiental e a saúde da população (LEITE et al.,
2004).
Com relação à disposição final dos resíduos sólidos, constata-se hoje que nenhum
dos locais até agora utilizados atende plenamente aos critérios sanitários e ambientais
exigidos pelos órgãos responsáveis. Esta prática tem sido fator de conflito de uso do solo e,
na maioria das vezes, resulta em um comprometimento da qualidade de vida da população
do entorno, devido à poluição do ar, da água e à degradação do solo. O lixo, espalhado
aleatoriamente, propicia a poluição atmosférica pela fumaça emanada da combustão não
controlada dos resíduos e odores desagradáveis resultantes da decomposição da matéria
orgânica. Os líquidos percolados, oriundos da massa de lixo, geralmente contaminam os
cursos d’água e, em casos mais graves, contaminam também as águas subterrâneas
(KREBS et al, 1999).
2.5 Resíduos sólidos no curso d’água
Podemos classificar os danos causados pela disposição do lixo no curso d’água da
seguinte forma: poluição física, química, bioquímica e biológica.
Poluição física: os mecanismos de poluição das águas são desenvolvidos a partir
do momento em que resíduos industriais e domésticos são lançados nos cursos d’água,
causando uma série de perturbações físicas. Estas perturbações são verificadas nas
variações do gradiente de temperatura e sedimentos inertes. Podem, ainda, trazer impactos
mais graves ao meio aquático, como por exemplo, a possível quebra do ciclo vital das
espécies, tornando a água biologicamente estéril (LIMA, 1983).
O aumento da temperatura da água diminui a quantidade de oxigênio que ela pode
reter em solução. Desta forma, os seres que habitam o meio aquático necessitam consumir
maiores volumes de água para conseguir o oxigênio exigido pelo metabolismo.
Poluição química: a poluição química dos recursos hídricos surge, em função de
resíduos industriais não-biodegradáveis e resíduos, e pelo uso intensivo de herbicidas,
fungicidas e outros.
Os resultados deste fenômeno podem ser verificados nos próprios locais de despejo
ou a determinadas distâncias deste local. As formas aparentes de revelação deste processo
8
são verificadas através da mudança de coloração das águas, da formação de correntes
ácidas e águas tóxicas (LIMA, 1983).
Poluição bioquímica: a poluição das águas superficiais ou subterrâneas, pelo lixo,
é propiciada por uma série de fenômenos naturais como a lixiviação, percolação e
arrastamento. A primeira conseqüência é a redução do nível de oxigênio presente na água.
Dependendo da intensidade deste processo, muitos danos podem ocorrer inclusive à
completa extinção da fauna e flora aquática (LIMA, 1983).
A descarga do chorume nas águas provoca depressão do nível de oxigênio,
elevando a DBO (demanda bioquímica de oxigênio). Quando o oxigênio desaparece ou é
reduzido a níveis baixos, os organismos aeróbios são quase que totalmente exterminados,
cedendo lugar aos anaeróbicos, responsáveis pelo desprendimento de gases (LUZ, 1969).
Mesmo após parar de receber lixo, o aterro continua a produzir chorume por cerca
de 50 anos (AL-MUZAINI, 1995). Sua composição físico-química é extremamente
variável dependendo de vários fatores que vão desde as condições ambientais locais, tempo
de disposição, forma de operação do aterro e até altas concentrações de sólidos suspensos,
metais pesados, compostos orgânicos originados da degradação de substâncias. Por
apresentar substâncias altamente solúveis, pode contaminar as águas do subsolo nas
proximidades do aterro. A presença do chorume em águas subterrânea pode ter
conseqüências extremamente sérias para o meio ambiente e para a saúde pública, por
apresentar compostos altamente tóxicos. Sua toxicidade não pode ser associada a uma
substância isoladamente e nem à soma de todas as substâncias presentes, mas sim ao efeito
sinérgico entre as diferentes substâncias existentes (SERAFIM et al, 2003). O chorume é
bem mais agressivo que o esgoto e precisa de um tratamento adequado. O tratamento do
chorume é uma medida de proteção ambiental, de manutenção da estabilidade do aterro e
uma forma de garantir uma melhor qualidade de vida para a população local.
Poluição biológica: normalmente um corpo d’água é habitado por muitos seres
vivos, dentre os quais podemos incluir os microrganismos (bactérias) que se alimentam de
matéria orgânica (responsáveis pela limpeza do rio). Além dos microrganismos próprios
dos rios, o mesmo recebe outras bactérias procedentes de cargas de esgotos que podem
prejudicar seriamente a saúde da população que faz uso desta água para seu consumo
diário. Essas bactérias são chamadas de coliformes (SERAFIM et al., 2003).
9
Os coliformes não fecais são constituídos pelos gêneros Citrobacter, Enterobacter
e Klebsiella, que estão presentes no solo e nos vegetais. Desta forma, não é possível
afirmar categoricamente que uma amostra de água com resultado positivo para coliformes
totais tenha entrado em contato com fezes (JAWETZ, 1989). Então Coliformes Totais =
Coliformes Fecais + Coliformes Não Fecais.
2.6 Resíduos sólidos urbanos e a contaminação por metais pesados
O gerenciamento de resíduos perigosos tem – se transformado, nas últimas décadas,
em um dos temas ambientais mais complexos. O número crescente de materiais e
substâncias identificadas como perigosas e a produção desses resíduos em quantidades
cada vez maiores, têm exigido soluções mais eficazes e investimentos maiores por parte de
seus geradores e da sociedade em geral. Além disso, com a industrialização crescente dos
países ainda em desenvolvimento, esses resíduos passam a ser gerados em regiões nem
sempre preparadas para processá-los ou, pelo menos, armazená-los e tratá–los
adequadamente (MUÑOZ, 2002).
As atividades com maior potencial de geração de resíduos perigosos são as
indústrias químicas, as refinarias de petróleo, a siderurgia, as indústrias de metais não
ferrosos, de papel e celulose, de processamento de couros e de instalações que executam
serviços de galvanoplastia, decapagem e pintura. Poder–se-ia mesmo afirmar que toda a
atividade industrial pode gerar algum tipo de resíduo classificado como perigoso pela
legislação ambiental (EYER, 1995).
Por outro lado, existem também os resíduos dos serviços de saúde (RSS), que
representam um risco à saúde humana e ambiental, pela presença, principalmente de
agentes biológicos, além de uma série de contaminantes químicos presentes nesses
resíduos, dentre os quais destacam–se os metais pesados (OSHA, 1991; TAKAYANAGUI,
1993; ALLERMAN & POULSEN, 2000; TAKAYANAGUI, 2000).
A expressão “metal pesado” é comumente utilizada para designar metais
classificados como poluentes, englobando um grupo muito heterogêneo de metais, semimetais e mesmo não metais como o selênio. Na lista de metais pesados estão, com maior
freqüência, os seguintes elementos: cobre, ferro, manganês, molibdênio, zinco, cobalto,
níquel, vanádio, alumínio, prata, cádmio, cromo e chumbo (CETESB, 2001).
10
A classe de metais pesados compreende o maior grupo dos elementos químicos,
sendo o termo “metal” referente às características de boa condutividade elétrica e térmica.
Compreende–se como “metais pesados” elementos cuja densidade excede 5,0g/cm3
(Tabela 01), (BAIRD, 2002; FOSTNER & WITTMANN, 1979 apud GALVÃO, 2003).
Tabela 01: Densidade dos principais metais pesados.
METAL (Símbolo)
CHUMBO (Pb)
DENSIDADE (g/cm3)
11,3
COBRE (Cu)
8,9
CROMO (Cr)
7,2
NÍQUEL (Ni)
8,9
COBALTO (Co)
8,9
ZINCO (Zn)
7,1
CADMIO (Cd)
8,4
MANGANÊS (Mn)
7,4
Fonte: Química Ambiental (BAIRD, 2002).
Metais pesados como chumbo, mercúrio, cádmio, arsênio, cromo, zinco e
manganês, dentre outros, estão presentes em diversos tipos dos resíduos levados para
lixões, aterros sanitários e incineradores, podendo ser encontrados nesse material:
lâmpadas, pilhas galvânicas, baterias, resto de tintas, resto de produtos de limpeza, óleos
lubrificantes usados, solventes, embalagens de aerossóis, resto de amálgama utilizada em
consultórios odontológicos, materiais fotográficos e radiográficos, embalagens de produtos
químicos, pesticidas, fungicidas e inseticidas, componentes eletrônicos descartados
isoladamente em placas de circuitos impressos, resíduos de produtos farmacêuticos,
medicamentos com prazos de validade vencidos, latarias de alimentos, aditivos
alimentares, e plásticos descartados (EYER, 1995).
A concentração de metais pesados no meio ambiente, com sua disseminação no
solo, água e atmosfera tem sido motivo de crescente preocupação no mundo. Os metais
pesados podem ser percolados por meio do chorume, que é o líquido resultante da
11
decomposição de resíduos. O chorume mistura-se com a água da chuva e outros líquidos,
originalmente existentes no lixo, infiltrando-se no solo e, quando alcança o lençol freático,
contamina a água subterrânea. A contaminação dessas águas tem consequências que
perduram por tempo indefinido e são de difícil controle. Além de provocar a contaminação
da água, essa disposição inadequada polui também o solo, atingindo as plantas, os animais
e o homem (MAGOSSI & BONACELLA, 1991; SERRA et al, 1998).
Por outro lado, a incineração de lixo forma materiais particulados que transportam
metais pesados, dioxinas e furanos policlorinados, que são carregados pela fumaça e
levados pelo vento, precipitando-se no solo contaminando, assim, o ambiente. Os metais
pesados, uma vez no solo, podem ser assimilados pelos vegetais, podendo ter um efeito
fitotóxico para o homem ao serem introduzidos na cadeia alimentar (GLASSER &
CHANG, 1991; SERRA et al, 1998, CERQUEIRA & ALVES, 1999).
Durante a incineração, os metais pesados são particularmente importantes pela
resistência que possuem; elementos cuja concentração é a mesma. Antes e depois da
incineração. Estes metais tóxicos são volatilizados e logo condensados na superfície das
partículas de cinza suspensas no ar, podendo passar para vegetação ou solo, e por sua vez,
podem ser facilmente inaladas ou ingeridas pelo homem (DENISON & SILBERGELD,
1988; SERRA et al, 1998).
2.7 Efeitos tóxicos dos metais pesados no ser humano
A toxicidade dos metais pesados depende, em grande parte, da forma química do
elemento, isto é, de sua especiação. Por exemplo, os quatro elementos Hg, Pb, Cd e As, nas
suas formas de elementos livres condensados, não são particularmente tóxicos. Porém, os
quatro são tóxicos nas suas formas catiônicas e também quando ligados a cadeias curtas de
átomos de carbono. Do ponto de vista bioquímico, o mecanismo de sua ação tóxica deriva
da forte afinidade dos cátions pelo enxofre. Assim, os grupos sulfidrila que ocorrem
comumente nas enzimas que controlam a velocidade de reações metabólicas de
importância crítica no corpo humano, ligam-se rapidamente aos cátions de metais pesados
ingeridos ou a moléculas contendo tais metais. Pelo fato de a ligação resultante metalenxofre afetar a enzima como um todo, ela não pode atuar com normalidade, e em
12
conseqüência, a saúde humana vê-se afetada de maneira desfavorável, às vezes fatal
(BAIRD, 2002).
A toxicidade do elemento químico também depende da dose (quantidade
absorvida), mesmo os elementos ditos essenciais podem vir a serem tóxicos, se absorvidos
acima dos limites toleráveis para o funcionamento normal dos seres vivos. Ferro e cobre
são elementos essenciais para os seres vivos, mas um ser humano adulto possui apenas 5g
de Fe e 0,8g de Cu em seu corpo. Isso mostra que a absorção de quantidades extras desses
metais mesmo pequenas, já pode causar desequilíbrios biológicos. O excesso de um
elemento pode inclusive produzir deficiência de outro (ou outros) em um ser vivo. Por
exemplo, elementos desnecessários podem saturar sítios metabólicos importantes,
impedindo a fixação, transporte e utilização de elementos essenciais ao organismo,
alterando assim as atividades fisiológicas e causando problemas de saúde. É o caso do
excesso de Pb no organismo, o qual irá interferir na absorção dos elementos Ca, Fe, Cu e
Zn, considerados essenciais (MELLO, 2003).
Outros elementos-traços (os não essenciais), como Hg, Pb, Cd, Cr e Ni, entretanto,
não têm função biológica conhecida e são geralmente tóxicos a uma grande variedade de
organismos. Mesmo aqueles elementos com função biológica definida podem quando em
grandes concentrações, apresentar alta toxicidade aos organismos vegetais e animais.
As principais características de alguns metais pesados, citados por Damasceno
(1996), são:
Cádmio (Cd): com densidade 8,6 g/cm3; é utilizado em indústrias de
galvanoplastia, na fabricação de baterias, em tubos de televisão, lâmpadas fluorescentes,
utilizado, também, como pigmento e estabilizador de plásticos polivinílicos. As águas não
poluídas contêm menos do que 1mg/L de Cd, e no caso de contaminação das águas
superficiais, esta se dá por descarga de resíduos industriais e lixiviação de lixão, ou de
solos que recebem lodo de esgoto. As principais vias de exposição ao Cd são os alimentos,
a água para o consumo humano, ar, cigarros e exposição industrial. Os efeitos de
intoxicação aguda por Cd são muito sérios, entre eles: hipertensão, problemas nos rins,
destruição dos tecidos dos testículos e destruição dos glóbulos vermelhos do sangue.
Acredita-se que grande parte da ação fisiológica do Cd é devido a sua similaridade ao Zn;
o Cd pode substituir o Zn em algumas enzimas, causando alterações e impedindo a
atividade catalítica de tais enzimas.
13
Chumbo (Pb): com densidade de 11,34 g/cm3; é utilizado na fabricação de
baterias, sendo usado, também, na gasolina, em pigmentos, munição e soldas. O teor de Pb
em rios e lagos encontra-se na faixa de 1 a 10mg/L, porém valores maiores têm sido
registrados onde a contaminação tem ocorrido como resultado de atividades industriais. As
principais vias de exposição ao Pb são a água para consumo humano, alimentos, ar,
cigarros. A toxidade aguda causada pelo Pb provoca várias disfunções nos rins, no sistema
reprodutivo, fígado, no cérebro e sistema nervoso central. A vítima pode ter dores de
cabeça e dores musculares, sentindo-se facilmente cansada e irritada e a toxicidade
moderada pode causar anemia.
Cromo (Cr): com densidade de 7,19 g/cm3; é usado na fabricação de ligas
metálicas empregadas nas indústrias de transporte, construções e fabricação de
maquinários, na fabricação de tijolos refratários; utilizado, também, na indústria têxtil,
fotográfica e de vidros. Os níveis de Cr na água, geralmente, são baixos (9,7mg/L), embora
níveis maiores já tenham sido relatados como conseqüência do lançamento nos rios de
resíduos contendo este metal. O Cr é um elemento essencial ao ser humano, que se mostra
necessário para o metabolismo da glicose, lipídeos e para a utilização de aminoácidos em
vários sistemas; parece ser necessário, também, para a prevenção de diabete e
arteriosclerose. As principais vias de exposição ao Cr são água para consumo humano,
alimentos, ar, cigarros. A forma hexavalente do Cr é reconhecida como carcinogênica,
causando câncer no trato digestivo e nos pulmões, podendo causar, também, dermatites e
úlceras na pele e nas narinas. Os níveis de 10 mg/kg de peso corporal o Cr6+ pode causar
necroses no fígado, nefrites e morte, e a níveis inferiores podem ocorrer irritações na
mucosa gastrointestinal.
Níquel (Ni): com densidade de 8,90 g/cm3; é utilizado na produção de ligas, na
indústria de galvanoplastia, na fabricação de baterias juntamente com o Cd (baterias NiCd), em componentes eletrônicos, produtos de petróleo, pigmentos e como catalisadores
para hidrogenação de gorduras. Problemas significantes de contaminação de águas com Ni
estão associados com a descarga de efluentes industriais contendo altos níveis desse metal.
Normalmente os níveis de Ni nas águas superficiais variam entre 5 a 20mg/L. As
principais vias de exposição ao Ni são a água para consumo humano, alimentos, ar,
exposição industrial, cigarros. O Ni, relativamente, não é tóxico e as concentrações a que,
normalmente, o homem encontra-se exposto são aceitáveis. As concentrações tóxicas de Ni
14
podem causar muitos efeitos, entre eles, o aumento da interação competitiva com cinco
elementos essenciais (Ca, Co, Cu, Fe, e Zn) provocando efeitos mutagênicos pela ligação
do Ni aos ácidos nucleicos, indução de câncer nasal, pulmonar e na laringe, indução ao
aparecimento de tumores malignos nos rins e também apresentar efeitos teratogênicos.
Zinco (Zn): com densidade de 7,14 g/cm3; é empregado na galvanização de
produtos de ferro; utilizado em baterias, fertilizantes, lâmpadas, televisores e aros de rodas;
componentes de Zn são usados em pinturas, plásticos, borrachas, em alguns cosméticos e
produtos farmacêuticos. O Zn é um elemento essencial, com uma média diária necessária
de 10 a 20 mg; tem uma função na síntese e metabolismo de proteínas e ácidos nucleicos e
na divisão mitótica das células. Este material tende a ser menos tóxico que os outros metais
pesados, porém, os sintomas de toxidade por Zn são vômitos, desidratação, dores de
estômago, náuseas, desmaios e descoordenação dos músculos. O Zn mostra uma relação
fortemente positiva sobre o Cd, à hipertensão induzida pelo Cd pode ser reduzida pelo Zn.
2.8 Espectrometria de absorção atômica
A espectrometria de absorção atômica se baseia na quantidade de radiação
absorvida pelos átomos neutros no estado fundamental do elemento de interesse, os quais
são produzidos no nebulizador-queimador. Esta absorção é proporcional à população de
átomos no estado fundamental, os quais, por sua vez, são proporcionais à concentração da
solução distribuída na chama. A quantidade absorvida é medida pela diferença entre o sinal
transmitido na presença e na ausência do elemento a ser determinado (CIENFUEGOS &
VAITSMAN, 2000).
Para que o processo da absorção atômica ocorra, é necessária a produção de átomos
livres no estado fundamental.
Nos instrumentos com chama, o processo de obtenção destes átomos inicia-se com
a nebulização da amostra em solução. A amostra é aspirada, transformada em fino aerosol
e misturada com gases combustíveis e oxidantes que produzem a chama. As finas gotículas
são transportadas até a mesma, aquecidas e dessolvatadas, sendo o solvente eliminado,
formando pequenas partículas de material sólido. Com mais calor, ocorre liquefação e
vaporização da amostra. Neste momento, o elemento a ser analisado, também chamado
15
analito, ainda está na forma de moléculas. Aplicando-se mais energia, estas moléculas
dissociam-se e transforma-se em átomos livres. O número de átomos livres no estado
fundamental, formado nesta etapa, irá determinar a quantidade de radiação absorvida. A
concentração da solução em análise pode ser obtida através da comparação de sua
absorvância com uma solução-padrão com concentração exatamente conhecida
(CIENFUEGOS & VAITSMAN, 2000).
Cada elemento possui um número específico de elétrons na estrutura orbital, que
está associada ao núcleo. A configuração orbital normal e mais estável de um átomo é
chamada de estado fundamental.
Quando se aplica certa quantidade de energia ao átomo, ela será absorvida e
ocorrerá a promoção de um elétron mais externo para a configuração menos estável,
conhecida como estado excitado (CIENFUEGOS & VAITSMAN, 2000).
Como esse estado é instável, o átomo retorna espontaneamente ao estado
fundamental, liberando energia luminosa com comprimento de onda diretamente
relacionado com a transição eletrônica que ocorre.
Para se dispor de átomos no estado excitado, a amostra deve ser submetida a um
ambiente de alta energia térmica, com a chama ou plasma. O espectro de emissão de um
elemento consiste em um conjunto de comprimentos de onda, chamados linhas de emissão,
devido à natureza discreta dos comprimentos de onda emitidos. A intensidade de uma linha
de emissão aumenta com o aumento do número de átomos excitados do elemento
(CIENFUEGOS & VAITSMAN, 2000).
No processo da absorção atômica, o átomo, no estado fundamental, absorve energia
luminosa de um dado comprimento de onda, para passar ao estado excitado.
Aumentando-se o número de átomos no percurso luminoso, a absorção da luz
também aumenta, e por sua medida pode-se determinar a quantidade de espécie de
interesse. Portanto, o uso de fontes de emissão de radiação luminosa e a seleção cuidadosa
de comprimento de onda permitem a determinação de diversos elementos.
Na absorção atômica a única função da chama consiste em converter o aerosol em
vapor atômico, capaz de absorver luz de uma fonte primária de energia como, por
exemplo, as lâmpadas de catodo oco (CIENFUEGOS & VAITSMAN, 2000).
16
2.9 Depósito de resíduos sólidos urbanos de Porto Velho - RO
Até meados de 1992, a disposição final dos resíduos sólidos gerados pela
população de Porto Velho era realizada em uma área distante 7 km do centro da cidade,
situada à margem direita do rio Madeira.
As operações no local eram realizadas sem quaisquer critérios técnicos, resultando
em um verdadeiro “lixão”. Este procedimento, com passar do tempo, ocasionou um grande
comprometimento ambiental da referida área. O seu posicionamento em local inadequado
do ponto de vista do meio físico e do ponto de vista legal é outro fator negativo para sua
utilização como área de disposição de resíduos sólidos (KREBS et al., 1999).
Todos estes aspectos negativos, aliados ao fato que os vetores de expansão urbana
apontavam no sentido da referida área, deram origem a conflitos de uso do solo,
transtornos às comunidades vizinhas e contribuíram para a desativação das operações neste
local, em 1992 (KREBS et al., 1999).
Com o encerramento das atividades, procurou-se outra área que se situasse a uma
distância adequada dos vetores de expansão urbana e que apresentasse características
favoráveis do ponto de vista do meio físico e ambiental. Desta maneira, foi definida a atual
área de disposição de resíduos sólidos do município, que está localizada a uma distância de
aproximadamente 4 km do Rio Madeira e 12 km da zona urbana de Porto Velho (KREBS
et al., 1999) (Figura 01).
Figura 01: Vista externa do Lixão de Porto Velho/RO.
Fonte: Biogeoquímica, 2009.
17
A disposição do lixo urbano de Porto Velho é realizada a semelhança de vazadouro
(forma de deposição do lixo, em que este é simplesmente descartado em determinado local,
sem qualquer técnica ou cuidado), onde o mesmo é simplesmente jogado a margem de um
vale, sendo posteriormente empurrado por um trator de esteira para dentro do mesmo. Não
há qualquer preocupação em termos de recobrimento ou disposição em camadas
regularmente cobertas com terra (NEUBAUER et al., 1999).
O lixo é empurrado para o vale que corresponde às nascentes de um igarapé.
Verificações no local indicaram que existem duas nascentes que já foram totalmente
encobertas com lixo, o qual, neste local, apresenta espessura de aproximadamente 10m e
largura de 100m. O chorume gerado neste depósito de lixo contamina as águas deste
igarapé, desde suas áreas de nascente. As observações realizadas no local permitiram
verificar que não foi efetuada nenhuma impermeabilização de fundo (selagem com
material argiloso compactado e/ou mantas geomecânicas), nem colocados drenos de gases
e estruturas para contenção e tratamento de chorume (KREBS et al., 1999).
Esta modalidade é um dos tipos de deposição mais utilizada, devido aos custos
operacionais e aos investimentos de implantação e operação serem relativamente baixos,
não havendo qualquer tipo de separação entre resíduos orgânicos e inorgânicos, os quais
são coletados de forma conjunta (NEUBAUER et al., 1999).
A composição do lixo urbano de Porto Velho apresenta sua maior fração
constituída por matéria orgânica, atingindo 50,7% de material reciclável e 40% de material
considerado rejeito (Porto Velho apud NEUBAUER et al., 1999) (Figura 02).
Dentro da área de domínio do depósito e próximo às áreas de disposição, está
inserida a Vila Princesa (uma distância de 1 km) a qual foi formada logo após a mudança
do antigo “lixão”. A população que reside na Vila é formada, principalmente, por
migrantes, com baixa escolaridade e, conseqüentemente, com profissões que proporcionam
baixa renda, sendo em média cinco pessoas por moradia.
Os primeiros catadores que residem na Vila Princesa moravam, anteriormente, no
centro urbano de Porto Velho e trabalhavam no antigo “lixão”, localizado na Estrada do
Santo Antônio a 7 quilômetros do centro. Como essas pessoas trabalhavam catando e
vendendo materiais para reciclagem, também já no antigo “lixão”, e esse se deslocou para
uma área fora do perímetro urbano, essas pessoas viram-se obrigadas a mudarem para as
proximidades do mesmo. Essa mudança de local do “lixão” ocorreu em razão do mau
gerenciamento do lixo e de sua destinação, comprometendo a qualidade ambiental do local
(COSTA, 2001).
18
Com relação ao abastecimento de água, 100% dos moradores utilizam, hoje, água
de um poço tubular construído em 2001. Cabe salientar que duas residências possuem
poços tipo “amazonas”. Porém nem sempre o abastecimento de água dá-se desta forma, em
situações semelhantes, com informa NEUBAUER (1999): “A água consumida em 95% das
moradias provém de fontes existentes nas proximidades, ou da chuva. O restante utiliza
água do Clube dos Trinta” (que fica próximo da Vila princesa).
Segundo informações da empresa responsável pelo saneamento básico em Porto
Velho – CAERD (Companhia de Águas e Esgoto de Rondônia), apenas 60% da população
da capital recebe água tratada, restando aos demais à utilização de poços escavados tipo
“amazonas”, os quais atingem a água do primeiro lençol freático.
É importante salientar que as pessoas que trabalham no “lixão” e residem na Vila
possuem uma função muito importante no que se refere à reciclagem e, conseqüentemente,
ao reaproveitamento de diversos materiais, diminuindo em parte a degradação ambiental.
Porém deve-se deixar claro que essas pessoas trabalham sem nenhum tipo de máscara, luva
ou botas, para proteger-se da contaminação, à qual estão expostos nesse local, pois ali é
depositado tanto o lixo doméstico e comercial, quanto o lixo hospitalar do município de
Porto Velho (COSTA, 2001).
Figura 02: Vista do Lixão, obtida de uma estrada lateral
de acesso.
Fonte: Biogeoquímica, 2009.
19
O atual depósito de lixo situa-se no km 13 da BR-364, à direita da referida rodovia,
no sentido Porto Velho - Rio Branco. As coordenadas da entrada do depósito (balança),
medidas com GPS são 851.005 x 6.356.557 (KREBS et al., 1999).
Como premissa básica, deve-se sempre levar em consideração a importância das
características do meio físico da área para se avaliar os impactos que esta atividade causa
ao meio ambiente e à saúde das comunidades que habitam os entornos do depósito.
No local ocorrem latossolos espessos, com horizonte concrecionário colunar,
desenvolvidos
sobre
sedimentos
argilo-arenosos.
Estes
solos,
mesmo
sendo
dominantemente argilosos, devido à sua estruturação interna, são bastante permeáveis. Por
outro lado, esta estruturação confere-lhes uma baixa suscetibilidade aos processos erosivos.
Nos vales próximos, de acordo com o Mapa Geológico (ADAMY & ROMANINI, 1990),
ocorrem rochas graníticas relacionadas ao Proterozóico Médio (granitos do tipo Santo
Antônio).
Do ponto de vista geomorfológico, a área apresenta um relevo moderadamente
ondulado, constituído por colinas, cujas cotas mais elevada situam-se em torno de 130m. O
local onde se situa o depósito corresponde a um pequeno divisor de águas, com geometria
alongada em forma de tabuleiro, intensamente dissecada pelas drenagens. Nas encostas
deste tabuleiro, ocorrem várias nascentes que dão origem aos pequenos cursos de água que
deságuam no igarapé Mato Grosso, e este segue em sentido ao Rio Madeira. No entorno do
depósito ainda existe floresta nativa, onde ocorrem árvores de grande porte.
A área total disponível é de 51 ha, já tendo sido ocupados cerca de 40 ha. O lote de
terras faz parte da Gleba Garças, que se constitui de terras devolutas arrecadadas pelo
Instituto Nacional de Colonização e Reforma Agrária – INCRA, no ano de 1972 (KREBS
et al, 1999).
A disposição inadequada dos resíduos sólidos leva à contaminação do solo pela
infiltração do chorume. O chorume (lixiviado ou percolado) apresenta elevadas
concentrações de matéria orgânica, bem como substâncias inorgânicas, tais como metais
pesados. O caráter ácido dos solos da região permite que o chorume, juntamente com a
água da chuva, transporte elementos orgânicos e inorgânicos. Esta contaminação pode
atingir as águas subterrâneas e, consequentemente, a população.
20
3 OBJETIVOS
3.1 Geral
Avaliar alguns parâmetros de potabilidade e balneabilidade das águas subterrâneas
e superficiais no entorno ao depósito de resíduos sólidos urbanos do município de Porto
Velho-RO.
3.2 Específicos
•
Analisar parâmetros físico-químicos e bacteriológicos dos cursos d’água na área
de estudo.
•
Determinar as concentrações de metais pesados metais (Cd, Cu, Cr, Ni, Zn, Pb,
Co e Mn) em águas superficiais e subterrâneas.
•
Comparar a qualidade da água disponibilizada à comunidade da Vila Princesa,
frente aos padrões estabelecidos pelo Conselho Nacional do Meio Ambiente –
CONAMA, Resolução nº.357, de 17 de março de 2005, Resolução nº.274 de 29
de novembro de 2000 e do Ministério da Saúde – MS, Portaria nº. 518, de 25 de
março de 2004.
21
4 METODOLOGIA
4.1 Delineamento da pesquisa
Esta pesquisa constitui-se num estudo transversal, definido como um estudo no
qual as observações ou mensurações das variáveis de interesse são feitas simultaneamente,
de forma que os dados obtidos representam uma “radiografia” de uma determinada
situação, em um dado momento (Forattini, 1992, Perreira, 1995). Deste modo, esta
investigação trata da avaliação dos níveis de metais, teste bacteriológico e parâmetro físico
- químico na área do depósito de lixo urbano de Porto Velho-RO, no ano de 2009.
Visando o alcance dos objetivos traçados para esta investigação, foi elaborada uma
metodologia que envolveu um conjunto de procedimentos que se iniciaram com a
delimitação do local do estudo, a escolha dos instrumentos e preparação dos materiais para
coleta, prosseguindo com a demarcação dos pontos para coleta das amostras, adoção de
técnicas analíticas, validação dos métodos, além do tratamento estatístico dos dados
levantados.
As variáveis estudadas constituíram-se pelos metais: cádmio, cobre, cromo, níquel,
zinco, chumbo, cobalto e manganês, parâmetros físico - químicos (pH e condutividade
elétrica) e coliformes fecais (E. coli) e não fecais, presente nas matrizes: água superficial e
subterrânea.
4.2 Reagentes e soluções
Todas as soluções foram preparadas com reagentes de grau analítico e água
deionizada de alta pureza e purificada através do sistema Milli-Q plus (Milipore). O ácido
nítrico (HNO3 a 70%) e ácido clorídrico (HCl a 37%) empregado foi da Merck e Spectrum,
respectivamente. As soluções padrões de 1000 ppm de Cu, Cd, Co, Pb, Ni , Cr, Mn e Zn e
o meio de cultura Chromocult Coliform Ágar empregados foram da Merck.
22
4.3 Equipamentos
Os equipamentos utilizados foram os seguintes: para demarcação dos pontos
utilizou-se um receptor de GPS (Sistema de Posicionamento Global), modelo
GARMIN’XL 12. Nas análises físico-químicos empregou-se o pHmetro da SCHOTTHANDYLAB digital para as medidas de pH e o condutivimetro da SCHOTT–HANDHELD CONDUCTIVITY METER – HANDYLAB, modelo LF1, para as medidas de
condutividade elétrica. O espectrofotômetro de absorção atômica modelo Avanta da GBC
foi empregado na determinação de metais pesados.
4.4 Pontos de amostragem
Para a realização deste trabalho, estabeleceu-se cinco pontos amostrais (Figura 04 a
08), sendo dois pontos de igarapés (Figura 04 e 05) e três pontos de poços um tipo tubular
e dois tipos amazonas (Figura 06 a 08). A localização geográfica (Tabela 02) de cada ponto
amostrado foi determinada, por GPS Em todos os pontos selecionados para amostragens da
água, foram medidos, in loco, os seguintes parâmetros físico-químicos: pH e
Condutividade elétrica.
Tabela 02: Localização dos pontos de coleta de água entorno do lixão urbano de Porto
Velho-RO, coletadas em abril de 2009.
Amostras
Coordenadas
Local de referência
______________________
S
W
P 01
08°50’44.0
063°56’24.7
Igarapé
P 02
08°50’46.5
063°56’32.2
Igarapé
P 03
08°50’57.9
063°56’25.6
Poço tubular
P 04
08°51’01.8
063°56’27.6
Poço amazonas
P 05
08°51’03.4
063°56’25.7
Poço amazonas
23
24
Figura 03: Mapa de localização da área e os pontos (P 01 a P 05) de coletas das amostras.
Fonte: Biogeoquímica, 2009.
4.4.1 Mapa da área de estudo
4.4.2 Descrição dos pontos amostrados
A coleta foi realizada em abril de 2009 (período chuvoso). Foram coletadas
amostras em 05 pontos:
•
Ponto 01: “Bica do Paulista” - igarapé que nasce antes do lixão. Atravessa
a Br 364 e deságua no igarapé Mato Grosso, o qual segue em direção ao
Rio Madeira (Figura 04).
Figura 04: Igarapé Bica do Paulista.
Fonte: Biogeoquímica, 2009.
•
Ponto 02: “Igarapé do Lixão”, nasce debaixo do lixão (10 m abaixo do
nível do solo do Lixão) e deságua no igarapé Mato Grosso seguindo em
direção ao Rio Madeira (Figura 05).
25
Figura 05: Igarapé do Lixão.
Fonte: Biogeoquímica, 2009.
•
Ponto 03: Poço tubular, que se encontra na parte central da Vila Princesa
(inserida a uma distância de 1 km do lixão), possui 56 metros de
profundidade e foi perfurado no ano de 2001 (Figura 06).
Figura 06: Poço tubular.
Fonte: Biogeoquímica, 2009.
26
•
Ponto 04: Poço tipo amazonas, que se encontra em uma residência da Vila
Princesa (próximo ao lixão), possui 20 metros de profundidade (Figura
07).
Figura 07: Poço tipo amazonas.
Fonte: Biogeoquímica, 2009.
•
Ponto 05: Poço tipo amazonas, que se encontra em outra residência da
Vila Princesa (próximo a Br 364), possui 19 metros de profundidade
(Figura 08).
Figura 08: Poço tipo amazonas.
Fonte: Biogeoquímica, 2009.
27
4.5 Coleta e conservação das amostras
Para a análise de metais pesados, todos os materiais utilizados para coleta e
acondicionamento eram de polietileno e foram previamente submergidos em solução de
ácido nítrico (HNO3) por 24hs, para a eliminação de metais interferentes (VARIAN, 1988;
APHA, 1998; VOEGBORLO et al., 1999) e, posteriormente, enxaguados com água
MILLI-Q. Foram coletados em cada ponto 5L de água e adicionado ácido nítrico (HNO3)
(Figura 09).
Figura 09: Acondicionamento das amostras em garrafas de
polietileno.
Fonte: Biogeoquímica, 2009.
Para a análise bacteriológica, foi utilizado frasco âmbar (Figura 10), previamente
esterilizado. As amostras foram armazenadas numa caixa de isopor, contendo gelo para
manter a preservação bacteriológica até a análise.
28
Figura 10: Amostras em frasco âmbar previamente esterilizado.
Fonte: Biogeoquímica, 2009.
4.6 Curva de calibração dos metais pesados
Os metais pesados nas amostras foram quantificados a partir das curvas de
calibração de cada elemento. Na Figura 11 é apresentada a curva de calibração do cobalto.
As soluções padrões foram obtidas por diluição dos padrões de 1000 mg L-1 de
metais pesados. Os intervalos de concentração, equação da reta e o coeficiente de
correlação usados na quantificação dos elementos químicos das amostras de água são
apresentados na Tabela 03 e estão dentro do intervalo ótimo de utilização do equipamento
de espectrometria de absorção atômica.
29
0,22
0,20
0,18
Abs
0,16
0,14
0,12
-2
0,10
Y= 2,35.10 + 0,10176X
r= 0,99811
0,08
0,06
0,2
0,4
0,6
0,8
1,0
1,2
1,4
1,6
1,8
2,0
Cadmio / ppm
Figura 11: Curva de calibração do elemento químico Cádmio (Cd).
0,018
0,016
0,014
Abs
0,012
0,010
0,008
-4
Y = 1,5405410 + 0,00592X
R = 0,99938
0,006
0,004
0,002
0,5
1,0
1,5
2,0
2,5
3,0
Chumbo / ppm
Figura 12: Curva de calibração do elemento químico Chumbo (Pb).
30
0,10
0,08
abs
0,06
0,04
0,02
-3
Y= 1,35.10 + 0,02835X
r= 0,99989
0,00
0,0
0,5
1,0
1,5
2,0
2,5
3,0
Cobalto / ppm
Figura 13: Curva de calibração do elemento químico Cobalto (Co).
0,14
0,12
0,10
Abs
0,08
0,06
0,04
-5
Y = 3,4090910 + 0,04197X
R = 0,99902
0,02
0,00
-0,02
-0,5
0,0
0,5
1,0
1,5
2,0
2,5
3,0
Cobre / ppm
Figura 14: Curva de calibração do elemento químico Cobre (Cu).
31
0,16
0,14
0,12
Abs
0,10
0,08
0,06
-3
0,04
Y= 2,83.10 + 0,0127X
r= 0,99821
0,02
0,00
0
2
4
6
8
10
12
Cromo / ppm
Figura 15: Curva de calibração do elemento químico Cromo (Cr).
0,25
0,20
Abs
0,15
0,10
-3
Y= 2,88.10 + 0,0602X
r= 0,99945
0,05
0,00
0,0
0,5
1,0
1,5
2,0
2,5
3,0
3,5
4,0
4,5
Manganês / ppm
Figura 16: Curva de calibração do elemento químico Manganês (Mn).
32
0,16
0,14
0,12
Abs
0,10
0,08
0,06
-3
Y= 1,32.10 + 0,03126X
r= 0,99985
0,04
0,02
0,00
0
1
2
3
4
5
Níquel / ppm
Figura 17: Curva de calibração do elemento químico Níquel (Ni).
0,55
0,50
Abs
0,45
0,40
0,35
-1
Y= 1,07.10 + 0,28383X
r= 0,99821
0,30
0,25
0,6
0,8
1,0
1,2
1,4
1,6
Zinco/ pppm
Figura 18: Curva de calibração do elemento químico Zinco (Zn).
33
4.7 Extração química para a determinação de metais pesados
Foram realizadas as digestões ácidas para abertura das amostras para a análise de
metais, de acordo com APHA (1992), sendo feitas adaptações no Laboratório de
Biogeoquímica Ambiental – Universidade Federal de Rondônia/Unir (Figura 19).
A análise iniciou-se com a transferência de 1L da amostra preservada para um
becker. Adicionou-se 5mL de ácido nítrico (HNO3), levou-se as amostras à chapa
aquecedora. Deixou-se evaporar até quase secar (redução de volume até aproximadamente
20mL) e colocou-se 3mL de ácido clorídrico(HCl), deixando reduzir o volume até
aproximadamente 10mL. Depois de evaporado, foi ressuspenso com 10mL de ácido
clorídrico (HCl 0,1 mol L-1), acondicionado em tubos de teflon (Figura 20).
Após a calibração do equipamento de absorção atômica foram analisados os metais
nas amostras de água (Figura 21). Cada metal foi analisado segundo suas curvas de
calibração com os seguintes limites de detecção apresentados na Tabela 04.
Tabela 03: Limites de Detecção da Técnica (LDT) para cada elemento analisado.
LDT
Cd
mg L-1
Co
mg L-1
Cr
mg L-1
Cu
mg L-1
Pb
mg L-1
Ni
mg L-1
0,01
0,01
0,01
0,38
0,01
0,01
Mn
mg L-1
0,01
Zn
mg L-1
0,01
Para métodos que empregam uma curva analítica, o limite de detecção é definido
como a concentração analítica que gera uma resposta com um fator de confiança.
34
Figura 19: Extração química das amostras para a determinação de metais pesados.
Fonte: Biogeoquímica, 2009.
Figura 20: Acondicionamento das amostras em tubos de teflon.
Fonte: Biogeoquímica, 2009.
35
Figura 21: Espectrofotômetro de absorção Atômica por chama.
Fonte: Biogeoquímica, 2009.
Para o controle de qualidade do processo analítico, as amostras foram analisadas
em triplicadas e acompanhas de três brancos (controles), o qual se pode subtrair as
contaminações do ambiente de trabalho e dos reagentes utilizados nas extrações químicas.
4.8 Análise bacteriológica
Para a análise bacteriológica, foi utilizada a técnica de membrana filtrante e o meio
de cultura Chromocult Coliform Ágar por ser um meio simples, econômico, e por
apresentar resultados rápidos (Figura 22).
O Chromocult é uma combinação de dois substratos cromogênicos (Salmon – Gal e
X – glicuronídeo – subtratos enzimáticos sintéticos) que possibilita a detecção de
coliformes totais e fecais (E. coli), em uma mesma placa, que é diferenciada pela cor.
O meio de cultura Chromocult Coliform Ágar é aprovado e certificado pelo USEPA
(United States Environmental Protection Agency - USEPA, 2009).
36
Figura 22: Método de membrana filtrante.
Fonte: PRO-ANALISE, 2009.
No laboratório a análise se iniciou com a diluição de 100 vezes, o qual uma
alíquota 1mL da amostra aferindo a 100mL de água deionizada estéril (previamente
autoclavada), passando em seguida pelo processo de filtração através da membrana
filtrante de acetato de celulose quadriculada (Millipore) de 0,45μm de porosidade (Figura
23). A seguir, as membranas foram colocadas sobre o meio de cultura chromocult. As
placas foram incubadas a 35ºC por 24h. Foi observada a presença de coliformes (colônias
rosa/lilás) e de coliformes fecais (E. coli) (colônias violetas/pretas), expressando-se o
resultado em número mais provável (NMP/100 mL) de amostra (Figura 24). A partir da
contagem destas colônias, foi calculado a densidade de coliformes presentes na amostra e
multiplicando pelo fator de
diluição (100/mL). O número de coliformes totais foi
determinado pela somatória das colônias rosa/lilás e violetas/pretas (CETESB, 1987).
37
Figura 23: Procedimento membrana filtrante.
Fonte: PRO-ANALISE, 2009.
Figura 24: Placa com colônias de coliformes fecais (E. coli) e coliformes não fecais.
Fonte: Biogeoquímica, 2009.
38
4.9 Análise dos dados
Após a obtenção dos dados, estes foram digitados em planilhas Excel e a partir
deles organizou-se matrizes de dados a partir da coleta, considerando-se as variáveis físicoquímicas (condutividade elétrica e pH) para o ambiente lótico; e variáveis geoquímicas da
água superficial e subterrânea (Cd, Co, Cu, Cr, Pb, Mn, Ni e Zn) e testes bacteriológicos.
Para a análise de dados das curvas de calibração linear, utilizou-se o programa
Origin (Data Analysis Technical Graphics) versão 6.0.
Os mapas foram confeccionados no Laboratório de Biogeoquímica Ambiental
Wolfgang Cristian Pfeiffer, utilizando a Base Cartográfica da SEDAM (2002) e imagens
de alta resolução de 2006 obtidas pelo programa Google Earth. Estas imagens foram
georreferenciadas no programa Global Mapper, versão 5.09 e o mapa foi elaborado no
programa ArcMap 9.2.
39
5 RESULTADOS E DISCUSSÃO
5.1 Parâmetros físico-químicos
5.1.1 Condutividade elétrica
Os resultados obtidos da condutividade elétrica encontram-se expostos na Figura
25. Observa-se que a condutividade se mostrou muito elevado no ponto 02. A grande
incidência da condutividade pode estar relacionada com a dissolução de ácidos carbônicos,
fúlvicos, húmicos e carbonatos resultantes da oxidação da matéria orgânica na vazante,
enquanto que no período de cheia se justifica pela elevada lixiviação de sólidos em
suspensão com grandes quantidades de íons e influência do chorume, que é impactante.
Figura 25: Condutividade elétrica, nos pontos amostrados.
Nos estudos realizado por Santos (2006), a condutividade elétrica do chorume da
lixeira urbana de Porto Velho-RO, apresentou uma média de 5526,00 µS/cm (nos períodos
de chuva e seca), sendo considerado bastante alto, se comparado ao valor obtido por
Sisinno & Moreira (1996), no aterro controlado do Morro do Céu-RJ, de 6,20 µS/cm,
indicando provável carga de compostos orgânicos e inorgânicos transportada.
40
5.1.2 Potencial Hidrogeniônico (pH)
Por influir em diversos equilíbrios químicos que ocorrem naturalmente, o pH é uma
variável importante do ponto de vista ambiental. A influência do pH sobre os ecossistemas
aquáticos naturais dá-se diretamente devido a seus efeitos sobre a fisiologia das diversas
espécies. Também o efeito indireto é muito importante, podendo, determinadas condições
de pH contribuir para a precipitação de elementos químicos tóxicos, como metais pesados;
outras condições podem exercer efeitos sobre as solubilidades de nutrientes. Os resultados
obtidos de pH encontram-se expostos na Figura 26, onde se observa que o pH variou entre
4,08 a 6,26.
Figura 26: Variação do pH entre os pontos amostrados.
De acordo com Segato & Silva (2000), valores altos de pH são características de
um chorume mais antigo, que se encontra na fase metanogênica. Nesta fase, organismos
estritamente anaeróbios decompõem os produtos da fermentação ácida (CO2, H2 e ácidos
graxos menores) e os convertem em CH4, substâncias húmicas e água. Tais substâncias
húmicas são responsáveis pela coloração parda encontrada no lixiviado o qual foi
observado no P02 (Figura 05 e Figura 26).
41
5.1.3 Coliformes fecais e coliformes não fecais
Os resultados de coliformes fecais (E. coli) foram maiores no ponto 02, conforme a
Figura 27.
Figura 27: Números de coliformes fecais (E. coli) das amostras.
Os coliformes fecais (E. coli) fora do seu “habitat natural”, o intestino de animais
homeotermos, causa grandes danos quando em contato com outras regiões internas do
corpo (infecção urinária de alta patogenicidade). A predominância desse grupo se deve à
evasão de excretas pelas águas das chuvas e pela lixiviação que possui alto teor
contaminante.
No igarapé do lixão (P02), os coliformes fecais (E. coli) apresentaram níveis altos
de 30000 NMP/100mL, portanto, não se enquadram na categoria de satisfatório dos
padrões de balneabilidade da resolução CONAMA nº. 274, de 29 de novembro de 2000,
Tabela 04.
42
Tabela 04: Padrões de balneabilidade através da resolução CONAMA nº. 274, de 29 de
novembro de 2000.
Categorias
Coliformes fecais (E. coli)
NMP/100 mL
Excelente
até 250
Muito boa
até 500
Satisfatória
até 1000
Imprópria
> 2500
Referente aos poços, todas as amostras coletadas nos pontos P03, P04 e P05
apresentaram-se acima do permitido do padrão de potabilidade recomendado pela Portaria
nº. 518, de 25 de março de 2004, do Ministério da Saúde (Tabela 05).
Tabela 05: Padrões de potabilidade para águas subterrâneas, conforme resolução nº. 518,
de 25 de março de 2004.
Coliformes fecais (E. coli)
NMP/100 mL
Portaria nº. 518/2004
ausente
A presença de coliformes fecais é um fato preocupante, uma vez que a água
proveniente destes poços é utilizada pela população da Vila Princesa. A presença de
coliformes pode estar associada à limitação do poder filtrante do solo.
Os resultados de coliformes não fecais foram maiores nos pontos 01 e 02, como
mostra a Figura 28.
Os coliformes não fecais apresentam uma estrutura diferente, pois estão presentes
no solo, na vegetação e ainda podem ser encontrados entericamente. Este grupo de
43
bactérias obteve um valor significativo, caracterizando a freqüência de Proteus e Serratia.
No período de cheia, a grande presença destas bactérias se deve à lixiviação de matéria
orgânica e inorgânica do solo pelas águas das chuvas em direção ao corpo d’água.
Figura 28: Números de coliformes não fecais das amostras.
Observando as Figuras 06, 07 e 08, nota-se que não há muito cuidado em relação à
limpeza em redor dos pontos P03, P04 e P05, os quais apresentam cobertura inadequada
(com exceção P03). Portanto, estão mais susceptíveis à contaminação oriunda da região.
Contudo, não se excluem problemas de má construção e conservação dos poços como
outros fatores que podem estar influenciando a composição das águas.
Nas Tabelas 06 e 07 são apresentados os resultados das análises feitas no presente
trabalho e os que foram feitas pela Companhia de Águas e Esgotos de Rondônia
(CAERD), em água dos poços, nascentes e igarapés, localizados no depósito de lixo de
Porto Velho-RO (COSTA & MALAGUTTI, 2008).
44
Tabela 06: Resultados das análises físico-químicos e bacteriológicos das amostras de água
dos poços e igarapés, localizados no depósito de lixo de Porto velho-RO, 2009.
Parâmetro
pH
Condutividade
Coliformes fecais
Unidades
Igarapés
________________
P 01
P 02
Poços
__________________
P 03
P 04
P 05
__
5,60
6,26
4,08
4,20
4,22
µ S/cm
8,80
437,00
39,00
27,00
31,00
500
30000
133
833
250
NMP/100 mL
P 03: poço tubular ; P 04: poço amazonas ;P 05: poço amazonas
__ sem unidade.
Tabela 07: Resultados das análises físico-químicos e bacteriológicos das amostras de água
dos poços e nascentes, localizados no depósito de lixo de Porto Velho-RO obtidos pelos
autores COSTA & MALAGUTTI, 2008.
Parâmetro
pH
Condutividade
Coliformes fecais
Unidades
Nascentes
_______________
NS1
NS2
Poços
__________________
P 03
P 04
P 05
__
4,54
6,89
5,39
4,80
4,74
µ S/cm
92,6
1114
21,1
16,3
18,6
1500
900
**
1700
800
NMP/100 mL
P 03: poço tubular; P 04: poço amazonas; P 05: poço amazonas
__ sem unidade.
** ausente.
Comparando os resultados obtidos em 2008 (Tabela 07) e 2009 (Tabela 06) pode-se
observar que houve um aumento dos valores de condutividade elétrica nos poços. Esse
aumento da condutividade elétrica está relacionado com a contaminação dos mesmos.
Porém, nas águas superficiais das nascentes apresentaram maiores valores de
condutividade elétrica do que dos igarapés.
Em 2008, no poço P03, foi observado ausência de coliformes fecais (E. coli),
entretanto, em 2009, pode-se observar quantidade elevadas de coliformes fecais (133
NMP/100mL). De acordo com a portaria 518 do Ministério da Saúde, as águas para o
consumo, não pode ter presença de coliformes fecais.
45
De acordo com Costa & Filho (2008), a contaminação das águas da nascente e dos
poços não pode ser atribuída exclusivamente à ação do chorume, mas aos objetos de rede
de esgotos, a grande quantidade de fossas sépticas próximas e às infiltrações das águas
superficiais no solo contaminado.
Esses resultados evidenciam o risco à saúde que esse tipo de fonte pode representar,
caso não sejam aplicadas medidas visando ao tratamento e à preservação da qualidade
microbiológica da água. Acredita-se, portanto, que o desenvolvimento de um trabalho de
educação sanitária para a população, a adoção de medidas preventivas visando à
preservação das fontes de água e o tratamento das águas já comprometidas, aliados às
técnicas de tratamento de dejetos, podem servir como ferramentas necessárias para
diminuir ao máximo o risco de ocorrência de enfermidades de veiculação hídrica.
5.1.4 Metais pesados
Os resultados (média e desvio padrão) das amostras e os valores máximos
permissíveis pela Resolução nº. 357, de 17 de Março de 2005 do Conselho Nacional do
Meio Ambiente (CONAMA) (Tabelas 08 e 09).
Tabela 08: Valores máximos permitidos para os elementos químicos pela resolução nº.
357, de 25 de março de 2005 (CONAMA).
CONAMA
(Cd)
(Co)
(Cu)
Elementos (mg/L)
(Cr)
(Pb)
(Mn)
(Ni)
(Zn)
0,001
0,05
0,009
0,05
0,025
0,18
0,01
0,1
46
Tabela 09: Concentração dos metais pesados do Lixão de Porto Velho-RO.
AMOSTRAGEM
Elementos
(mg/L)
P 01
P 02
P 03
P 04
P 05
Cd
<LDT
<LDT
<LDT
<LDT
<LDT
Co
<LDT
1,00 ± 0,08
<LDT
<LDT
<LDT
Cu
<LDT
1,68 ± 0,24
2,30 ± 0,19
0,77 ± 0,00
0,48 ± 0,16
Pb
0,52 ± 0,08
1,44 ± 0,45
0,15 ± 0,14
<LDT
<LDT
Cr
<LDT
<LDT
<LDT
<LDT
<LDT
Mn
5,06 ± 0,13
366,08 ± 43,28
0,70 ± 0,32
<LDT
1,16 ± 0,07
Ni
0,73 ± 0,03
2,79 ± 0,17
0,97 ± 0,17
0,78 ± 0,26
0,66 ± 0,31
Zn
1,13 ± 0,04
6,31 ± 0,61
3,72± 1,01
1,32 ± 0,19
0,78 ± 0,86
<LDT: Menor que o limite de detecção da técnica.
Pode-se verificar na Tabela 09, que foram detectados os metais pesados Co, Cu, Pb,
Mn, Ni e Zn , porém as concentrações encontradas estão acima dos padrões estabelecidos
pelo CONAMA, como observado.
Com o aumento da pluviosidade, os elementos químicos tendem a tornar-se mais
disponíveis no solo, além disso, o chorume torna-se mais abundante e acaba carregando
esses elementos com maior intensidade.
Os valores de Cd e Cr de todas as amostras encontram-se abaixo do limite de
detecção da técnica utilizada. As baixas concentrações desses íons metálicos podem ser
atribuídas á baixa solubilidade dos mesmos, nas condições prevalentes, tais como pH
ácido, elevado teor de matéria orgânica, redução de sulfato, uma vez que podem precipitar
como hidróxidos e/ou com sulfetos, aos mecanismos de retenção pelo solo, sedimentos e
material em suspensão, a complexação dos metais com a matéria orgânica
(BUSCHINELLI apud SISINNO & MOREIRA, 1996).
Como pode ser observado, a amostra do P02 apresentou as maiores concentrações
(exceto Cd e Cr), sendo que Co, Cu, Pb, Mn, Ni e Zn excederam todos os limites
estabelecidos pelo CONAMA. As demais amostras dos pontos P01, P03, P04 e P05
47
apresentaram valores menores de concentração desses elementos (exceto Cd e Cr),
entretanto excederam todos os limites estabelecidos pelo CONAMA.
Os elementos Mn e Zn tiveram as maiores concentrações acima do limite tolerável
de 0,1 e 0,18 mg/L, respectivamente. As concentrações de Zn podem estar relacionadas
com a presença de materiais de borracha e pilhas observado em campo, na área ativa do
lixão. O caso do Mn pode estar relacionado a processos biogeoquímicos do solo, mas nesse
caso é provável que esteja associada também à contaminação oriunda de materiais que
contém esse elemento, já que esse metal atingiu concentrações de 366,08 mg/L durante
esse período. As principais fontes de Mn, dispostas no lixo, que contribuem para o
aumento de suas concentrações, são as pilhas comuns e alcalinas e as lâmpadas
fluorescentes.
O cobre apresenta-se em quantidades importantes em metais ferrosos, restos de
materiais eletrônicos, latas, tampas de garrafas e fios elétricos. Em muitas situações, os
catadores de lixo queimam os fios para retirar o cobre neles contido, o que acaba
disponibilizado partículas do mesmo para o solo. O Pb manifesta-se também em metais
ferrosos e é muito utilizado na indústria de tintas, pintura em cerâmica e soldagem, latas de
estanho, tubos de creme dental, pilhas e baterias (SEGATO & SILVA, 2000).
De acordo com Santos (2006), ao comparar os resultados obtidos no seu trabalho
(análise do chorume da Lixeira Urbana de Porto Velho-RO), com os resultados de Sisinno
& Moreira, observou que as concentrações médias (exceto para Cd e Co) totais de metais
foram maiores no chorume do lixão de Porto Velho-RO, do que aqueles encontrados no
aterro sanitário do Morro do Céu-RJ.
A tendência natural do chorume através do processo de lixiviação, é de se
concentrar na parte inferior do depósito (o que acontece no lixão). O solo deve atuar como
um filtro, sendo indispensável sua baixa permeabilidade á medida em que o chorume se
movimenta através dele, para reduzir seu poder contaminante.
O solo onde está instalada a lixeira pública de Porto Velho apresenta alta
permeabilidade tendo como principais litologias os lateritos e a formação Jaci Paraná, que
apresentam esta particularidade. Sendo assim, levando-se em consideração a necessidade
de baixa permeabilidade do solo para uma deposição de resíduos mais segura as
características das litologias presentes na área de estudo e os resultados obtidos neste
estudo considera-se que o lugar utilizado para deposição de lixo não é adequado para a
finalidade a que se destina (NEUBAUER et al., 1999).
48
6 CONCLUSÕES
A informação gerada traz novos conhecimentos sobre a situação ambiental da área
estudada, no que se refere à presença de metais e coliformes fecais, trazendo subsídios para
ações político-administrativas municipais.
- As concentrações de metais (Co, Cu, Pb, Mn, Ni e Zn), tanto na água superficial e
subterrânea, apresentaram valores inadequados de concentrações .
- A condutividade elétrica e análise bacteriológica mostraram-se significativas no
ponto mais próximo ao lixão. Os resultados demonstraram que a água do igarapé está
sendo contaminada por coliformes fecais (E. coli) e coliformes totais. O número mais
provável (NMP/100mL) de coliformes fecais ultrapassou a categoria de satisfatória para
balneabilidade (CONAMA, 2005) e dos padrões de potabilidade (Ministério da Saúde,
2004).
Os resultados obtidos nesse estudo, indicam a necessidade de dar continuidade ao
monitoramento nesses corpos d’água.
Fica evidente que o referido local não é adequado, considerando-se os critérios
constantes na legislação Ambiental Federal, no que se refere à distância de corpos d’água.
Além disso, o tipo de solo que ocorre na área é permeável e permite a infiltração do
chorume no substrato.
Nestas análises, foi possível alcançar os objetivos traçados inicialmente, sendo
caracterizados os níveis de metais pesados, testes bacteriológicos e parâmetros físicoquímicos em uma matriz ambiental (água) na área no entorno do Lixão Urbano de Porto
Velho-RO.
.
49
7 REFERÊNCIAS
APHA, AWWA & WPCF. Métodos normalizados, para el analisis de águas potables y
residuales. ed. 17ª. Diaz de Santos, S.A., Madrid-España, 1992.
ALLERMANN, L., POULSEN, O. M. Inflammatory potential of dust from waste handling
facilities measured as IL-8 secretion from lug epithelial cells in vitro. The Annals of
Ocupational Hygiene. V.44, n.4. p. 259-269, 2000.
AL-MUZAINI, S., BEG. M.U., MUSLMANI, K. Environ Science Technol., 21: 399-405.
1995.
AMBIENTE BRASIL. Resíduos sólidos. Disponível em: www.ambientebrasil.com.br
acesso em 25/05/2007.
BAIRD, C. Química Ambiental. 2. ed. Porto alegre: Bookman, 2002.
BRANCO, S. M. O meio ambiente em debate. 27 ed. Revis. e ampl. – São Paulo.
Moderna, 1997.
CERQUEIRA, L. A. F. Incineração e Co-processamento: Alternativas para a gestão de
resíduos perigosos. Saneamento Ambiental, n. 59. P. 18-23, 1999.
CETESB.
Companhia
de
tecnologia
de
saneamento
ambiental.
Relatório
de
estabelecimento de valores orientadores para solos e águas subterrâneas. São Paulo.
CETESB, 2001.
CHARNOCK, D., WELLS, C. The challenge of waste disposal. Journal of the Royal
Society of Health, v. 105, n. 5, p. 171-178, 1985.
CONAMA: Conselho Nacional do Meio Ambiente. Resolução nº. 357, de março de 2005.
CONAMA. Conselho Nacional do Meio Ambiente. Resolução nº.274, de 29 de novembro
de 2000.
50
COSTA, A. F. & MALAGUTTI, W.F. Caracterização Estrutural e Geofísica da Lixeira
de Porto Velho (RO). Geociência, v. 27, n 2, p.229-236. Unesp/São Paulo, 2008.
COSTA, F. B. Os catadores de lixo: Condições de moradia e razão da residência na
Vila Princesa em Porto Velho, monografia – Unir, 2001.
CIENFUEGOS, F. VAITSMAN. Análise instrumental. Rio de Janeiro: Interciência, 2000.
DAMASCENO, S. Remoção de metais pesados em sistemas de tratamento de esgoto
sanitário por processo de lodo ativado e por um reator compartimento anaeróbio. São
Carlos, 1996. 141p. Dissertação (Mestrado em Hidráulica e Saneamento) – Escola de
Engenharia de São Carlos, Universidade de São Paulo.
DENISON, R. SILBERGELD, E. Risk of municipal solid waste incineration na
environmental perspective. Risk Analysis. V.8, n.3, p. 343-355, 1988.
EYER, C. Qualidade ambiental. O desafio de ser competitivo protegendo o meio
ambiente. 1 ed. Brasil, Pioneira - ABIMAQ/SINDIMAQ, 1995.
FORATINI, O. P. Ecologia, epidemiologia e Sociedade. São Paulo. Editora da
Unversidade Federal de São Paulo, 1992.
GALVÃO, P. M. A. Metais Pesado (Cd, Mn, Fe, Ni, Cu, Zn, Pb, Cd) em sedimentos e
material particulado em suspensão no baixo rio Paraíba do Sul: Uma descrição após
contaminação por rejeitos da produção de papel e celulose. Rio de Janeiro: UFRJ.
Monografia (Bacharel em Biologia Marinha), Universidade Federal do Rio de Janeiro,
2003.
GLASSER, H., CHANG, D. Na analysis of biochemical waste incineration. J. Air Waste
Management Assoc, n. 41. p. 1180-1188, 1991.
IBGE. Instituto Brasileiro de Geografia e Estatística. Pesquisa Nacional de saneamento
Básico. Rio de Janeiro: IBGE, 1992.
51
IPT. Instituto de Pesquisas Tecnológicas do Estado de São Paulo. Lixo Municipal:
Manual de gerenciamento integrado. São Paulo: IPT/CEMPRE, 2000.
KREBS, A. S. J., ADAMY, A., REIS, M. R. Alternativas locacionais para disposição de
resíduos sólidos urbanos na área de Porto Velho-RO. Porto Alegre: CPRM, 1999.
LEITE, C. M. B., BERNARDES, S. & OLIVEIRA, S. A. Método Walkley-Black na
determinação da matéria orgânica em solos contaminados por, chorume. Revista
brasileira de Engenharia Agrícola e ambiental, v. 8, n. 1, p. 111-115, 2004.
LIMA, L.M.Q. Tratamento de Lixo. 2ªed. Hemus. São Paulo. 1983.
LUZ, F. X. R. Lixo e Limpeza Pública. São Paulo. Cap.7:266p.1969.
MAGOSSI, L., BONACELLA, P. Poluição da águas. 2. ed. São Paulo. Editora Moderna,
1991.
MELO, O. Poluição química das águas. In: IX congresso brasileiro de geoquímica, 2003.
Belém-PA.
MORITZ, J. M. Current Legistation Governing Clinical. Waste Disposal. J. Hosp.
Infect, v.30, p. 521-530, 1995.
MS. Ministério da Saúde. Portaria nº. 518, de 25 de março de 2004.
MUÑOZ, S. I. Impacto ambiental na área do aterro sanitário e incinerador de
resíduos sólidos de Ribeirão Preto, SP: avaliação dos níveis de metais pesados. 2002.
Tese Doutorado – Escola de Enfermagem de Ribeirão Preto, Universidade de São Paulo.
NEUBAUER, A., POSSARI, I. A., HERRMANN, J. C., SILVA, L.P., SILVEIRA, M. A.
P. A., ROSARIO, N. R. & FEITOSA, S.C., Análise ambiental da lixeira urbana de
Porto Velho, monografia – Unir, Rondônia, 1999.
52
OLIVEIRA, S., PASQUAL, A. Avaliação de Parâmetros indicadores de Poluição por
Efluente Líquido de um aterro sanitário. Eng. Sanit. e Amb., v.9, p. 240-249, 2004.
OSHA. Ocupational Safety and Health. Administration. Genera Industry Standard, Federal
Register. Bloodborne pathogens. Part 1910.10130. n. 56. P. 64175-64182, 1991.
PERREIRA, M. G. Epidemiologia: Teoria e Pratica. Rio de Janeiro. Editora Guanabara
Koogan S. A., 1995.
ROCCA, A. C.C. IACOVONE, A.M.M.B., BARROTTI, A.J., CASARINI, D.C.P.,
GLOEDEDEN, E., STRAUS, E.L., ROMANO, J.A., RUIZ, L.R., SILVA, L.M., SAITO,
L.M., PIRES, M.C., LEÃO, M.L.G., NETO, P.P. DE C. & COLLUCCI, R., CUNHA,
R.C.A. Resíduos sólidos industriais. 2. ed. São Paulo: CETESB, P.234, 1993.
RONDONIA. Secretaria de Estado do Desenvolvimento Ambiental (SEDAM), Base
Cartográfica da SEDAM – 2002. Porto Velho-RO.
SANTOS, J. P. Caracterização de Cd, Co, Cu, Pb, Cr, Fe, Mn, Zn e Hg na Lixeira Urbana
de Porto Velho/RO. Monografia-Unir, 2006.
SCHALCH, V. Produção e características do chorume em processo de decomposição
de lixo urbano, Dissertação de mestrado em hidráulica e saneamento. Escola de
Engenharia. São Carlos, SP, 1984.
SERRA, V., GROSSI, M., PIMENTEL, V. Lixão, aterro controlado e aterro sanitário.
Dpto. De Química e Bioquímica. Unesp. Botucatu. São Paulo.
SERAFIM, A. C., GUSSKOV, K. C., SILVA, F., CONEGLIAN, C. M. R., BRITOPELEGRINI, N. N., SOBRINHO, G. D., TONSO, S. & PELEGRINI R. 2003. Chorume,
impactos ambientais e possibilidade de tratamentos. III Fórum de Estudos Contábeis (área
ambiental). Rio Claro.
53
SEGATTO, L. M. & SILVA, C. L. Caracterização do Chorume do Aterro Sanitário de
Bauuru. IN:XXVII Congresso Interamericano de Engenharia Anitária e Ambiental-AIDIS,
2000, Porto Alegre-RS.
SISINNO, C. L. S. & MOREIRA, J.C. Avaliação da contaminação e poluição ambiental
na área de influência do aterro controlado do Morro do Céu, Niterói, Brasil. Cad.
Saúde Pública, v. 12 n. 4. Rio de janeiro out.-dez, 1996.
TAKAYANAGUI, A. M. Trabalhadores de saúde e meio ambiente: Ação educativa do
enfermeiro na conscientização ara o gerenciamento de resíduos sólidos. Ribeirão Preto,
1993. Tese (Doutorado). Universidade de São Paulo.
TAKAYANAGUI, A. M. Avaliação de risco ambiental no gerenciamento de resíduos
de serviços de saúde. Ribeirão Preto, 2000. (Relatório científico de Pós-Doutoramento
junto a Mamaster University – MIEH-Canadá).
TORRES, P., BARRA, L. E., RIASCOS, J. & VIDAL, J.C. Tratabilidade biológica de
chorume produzido em aterro não controlado. Eng. Sanit. e Amb., v. 2, p. 55-62, 1197.
VARIAN. Analytical methods for graphite tube atomizers. Variam Austrália pty Ltd,
Victoria, Austrália, 1998.
VOEGBORLO, R. B., EL-METHNANI, A. M., ADEDIN, M. Z. Mercury, Cadmum and
lead contento f canned tuna fish. Food Chemistry, v.67, p.341-345, 1999.
54
ANEXO
55
ANEXO 01. Banco de dados das variáveis físico-químicas da água no período da Cheia. Condutividade elétrica em µScm-1 ;
pH; Coliformes fecais/100mL; Coliformes não fecais/100mL; Coliformes totais/100mL.
PONTOS
56
S
W
CONDUTIVIDADE
ELÉTRICA/µScm-1
pH
P 01
08°50’44.0
063°56’24.7
8,80
5,60
P 02
08°50’46.5
063°56’32.2
437,00
6,26
P 03
08°50’57.9
063°56’25.6
39,00
4,08
P 04
08°51’01.8
063°56’27.6
27,00
4,20
P 05
08°51’03.4
063°56’25.7
31,00
4,22
COLIFORMES
FECAIS/100ml
300
500
700
25000
30000
35000
100
100
200
700
1000
800
400
100
000
COLIFORMES NÃO
FECAIS/100ml
9000
8300
7000
11800
11500
8900
100
100
100
1500
1500
1700
1000
300
900
COLIFORMES
TOTAIS/100mL
9300
8800
7700
36800
41500
43900
200
200
300
2200
2500
2500
1400
400
900