1
1. (Puc-rio 2000) Devido a um resfriado, um homem de 80 kg tem temperatura do corpo igual a 39°C ao invés da
temperatura normal de 37°C. Supondo que o corpo humano seja constituído basicamente de água, qual a
quantidade de calor produzida pelo corpo para causar este aumento de temperatura?
Calor específico da água = 1 cal/g°C.
2. (Puc-rio 2006) Para descobrir o calor específico por unidade de massa de uma certa substância, misturamos
0,50kg desta substância, a uma temperatura de 80°C, com uma certa massa de água a 20°C. A temperatura
final do sistema é de 40°C. O calor especifico da água é 1,0 cal/g°C.
a) Se a massa de água a 20°C utilizada for o dobro, calcule a temperatura final do sistema.
b) Calcule o calor específico, por unidade de massa da substância, se a massa de água utilizada em (a) for de
1,0 kg.
3. (Ufal 2000) Um calorímetro de capacidade térmica 100cal/°C contém 300g de água a 20°C. Introduz-se no
calorímetro um bloco de alumínio, de massa 500g, à temperatura de 170°C. Determine a temperatura de
equilíbrio térmico do sistema, admitindo que não há trocas de calor com o ambiente.
Dados: Calor específico da água = 1,0 cal/g°C
Calor específico do alumínio = 0,20 cal/g°C
4. (Uff 2005) Um sistema básico de aquecimento de água por energia solar está esquematizado na figura a
seguir. A água flui do reservatório térmico para as tubulações de cobre existentes no interior das placas
coletoras e, após captar a energia solar, volta ao reservatório pelo outro trecho do encanamento. A caixa de
água fria alimenta o reservatório, mantendo-o sempre cheio.
Suponha que em um determinado instante o reservatório tenha em seu interior 200 litros de água, em equilíbrio
térmico.
Dados:
massa específica da água › = 1,0 kg / litro
calor específico da água c = 1,0 cal /g °C
1,0 cal = 4,2 J
a) Determine a quantidade de calor absorvida por esse volume de água para que sua temperatura aumente 20°
C, supondo que não haja renovação da água do reservatório.
b) Estime o tempo necessário para este aquecimento, em horas. Para isto, considere que a potência solar
incidente nas placas coletoras seja de 4,2 kW e que, devido a perdas, apenas 40% dessa potência seja utilizada
no aquecimento da água.
5. (Ufg 2003) O Brasil possui aproximadamente 27 milhões de chuveiros elétricos instalados em residências.
Mesmo que apenas uma fração desses chuveiros esteja ligada ao mesmo tempo, o consumo de energia desses
aparelhos ainda é muito grande, principalmente em horários de maior demanda de energia. Uma alternativa
viável é a utilização de coletores de energia solar com o objetivo de aquecer água. Suponha que um sistema de
aquecimento solar de água, com placas coletoras de área igual a 8 m£, seja utilizado em uma residência para
aquecer 1 m¤ de água contido em um reservatório. O sistema possui uma eficiência de 60%, isto é, ele converte
60% da energia solar incidente em calor. Considere que a intensidade da radiação solar vale I = 700 W/m£, que
o calor específico da água vale c(água) = 4.200 J/kg°C e que a densidade da água vale d = 1,0×10¤ kg/m¤.
a) Calcule, em horas, o tempo necessário para que a temperatura da água no reservatório aumente 10 °C.
b) Sabendo que um kWh de energia elétrica custa R$ 0,27, calcule quanto se gastaria para realizar o mesmo
aquecimento usando energia elétrica.
6. (Ufpe 2006) Considere que uma pequena boca de fogão a gás fornece tipicamente a potência de 250 cal/s.
Supondo que toda a energia térmica fornecida é transmitida a 200 g de água, inicialmente a 30°C, calcule o
tempo, em segundos, necessário para que a água comece a ferver. Considere a pressão atmosférica de 1 atm.
7. (Ufpr 2003) A uma caneca contendo 50ml de café, inicialmente a 70°C, adicionam-se 5g de um adoçante,
inicialmente a 28°C. Considere o calor específico do café igual a 1cal/(g.°C), o do adoçante igual a 2cal/(g.°C) e
a densidade do café igual a 1g/ml. Despreze as trocas de calor com a caneca e com o ambiente. Determine a
temperatura final da mistura, expressando-a em graus Celsius.
8. (Ufrj 2006) Em um calorímetro ideal, há 98g de água à temperatura de 0°C. Dois cubinhos metálicos são
introduzidos no calorímetro. Um deles tem massa 8,0g, calor específico 0,25cal/g°C e está à temperatura de
400°C. O outro tem 10g de massa, calor específico 0,20cal/g°C e está à temperatura de 100°C.
Posteriormente, esse último cubinho é retirado do calorímetro e verifica-se, nesse instante, que sua temperatura
é 50°C.
Calcule a temperatura final de equilíbrio da água e do cubinho que permanece no calorímetro.
9. (Ufrn 99) O projeto de um grupo de alunos para a feira de ciências da escola Ciência para Todos consiste de
uma miniatura, na forma de maquete, de um sistema de produção, transporte e consumo de energia elétrica,
conforme esquematizado na figura a seguir.
O sistema é iniciado com um fluxo de água dado por •, caindo de uma altura h sobre uma roda d'água, fazendo
com que esta gire. O fluxo • é medido em quilogramas por segundo. Através de uma correia, o giro da roda é
transmitido a um gerador elétrico. Fios condutores são conectados dos terminais do gerador a um liqüidificador,
cujo copo, termicamente isolado, contém um líquido cuja massa é mØ e cujo calor específico é cØ. O módulo da
aceleração da gravidade é g.
a) Especifique, em ordem seqüencial, as transformações de energia que ocorrem no sistema.
b) Expresse literalmente a energia mecânica por unidade de tempo (potência), P, inicialmente disponível, em
função de •, h e g.
c) Expresse literalmente a quantidade de calor, QØ, recebia pelo líquido, em função de mØ, cØ e ÐT,
considerando que ÐT foi o aumento de temperatura que o líquido sofreu.
d) Considerando que a temperatura do líquido, aumente de ÐT e o liqüidificador funcione durante um intervalo
de tempo Ðt, expresse literalmente a potência transferida ao líquido, PØ, em função de mØ, cØ, ÐT e Ðt.
e) Expresse literalmente o aumento de temperatura, ÐT, do líquido, em função de •, h, g, mØ, cØ e Ðt,
considerando que apenas 20% da potência inicialmente disponível, P, é transferida para o líquido.
10. (Ufrn 2005) Professor Jaulito mora à beira de um precipício de 100 m de desnível. Ele resolveu, então, tirar
vantagem de tal desnível para tomar água gelada. Para tal, enrolou uma corda na polia do compressor de um
pequeno refrigerador, passou-a por uma roldana, amarrou, na outra extremidade da corda, uma pedra de massa
10 kg e jogou-a precipício abaixo, conforme representado na figura.
Com esse experimento, Professor Jaulito consegue resfriar 50 g de água, que estava inicialmente a 25°C, para
5°C.
Suponha-se que
- todo o trabalho realizado pelo peso da pedra na queda é convertido em trabalho no compressor;
- a eficiência do refrigerador é de 40%;
- o calor específico da água é 1 cal/g°C;
- o valor da aceleração da gravidade no local é 10 m/s£;
- todas as forças resistivas são desprezíveis.
As informações e expressões necessárias para os cálculos envolvidos são as seguintes:
- trabalho realizado pela força gravitacional sobre um corpo de massa m : = mgh, em que g é a aceleração da
gravidade e h variação de altura que o corpo sofre;
- quantidade de calor recebida ou cedida por um corpo de massa m(c) : Q = m(c)cК em que c é seu calor
específico e К é a variação de temperatura sofrida pelo corpo;
- eficiência de um refrigerador: e = Q/
Com base no exposto, atenda às solicitações a seguir.
a) Calcule o trabalho realizado pelo peso da pedra.
b) Calcule a quantidade de calor cedida pelos 50g de água durante a queda da pedra.
c) Calcule o equivalente mecânico do calor que se pode obter a partir dos resultados desse experimento.
11. (Ufscar 2005) Para completar a higienização, uma mãe ferve o bico da mamadeira e, depois de retirá-lo da
água, aguarda que ela retome a fervura. Verte, então, 250 mL dessa água dentro do copo da mamadeira, que
mantém enrolado em um pano a fim de "conservar o calor". Aguarda o equilíbrio térmico e então joga fora a
água.
a) No passado, o copo das mamadeiras era feito de vidro. Em uma seqüência de ações como a descrita para
escaldar a mamadeira, ao preencher parcialmente recipientes de vidro com água quente, esses podem se partir
em dois pedaços, nitidamente separados na altura em que estava o nível d'água: um pedaço contendo a água
aquecida e o outro seco. Qual o nome do processo físico relacionado? Explique a razão da ruptura de frascos
de vidro submetidos a essas condições.
b) Em determinado dia quente a mãe inicia um dos seus "processos de esterilização". Dentro do copo da
mamadeira, que já se encontrava a 32°C - temperatura ambiente - derrama a água fervente que, devido à
localização geográfica de seu bairro, ferve a 98°C. Considerando que não houve perda de calor para o meio
externo, se após o equilíbrio a água derramada estava a 92°C e sabendo que a densidade da água é 1 g/mL e o
calor específico é 1 cal/(g.°C), determine a capacidade térmica do copo da mamadeira.
12. (Unesp 2003) Um cowboy atira contra uma parede de madeira de um bar. A massa da bala de prata é 2 g e
a velocidade com que esta bala é disparada é de 200 m/s. É assumido que toda a energia térmica gerada pelo
impacto permanece na bala.
a) Determine a energia cinética da bala antes do impacto.
b) Dado o calor específico da prata 234 J/kg°C, qual a variação de temperatura da bala, supondo que toda a
energia cinética é transformada em calor no momento que a bala penetra na madeira?
13. (Unicamp 2004) Para resfriar um motor de automóvel, faz-se circular água pelo mesmo. A água entra no
motor a uma temperatura de 80°C com vazão de 0,4L/s, e sai a uma temperatura de 95°C. A água quente é
resfriada a 80°C no radiador, voltando em seguida para o motor através de um circuito fechado.
a) Qual é a potência térmica absorvida pela água ao passar pelo motor? Considere o calor específico da água
igual a 4200J/kg°C e sua densidade igual a 1000kg/m¤.
b) Quando um "aditivo para radiador" é acrescentado à água, o calor específico da solução aumenta para 5250
J/kg°C, sem mudança na sua densidade. Caso essa solução a 80°C fosse injetada no motor em lugar da água,
e absorvesse a mesma potência térmica, qual seria a sua temperatura na saída do motor?
14. (Unicamp 2004) As temperaturas nas grandes cidades são mais altas do que nas regiões vizinhas não
povoadas, formando "ilhas urbanas de calor". Uma das causas desse efeito é o calor absorvido pelas superfícies
escuras, como as ruas asfaltadas e as coberturas de prédios. A substituição de materiais escuros por materiais
alternativos claros reduziria esse efeito. A figura mostra a temperatura do pavimento de dois estacionamentos,
um recoberto com asfalto e o outro com um material alternativo, ao longo de um dia ensolarado.
a) Qual curva corresponde ao asfalto?
b) Qual é a diferença máxima de temperatura entre os dois pavimentos durante o período apresentado?
c) O asfalto aumenta de temperatura entre 8h00 e 13h00. Em um pavimento asfaltado de 10.000 m£ e com uma
espessura de 0,1 m, qual a quantidade de calor necessária para aquecer o asfalto nesse período? Despreze as
perdas de calor. A densidade do asfalto é 2.300 kg/m¤ e seu calor específico C = 0,75kJ/kg°C.
15. (Unicamp 2005) Uma sala tem 6 m de largura, 10 m de comprimento e 4 m de altura. Deseja-se refrigerar o
ar dentro da sala. Considere o calor específico do ar como sendo 30 J/ (mol K) e use R= 8 J/ (mol K).
a) Considerando o ar dentro da sala como um gás ideal à pressão ambiente (P = 10¦ N/m£), quantos moles de
gás existem dentro da sala a 27 °C?
b) Qual é a quantidade de calor que o refrigerador deve retirar da massa de ar do item (a) para resfriá-Ia até 17 °
C?
16. (Uem 2004) Um calorímetro de capacidade térmica 48,0 cal/°C contém 6,5 kg de mercúrio. A temperatura do
conjunto é de 20°C. Coloca-se, em seu interior, um bloco de uma liga de alumínio cuja massa é de 810 g e cuja
temperatura é de 45°C. Assuma que os calores específicos do mercúrio e da liga de alumínio valem,
respectivamente,
c(Hg) = 0,03 cal/g.K e c(AØ) = 0,2 cal/g.K, que suas massas específicas valem, respectivamente, ˜(Hg) = 13,0
g/cm¤ (a 20°C) e ˜(AØ) = 2,7 g/cm¤ (a 45°C), que o coeficiente de dilatação volumétrica do mercúrio vale –(Hg) =
1,8x10¥ °C¢ e que o coeficiente de dilatação linear da liga de alumínio vale ‘(AØ) = 2,0x10¦ °C¢. Assinale o que
for correto.
01) A temperatura de equilíbrio térmico do sistema calorímetro+mercúrio+bloco de liga de alumínio vale 32,5°C.
02) Desde o instante em que o bloco de liga de alumínio foi incorporado ao sistema calorímetro+mercúrio até o
instante em que foi atingida a temperatura de equilíbrio térmico, o mercúrio recebeu 1,95 kcal.
04) A utilização do calorímetro permitiu que as trocas de calor ocorressem somente entre o bloco de liga de
alumínio e o mercúrio.
08) O calorímetro recebeu 480 cal da vizinhança em que se encontrava.
16) Na temperatura de 20°C, o volume do mercúrio era de 500 cm¤ e, na temperatura de 45°C, o volume do
bloco de liga de alumínio era de 300 cm¤.
32) Na temperatura de equilíbrio térmico, o volume de mercúrio estava 0,9 cm¤ maior e o do bloco de liga de
alumínio estava 0,27 cm¤ menor.
17. (Ufal 99) Uma panela de ferro, de massa igual a 600g, tem calor específico igual a 0,11cal/g°C e outra
panela de alumínio, de massa igual a 300g, tem calor específico igual a 0,22cal/g°C.
Analise as afirmações que seguem referentes a essas panelas
(
) A capacidade térmica da panela de ferro é igual a 66cal/°C.
(
) A energia interna das duas panelas tem o mesmo valor.
(
(
) A capacidade térmica da panela de alumínio é 220cal/°C.
) Para aquecer 200g de água na panela de ferro, de 20°C para 30°C, a água absorverá 660 calorias.
( ) Para aquecer 200g de água na panela de alumínio, de 20°C para 30°C, a panela sozinha absorverá 660
calorias.
18. (Ufal 99) Analise as proposições a seguir.
(
) O calor deve ser medido somente em calorias.
(
) Calor pode ser transformado em trabalho e vice-versa.
(
(
(
) O trabalho é energia transferida e, portanto, pode ser medido em joules.
) Calor e temperatura são grandezas de mesma natureza.
) O calor é equivalente à temperatura absoluta.
19. (Ufsc 2003) Em um dia calmo de verão, Paula encontra-se em uma praia sob forte incidência de raios
solares. Lembrando-se de que o calor específico da água é bem maior do que o da terra, ela observou
atentamente alguns fenômenos, buscando relacioná-los com as explicações e comentários apresentados pelo
seu professor de Física para os mesmos.
Considerando a situação descrita, assinale a(s) proposição(ões) CORRETA(S).
(01) Durante o dia, a temperatura da terra é maior do que a da água porque o calor específico da terra é menor
do que o da água.
(02) Durante a noite, a temperatura da água é menor do que a da terra porque o calor específico da água é
maior do que o da terra.
(04) Durante o dia, percebia-se na praia uma brisa soprando da terra para o mar. Uma possível justificativa é
porque a massa de ar junto à terra estava mais aquecida do que a massa de ar junto ao mar.
(08) Durante a noite, percebia-se na praia uma brisa soprando do mar para a terra. Uma possível justificativa é
porque a massa de ar junto ao mar estava mais aquecida do que a massa de ar junto à terra.
(16) Após o pôr-do-sol, a água se resfriou mais rapidamente do que a terra, porque o calor específico da água é
maior do que o da terra.
(32) Após o pôr-do-sol, a terra se resfriou mais rapidamente do que a água do mar, porque o calor específico da
água é bem maior do que o da terra.
(64) Foi possível observar que a água e a terra apresentaram a mesma temperatura, sempre.
Soma (
)
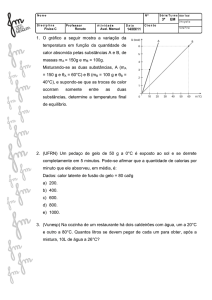
20. (Ufsc 2006) O gráfico a seguir representa a quantidade de calor absorvida por dois objetos A e B ao serem
aquecidos, em função de suas temperaturas.
Observe o gráfico e assinale a(s) proposição(ões) CORRETA(S).
(01) A capacidade térmica do objeto A é maior que a do objeto B.
(02) A partir do gráfico é possível determinar as capacidades térmicas dos objetos A e B.
(04) Pode-se afirmar que o calor específico do objeto A é maior que o do objeto B.
(08) A variação de temperatura do objeto B, por caloria absorvida, é maior que a variação de temperatura do
objeto A, por caloria absorvida.
(16) Se a massa do objeto A for de 200 g, seu calor específico será 0,2 cal/g°C.
GABARITO
1. ÐQ = 160.000 cal
2. a) 32°C.
b) 0,5 cal/g °C.
3. 50°C
4. a) 4,0 × 10§ cal.
b) 2,77 h.
5. a)¸3,5 h
b) R$ 3,15
6. 56 s.
7. 63
8. Numa troca de calor o somatório das trocas de calor entre os participantes da troca é zero.
98.1.[T- 0]+8.0,25.[T-400]+10.0,2.(50 -100)=0
Simplificando e resolvendo essa equação, obtem-se:
100.T - 800 - 100 = 0;
T = 9°C
9. a) GRAVITACIONAL ë CINÉTICA ë ELÉTRICA ë CINÉTICA
b) P = • . g . h
c) Q(L) = M(L).C(L).ÐT
d) P(L) = (M(L).C(L).ÐT/ÐT)
e) Ð T = (0,2.•ghÐT/M(L)C(L))
10. a) O trabalho realizado pelo peso da pedra é
= (mp) . g . h = 10 . 10 . 100 = 10000 J
b) A quantidade de calor cedida pela água é
Q = (ma) . c . К = 50 . 1 . ( 5 - 25 ) = -1000 cal
c) Como a eficiência é a relação e = Q/, temos que Q = e (onde Q e devem ser expressos numa mesma
unidade de energia). Para transformar Q(cal) em Q(J), devemos fazer
Q(J) = Q(cal) × Eq, onde Eq é o equivalente mecânico do calor. Desta forma teremos
Q(cal) × Eq = e (J)
Logo, Eq = e (J)/ Q(cal)
Eq = 0,4 . 10.000 J/1.000 cal;
logo, Eq = 4 J/cal
Resultados válidos
1.000 cal = 0,4 . 10.000 J ; logo, 1 cal = 4 J
11. a) Dilatação térmica. Levando-se em conta que o vidro é mau condutor de calor ocorrem dilatações
desiguais, e isto produz a ruptura.
b) 25 cal/°C
12. a) 40J
b) 85,5°C
13. a) 25200 W
b) 92°C
14. a) a curva A
b) 10°C no mesmo horário
c) 4,3.10¨kJ
15. a) 1 × 10¥ mols
b) 3 × 10§ J
16. 50
17. V F V F V
18. F V V F F
19. 01 + 32 = 33
20. 01 + 02 + 08 + 16 = 27