ISSN 1413-9979
Revista
diagnóstico
& Tratamento
Volume 19 • edição 3
Federada da
JUL-SET 2014
Sumário
revista diagnóstico e tratamento • Volume 19 • edição 3
Expediente
Editorial
ii
103
105
Artigo original
110
115
Relato de caso
119
Patentes: unir para conquistar
Alessandro Wasum Mariani, Paulo Manuel Pêgo-Fernandes
Medicamentos usados por idosos e critério de Beers e colaboradores
Aline Cristina Henriques da Silva, Leonardo Affonso Pedrosa Sibillo, Marcelo Rozenfeld Levites,
Maria Alenita de Oliveira
Estudo comparativo das bombas de rolete e centrífuga em pacientes
submetidos à cirurgia de revascularização do miocárdio
Carolina Teles Taipina Matias, Paulo Manuel Pêgo-Fernandes, Ramez Anbar, Nádia Taylor,
Aristides Correia, Ludhmila Abrahão Hajjar, Roberto Kalil Filho, Fabio Biscegli Jatene
Pancitopenia associada a tratamento com azatioprina e mesalazina em
paciente com colite ulcerativa: relato de caso
Gerson Julio de Freitas, Maycon Paulo de Oliveira, Virginia Fernandes Moça Trevisani,
Marcelo Moock, Sergio Elia Mataloun
Imunodeficiência comum variável: relato de caso
Patrícia Estrela Evangelista, Elenice Stroparo
Impetigo bolhoso disseminado
Dermatologia
125
Nutrologia
129
Efetividade e segurança do vegetal Cissus sicyoides (“insulina vegetal”)
como fitoterápico hipoglicemiante
132
Sequência de testes pode melhorar identificação do delirium em idosos
atendidos na emergência
134
Purulência do escarro e proteína C-reativa são preditores de mau
prognóstico na exacerbação da doença pulmonar obstrutiva crônica
POEMs: Patients-oriented
evidence that matters
Linguagens
136
Residência e ensino médico
139
Eletrocardiograma
141
Medicina sexual
144
Vanessa Mello Tonolli, Juliana Polizel Ocanha, Hamilton Ometto Stolf
Hernani Pinto de Lemos Júnior, André Luis Alves de Lemos
Autores da tradução: Pablo Gonzáles Blasco, Marcelo Rozenfeld Levites, Cauê Monaco
Autores da tradução: Pablo Gonzáles Blasco, Marcelo Rozenfeld Levites, Cauê Monaco
Lógicas
Alfredo José Mansur
A vocação médica e a academia
Ricardo Aun
Fibrilação atrial na síndrome de Wolff-Parkinson-White
Antonio Américo Friedmann
Desejo sexual em mulheres jovens em relacionamentos estáveis
Heloisa Junqueira Fleury, Mirian Bernardes Lopes Alves, Carmita Helena Najjar Abdo
Medicamentos orais para o tratamento do pé de atleta (tinea pedis)
148
Destaques Cochrane
Intervenções para a prevenção da obesidade infantil
150
Instruções aos autores
Imagem da capa: shutterstock.com
Tradução: Centro Cochrane do Brasil e Liga de Medicina Baseada em Evidências da Escola
Paulista de Medicina — Universidade Federal de Medicina (EPM-Unifesp)
Autora dos comentários independentes: Leontina da Conceição Margarido
I
Tradução: Centro Cochrane do Brasil e Liga de Medicina Baseada em Evidências da Escola
Paulista de Medicina — Universidade Federal de Medicina (EPM-Unifesp)
Autora dos comentários independentes: Angela Maria Spinola e Castro
EXPEDIENTE
Revista
diagnóstico
Tratamento
A Revista Diagnóstico & Tratamento (indexada na base LILACS)
é uma publicação trimestral da Associação Paulista de Medicina
Disponível na versão para smartphone e tablet (iOS e Android)
Editores
Paulo Manuel Pêgo-Fernandes
Álvaro Nagib Atallah
Assistente Editorial
Marina de Britto
Assessora Editorial
Rachel Riera
Auxiliar Editorial
Joyce de Fátima Silva Nakamura
Editores Associados
Aytan Miranda Sipahi
Edmund Chada Baracat
Elcio dos Santos Oliveira Vianna
Heráclito Barbosa de Carvalho
José Antonio Rocha Gontijo
Julio César Rodrigues Pereira
Olavo Pires de Camargo
Orlando César de Oliveira Barreto
Jornalista Científica e Editora
Patrícia Logullo (MTb 26.152)
Palavra Impressa Editora – Fone (11) 3032-6117
Produção Editorial
Zeppelini Editorial Ltda
www.zeppelini.com.br
[email protected] – Fone (11) 2978-6686
Conselho Editorial
Adauto Castelo Filho (Doenças Infecciosas e Parasitárias)
Alberto José da Silva Duarte (Alergia e Imunologia)
Antônio José Gonçalves (Cirurgia Geral)
Armando da Rocha Nogueira (Clínica Médica/Terapia Intensiva)
Artur Beltrame Ribeiro (Clínica Médica)
Bruno Carlos Palombini (Pneumologia)
Carmita Helena Najjar Abdo (Psiquiatria)
Délcio Matos (Coloproctologia/Gastroenterologia Cirúrgica)
Eduardo Katchburian (Microscopia Eletrônica)
Edmund Chada Baracat (Ginecologia)
Enio Buffolo (Cirurgia Cardiovascular)
Ernani Geraldo Rolim (Gastroenterologia)
Fernando Antonio Patriani Ferraz (Neurocirurgia)
Flávia Tavares Elias (Avaliação Tecnológica em Saúde)
Guilherme Carvalhal Ribas (Neurocirurgia)
Irineu Tadeu Velasco (Clínica Médica/Emergências)
Jair de Jesus Mari (Psiquiatria)
João Baptista Gomes dos Santos (Ortopedia)
João Carlos Bellotti (Ortopedia e Traumatologia)
Lilian Tereza Lavras Costallat (Reumatologia)
Manoel Odorico de Moraes Filho (Oncologia Clínica)
Marcelo Zugaib (Obstetrícia/Ginecologia)
Marco Antonio Zago (Hematologia)
Maurício Mota de Avelar Alchorne (Dermatologia)
Milton de Arruda Martins (Clínica Médica)
Moacyr Roberto Cuce Nobre (Reumatologia)
Nestor Schor (Clínica Médica, Nefrologia)
Noedir Antonio Groppo Stolf (Cirurgia)
Orsine Valente (Clínica Geral, Endocrinologia e Metabologia)
Raul Cutait (Gastroenterologia e Proctologia)
Rubens Belfort Mattos Junior (Oftalmologia)
Rubens Nelson A. de Assis Reimão (Neurologia)
Sérgio Luiz Faria (Radioterapia)
Ulysses Fagundes Neto (Gastroenterologia Pediátrica)
Ulysses G. Meneghelli (Gastroenterologia)
Correspondências para
Associação Paulista de Medicina
Departamento Científico – Publicações Científicas
Av. Brig. Luís Antônio, 278 – 7o andar – São Paulo – SP – Brasil – CEP 01318-901
Tel: (11) 3188-4310 / 3188-4311
Home page: http://www.apm.org.br/revista-rdt.aspx – E-mail: [email protected]; [email protected]
TODOS OS DIREITOS RESERVADOS À ASSOCIAÇÃO PAULISTA DE MEDICINA
A revista Diagnóstico & Tratamento não se responsabiliza pelos conceitos emitidos nos artigos assinados. A reprodução impressa,
eletrônica ou por qualquer outro meio, total ou parcial desta revista só será permitida mediante expressa autorização da APM.
Diretoria Executiva da Associação Paulista de Medicina (Triênio 2011-2014)
Presidente
1o vice-presidente
o
2 vice-presidente
3o vice-presidente
4o vice-presidente
Secretário geral
1o Secretário
Diretor administrativo
Diretor administrativo adjunto
1o diretor de patrimônio e finanças
o
2 diretor de patrimônio e finanças
Diretor científico
Diretor científico adjunto
Diretor de defesa profissional
Diretor de defesa profissional adjunto
Diretor de comunicações
Diretor de comunicações adjunto
Diretor de marketing
Diretor de marketing adjunto
Diretora de eventos
Diretora de eventos adjunta
Diretor de tecnologia da informação
Diretor de tecnologia de informação adjunto
Diretor de previdência e mutualismo
Diretor de previdência e mutualismo adjunto
Florisval Meinão
Roberto Lotfi Júnior
Donaldo Cerci da Cunha
Paulo De Conti
Akira Ishida
Paulo Cezar Mariani
Ruy Yukimatsu Tanigawa
Lacildes Rovella Júnior
Roberto de Mello
Murilo Rezende Melo
João Márcio Garcia
Paulo Manuel Pêgo Fernandes
Álvaro Nagib Atallah
João Sobreira de Moura Neto
Marun David Cury
Renato Françoso Filho
Leonardo da Silva
Nicolau D’Amico Filho
Ademar Anzai
Mara Edwirges Rocha Gândara
Regina Maria Volpato Bedone
Desiré Carlos Callegari
Antônio Carlos Endrigo
Paulo Tadeu Falanghe
Clóvis Francisco Constantino
Diretor social
Diretor social adjunto
Diretora de responsabilidade social
Diretora de responsabilidade social adjunta
Diretor cultural
Diretor cultural adjunto
Diretor de serviços aos associados
Diretor de serviços aos associados adjunto
Diretor de economia médica
Diretor de economia médica adjunto
1o diretor distrital
2o diretor distrital
3o diretor distrital
4o diretor distrital
5o diretor distrital
6o diretor distrital
7o diretor distrital
8o diretor distrital
9o diretor distrital
10o diretor distrital
11o diretor distrital
12o diretor distrital
13o diretor distrital
14o diretor distrital
Alfredo de Freitas Santos Filho
Nelson Álvares Cruz Filho
Denise Barbosa
Yvonne Capuano
Guido Arturo Palomba
Carlos Alberto Monte Gobbo
José Luiz Bonamigo Filho
João Carlos Sanches Anéas
Tomás Patrício Smith-Howard
Jarbas Simas
Airton Gomes
Arnaldo Duarte Lourenço
Lauro Mascarenhas Pinto
Wilson Olegário Campagnone
José Renato dos Santos
José Eduardo Paciência Rodrigues
José Eduardo Marques
Helencar Ignácio
José do Carmo Gaspar Sartori
Paulo Roberto Mazaro
José de Freitas Guimarães Neto
Marco Antônio Caetano
Marcio Aguilar Padovani
Wagner de Matos Rezende
EDITORIAL
Patentes: unir para conquistar
Alessandro Wasum MarianiI, Paulo Manuel Pêgo-FernandesII
Instituto do Coração (InCor), Hospital das Clínicas (HC), Faculdade de Medicina da Universidade de São Paulo (FMUSP)
Os últimos 20 anos foram importantes para a ciência brasileira, saímos de uma posição quase obscura para alcançar
uma posição relevante no cenário internacional. A prova mais
contundente é a grande evolução no número de publicações
e de citações alcançados por autores e instituições brasileiras.
Os esforços empregados pelo governo, pelas universidades,
centros de pesquisa e pesquisadores geraram frutos mensuráveis no número de publicações produzidas no Brasil.
Informação divulgada demonstra que, em 2011, atingimos o
número total de 49.664 artigos, o que nos fez saltar para o 13o
lugar no ranking entre os países com maior número de publicações.1 Por outro lado, questiona-se que o impacto dessas publicações ainda é menor que o esperado. Todavia, um informe
de relevância nesse sentido é a constatação de que diversas
Universidades Brasileiras encontram-se em posição de destaque no “Ranking Web of Universities” da Webometrics, principalmente no quesito “Impacto”.2
Entretanto, é notável que outra importante faceta da atividade científica não acompanhou essa evolução: a produção de patentes. Estudo demostrou que o total de pedidos de
patentes no Brasil entre 2001 e 2010, aumentou 64%, todavia,
o número final, 5,5 mil em 2010, ainda é pequeno no contexto mundial.3 Outra informação negativa é que, entre as economias emergentes do mundo, o Brasil ainda tem posição de
pouca relevância quando estudamos o número de patentes
aqui desenvolvidas bem como quantas dessas acabam por
gerar um produto final comercializável. Em 2011 foram registradas pouco mais de 20 mil patentes no Brasil, número
pequeno se comparada à produção da China, 400 mil no
mesmo ano.3
Segundo a Agência USP de Inovação, patente, por conceito, é “... um título de propriedade temporária sobre uma
invenção ou modelo de utilidade, outorgado pelo Estado aos
inventores ou outras pessoas físicas ou jurídicas detentoras
de direitos sobre a criação”.4 O racional e a justificativa para
a existência das patentes residem no fato de que: “a pesquisa e o desenvolvimento para elaboração de novos produtos
requerem, na maioria das vezes, grandes investimentos humanos e financeiros. Proteger esse produto através de uma
patente significa prevenir-se de competidores, inibindo a
concorrência desleal”.4
Algumas considerações são importantes:
A patente se justifica pelo produto que ela pode gerar, patente não é título, tampouco não pode ser encarada apenas
como item curricular.
Quem mais tem a ganhar com o desenvolvimento na produção de patentes é o Brasil enquanto país, afinal, isso pode,
em última análise, representar uma inserção positiva na matriz produtiva brasileira.
Em países desenvolvidos, podemos identificar claramente
um “círculo virtuoso” que mantém ativo um “sistema” de produção de patentes: as empresas injetam dinheiro em centros
Este editorial foi publicado na versão em inglês no periódico São Paulo Medical Journal/Evidence for Health Care, volume 131, edição número 6, de
novembro a dezembro de 2013.
Cirurgião torácio, Instituto do Coração (InCor), Hospital das Clínicas (HC), Faculdade de Medicina da Universidade de São Paulo (FMUSP).
Professor titular, Disciplina de Cirurgia Torácica, Instituto do Coração (InCor), Hospital das Clínicas (HC), Faculdade de Medicina da Universidade de São
Paulo (FMUSP).
I
II
Endereço para correspondência:
Alessandro Wasum Mariani
Rua Treze de Maio, 1.217 — apto 31 — Bela Vista — São Paulo (SP) — CEP 01327-001
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 18 de setembro de 2013 — Última modificação: 18 de setembro de 2013 — Aceite: 27 de setembro de 2013
Diagn Tratamento. 2014;19(3):103-4.
103
Patentes: unir para conquistar
de pesquisa que desenvolvem projetos, que se transformam
em patente para a empresa, que a confecciona e comercializa
como um produto final, gerando capital, que é frequentemente
reinvestido no ponto de partida. A participação dos governos
não se limita apenas à regulação, mas deve ocorrer intervenção quando esta se faz necessária.
Voltando ao Brasil, iniciativas positivas nesse sentido podem ser identificadas. Por exemplo, a criação, pela
Fundação de Amparo à Pesquisa do Estado de São Paulo
(Fapesp), dos novos Centros de Pesquisa, Inovação e
Difusão (Cepids). Estes centros têm como uma de suas características a busca e consolidação de parcerias com setor
produtivo com o objetivo final de promover a transformação à cultura da inovação.5
Outra iniciativa importante tem partido das próprias
Universidades por meio da criação de agências com a meta
comum de dar apoio à inovação, seja dentro da Universidade,
ou mesmo fora dela, pela parceria com empresas, pesquisadores e centros de pesquisas. Notadamente o foco dessas
chamadas “Agências de Inovação” é o desenvolvimento de
patentes. Importantes Universidades já abarcaram a ideia:
Universidade de São Paulo (USP), Universidade Estadual de
Campinas (Unicamp), Universidade Estadual Paulista (Unesp),
Universidade Federal de São Carlos (UFSCar), Universidade
Estadual de Londrina (UEL), Universidade Federal do Rio de
Janeiro (UFRJ), entre outras.
Governo, universidades e empresas precisam não somente
unir esforços, mas, sobretudo, coordená-los de uma melhor
forma para que as atividades de cada segmento se completem,
iniciando processo produtivo que gere patentes e produtos,
determinando assim não só uma alavancagem na ciência, mas
também na atual cadeia produtiva da economia brasileira.
REFERÊNCIAS
1. Righetti S. Produção científica do Brasil aumenta, mas qualidade
cai. Folha de S.Paulo. 22 abr. 2013: Ciência + Saúde. Disponível
em:
http://www1.folha.uol.com.br/fsp/cienciasaude/105099producao-cientifica-do-brasil-aumenta-mas-qualidade-cai.
shtml. Acessado em 2013 (24 set).
2. Ranking Web of Universities. World. Disponível em: http://
www.webometrics.info/en/world?sort=asc&order=ranking.
Acessado em 2013 (24 set).
3. Garcia R. Países emergentes quase alcançam G7 em
patentes. Folha de S.Paulo. 6 mar. 2013: Ciência. Disponível
104
Diagn Tratamento. 2014;19(3):103-4.
em: http://www1.folha.uol.com.br/ciencia/1241294-paisesemergentes-quase-alcancam-g-7-em-patentes.shtml.
Acessado em 2013 (24 set).
4. Agência USP de Inovação. Patentes. USP Inovação. Disponível
em:
http://www.inovacao.usp.br/propriedade/patentes.php.
Acessado em 2013 (24 set).
5. Marques F. A expansão do conhecimento. Pesquisa FAPESP.
2013;208:17-25. Disponível em: http://revistapesquisa.fapesp.
br/wp-content/uploads/2013/06/016-025_CAPA_CEPIDS_208.
pdf. Acessado em 2013 (24 set).
ARTIGO ORIGINAL
Medicamentos usados por idosos
e critério de Beers e colaboradores
Aline Cristina Henriques da SilvaI, Leonardo Affonso Pedrosa SibilloI, Marcelo Rozenfeld LevitesII,
Maria Alenita de OliveiraIII
Hospital Beneficência Portuguesa de São Paulo, São Paulo
RESUMO
Contexto e objetivo: A população idosa apresenta interações medicamentosas e efeitos adversos devidos a alterações corporais, comorbidades associadas e polifarmácia. O objetivo deste trabalho foi caracterizar o padrão dos medicamentos usados por idosos em um hospital,
identificar a polifarmácia e os medicamentos potencialmente inadequados através dos critérios de Beers e colaboradores. Desenho e local: Estudo transversal realizado no Hospital Beneficência Portuguesa de São Paulo, em 2012 e 2013. Métodos: Foram analisados 123 prontuários
de pacientes internados no Hospital Beneficência Portuguesa em 2011, entre 65 e 89 anos de idade, e seus dados analisados por análise de
variância (ANOVA) de uma via, seguido do teste de Student-Newman-Keuls para comparações múltiplas. Resultados: Não houve diferença
entre o número de medicamentos utilizados por idosos entre gêneros. Verificou-se prevalência de 56,91% de polifármácia entre os pacientes.
Ocorreu maior tendência a polifarmácia no sexo masculino entre 65 e 70 anos e no sexo feminino, entre 80 e 85 anos. Observou-se maior
prevalência no uso de ácido acetilsalicílico, espironolactona, amiodarona, glibenclamida, lorazepam/clonazepam. Conclusão: Existe prevalência relevante de polifarmácia e há aumento gradual conforme a idade. Existe número alto de prescrições de medicações potencialmente
inadequadas para os idosos, mostrando a importância do conhecimento do critério de Beers e colaboradores. Tornam-se necessários novos
estudos em populações mais abrangentes.
PALAVRAS-CHAVE: Idoso, envelhecimento, polimedicação, toxicidade de drogas, /efeitos de drogas
INTRODUÇÃO
Com o aumento da expectativa de vida devido ao investimento em ações de saúde pública e avanços na terapêutica
e na área de pesquisa médica, e tendo o apoio da renovação
tecnológica constante, a população de idosos brasileiros vem
crescendo junto a um perfil de doenças crônicas e múltiplas
comorbidades.1,2 Entre 1950 e 2025 a população idosa brasileira terá crescido 16 vezes contra 5 vezes a população total,
chegando a um total estimado de 33,4 milhões de idosos.2
A população idosa é a mais predisposta a apresentar efeitos
adversos dos medicamentos e interações medicamentosas,
sendo estimado que cerca de 24% das admissões hospitalares
estejam relacionadas a problemas com medicamentos e seus
efeitos adversos, representando 5% a 10% do total dos custos
hospitalares e sendo a quinta colocada entre as principais
causas de morte.1-3 A polifarmácia (definida como o uso de
cinco ou mais medicamentos) tem alta prevalência em idosos devido às diversas comorbidades associadas encontradas,
além do acompanhamento concomitante por profissionais
de diversas especialidades médicas, sendo comum que sejam
Acadêmicos do sexto ano do curso de Medicina da Universidade Anhembi Morumbi, São Paulo.
Médico de família e diretor da Sociedade Brasileira de Medicina de Família (Sobramfa).
III
Pneumologista no Hospital Beneficência Portuguesa de São Paulo. Professora de graduação do curso de medicina da Universidade Anhembi Morumbi, São Paulo.
I
II
Endereço para correspondência:
Aline Cristina Henriques da Silva
Rua José Benedetti, 158 — apto 151 — São Caetano do Sul (SP) — CEP 09531-000
Tel. (11) 2376-8724 — Cel. (11) 99596-5563
E-mail: [email protected]
Este artigo foi apresentado como Trabalho de Conclusão de Curso (TCC) pelos alunos do curso de medicina da Universidade Anhembi Morumbi, São Paulo,
no ano de 2013
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 19 de agosto de 2013 — Última modificação: 19 de março de 2014 — Aceite: 25 de março de 2014
Diagn Tratamento. 2014;19(3):105-9.
105
Medicamentos usados por idosos e critério de Beers e colaboradores
acrescentadas drogas em vez de suspensas ou modificada
a posologia.2-4
Uma lista de medicamentos potencialmente inadequados
para idosos foi criada e publicada por Beers e colaboradores,
baseados na frequência de prescrições de um grupo de instituições de repouso para idosos em Los Angeles (Estados
Unidos), em 1991,5 sendo estabelecido critério após análise de
13 especialistas dos Estados Unidos e 1 especialista do Canadá.
O critério foi revisado e expandido em 1997, 2003 e mais recente em 2012. O critério atualmente inclui 53 medicamentos ou
classes de medicamentos que são subdivididos entre aqueles
que não devem ser usados por idosos, que devem ser evitados
quando da existência de determinada doença, que pode ser
exacerbada, e medicamentos que devem ser usados com cautela. De acordo com a última atualização do critério de Beers
e colaboradores de 2012, estima-se que, nos Estados Unidos,
40% dos idosos recebem um ou mais medicamentos da lista
de Beers considerados inadequados para idosos.6
O presente estudo procura identificar e caracterizar os medicamentos mais utilizados por idosos e, por meio do critério de Beers e colaboradores, avaliar quais merecem atenção
devido ao seu alto risco de levar a reações adversas, e como
proposta mostrar para o clínico a importância de se pesar os
riscos e benefícios das drogas e de adaptações individualizadas na conduta farmacológica das doenças em idosos.
OBJETIVO
Os objetivos do presente estudo são caracterizar o padrão
dos medicamentos e quais são prescritos e potencialmente
inadequados para os idosos e também classificar a polifarmácia nesse grupo, de acordo com gênero e idade, investigando a
quantidade e tipos de medicamentos usados.
MÉTODOS
Trata-se de estudo transversal. Fizeram parte deste estudo 123 prontuários de pacientes internados no Hospital
Beneficência Portuguesa de São Paulo na faixa etária entre 65 e
89 anos de idade de ambos os sexos no período entre janeiro
e dezembro de 2011.
Foram coletados os dados: número de prontuário, idade,
gênero, quantidade e nome dos medicamentos em uso no
momento da internação hospitalar no período de janeiro
a dezembro de 2011; tabulados em planilhas. Foram considerados medicamentos com alto potencial de desencadear
efeitos adversos em idosos aqueles inclusos no critério de
Beers e colaboradores atualizado em 2012 pela Sociedade
Americana de Geriatria.6 A partir desse ponto, a casuística
foi dividida em dois grupos: grupo de polifarmácia (uso de
106
Diagn Tratamento. 2014;19(3):105-9.
cinco ou mais medicamentos) e grupo não polifarmácia (uso
de menos de cinco medicamentos) para análise de prevalência de medicamentos potencialmente inadequados e comparação entre os grupos.
Os resultados foram apresentados como média ± erro padrão da média (EPM) para valores absolutos ou porcentagem
de indivíduos analisados. As diferenças entre grupos foram
analisadas por análise de variância (ANOVA) de uma via, seguida do teste de Student-Newman-Keuls para comparações
múltiplas. Valores de P < 0,05 foram considerados estatisticamente significativos.
RESULTADOS
Prevalência de polifarmácia na população idosa
Foram utilizados 123 prontuários (n = 123 idosos). Foram
analisados um total de 615 medicamentos, sendo que 220
desses medicamentos estão representados no critério de
Beers. A prevalência de polifarmácia na população estudada
foi de 56,91%.
Medicamentos de uso mais frequente em idosos
À análise da porcentagem de frequência de medicamentos
utilizados por idosos, obteve-se que a soma dos fármacos do
grupo polifarmácia representou 76,09% da amostragem total.
Dentre os medicamentos analisados (Tabela 1), no grupo polifarmácia foi observada maior prevalência no uso de ácido
acetilsalicílico, representando 7,97% do total de medicamentos, atenolol/metoprolol 4,39%, captopril/enalapril 4,71%, hidroclortiazida 3,1% e sinvastatina 5,36%.
Medicamentos de uso mais frequente em idosos segundo o
critério de Beers
À análise da porcentagem de frequência de medicamentos utilizados por idosos, obteve-se que os medicamentos
considerados inadequados para idosos tinham prevalência
de 35,47% na análise da amostragem total. Dentre os medicamentos considerados inadequados para idosos analisados
(Gráfico 1), principalmente no grupo polifarmácia foi observada maior prevalência no uso de ácido acetilsalicílico,
22,27% seguido de, espironolactona 12,63%, cloridrato de
amiodarona 4,09%, glibenclamida 2,27%, lorazepam/clonazepam também 2,27% e metildopa 1,36%. Já no grupo não
polifarmácia, foi obtida maior prevalência no uso de ácido
acetilsalicílico, sendo 11,09%.
Número de medicamentos utilizados por idosos
À análise comparativa da média de medicamentos utilizados por idosos observou-se que não há diferença significativa
(P < 0,05) entre o número de medicamentos utilizados pelos
Aline Cristina Henriques da Silva | Leonardo Affonso Pedrosa Sibillo | Marcelo Rozenfeld Levites | Maria Alenita de Oliveira
Tabela 1. Frequência dos medicamentos usados por 220 idosos de acordo com os critérios de Beers e cols.6
% total de
Frequência
Preenche
medicamentos
(não polifarmácia)
critérios?
em uso
20
3
3
8
12
10
3
3
8
6
14
5
5
10
6
10
19
Ácido acetilsalicílico
Cloridrato de amiodarona
Besilato de anlodipino
Atenolol/metoprolol
Captopril/enalapril/benazepril
Carvedilol
Clorpropamida
Bissulfato de clopidogrel
Digoxina
Espironolactona
Glibenclamida
Hidroclorotiazida
Lorazepam/clonazepan
Losartana/valsartana/candesartana
Cloridrato de metformina
Metildopa
Mononitrado de isossorbida
Omeprazol/esomeprazol
Propanolol
Sinvastatina/atorvastatina/rosuvastatina
Outros medicamentos
3,25
0,49
0,49
1,30
1,95
1,63
0,49
0,49
1,30
0,98
2,28
0,81
0,81
1,63
0,98
1,63
3,09
Sim
Sim
Não
Não
Não
Não
Sim
Não
Sim
Sim
Sim
Não
Sim
Não
Não
Sim
Não
Não
Não
Não
Não
%
total
9,09
1,36
1,36
1,36
2,73
-
Total de medicamentos em uso
615
Total de medicamentos em uso*
220
Frequência % do total de
Preenche % do
de
medicamentos
critérios? total
polifarmácia
em uso
49
13
11
27
29
23
1
10
1
19
5
25
5
19
10
3
19
21
11
33
100
7,97
2,11
1,79
4,99
4,72
3,74
0,16
1,63
0,16
3,09
0,81
4,07
0,81
3,09
1,63
0,49
3,09
3,41
1,79
5,37
16,26
Sim
Sim
Não
Não
Não
Não
Sim
Não
Sim
Sim
Sim
Não
Sim
Não
Não
Sim
Não
Não
Não
Não
Não
22,27
5,91
0,45
0,45
8,64
2,27
2,27
1,36
-
80
70
60
50
40
30
20
10
0
r
pr ona
op
am
id
Es
a
D
pi
ig
ro
ox
no
in
la
a
ct
on
G
o
lib
m
a
en
cl
am
Lo
id
ra
a
ze
pa
m
/..
M
.
et
ild
op
a
Cl
or
io
da
AA
S
Polifarmácia (> 5)
No de medicamentos (< 5)
Am
To
ta
l
Frequência (% total)
*Segundo os critérios de Beers e colaboradores.
Análise da porcentagem de frequência de medicamentos utilizados por idoso.
Os dados estão expressos como média ± erro padrão da média (EPM) para
n = 220, sendo *P < 0,05 versus respectivo grupo no de medicamentos
(< 5); †P < 0,05 versus polifarmácia (> 5) Total, AAS (ácido acetilsalicílico),
clorpropamida, espironolactona e digoxina; ‡P < 0,05 versus no de
medicamentos (< 5) Total, cloridrato de amiodarona, espironolactona e
gliblenclamida.
Gráfico 1. Frequência de medicamentos utilizados por idoso
segundo critério de Beers e cols.6
pacientes do sexo masculino e feminino, tanto entre o grupo
não polifarmácia como entre o grupo polifarmácia.
Influência da idade na frequência e número de medicamentos utilizados por idosos
A análise comparativa da frequência e o número de
medicamentos utilizados por idoso em relação à idade demonstrou que há maior frequência na utilização de medicamentos em idosos do sexo masculino com idade entre
65 e 70 anos, com média de 6,14 medicamentos por idoso
(desvio padrão, DP ± 2,67). Já no sexo feminino, foi observada maior frequência na utilização de medicamentos em
idosas entre 80 e 85 anos com média de 6,2 medicamentos
por idoso (DP ± 1,64; P < 0,05).
DISCUSSÃO
De acordo com o Instituto Brasileiro de Geografia e
Estatística 2012 o aumento da proporção de idosos de
2000 para 2005 (de 13,8% para 14,4%) e queda do número
de jovens na mesma época (de 47,9% para 42,5%) ressalta
a importância em investimentos futuros em previdência
Diagn Tratamento. 2014;19(3):105-9.
107
Medicamentos usados por idosos e critério de Beers e colaboradores
social e controle e prevenção de doenças crônico-degenerativas, contrastando a uma diminuição de contribuintes
efetivos na sociedade.7
Um estudo norte-americano evidenciou que, nos Estados
Unidos, um total de gastos em saúde estimados para medicações potencialmente inadequadas para idosos chegou
a 7,2 bilhões de dólares. Estima-se que 27% dos eventos
adversos relacionados ao uso de medicações em cuidados
primários e 46% em crônicos podem ser prevenidos.6 Nesse
contexto, o presente estudo procurou identificar os principais medicamentos considerados inadequados para idosos
em um hospital brasileiro e a relação de uso deles entre gênero, idade e polifarmácia.
O critério de Beers é um instrumento para identificação
de medicações potencialmente inadequadas para idosos,
utilizado em um contexto internacional e consagrado na
literatura, porém não contempla realidades específicas de
cada região, conforme a comercialização de determinadas
medicações naquele país e suas respectivas dosagens, dificultando a análise em um contexto fora da realidade dos
Estados Unidos.8-13
Estudos feitos nas cidades de Fortaleza,9 São Paulo10 e
Carlos Barbosa11 apresentaram prevalência de polifarmácia
de 13,6%, 36% e 13,9% respectivamente. Evidenciamos prevalência de 56,91% no presente estudo, sendo esse resultado
elevado por provável influência do serviço de estudo ser em
ambiente hospitalar e terciário, apresentando maior prevalência de doenças mais complexas e que necessitam de
maior número de medicações e intervenções de múltiplos e
diferentes profissionais.
À análise das características sociodemográficas do estudo de São Paulo, obteve-se associação significativa entre
polifarmácia, sexo feminino, idade superior a 75 anos, maior
faixa de renda e atuação no mercado de trabalho.10 Estudo
de Fortaleza demonstrou maior incidência de polifarmácia
no centro (13,4%), comparado à periferia (5,4%),9 atentando para futuro aumento da incidência de polifarmácia no
Brasil conforme o desenvolvimento no país.
Sobre a maior prevalência de mulheres em uso de mais de
cinco medicações, diferente do estudo de São Paulo,10 no presente estudo não foram identificadas diferenças entre gêneros.
Identificamos uso de medicamentos segundo critério de
Beers no grupo polifarmácia 75% maior que o grupo que
fazem uso de menos de cinco medicamentos. Por vezes,
equivocadamente, reações adversas a medicamentos são
interpretadas como novas entidades clínicas e tratadas com
novos agentes, constituindo a cascata iatrogênica, onde,
quanto maior o número de medicações utilizadas, maior a
probabilidade de se prescrever medicação potencialmente
inadequada para o idoso.10
108
Diagn Tratamento. 2014;19(3):105-9.
Outro estudo recente em São Paulo identificou medicamentos do critério de Beers e colaboradores como mais
frequentes: benzodiazepínicos, metildopa, derivados do
ergot, amitriptilina e amiodarona.8 Em Fortaleza,9 os benzodiazepínicos de longa duração foram os de maior proporção naquela população.
Estudo norte-americano mostrou que os principais medicamentos, do critério de Beers e colaboradores atualizado
em 2003, utilizados por idosos em um grupo de hospitais de
pequeno e médio porte foram: prometazina, difenidramina e
propoxífeno representando um quarto de todas as drogas.14
Foi identificada neste estudo, maior prevalência no uso
ácido acetilsalicílico (22,27%), seguido de espironolactona
(12,63%), amiodarona (4,09%), glibenclamida (2,27%) e lorazepam/clonazepam (2,27%).
Conforme o critério de Beers, o uso de ácido acetilsalicílico de forma crônica deve ser associado ao de um protetor
gástrico, pois os riscos dos efeitos gastrointestinais, incluindo
úlceras pépticas e hemorragia digestiva alta, aumentam acima dos 75 anos de idade, se estiver associado aos corticosteroides, anticoagulantes, ou antiplaquetários.6
O uso de espironolactona deve ser evitado acima da
dosagem de 25 mg por dia, principalmente em idosos com
falência cardíaca ou insuficiência renal moderada ou grave,
devido o risco de hipercalemia, principalmente se associado
ao uso de inibidor da enzima de conversão da angiotensina,
bloqueador dos receptores da angiotensina, anti-inflamatórios
não esteroidais e suplementação com potássio.6
Recomenda-se evitar amiodarona como primeira linha no
tratamento de fibrilação atrial. Amiodarona está associada a
alterações tireoidianas, doenças pulmonares, prolongamento
do intervalo QT e microdepósitos na córnea.6-16 Embora não
existam protocolos bem definidos, é preconizada a realização de testes de função tireóidea e hepática antes de iniciar
o tratamento e, posteriormente, a cada seis meses, avaliação
oftalmológica, se surgirem alterações visuais, e radiografia
torácica e eletrocardiograma anualmente.16 A incidência da
toxicidade relacionada com a amiodarona varia entre 34% a
93%, conforme estudos.16
Assim como na literatura nacional8-11,13 identificamos
maior prevalência dos medicamentos que atuam no sistema cardiovascular e sistema nervoso central, caracterizando as doenças crônico-degenerativas como as de maior
incidência nessa faixa etária e responsáveis por tratamentos contínuos a fim de prevenção nos três níveis, primária,
secundária e terciária, conforme a situação de cada indivíduo, facilitando assim a polifarmácia acima dos 65 anos
de idade. Porém, conforme diferenças na prática clínica,
assim como na comercialização de medicamentos, na
cultura de automedicação regional e na política de saúde
Aline Cristina Henriques da Silva | Leonardo Affonso Pedrosa Sibillo | Marcelo Rozenfeld Levites | Maria Alenita de Oliveira
diferente adotada em cada país, identificamos grande diferença entre as medicações mais prescritas nos Estados
Unidos14 e no Brasil, sendo lá mais frequentes os anti-histamínicos e os analgésicos opioides, mostrando ser importante a criação de um critério nacional de medicações
inadequadas para idosos. A realização do estudo num serviço terciário-quaternário,
sendo referência no setor de doenças cardiovasculares, tornou-se um viés ao presente estudo. Se o mesmo estudo fosse
realizado em outra população, de atenção primária, os resultados encontrados tenderiam a apresentar maior prevalência
de medicações de outras classes.
CONCLUSÃO
Existe prevalência relevante de polifarmácia no idoso. Há
um número alto de prescrições de medicações potencialmente inadequadas para os idosos, mostrando a importância
do conhecimento do critério de Beers e colaboradores.
Pelo fato de o estudo ter sido realizado em um serviço terciário-quaternário, referência no setor de doenças cardiovasculares, tornam-se necessários novos estudos em populações
mais abrangentes para determinar a real situação dentro da
cidade de São Paulo.
REFERÊNCIAS
1. Bortolon PC, de Medeiros EF, Naves JO, Karnikowski MGO,
Nóbrega Ode T. Análise do perfil de automedicação em mulheres
idosas Brasileiras [Analysis of the self-medication pattern among
Brazilian elderly women]. Cienc Saude Coletiva. 2008;13(4):1219-26.
2. Marin MJ, Cecílio LC, Perez AE, et al. Caracterização do uso de
medicamentos entre idosos de uma unidade do Programa Saúde
da Família [Use of medicines by the elderly in a Family Health
Program unit in Brazil]. Cad Saude Publica. 2008;24(7):1545-55.
3. Passarelli MCG, Jacob Filho W. Reações adversas a
medicamentos em idosos: como prevê-las? [Adverse drug
reactions in elderly patients: how to predict them?] Einstein (São
Paulo). 2007;5(3):246-51.
4. Secoli SR. Polifarmácia: interações e reações adversas no uso
de medicamentos por idosos [Polypharmacy: interaction and
adverse reactions in the use of drugs by elderly people]. Rev
Bras Enferm. 2010;63(1):136-40.
5. Beers MH, Ouslander JG, Rollingher I, et al. Explicit criteria for
determining inappropriate medication use in nursing home
residents. UCLA Division of Geriatric Medicine. Arc Intern Med.
1991;151(9):1825-32.
6. American Geriatrics Society 2012 Beers Criteria Update Expert
Panel. American Geriatrics Society updated Beers Criteria for
potentially inappropriate medication use in older adults. J Am
Geriatr Soc. 2012;60(4):616-31.
7. Brasil. Instituto Brasileiro de Geografia e Estatística. Indicadores
de desenvolvimento sustentável. Brasil 2012. Rio de Janeiro:
Instituto Brasileiro de Geografia e Estatística; 2012. Disponível
em: ftp://geoftp.ibge.gov.br/documentos/recursos_naturais/
indicadores_desenvolvimento_sustentavel/2012/ids2012.pdf.
Acessado em 2014 (6 mar).
8. Gorzoni ML, Fabbri RMA, Pires SL. Medicamentos potencialmente
inapropriados para idosos [Potentially inappropriate medications
in elderly]. Rev Assoc Med Bras (1992). 2012;58(4):442-6. 9. Coelho Filho JM, Marcopito LF, Castelo A. Perfil de utilização
de medicamentos por idosos em área urbana do Nordeste
do Brasil [Medication use patterns among elderly people
in urban area in Northeastern Brazil]. Rev Saúde Pública.
2004;38(4):557-64.
10. Carvalho MF, Romano-Lieber NS, Bergsten-Mendes G, et
al. Polifarmácia entre idosos do Município de São Paulo Estudo SABE [Polypharmacy among the elderly in the city
of São Paulo, Brazil - SABE Study]. Rev Bras Epidemiol.
2012;15(4):817-27.
11. Dal Pizzol Tda S, Pons Eda S, Hugo FN, et al. Uso de
medicamentos entre idosos residentes em áreas urbanas e rurais
de município no Sul do Brasil: um estudo de base populacional
[Use of medication by the elderly in urban and rural areas in
southern Brazil: a population-based study]. Cad Saude Publica.
2012;28(1):104-14.
12. Linjakumpu T, Hartikainen S, Klaukka T, et al. Use of medications
and polypharmacy are increasing among the elderly. J Clin
Epidemiol. 2002;55(8):809-17.
13. Varallo FR, Ambiel ISS, Nanci LO, Galduróz JCF, Mastroianni
PC. Assessment of pharmacotherapeutic safety of medical
prescriptions for elderly residents in a long-term care facility.
Braz J Pharm Sci. 2012;48(3):477-85.
14. Rothberg MB, Pekow PS, Liu F, et al. Potentially inappropriate
medication use in hospitalized elders. J Hosp Med.
2008;3(2):91-102.
15. Vianna CA, González DA, Matijasevich A. Utilização de ácido
acetilsalicílico (AAS) na prevenção de doenças cardiovasculares:
um estudo de base populacional [Aspirin use in cardiovascular
disease prevention: a population-based study]. Cad Saude
Publica. 2012;28(6):1122-32.
16. Melo N, Jaraquemada T, Gonçalves A. Toxicidade da
amiodarona: caso clínico. Arq Med. 2005;19(5-6):199-202.
Diagn Tratamento. 2014;19(3):105-9.
109
ARTIGO ORIGINAL
Estudo comparativo das
bombas de rolete e centrífuga em
pacientes submetidos à cirurgia de
revascularização do miocárdio
Carolina Teles Taipina MatiasI, Paulo Manuel Pêgo-FernandesII, Ramez AnbarIII, Nádia TaylorI,
Aristides CorreiaIV, Ludhmila Abrahão HajjarV, Roberto Kalil FilhoVI, Fabio Biscegli JateneVII
Hospital Sírio-Libanês
Resumo
Contexto e objetivos: Estudos sugerem que a utilização da bomba centrífuga na circulação extracorpórea é melhor do ponto de vista fisiológico se comparada a bomba de rolete nos pacientes submetidos a cirurgia cardíaca. O objetivo do trabalho é avaliar os níveis séricos de
lactato em pacientes submetidos a cirurgia de revascularização do miocárdio utilizando as bombas de rolete e centrífugas durante a circulação
extracorpórea (CEC) como um marcador prognóstico. Desenho e local: Trata-se de um estudo observacional retrospectivo, baseado em levantamento de dados de prontuários médico-hospitalares, realizado no Hospital Sírio-Libanês. Método: Foi estudada uma coorte histórica de
pacientes, dividida em dois grupos: o primeiro grupo, de 61 pacientes, operados no período de março de 2007 a julho de 2008, com bomba
rolete, e o segundo grupo, de 74 pacientes, no período de julho de 2008 a fevereiro de 2011, com bomba centrífuga. As amostras sanguíneas
dos pacientes foram colhidas em quatro diferentes tempos durante a operação: pré-circulação extracorpórea (T1); hipotermia a 32 °C (T2);
hipotermia a 34 °C (T3); pós-circulação extracorpórea (T4). Resultados: Houve diferença significativa na amostra do lactato em T4 (P = 0,049).
Conclusão: Na bomba centrífuga, observamos melhora do lactato ao final da circulação extracorpórea em comparação com a bomba rolete.
PALAVRAS-CHAVE: Cirurgia torácica, revascularização miocárdica, bombas de infusão, circulação extracorpórea, l-lactato desidrogenase
INTRODUÇÃO
Novas técnicas e componentes têm sido utilizados para o
aperfeiçoamento do circuito extracorpóreo com a finalidade
de reduzir as complicações nos pacientes submetidos a cirurgia cardíaca. Nos últimos anos, houve um avanço notável nas
pesquisas relacionadas à utilização das bombas de rolete e centrífuga na circulação extracorpórea, com a finalidade de reduzir
os danos causados pela circulação extracorpórea. Hoje, as bombas centrífugas têm sido empregadas na circulação extracorpórea tanto em procedimentos de revascularização do miocárdio
como em cirurgias valvares.
Biomédica (perfusionista), Sociedade Beneficente de Senhoras do Hospital Sírio-Libanês.
Professor titular, Disciplina de Cirurgia Torácica, Instituto do Coração (InCor), Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
Médico Cardiologista, Sociedade Beneficente de Senhoras do Hospital Sírio-Libanês.
IV
Biólogo, Disciplina de Cirurgia Torácica, Instituto do Coração (InCor), Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
V
Professora doutora, Disciplina de Cardiologia, Instituto do Coração (InCor), Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
VI
Professor titular, Disciplina de Cardiologia, Instituto do Coração (InCor), Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
VII
Professor titular, Disciplina de Cirurgia Cardiovascular, Instituto do Coração (InCor), Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
I
II
III
Endereço para correspondência:
Paulo Manuel Pêgo-Fernandes
Rua Itapeva, 240 — conjunto 902 — Bela Vista — São Paulo (SP) — CEP 01332-000.
Tel. (11) 3171-1320
E-mail: [email protected]
Fonte de fomento: Braile Biomédica Indústria Comércio e Representações S/A e Cardio Medical Com. Repres. e Import. de Material Médico Hospitalar Ltda
ofereceram os equipamentos utilizados na pesquisa — Conflito de interesse: nenhum declarado
Entrada: 13 de fevereiro de 2014 — Última modificação: 1 de abril de 2014 – Aceite: 8 de abril de 2014
110
Diagn Tratamento. 2014;19(3):110-4.
Carolina Teles Taipina Matias | Paulo Manuel Pêgo-Fernandes | Ramez Anbar | Nádia Taylor | Aristides Correia | Ludhmila Abrahão Hajjar | Roberto Kalil Filho | Fabio Biscegli Jatene
O uso de bombas centrífugas na circulação extracorpórea
está se tornando cada vez mais frequente nos centros de cirurgias cardíacas, devido aos benefícios observados.1 A utilização
dessas bombas provoca menor trauma sanguíneo comparado
a bomba de rolete, resulta em menor ativação plaquetária e redução da hemólise e, consequentemente, em melhor hemostasia. No entanto, resultados conflitantes são relatados sobre
o efeito dos dois tipos de bomba.2,3
Do ponto de vista hematológico, alguns autores4 não observaram difereça entre o uso rotineiro da bomba de rolete
e centrífuga, em pacientes eletivos submetidos a cirurgia
de revascularização do miocárdio. Em pacientes não obesos, em boas condições clínicas e eletivos, não há diferenças
hematológicas em relação à bomba de rolete comparada à
bomba centrífuga.5 No entanto, há evidências de aumento
significativo na agregação plaquetária com o uso da bomba
de rolete em comparação com a bomba centrífuga, indicando assim maior suscetibilidade no pós-operatório para risco
de complicações trombóticas.6
A acidose láctica ocorre em decorrência da distribuição
inadequada de oxigênio pelos tecidos, sendo consequência
do metabolismo anaeróbico. O aumento dos níveis séricos de
lactato consiste da hipoperfusão sistêmica e hipóxia tecidual.7
Os níveis séricos de lactato, antes, durante e depois da circulação extracorpórea, têm sido utilizados como marcadores
prognósticos de confiança nos últimos anos. Existem estudos
revelando intensa relação entre o aumento do risco de morbidade e mortalidade com os altos níveis séricos de lactato.1,7
OBJETIVO
Este estudo foi realizado para avaliar os níveis séricos de
lactato em pacientes submetidos a cirurgia de revascularização do miocárdio utilizando as bombas de rolete e centrífugas.
MÉTODO
Este estudo foi aprovado pelo Comitê de Ética em Pesquisa
do Hospital Sírio-Libanês (CEPesq/HSL). Foi realizado um estudo de coorte histórica, durante o período de março de 2007
a fevereiro de 2011, com todos os pacientes adultos consecutivamente operados no período de ambos os sexos, sem exclusão. No período, 135 pacientes foram submetidos à cirurgia de
revascularização do miocárdio no Hospital Sírio-Libanês, com
idades entre 37 e 94 anos, apresentando média de 64,83 anos
(± 11,24). O peso desses pacientes era de 60 kg a 116 kg, com
média de 83,32 kg (± 13,60).
Nas operações, a bomba centrífuga foi empregada em
74 pacientes, sendo 68 do sexo masculino e 6 do sexo feminino, e a bomba de rolete foi utilizada em 61 pacientes, sendo
53 do sexo masculino e 8 do sexo feminino. A idade dos pacientes variou entre 37 a 82 anos nos pacientes de bomba centrífuga e entre 38 a 94 anos nos pacientes de bomba rolete.
No período de março de 2007 a julho de 2008 utilizou-se
a bomba de rolete; já a bomba centrífuga foi aplicada, após
a incorporação dessa tecnologia pelo hospital no período entre julho de 2008 a fevereiro de 2011. O tempo de circulação
extracorpórea nas cirurgias foi de 35 a 175 minutos apresentando média de 103,71 minutos (± 25,53). Não houve diferenças estatísticas em relação às características entre os grupos.
A equipe cirúrgica foi a mesma em todas as cirurgias, assim
como a técnica cirúrgica, anestésica e perfusionista. O tempo
de internação dos pacientes foi calculado a partir da data da
operação até o momento da alta hospitalar.
Os pacientes foram heparinizados com dosagem de
5 mg/kg, além de 100 mg de heparina no perfusato. O tempo de coagulação ativada em todos os pacientes foi superior a 400 segundos a partir do momento em que a heparina
(Bergamo) foi administrada; quando necessário, usou-se
heparina adicional para garantir um nível seguro no tempo
de coagulação ativado. A partir do momento em que todo o
volume sanguíneo foi reposto ao paciente, a heparina foi revertida com a ação do sulfato de protamina (Bergamo); caso
necessário, doses adicionais foram administradas para normalizar o tempo de coagulação.
O circuito extracorpóreo consistiu de membrana oxigenadora (Braile Biomédica), reservatório venoso (Braile
Biomédica), reservatório de cardiotomia (Braile Biomédica),
bem como o filtro de linha arterial (Braile Biomédica). Todo
o circuito foi preenchido com perfusato igual para todos
os pacientes à temperatura ambiente, compreendendo
de 1.500 ml de ringer simples (Baxter), 100 mg de heparina sódica (Bergamo) e 100 ml de albumina humana a 20%
(Grifols). A administração de manitol a 20% (Baxter) foi efetuada em todos os pacientes logo após o início da circulação extracorpórea. A perfusão foi realizada com hipotermia
leve de 32 °C. O fluxo da circulação extracorpórea foi de
1,8 L/min/m2 a 2,2 L/min/m2. Utilizamos a bomba centrífuga da Medtronic (Bio-Pump BP-80, Medtronic BioMedicus,
Eden Prairie, Minnesota, Estados Unidos). A bomba rolete
utilizada faz parte do circuito da máquina de circulação
extracorpórea da Braile Biomédica, com tubo de 0,5 polegadas (BEC Módulo bomba, Braile Biomédica, São José do
Rio Preto, São Paulo, Brasil).
A técnica de pinçamento intermitente da aorta foi empregada. Logo após o resfriamento sistêmico para 32 ºC os
pinçamentos da aorta foram iniciados. A cada pinçamento
da aorta, foi realizada anastomose entre a artéria coronária a ser revascularizada e o enxerto. Para cada 3 a 4 minutos de pinçamento, foi realizado 1 minuto de reperfusão.
Diagn Tratamento. 2014;19(3):110-4.
111
Estudo comparativo das bombas de rolete e centrífuga em pacientes submetidos à cirurgia de revascularização do miocárdio
Esse procedimento foi utilizado tanto para as anastomoses
distais quanto para as proximais, porém, com cada pinçamento não superior a 12 minutos.
Ao término da circulação extracorpórea, todo o volume do
circuito extracorpóreo foi reposto ao paciente. Em seguida, a
heparina foi neutralizada com a ação da protamina.
Os pacientes foram divididos em dois grupos: grupo
I – utilização de bomba centrífuga, grupo II – utilização
de bomba rolete. As amostras de sangue foram colhidas
da linha arterial da anestesia, quando colhidas antes da
circulação extracorpórea e pós-circulação extracorpórea.
Durante a circulação extracorpórea, as amostras arteriais
foram colhidas da linha do filtro arterial da máquina de
extracorpórea.
Os exames laboratoriais realizados durante as operações
foram dosagem de hematócrito (Ht), dosagem de hemoglobina (Hb), gasometria arterial, dosagem de sódio (Na) e potássio (K), dosagem de lactato dehidrogenase (LDH) e dosagem de glicemia. Todas as amostras colhidas foram arteriais
em quatro diferentes tempos da cirurgia e em seguida encaminhadas ao laboratório de análises clínicas do hospital.
A primeira amostra (T1) foi colhida antes da circulação extracorpórea, a partir do momento em que o paciente estava
anestesiado. Após 20 minutos de perfusão, foi coletada a segunda amostra (T2). No momento em que o paciente estava
com a temperatura corporal a 34 ºC, a terceira amostra (T3)
foi colhida. A quarta amostra (T4) foi coletada após a reposição volêmica total do paciente.
Os dados foram analisados usando o software SPSS Inc.,
Chicago, IL. Todos os resultados foram expressos com média
± desvio padrão (DP). A análise de variância (ANOVA) de duplo fator foi realizada para determinar se haveria diferenças
significativas entre as médias dos parâmetros analisados.
Valores de P < 0,05 foram aceitos como significantes.
Rotineiramente, dosamos, nos quatro tempos, glicose,
hematócrito, potássio, bicarbonato de sódio e lactato. A dosagem de glicose obteve média semelhante entre os grupos,
nos diferentes tempos. No entanto, não houve diferenças significativas (P < 0,05) da glicose entre os grupos nas amostras:
normotermia T1 (P = 0,362); hipotermia T2 (P = 0,432); hipotermia T3 (P = 0,298); normotermia T4 (P = 0,619).
O hematócrito, devido à hemodiluição, declinou nas
amostras em hipotermia (T2 e T3). Porém, a amostra T3 foi
a única em que houve diferença significativa na comparação
entre as bombas (P = 0, 042), enquanto em T1 (P = 0,412), T2
(P = 0,585) e T4 (P = 5,14) (Gráfico 1) não houve diferença
significativa.
O potássio apresentou média semelhante entre os
grupos, nos diferentes tempos. Entretanto, não houve diferenças significativas (P = < 0,05) do potássio em comparação com as bombas: normotermia T1 (P = 0,377);
hipotermia T2 (P = 0,761); hipotermia T3 (P = 0,685); normotermia T4 (P = 0,860).
A média da dosagem de bicarbonato de sódio também
foi semelhante em ambas as bombas. A amostra em normotermia foi a que apresentou diferença significativa na comparação do bicarbonato de sódio entre as bombas, em que
P = 0,033 em T1. Nas amostras seguintes, não houve diferenças significativas da dosagem entre as bombas: T2 (P = 0,249);
T3 (P = 0,521); T4 = (P = 0,545) (Gráfico 2).
Na dosagem do lactato, o valor da média de cada bomba
foi crescente, ou seja, o lactato da amostra T1 foi aumentando conforme o tempo em comparação com a amostra T4.
No entanto, a única amostra que mostrou diferença significativa entre a bomba centrífuga e rolete foi a amostra T4,
em que P = 0,049, enquanto T1 (P = 0,902); T2 (P = 0,176) e
T3 (P = 0,228) (Gráfico 3).
RESULTADOS
112
Diagn Tratamento. 2014;19(3):110-4.
%
Ht
Nas operações em que se utilizou a bomba centrífuga, a
média do tempo de circulação extracorpórea foi de 100,13
minutos (± 23,49); já nas operações com bomba rolete, a média do tempo de circulação extracorpórea foi 105,24 minutos
(± 27,55). O tempo de circulação extracorpórea entre os grupos não apresentou diferenças significativas.
O tempo médio de internação no grupo da bomba centrífuga foi de 12,90 (± 8,41), no grupo de bomba rolete, o tempo
médio foi de 15,39 (± 12,72). Não houve diferenças significativas entre os grupos com relação ao tempo de internação.
Entre todos os pacientes operados neste estudo, houve um
óbito hospitalar. Ocorreu no 27o dia do pós-operatório, e esse
paciente pertencia ao grupo de bomba rolete.
45
40
35
30
25
20
15
10
5
0
T1
T2
Bomba centrífuga
T3
T4
Bomba rolete
Gráfico 1. Comparação do hematócrito (Ht) (%) entre as
bombas ao longo do tempo.
Carolina Teles Taipina Matias | Paulo Manuel Pêgo-Fernandes | Ramez Anbar | Nádia Taylor | Aristides Correia | Ludhmila Abrahão Hajjar | Roberto Kalil Filho | Fabio Biscegli Jatene
HCO3
25
mg/dL
20
15
10
5
0
T1
T2
Bomba centrífuga
T3
T4
Bomba rolete
Gráfico 2. Comparação do HCO3ˉ (mg/dL) entre as bombas
ao longo do tempo.
mg/dL
Lactato
50
45
40
35
30
25
20
15
10
5
0
T1
T2
Bomba centrífuga
T3
T4
Bomba rolete
Gráfico 3. Comparação do lactato (mg/dL) entre as bombas
ao longo do tempo.
DISCUSSÃO
Diversos fatores contribuem para a hipoperfusão durante a circulação extracorpórea, tais como a duração da
circulação extracorpórea e da anóxia miocárdica, o grau de
hipotermia e a estratégia de manipulação do valor do hematócrito e pH sanguíneo.8
A bomba centrífuga Medtronic BP-80 consiste de um cone
de acrílico em que internamente existem três cones magnéticos vinculados e rotativos, que, ao se moverem, deslocam o
sangue por meio de força centrífuga. Tem como princípio um
vórtex que permite fluxo unidirecional sem necessidade do
uso de válvulas, permitindo deslizamento suave e contínuo
do dispositivo, possibilitando vantagens comparadas a outros sistemas, tais como menores complicações trombóticas
e embólicas, e reduzindo os danos aos elementos figurados
do sangue devido a menor turbulência.9 Além disso, sabe-se
que a bomba centrífuga possui menor risco da formação de
pressão negativa e, consequentemente, não oferece risco
de rotura da linha arterial devido a não oclusão.1 O custo
maior e um sistema mais sofisticado podem ser compreendidos como desvantagem deste sistema.
Muitos estudos demonstram que o uso de bombas centrífugas, comparados com a bomba de rolete, resulta em redução
na ativação do sistema complemento3,10 e menor hemólise.3
Neste trabalho, houve diferenças significativas entre as bombas
em relação ao hematócrito apenas na amostra T3, na qual o
valor do hematócrito da bomba rolete foi superior ao da bomba centrífuga, porém, na amostra em normotermia, o valor do
hematócrito dos pacientes submetidos a cirurgia com bomba
centrífuga foi superior.
Os valores de bicarbonato arterial, durante a circulação
extracorpórea, reduzem significativamente em comparação
aos valores iniciais devido a elevação da concentração de
íons hidrogênio.11 No presente estudo, os valores de bicarbonato de sódio também foram inferiores no decorrer da circulação extracorpórea comparados aos valores iniciais, porém,
em nenhum momento durante a circulação extracorpórea,
houve diferenças significativas dos valores do bicarbonato
em relação aos diferentes tipos de bomba. A amostra inicial
apresentou diferença significativa entre os pacientes, porém,
não há relação com as bombas, uma vez que a circulação extracorpórea não havia iniciado.
O metabolismo da glicose é alterado durante a circulação
extracorpórea, porém a intensidade depende de fatores, dos
quais o mais importante é o grau de hipotermia.12 No presente estudo, não observamos diferenças significativas na dosagem de glicose entre as bombas, porém, podemos observar
que, no momento em que o paciente é submetido à circulação extracorpórea e a hipotermia se inicia, a glicose circulante aumenta gradativamente; no momento em que o paciente
está em normotermia, a glicemia tende a normalizar.
O potássio, durante a circulação extracorpórea, é constantemente dosado, e corrigido quando necessário, principalmente para preservar a contração miocárdica. Neste
trabalho, observamos que não houve diferenças significativas na dosagem de potássio entre as bombas durante a
circulação extracorpórea. Analisamos que houve aumento
no nível de potássio em ambas as bombas no intervalo entre as amostras T2 e T3, mas que, no momento em que os
pacientes saíram de circulação extracorpórea, o potássio se
manteve em níveis normais.
A redução da oferta de oxigênio aos tecidos pode ser diagnosticada pelo aumento da concentração do lactato sanguíneo.13 Após o pinçamento da aorta, ocorre produção de
lactato.14 A circulação extracorpórea pode ser responsável
pela privação de oxigênio aos tecidos e, consequentemente,
Diagn Tratamento. 2014;19(3):110-4.
113
Estudo comparativo das bombas de rolete e centrífuga em pacientes submetidos à cirurgia de revascularização do miocárdio
eleva os níveis de lactato sanguíneo.4 Embora inespecífico, o
excesso de lactato durante a circulação extracorpórea pode
ser marcador de aumento da demanda metabólica ou hipoperfusão regional. Os órgãos que comumente se encarregam
de produzir o lactato são o cérebro, fígado, intestinos, rins e
músculos esqueléticos.15,16
Sabe-se que a acidose láctica se dá pela hipoperfusão tecidual, de defeitos inatos do metabolismo dos carboidratos
ou pelo efeito de certas drogas.17 Além disso, foi relatado que
o nitroprussiato de sódio (0,6 µg.kg-1.min-1) pode ser benéfico no tratamento de pacientes com acidose lática por, provavelmente, melhorar a redistribuição do fluxo sanguíneo.18
Em contrapartida, há relatos de que a administração da norepinefrina acentua a acidose lática.4
Neste trabalho, não foi considerada a exposição da
utilização de drogas vasoativas durante as operações.
Observamos que houve diferença significativa na dosagem
de lactato apenas na amostra pós-circulação extracorpórea
(T4). Acredita-se que, ao longo do tempo, o lactato na bomba
centrífuga tende a diminuir em comparação com a bomba rolete, como podemos observar no Gráfico 3.
CONCLUSÃO
Neste trabalho, não notamos diferenças clínicas significantes entre as bombas em relação aos parâmetros utilizados, exceto o lactato. Sendo assim, podemos concluir
que, com a utilização da bomba centrífuga, apenas o lactato pós-circulação extracorpórea foi melhor nos pacientes
submetidos à circulação extracorpórea com o auxílio da
bomba centrífuga, uma vez que houve diferença significativa na amostra final.
REFERÊNCIAS
1. Mejak BL, Stammers A, Rauch E, Vang S, Viessman T. A
retrospective study on perfusion incidents and safety devices.
Perfusion. 2000;15(1):51-61.
2. Morgan IS, Codispoti M, Sanger K, Mankad PS. Superiority
of centrifugal pump over roller pump in paediatric cardiac
surgery: prospective randomised trial. Eur J Cardiothorac Surg.
1998;13(5):526-32.
3. Valeri CR, MacGregor1 H, Ragno G, et al. Effects of centrifugal
and roller pumps on survival of autologous red cells in
cardiopulmonary bypass surgery. Perfusion. 2006;21(5):291-6.
4. Moen O, Fosse E, Bråten J, et al. Differences in blood activation
related to roller/centrifugal pumps and heparin-coated/
uncoated surfaces in a cardiopulmonary bypass model circuit.
Perfusion. 1996;11(2):113-23.
5. Pêgo-Fernandes PM, Miura F, Higa SS, et al. Hemólise em
circulação extracorpórea: estudo comparativo entre bomba
de rolete e bomba centrífuga [Hemolysis in extracorporeal
circulation: a comparative study between roller and centrifugal
pumps]. Rev Bras Cir Cardiovasc.1989;4(3):220-4.
6. Andersen KS, Nygreen EL, Grong K, Leirvaag B, Holmsen
H. Comparison of the centrifugal and roller pump in elective
coronary artery bypass surgery--a prospective, randomized
study with special emphasis upon platelet activation. Scand
Cardiovasc J. 2003;37(6):356-62.
7. Yee S, Qiu F, Su X, et al. Evaluation of HL-20 roller pump and
Rotaflow centrifugal pump on perfusion quality and gaseous
microemboli delivery. Artif Organs. 2010;34:(11):937-43.
8. Atik FA. Monitorização hemodinâmica em cirurgia cardíaca
pediátrica [Hemodynamic monitoring in pediatric heart surgery].
Arq Bras Cardiol. 2004;82(2):199-208.
9. Blackshear PL, Forstrom R, Watters C, Dorman FD. Effect of
flow and turbulence on the formed elements of blood. In:
Brewer LA, ed. Prostect heart valves. Springfield (Illinois):
Thomas; 1969. p. 52-67.
114
Diagn Tratamento. 2014;19(3):110-4.
10. Wheeldon DR, Bethune DW, Gill RD. Vortex pumping for
routine cardiac surgery: a comparative study. Perfusion.
1990;5(2):135-43.
11. Piccioni MA, Auler Júnior JOC. Efeitos dos fármacos vasoativos
na acidose lática consequente à circulação extracorpórea em
cirurgia cardíaca [Effects of vasoactive drugs in lactic acidosis as
a consequence of extracorporeal circulation in cardiac surgery].
Rev Bras Anestesiol. 1999;49(3):151-9.
12. Souza MHL, Elias DO. Fundamentos da circulação extracorpórea.
2a ed. Rio de Janeiro: Alfa Rio; 2006.
13. Kruse JA, Haupt MT, Puri VK, Carlson RW. Lactate levels as
predictors for the relationship between oxygen delivery and
consumption in ARDS. Chest. 1990;98(4):959-62.
14. Pêgo-Fernandes PM, Jatene FB, Kwasnicka K, et al. Influência
do pré-condicionamento isquêmico na proteção miocárdica em
revascularização do miocárdio com pinçamento intermitente
da aorta [Influence of the ischemic preconditioning in the
myocardial protection in myocardial revascularization with
intermittent aortic cross-clamping]. Rev Bras Cir Cardiovasc.
2001;16(1):7-13.
15. Atik FA. Monitorização hemodinâmica em cirurgia cardíaca
pediátrica [Hemodynamic monitoring in pediatric heart surgery].
Arq Bras Cardiol. 2004;82(2):199-208.
16. McDaniel LB, Zwischenberger JB, Vertrees RA, et al. Mixed
venous oxygen saturation during cardiopulmonary bypass
poorly predicts regional venous saturation. Anesth Analg.
1995;80(3):466-72.
17. Rocha TS, Silveira AS, Botta AM, et al. Lactato sérico como
marcador de morbimortalidade no pós-operatório de operação
de Jatene em lactentes [Serum lactate as mortality and
morbidity marker in infants after Jatene’s operation]. Rev Bras
Cir Cardiovasc. 2010;25(3):350-8. 18. Taradash MR, Jacobson LB. Vasodilator therapy of idiopathic
lactic acidosis. N Engl J Med. 1975;293(10):468-71.
RELATO DE CASO
Pancitopenia associada a
tratamento com azatioprina e
mesalazina em paciente com colite
ulcerativa: relato de caso
Gerson Julio de FreitasI, Maycon Paulo de OliveiraI, Virginia Fernandes Moça TrevisaniII, Marcelo MoockIII,
Sergio Elia MatalounIII
Hospital Geral do Grajaú e Universidade de Santo Amaro, São Paulo
RESUMO
Contexto: As doenças inflamatórias intestinais têm se tornado cada vez mais prevalentes, o que leva ao uso cada vez maior de medicações
como os imunossupressores tiopurinas (azatioprina e 6-mercaptopurina) e os salicilatos (como a sulfasalazina e a mesalazina). O objetivo deste
artigo é destacar aspectos de um efeito colateral potencialmente grave com essas medicações, a mielotoxicidade. Relato do caso: Mulher de
39 anos com história de colite ulcerativa em uso de azatioprina e mesalazina procurou o serviço com queixa de cefaleia inespecífica e febre.
Hemograma de entrada apresentava pancitopenia (hemoglobina 3,8 g/dL, leucócitos de 1.800/mm3 com 486/mm3 segmentados e plaquetas de 15.000/mm3). A paciente foi admitida com a hipótese de pancitopenia induzida por medicamentos, sendo a azatioprina e mesalazina
suspensos. Após 10 dias de suspensão e suporte com antibióticos para neutropenia febril, hemoderivados e filgrastina, os valores das séries
sanguíneas começaram a ascender, a paciente recebeu alta no 19o dia, com melhora clínica e hematológica. Conclusão: A azatioprina é classicamente descrita como causadora de mielotoxicidade, enquanto a mesalazina isoladamente raramente é mencionada. A enzima tiopurinametiltransferase (TPMT) é relacionada ao metabolismo da azatioprina, e baixos níveis de sua atividade estão relacionados à maior toxicidade.
No contexto brasileiro não foi estudada a relação custo/efetividade da genotipagem de TPMT ou da verificação de sua atividade antes de
iniciar o tratamento. É prudente colher hemograma semanalmente nas primeiras oito semanas após o início de tratamento com azatioprina.
Palavras-chave: Pancitopenia, azatioprina, mesalamina, colite ulcerativa, neutropenia
INTRODUÇÃO
A doença de Crohn e a colite ulcerativa são doenças inflamatórias intestinais cuja etiopatogenia ainda não é bem esclarecida, mas que possivelmente podem dever-se à interação
entre fatores ambientais, genéticos, microbianos e imunológicos. Há evidências de que sua prevalência esteja aumentando pelo mundo. Estudo realizado na Califórnia1 avaliando um
período de seis anos mostrou incidência de 6,3 casos de doença de Crohn/100.000 habitantes/ano e de 12 casos de colite
ulcerativa/100.000 habitantes por ano.2,3
Os corticosteroides são eficientes e fornecem alívio aos
sintomas de pacientes com doença inflamatória intestinal.
Entretanto, apesar da resposta inicial dos pacientes, cerca de
25% deles se tornam dependentes dessas medicações.4
Para os pacientes dependentes ou resistentes aos corticoides, ensaios clínicos randomizados duplo-cegos e controlados,
Médicos graduados pelo curso de Medicina da Universidade de Santo Amaro, São Paulo.
Professora da Disciplina de Reumatologia do Curso de Medicina da Universidade de Santo Amaro, São Paulo.
III
Professores da Disciplina de Medicina Intensiva da Universidade de Santo Amaro e responsáveis pela Unidade de Terapia Intensiva do Hospital Geral do
Grajaú, São Paulo.
I
II
Endereço para Correspondência:
Gerson Julio de Freitas
Avenida João de Barros, 155 — Bloco B — Apto 164 — Socorro — São Paulo (SP) — CEP 04764-090
Tel. (11) 5927-5039
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 3 de janeiro de 2013 — Última modificação: 20 de março de 2014 — Aceite: 28 de março de 2014
Diagn Tratamento. 2014;19(3):115-8.
115
Pancitopenia associada a tratamento com azatioprina e mesalazina em paciente com colite ulcerativa: relato de caso
bem como metanálises, já foram realizados e apontaram a
importância das tiopurinas — azatioprina e 6-mercaptopurina — na indução e manutenção da remissão das doenças
inflamatórias intestinais.5,6
A azatioprina é um imunossupressor, pró-droga da 6-mercaptopurina. Seu mecanismo de ação parece decorrer do fato
de que seus metabólitos, nucleotídeos 6-tioguanina, incorporarem-se ao DNA (ácido desoxirribonucleico) e RNA (ácido
ribonucleico), resultando em efeito citotóxico, além de estimularem mitocôndrias a fim de levar a apoptose de certas linhagens linfocitárias CD3 e CD28. Tanto a azatioprina quanto
a 6-mercaptopurina têm sido utilizadas há décadas no tratamento da doença inflamatória intestinal, com taxas de eficácia que variam entre 55% a 70%. Entretanto, até um terço dos
pacientes pode sofrer efeitos adversos que os levem a deixar o
tratamento, como náusea, febre, pancreatite, aumento do risco de neoplasia e supressão da medula óssea.7,8
A mesalazina (também chamada mesalamina), derivada
da sulfasalazina, é um aminosalicilato também bastante utilizado no controle de doenças inflamatórias intestinais. Seu
mecanismo de ação é atribuído à modulação do metabolismo
do ácido araquidônico, com inibição da cicloxigenase e lipoxigenase, além de inibir células inflamatórias, reduzir a atividade do fator de necrose tumoral e a produção de interleucina 1
e também reduzir radicais livres. Entretanto, algumas reações
idiossincrásicas podem acontecer em alguns pacientes, dentre elas, agranulocitose e anemia aplástica.9
Tendo em vista a prevalência das doenças inflamatórias
intestinais e consequentemente o uso mais frequente da mesalazina e azatioprina, esta última também utilizada em algumas doenças reumatológicas e em pacientes transplantados,
o objetivo deste relato de caso é descrever e alertar aos profissionais da área médica sobre a ocorrência de efeito adverso
grave: a pancitopenia.
RELATO DO CASO
Mulher, de 39 anos, casada, auxiliar de escritório, natural
e procedente de São Paulo, compareceu ao Hospital Geral do
Grajaú com queixa inicial de cefaleia inespecífica há quatro
dias com piora nas últimas horas, intensidade 5/10, difusa,
sem fatores de melhora ou piora, sem sintomas associados.
Referiu também dois episódios de febre (não aferidos) nos últimos dois dias. Nenhuma outra queixa quanto a outros aparelhos e sistemas. Relatou história de colite ulcerativa há três
anos, controlada utilizando azatioprina (125 mg/dia) e mesalazina (3.200 mg/dia), tendo o último aumento da dose dessas
medicações ocorrido há dois meses.
O exame físico de admissão destacou paciente descorada 3+/4+, sem outras alterações relevantes. Foram
116
Diagn Tratamento. 2014;19(3):115-8.
solicitados exames laboratoriais e tomografia de crânio, a
qual não apresentava nenhuma alteração, entretanto o hemograma apresentava pancitopenia (hemoglobina 3,8 g/dL; leucócitos de 1.800/mm3 com 486/mm3 segmentados e plaquetas de 15.000/mm3). Foi levantada a hipótese de pancitopenia
secundária ao uso dos imunossupressores, e a azatioprina e
mesalazina foram suspensas. A paciente foi internada e foram coletadas culturas e iniciada terapia com cefepime em
virtude da neutropenia febril.
Durante os próximos quatro dias a paciente manteve febre
(entre 38,1 °C e 39 °C) e queda do estado geral, sendo o cefepime trocado por meropenem, além da adição de vancomicina e
fluconazol. Paralelamente a paciente desenvolveu sangramento uterino, com elevação do índice internacional normalizado
(INR) (chegando a 1,56), e foi enviada à unidade de terapia intensiva (UTI) para controle do quadro séptico e sangramento.
O sangramento foi avaliado pela ginecologia, que descartou patologia ginecológica que o justificasse. Foi cogitada a possibilidade de realização de mielograma para excluir outras causas de
pancitopenia, entretanto, em virtude da coagulopatia, optou-se
por não realizar o procedimento. Diariamente, a paciente recebia hemoderivados em virtude do sangramento e pancitopenia.
A febre cedeu no 7o dia, mas a neutropenia se manteve, por
isso foi adicionada filgrastina à prescrição, além de terem sido
mantidos os antibióticos até o 14o dia.
A partir do 10o dia, a paciente começou a apresentar melhora nos valores de todas as linhagens sanguíneas e melhora
do estado geral, tendo sido transferida para a enfermaria no
13o dia. Apresentou reativação da retocolite ulcerativa (diarreia e dor abdominal), a qual foi bem controlada com introdução de terapia com prednisona.
Em virtude da melhora clínica e hematológica (hemoglobina 8 g/dL, leucócitos 8.700/mm3 com 4.698/mm3 segmentados e plaquetas de 36.000/mm3, sem sangramentos), teve alta
no 19o dia de internação, com encaminhamento para hematologia e gastroenterologia.
DISCUSSÃO
Após realização de busca em diferentes bases de dados
(Tabela 1), percebemos que, apesar de os efeitos colaterais
das medicações já serem descritos há bastante tempo, há
poucos relatos de caso publicados a respeito. Com o intuito
de obter maiores informações, começamos então a pesquisar
a partir das referências bibliográficas dos artigos encontrados.
Sabe-se há bastante tempo que a terapia com azatioprina
pode causar mielossupressão. Entretanto a pancitopenia grave
é incomum. Em pacientes com doença inflamatória intestinal,
ela é reportada em cerca de 0,4% a 2% dos casos.10 A mielotoxicidade usualmente se apresenta com citopenias isoladas,
Gerson Julio de Freitas | Maycon Paulo de Oliveira | Virginia Fernandes Moça Trevisani | Marcelo Moock | Sergio Elia Mataloun
sendo a neutropenia e leucopenia as complicações mais comuns. A anemia isoladamente é rara, porém descrita.11,12
O metabolismo das tiopurinas é complexo. As enzimas
xantina oxidase (XO) e tiopurinametiltransferase agem realizando seu clearance. A xantina oxidase é inibida pelo alopurinol. Por essa razão, o uso de alopurinol em pacientes em
tratamento com azatioprina pode potencializar o risco de
efeitos citotóxicos. A tiopurinametiltransferase, por sua vez,
tem papel fundamental no metabolismo das tiopurinas, sendo que níveis baixos na atividade de tiopurinametiltransferase estão associados com toxicidade aumentada. Além disso,
a tiopurinametiltransferase é regulada por um complexo polimorfismo genético, o que explica a susceptibilidade maior
de alguns indivíduos à mielossupressão.8 Outras enzimas
envolvidas no metabolismo das tiopurinas são a hipoxantina
guanina fosforibosiltransferase (HGPRT) e a trifosfato de inosina pirofosfohidrolase (ITPase), mas ainda não se encontrou
importância clínica significativa relacionada a elas, permanecendo a tiopurinametiltransferase como a enzima mais relevante e estudada.13
Aproximadamente 0,3% dos caucasianos são homozigotos
para a deficiência de tiopurinametiltransferase. Outros 11%
são heterozigotos, apresentando atividade intermediária da
enzima.14 Entretanto, não se pode afirmar que a genética e a
atividade da tiopurinametiltransferase sejam os únicos responsáveis pela mielotoxicidade, uma vez que já foram relatados casos de pacientes que sofreram mielossupressão em
uso de 6-mercaptopurina (metabólito ativo da azatioprina)
mesmo com tiopurinametiltransferase normal.15
Algumas maneiras de se identificar maior risco de possíveis efeitos citotóxicos das tiopurinas já foram propostas,
dentre elas a genotipagem da tiopurinametiltransferase, a
fenotipagem da tiopurinametiltransferase, a determinação
da atividade enzimática da tiopurinametiltransferase e a dosagem de metabólitos da tiopurina.16,17 A determinação da
atividade enzimática da tiopurinametiltransferase possivelmente tem maior poder preditivo do que a mera genotipagem da enzima. Estudos internacionais já tentaram mostrar
que é custo-efetivo realizar esse monitoramento em pacientes que utilizem azatioprina, seja para doença inflamatória
intestinal ou condições reumatológicas ou dermatológicas.18
Levantamento realizado na Inglaterra mostrou que dois
terços dos médicos pesquisados utilizam testes para verificar os níveis de tiopurinametiltransferase antes de prescrever
azatioprina.19 Entretanto não encontramos estudos brasileiros que nos permitam avaliar a custo/efetividade desse tipo
de prática em nosso sistema de saúde.
Quanto ao uso de mesalazina isoladamente, as discrasias
sanguíneas, incluindo pancitopenia, trombocitopenia, anemia aplástica e neutropenia são raras, porém há alguns relatos dessas complicações.20 Entretanto, já foi demonstrado
in vitro que a sulfasalazina e seus isômeros podem inibir a
atividade da tiopurinametiltransferase. Dessa forma, existe
interação sinérgica entre as tiopurinas e os aminosalicilatos,
que apesar de teoricamente aumentarem o efeito terapêutico, talvez resultem em maior risco de mielotoxicidade.21,22
Para os pacientes em tratamento com azatioprina, hemogramas semanais durante as primeiras oito semanas, e
posteriormente trimestrais, são recomendados tanto pelos
fabricantes quanto por especialistas, pois já se observou que
a mielossupressão ocorre principalmente nas primeiras oito
semanas após o início do tratamento.11,23
CONCLUSÃO
O caso relatado mostrou paciente com colite ulcerativa em tratamento com mesalazina e azatioprina há dois
anos e que, após o último aumento de dose, há dois meses,
apresentou pancitopenia e neutropenia febril. Após a suspensão das medicações, em 10 dias suas séries sanguíneas
retornaram a valores ascendentes. Julgamos importante
ressaltar esse tempo entre a suspensão e a recuperação,
pois a maioria dos relatos de caso encontrados não deixou
clara essa informação.
Quanto aos fármacos, salientamos que a mesalazina isoladamente pode levar a mielotoxicidade de forma idiossincrásica, mas essa condição é bastante rara e pouco relatada na
literatura. Por outro lado, a azatioprina é descrita há décadas
como causadora de mielotoxicidade em parte dos pacientes
que a utilizam. Essa mielotoxicidade manifesta-se principalmente como neutropenia isolada ou leucopenia, trombocitopenia e, raramente, pancitopenia.
Lembramos que, em virtude da prevalência de efeitos
mielotóxicos, alguns autores admitem ser prudente, na
Tabela 1. Busca sistematizada, realizada em 12/02/2013, e quantidade de artigos encontrados
Bases
Portal de Periódicos CAPES
PubMed
Lilacs
Descritores utilizados
“ulcerative colitis” AND pancytopenia AND (azathioprine AND mesalamine)
AND “Case Report”
((ulcerative colitis) AND pancytopenia) AND (azathioprine AND mesalamine)
Article type: Case report
“colite ulcerativa” AND pancitopenia AND (azatioprina AND mesalamina)
[Palavras] AND “Relato de Caso” [Tipo de Publicação]
Número de artigos
12
0
0
Diagn Tratamento. 2014;19(3):115-8.
117
Pancitopenia associada a tratamento com azatioprina e mesalazina em paciente com colite ulcerativa: relato de caso
prática clínica, obter hemograma basal dos pacientes no início do tratamento e repeti-lo semanalmente nas primeiras
oito semanas, quando há chance maior de mielotoxicidade.
Entretanto, como no caso apresentado, mesmo após longo
período em tratamento, é possível que a paciente apresente
os efeitos adversos.
Medidas mais específicas como a genotipagem ou a mensuração da atividade da enzima tiopurinametiltransferase podem
ser utilizadas e auxiliam a identificar os pacientes com maior
risco de desenvolver toxicidade. Entretanto o custo/efetividade dessas medidas no cenário nacional não foi estudado, sendo
relevante a realização de novos estudos com esse enfoque.
REFERÊNCIAS
1. Herrington LJ, Liu L, Lewis JD, Griffin PM, Allison J. Incidence
and prevalence of inflammatory bowel disease in a Northern
California managed care organization, 1996-2002. Am J
Gastroenterol. 2008;103(8):1998-2006.
2. Scaldaferri F, Fiocchi C. Inflammatory bowel disease: progress
and current concepts of etiopathogenesis. J Dig Dis.
2007;8(4):171-8.
3. Schirbel A, Fiocchi C. Inflammatory bowel disease: Established
and evolving considerations on its etiopathogenesis and
therapy. J Dig Dis. 2010;11(5):266-76.
4. Gisbert JP, Niño P, Cara C, Rodrigo L. Comparative effectiveness
of azathioprine in Crohn’s disease and ulcerative colitis:
prospective, long-term, follow-up study of 394 patients. Aliment
Pharmacol Ther. 2008;28(2):228-38.
5. Prefontaine E, Macdonald JK, Sutherland LR. Azathioprine or 6‐
mercaptopurine for induction of remission in Crohn’s disease.
Cochrane Database Syst Rev. 2010;(6):CD000545.
6. Gisbert JP, Linares PM, McNicholl AG, Maté J, Gomollón F.
Meta-analysis: the efficacy of azathioprine and mercaptopurine
in ulcerative colitis. Aliment Pharmacol Ther. 2009;30(2):126-37.
7. Ansari A, Arenas M, Greenfield SM, et al. Prospective evaluation
of the pharmacogenetics of azathioprine in the treatment
of inflammatory bowel disease. Aliment Pharmacol Ther.
2008;28(8):973-83.
8. Hadda V, Pandey BD, Gupta R, Goel A. Azathioprine induced
pancytopenia: a serious complication. J Postgrad Med.
2009;55(2):139-40.
9. Schroeder KW. Is mesalamine safe? Gastroenterol Hepatol (N
Y). 2007;3(11):878-9.
10. Telml A, Schaeffeler E, Herrlinger KR, Klotz U, Schwab M.
Thiopurine treatment in inflammatory bowel disease: clinical
pharmacology and implication of pharmacogenetically guided
dosing. Clin Pharmacokinet. 2007;46(3):187-208.
11. Lewis JD, Abramson O, Pascua M, et al. Timing of
myelosuppression during thiopurine therapy for inflammatory
bowel disease: implications for monitoring recommendations.
Clin Gastroenterol Hepatol. 2009;7(11):1195-201; quiz 1141-2.
12. Suto M, Nagai Y, Hasegawa M, Handa H, Ishikawa O.
Azathioprine-induced pure red cell aplasia in a systemic sclerosis
patient with interstitial pneumonia. J Dermatol. 2011;38(3):285-7.
118
Diagn Tratamento. 2014;19(3):115-8.
13. Ford LT, Berg JD. Thiopurine S-methyltransferase (TPMT)
assessment prior to starting thiopurine drug treatment; a
pharmacogenomic test whose time has come. J Clin Pathol.
2010;63(4):288-95.
14. Frohman EM, Havrdova E, Levinson B, Slanar O. Azathioprine
myelosuppression in multiple sclerosis: characterizing
thiopurine methyltransferase polymorphisms. Mult Scler.
2006;12(1):108-11.
15. Best C, Sudel B. Bone marrow suppression in the setting of
normal thiopurine methyltransferase phenotype testing. Clin
Pediatr (Phila). 2010;49(9):901-3.
16. Derijks LJ, Gilissen LP, Hooymans PM, Hommes DW. Review
article: thiopurines in inflammatory bowel disease. Aliment
Pharmacol Ther. 2006;24(5):715-29.
17. Gilissen LP, Derijks LJ, Verhoeven HM, et al. Pancytopenia due
to high 6-methylmercaptopurine levels in a 6-mercaptopurine
treated patient with Crohn’s disease. Dig Liver Dis.
2007;39(2):182-6.
18. Winter JW, Gaffney D, Shapiro D, et al. Assessment of thiopurine
methyltransferase enzyme activity is superior to genotype in
predicting myelosuppression following azathioprine therapy in
patients with inflammatory bowel disease. Aliment Pharmacol
Ther. 2007;25(9):1069-77.
19. Fargher EA, Tricker K, Newman W, et al. Current use of
pharmacogenetic testing: a national survey of thiopurine
methyltransferase testing prior to azathioprine prescription. J
Clin Pharm Ther. 2007;32(2):187-95.
20. Fowler BT, Gupta T, Bilal M. Asacol®-induced neutropenia
resolution without the use of granulocyte colony-stimulating
factor. South Med J. 2010;103(11):1167-9.
21. Bermejo F, Gisbert JP. Usefulness of salicylate and thiopurine
coprescription in steroid-dependent ulcerative colitis and
withdrawal strategies. Ther Adv Chronic Dis. 2010;1(3):107-14.
22. Oselin K, Anier K. Inhibition of human thiopurine
S-methyltransferase by various nonsteroidal anti-inflammatory
drugs in vitro: a mechanism for possible drug interactions. Drug
Metab Dispos. 2007;35(9):1452-4.
23. Peyrin-Biroulet L, Cadranel JF, Nousbaum JB, et al. Interaction
of ribavirin with azathioprine metabolism potentially induces
myelosuppression. Aliment Pharmacol Ther. 2008;28(8):984-93.
RELATO DE CASO
Imunodeficiência comum variável:
relato de caso
Patrícia Estrela EvangelistaI, Elenice StroparoII
Faculdade de Biomedicina da Universidade Tuiuti do Paraná de Curitiba
Resumo
Contexto: A imunodeficiência comum variável é uma síndrome caracterizada por hipogamaglobulinemia de início tardio, infecções bacterianas de repetição e várias anormalidades imunológicas, incluindo incidência aumentada de doenças autoimunes e malignidade. Descrição do
caso: Paciente L. J. G., do sexo masculino, de 21 anos, caucasiano, apresentava histórico de infecções bacterianas e infecções sinopulmonares
recorrentes, destacando-se pelos quadros de pneumonias de repetição extensas e necessidade de tratamento prolongado. Nos anos de 2007
e 2008, apresentou pneumonia, e radiografias de tórax realizadas neste período sugeriam imagens de bronquiectasias, o que ocasionou a
continuidade do tratamento, nos anos de 2009 e 2010, com pneumologista e infectologista. Em 2010, os exames revelaram hipogamaglobulinemia acentuada de imunoglobulinas IgM, IgA, IgE e IgG. A partir desse momento, o paciente começou a receber reposição intravenosa de
imunoglobulina humana. Discussão: O tratamento por substituição de imunoglobulina sérica visa manter o doente sem infecções e prevenir o
desenvolvimento de doenças crônicas. As infusões mensais de imunoglobulina apresentam risco residual para os pacientes como aquisição de
infecções hematogênicas, reações pirogênicas, autoimunidade, entre outras. Além disso, o atraso para o tratamento é situação frequente que
contribui para a morbidade e a mortalidade nesses pacientes. Conclusões: As perspectivas dos doentes com imunodeficiência comum variável
dependem da dimensão dos danos que ocorreram nos órgãos antes do diagnóstico e tratamento de substituição com imunoglobulina, além
do sucesso com que as infecções são prevenidas, utilizando a terapia com imunoglobulina e antibióticos e controle rigoroso em relação ao
tratamento intravenoso, monitorando possíveis riscos residuais que o tratamento invasivo pode causar.
PALAVRA-CHAVE: Agamaglobulinemia, imunoglobulinas, imunoglobulinas intravenosas, síndromes de imunodeficiência, infecções
bacterianas
INTRODUÇÃO
A imunodeficiência comum variável (ICV) é uma síndrome de imunodeficiência heterogênea caracterizada por hipogamaglobulinemia de início tardio, infecções bacterianas
de repetição e várias anormalidades imunológicas, incluindo
incidência aumentada de doenças autoimunes e malignidade.
Essa é uma síndrome rara, com prevalência estimada de
1:50.000 até 1:200.000 na população geral,1-3 e de 1:79.000 em
pacientes pediátricos no Brasil.4,5
É uma imunodeficiência primária que afeta ambos os sexos de
forma equivalente e pode apresentar-se em qualquer faixa etária,
porém tem distribuição bimodal, com picos na infância em torno
dos 10 anos ou na fase adulta, na segunda e/ou terceira décadas
de vida.2,3,5-7 Sua causa ainda é desconhecida, no entanto, está relacionada ao percurso clínico, grau e tipo de deficiência de imunoglobulinas séricas, que variam de doente para doente.8
Bacharel em Biomedicina e especialista em Análises Clínicas pela Universidade Tuiuti do Paraná de Curitiba.
Docente da Faculdade de Biomedicina da Universidade Tuiuti do Paraná. Doutora em Saúde da Criança e do Adolescente do Setor de Ciências da Saúde
pela UFPR do Hospital de Clínicas, área de concentração Infectologia Pediátrica. Mestre em Biologia Celular e Molecular e bacharel em Farmácia-Bioquímica
graduada pela Universidade Federal do Paraná.
I
II
Endereço para correspondência:
Patrícia Estrela Evangelista
Rua Jorge Gomes Rosa, 530 — Curitiba (PR) — CEP 81540-480
Tel. (41) 3535-0904/3369-2846 — Cel. (41) 9656-6714
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 24 de setembro de 2013 — Última modificação: 7 de abril de 2014 — Aceite: 7 de maio de 2014
Diagn Tratamento. 2014;19(3):119-24.
119
Imunodeficiência comum variável: relato de caso
Alguns pacientes apresentam diminuição tanto da imunoglobulina G (IgG), como da imunoglobulina A (IgA). Outros
podem apresentar níveis baixos em todos os três principais
tipos de imunoglobulinas (IgG, IgA e IgM).8
Nas últimas décadas, os estudos sobre as células do sistema
imunológico em doentes com ICV têm revelado espectro amplo de anomalias nos linfócitos. A maioria dos pacientes apresenta níveis normais de linfócitos B, mas estes não conseguem
passar por maturação normal para se tornarem plasmócitos
capazes de produzir diferentes tipos de imunoglobulinas.
Outros pacientes não possuem função suficiente dos linfócitos T “helper” (auxiliadores), necessária para resposta normal
dos anticorpos.3,7,9 Um terceiro grupo apresenta número excessivo de linfócitos T citotóxicos, apesar de o papel destas
células na doença não ser claro.8
O tratamento baseia-se na reposição de gamaglobulina humana, que no Brasil geralmente é feita por via endovenosa,
em intervalos de três a quatro semanas, na dose de 300 mg/kg
a 600 mg/kg, com objetivo de manter níveis séricos acima de
600 mg/dL. Além disso, é necessário instituir tratamentos específicos para cada uma das complicações apresentadas.4,10-12
O estudo tem como objetivo avaliar as metodologias utilizadas e estudos realizados para a obtenção do diagnóstico
positivo para ICV; acompanhar o tratamento do paciente,
confrontando os exames de rotina realizados com a evolução
do quadro clínico; avaliar a relação risco-benefício que o tratamento invasivo apresenta para o paciente; realizar avaliação
crítica sobre a qualidade de vida do paciente ao longo deste
período e analisar se o tratamento vigente está atendendo às
expectativas benéficas de evolução para o paciente.
DESCRIÇÃO DO CASO
Paciente L. J. G., do sexo masculino, de 21 anos, caucasiano, apresentava histórico de infecções bacterianas e infecções sinopulmonares recorrentes, destacando-se pelos
quadros de pneumonias de repetição extensas e necessidade de tratamento prolongado cada vez mais frequentes
desde 2007. Com início em dezembro de 2007, o tratamento
da pneumonia foi realizado com os antibióticos azitromicina e amoxicilina com clavulanato, para controle da infecção e sintomas. Em abril de 2008, o quadro se repetiu;
no entanto, o tratamento dessa vez foi realizado com cloridrato de moxifloxacino e foram monitorados os sinais e
sintomas. Nos meses posteriores, foram observados outros
quadros de infecção bacteriana; contudo, com caráter menos agressivo, como sinusite e gripes.
Em julho de 2008, foram realizados exames de radiografia de tórax, hemograma e testes sorológicos para hepatites
B, C e vírus da imunodeficiência humana (HIV), os quais
120
Diagn Tratamento. 2014;19(3):119-24.
apresentaram resultados estáveis para os parâmetros hemodinâmicos e sorologias negativas. As radiografias de tórax
sugeriam imagens de bronquiectasias, posteriormente confirmadas por tomografia torácica.
O quadro clínico associado aos exames de imagem levaram, em julho de 2008, à retomada do tratamento com os antibióticos amoxicilina com clavalunato. O acompanhamento foi
realizado, por meio de novos exames, nos meses de outubro e
dezembro de 2008.
Nos períodos de fevereiro e março de 2009, o quadro foi
apresentado a um pneumologista e a um infectologista. Foram
repetidos os exames de radiografia e hemograma e adicionados exames complementares como tomografia, ultrassonografia, testes de alergia, cultura de secreção nasal e testes de
função pulmonar. Nesse mesmo período, foram utilizados pelo
paciente cloridrato de fexofenadina (antialérgico/anti-histamínico), fosfato sódico de prednisolona (antialérgico/adrenocorticosteroide), fumarato de formoterol diidratado/budesonida
(anti-inflamatório/corticosteroide inalatório com agonista beta
de ação prolongada), furoato de mometasona (anti-inflamatório/glicocorticoide tópico) e cloranfenicol (antibiótico/inibidor
da síntese proteica bacteriana).
Nos meses de junho de 2009, setembro de 2009 e janeiro de
2010, o tratamento foi realizado novamente com cloridrato
de moxifloxacino (antibiótico/fluoroquinolônico de amplo espectro) por um período de 14 dias a cada mês de reincidência
e, em fevereiro de 2010, com mesilato de gemifloxacino (antibiótico/quinolônico) por um período de 7 dias.
Visto que não há um diagnóstico definitivo para ICV, o
diagnóstico foi realizado pelo método de exclusão. Após
uma série de exames e estudo mais aprofundado do caso,
foram levantadas as possíveis doenças para o quadro, dentre elas a ICV. Sua posterior confirmação, no entanto, só
foi dada após os exames realizados no período de abril de
2010, quando foi realizada a dosagem de imunoglobulinas
IgA, IgG e IgM (Tabela 1), que revelaram hipogamaglobulinemia acentuada com níveis alterados das três classes de
imunoglobulinas em discussão.
Através do quadro clínico, histórico do paciente, análise dos exames realizados e níveis alterados de imunoglobulinas, foi identificado que o tratamento mais adequado
para o paciente L.J.G. seria a reposição intravenosa de imunoglobulina humana, que já é tratamento usual para este
tipo de imunodeficiência. As preparações de imunoglobulina humana para uso terapêutico são obtidas a partir do
fracionamento industrial do plasma.13 O tratamento tem
como objetivo manter níveis de imunoglobulina estáveis
e tem caráter contínuo, uma vez identificada a necessidade do paciente para tal procedimento e definida a dose a
ser utilizada.14
Patrícia Estrela Evangelista | Elenice Stroparo
De acordo com a Portaria da Secretaria de Atenção
à Saúde do Ministério da Saúde (SAS/MS) n o 495 de
11/09/2007; a dose recomendada para o início do tratamento é de 300 mg/kg a 400 mg/kg a cada três semanas,
ou 400-500 mg/kg a cada quatro semanas. A dose máxima
recomendada é de 600 mg/kg a cada quatro semanas, ou
800 mg/kg a cada quatro semanas.14
Em julho de 2010, o tratamento por meio de reposição de
imunoglobulina do paciente L.J.G. foi estabelecido com doses de 45 gramas a cada quatro semanas de imunoglobulina
humana normal, marca Octagam. São imunoglobulinas poliespecíficas, constituídas a partir de um pool de plasma de
imunoglobulina G e suas subclasses, distribuídas respectivamente em 60% de IgG1, 32% IgG2, 7% IgG3 e 1% IgG4, representando assim as frações correspondentes da composição
original do plasma humano.
Os exames de acompanhamento foram definidos conforme diretrizes estabelecidas no I Consenso Brasileiro sobre o
Uso de Imunoglobulina em Pacientes com Imunodeficiências
Primárias,15 através de exames de dosagem de imunoglobulinas G (IgG, IgG1, IgG2, IgG3 e IgG4) realizados semestralmente, exceto em casos em que sejam observadas alterações no
quadro de saúde do paciente que possam indicar a necessidade de revisão do tratamento estabelecido.
Para a avaliação e monitoramento da qualidade de vida
do paciente, foram seguidos os critérios estabelecidos na
Portaria da SAS/MS no 495 de 11/09/2007; além dos relatos
e observações do paciente a respeito do seu quadro clinico
e qualidade de vida durante o tratamento.
Foram realizados testes laboratoriais de acompanhamento nos meses de julho de 2010, dezembro de 2010, agosto de
2011 e agosto de 2012. Desde então, o paciente tem apresentado quadro de melhora gradual tanto em relação às dosagens de IgG, que estão aumentando rumo à normalização
(Tabela 2), quanto à qualidade de vida que se mantém estável, sem maiores complicações ou infecções recorrentes,
apesar do tratamento de caráter invasivo.
DISCUSSÃO
Realizou-se busca sistematizada, conforme o Medical
Subject Headings (MeSH), às principais bases de dados utilizando o termo “common variable immunodeficiency”, como
ilustrado na Tabela 3. Além disso, com o propósito de filtrar
e fornecer um melhor direcionamento, foram considerados
durante a busca apenas relatos de caso. Ao final da busca
sistematizada, foram encontrados 547 estudos no Medline
(Medical Literature Analysis and Retrieval System Online)
via PubMed, 743 no Lilacs (Literatura Latino-Americana e do
Caribe em Ciências da Saúde) via Bireme/BVS, 7 no SciELO
e nenhum relato de caso no Embase (Excerpta Medica
Database) via Elsevier. Através dos dados obtidos na busca
sistematizada, foi observado que, apesar de existirem referências na literatura em relação ao relato de caso tratado, há
grande variação no tempo para diagnóstico e tratamento da
doença, dificultando um padrão de análise.
Ao avaliar o tempo entre a obtenção de diagnóstico positivo para ICV, realizado no período de dezembro de 2007 a
abril de 2010, e o tempo de tratamento vigente do paciente,
Tabela 1. Resultados laboratoriais de abril de 2010 do paciente L.J.G. Fase diagnóstica
Exames imunológicos
Imunoglobulina E (IgE)
Imunoglobulina M (IgM)
Imunoglobulina A (IgA)
Imunoglobulina G (IgG)
IgG 1
IgG 2
IgG 3
IgG 4
Método utilizado
Quimioluminescência
Imunoturbidimetria
Imunoturbidimetria
Imunoturbidimetria
Nefelometria
Nefelometria
Nefelometria
Nefelometria
Valores de referência
inferior a 120 UI/mL
50 a 300 mg/dL
50 a 400 mg/ dL
600 a 1500 mg/dL
370 a 1280 mg/dL
106 a 610 mg/dL
23 a 196 mg/dL
8 a 140 mg/dL
Abril 2010
inferior a 2UI/mL
4 mg/dL*
7 mg/dL†
63 mg/dL*
76 mg/dL
51 mg/ dL
10 mg/dL
7 mg/dL
*Valor de referência inferior aos valores de crianças de quatro meses; †Valor de referência para criança de quatro meses.
Tabela 2. Resultados laboratoriais de julho de 2010 a agosto de 2012, do paciente L.J.G.
Exames
IgG
IgG 1
IgG 2
IgG 3
IgG 4
Método utilizado
Valores de referência
Imunoturbidimetria
Nefelometria
Nefelometria
Nefelometria
Nefelometria
600 a 1500 mg/dL
2396 a 10835 mg/dL
1235 a 5487 mg/dL
276 a 1344 mg/dL
84 a 888 mg/dL
Julho
Dezembro
Agosto
Agosto
2010
57 mg/dL*
< 76 mg/dL*
51 mg/dL*
10 mg/dL*
< 7mg/dL*
2010
1110 mg/dL
647 mg/dL†
329 mg/dL†
17 mg/dL†
13 mg/dL†
2011
924 mg/dL
2265 mg/dL
642 mg/dL
101 mg/dL
59 mg/dL
2012
1010 mg/dL
5730 mg/L
2390 mg/L
185 mg/L
106 mg/L
*Valor de referência inferior aos valores de crianças de 4 meses; †Valor de referência para criança de 12 a 36 meses. IgG = imunoglobulina G.
Diagn Tratamento. 2014;19(3):119-24.
121
Imunodeficiência comum variável: relato de caso
Tabela 3. Resultados da busca sistematizada nas bases de
dados médicas, com descritores em saúde (DeCS), utilizando
filtro para relato de caso, realizada em 27 de março de 2014
Base de Dados
Embase
(via Elsevier)
Lilacs
(via Bireme/BVS)
Medline
(via PubMed)
SciELO
122
Estratégia de busca
“Common Variable
Immunodeficiency”[Mesh]
“Common Variable
Immunodeficiency”[Mesh]
Filtro: Relatos de Caso
“Common Variable
Immunodeficiency”[Mesh]
Filtro: Case Reports
“Common Variable
Immunodeficiency”[Mesh]
Filtro: Relatos de Caso
Diagn Tratamento. 2014;19(3):119-24.
Total de relatos
de caso
0
743
547
7
observada e confirmada por meio do Gráfico 1, com as dosagens de IgG obtidas nos períodos de julho de 2010 a agosto de
2012, em que se constata aumento significativo dos níveis
de imunoglobulinas após o início do tratamento de reposição de
imunoglobulinas por via endovenosa.
7000
6000
Imunoglobulinas x valores de referência
(julho de 2010 - agosto de 2012)
Valores de referência
Agosto de 2011
Dezembro de 2010
Julho de 2010
Agosto de 2012
5000
Dosagens (mg/dL)
com início em julho de 2010 e com caráter contínuo, é possível constatar que ambas as situações mencionadas por
Grumach e cols.16 e Collanieri17 podem ser observadas no caso
do paciente L.J.G. De acordo com Collanieri17 aproximadamente 60% dos pacientes portadores de agamaglobulinemia
de herança autossômica e mais de 90% das hipogamaglobulinemias não são definidas geneticamente, dificultando,
assim, o desenvolvimento de terapia curativa mais eficiente,
necessária para a substituição das infusões mensais de imunoglobulina, que apresentam risco residual para os pacientes, como aquisição de infecções hematogênicas, reações
pirogênicas, autoimunidade, entre outros. Grumach e cols.,16
por sua vez, afirmam que tanto o comprometimento da imunidade através da aquisição de infecções e reações residuais
quanto a eficácia da resposta terapêutica estão diretamente
ligados com o tempo de diagnóstico.
Segundo Grumach e cols.,16 o longo período decorrido entre as manifestações clínicas e o diagnóstico dos casos de ICV
se torna um agravante que influi diretamente no prognóstico
do paciente. No caso do paciente L. J. G, apesar de não terem
sido identificados danos residuais ou comprometimento de
órgãos, observa-se que a partir do período em que houve a
observação das primeiras manifestações clínicas, em dezembro de 2007, até o momento de diagnóstico definitivo para
ICV, em abril de 2010, o paciente permaneceu dois anos e
meio sem o tratamento adequado.
Nobre e cols.18 também relatam que, em geral, o longo
período para o diagnóstico e o atraso para o tratamento
são situações frequentes que contribuem para morbidade e
mortalidade nesses pacientes. Já o diagnóstico e intervenção
precoces levam a melhora importante no prognóstico e qualidade de vida dos pacientes com deficiência de anticorpos.
Segundo Bayri e cols.,19 a reposição endovenosa de imunoglobulinas induz à proliferação e produção de imunoglobulinas, especialmente IgG e IgM, pelos linfócitos B de pacientes
com ICV. No caso do paciente L. J. G., esta situação pode ser
4000
3000
2000
1000
0
IgG
IgG1
IgG2
IgG3
IgG4
-1000
Gráfico 1. Imunoglobulinas (Ig) e valores de referência
(julho de 2010 a agosto de 2012).
Após o tratamento, foram acompanhados os resultados
dos exames e evidenciados aumentos significativos dos níveis de IgG, IgG1, IgG2, IgG3 e IgG4 nos meses dezembro
de 2010, julho de 2010, agosto de 2011 e em agosto de 2012.
No entanto, apesar de os níveis de imunoglobulinas apresentarem índice de crescimento constante, os valores de IgG do
paciente L. J. G. ainda permaneceram com níveis abaixo dos
valores de referência durante o período de junho de 2010 a
agosto de 2012. A normalização dos valores de IgG foi observada apenas durante os exames de acompanhamento no período de agosto de 2012 (Tabela 2).
conCLUSÃO
Por se tratar de doença relativamente desconhecida,
com sintomas e sinais clínicos muito semelhantes aos de
outras doenças, uma das maiores dificuldades encontradas nos casos de ICV é, primeiramente, o seu diagnóstico.
Além disso, por se tratar de imunodeficiência, em que uma
de suas principais características é a variabilidade, quando diagnosticada corretamente, ainda se corre o risco de
não haver metodologias de tratamento validadas na área
da saúde para o tipo específico.
Atualmente, a terapêutica utilizada em pacientes com ICV
é realizada por meio de substituição com imunoglobulina,
Patrícia Estrela Evangelista | Elenice Stroparo
combinada com a terapia com antibióticos. Este procedimento,
apesar dos riscos anteriormente mencionados, tem melhorado
significativamente as perspectivas dos doentes com ICV.8
O tratamento por substituição de imunoglobulina sérica
visa manter o doente sem infecções e prevenir o desenvolvimento de doenças crônicas. No entanto, é importante ressaltar
que as perspectivas dos doentes com ICV dependem da dimensão dos danos causados nos órgãos antes do diagnóstico, além
do sucesso com que as infecções são prevenidas, com a utilização da terapia com imunoglobulina e antibióticos. No caso do
paciente L. J. G, apesar do tempo decorrido para o diagnóstico,
após o início do tratamento, sua evolução clínica vem sendo
apresentada de maneira positiva, com resultados que mantêm
um nível de evolução crescente quando comparamos os valores de IgG apresentados pelo paciente no período de abril de
2010, fase diagnóstico antes do tratamento com imunoglobulina humana, com sua melhora gradual nos exames posteriores,
até sua fase de normalização, no período de 2012.
No entanto, é importante lembrar que esses parâmetros
permanecem estáveis e com quadro de melhora positivo apenas se houver controle rigoroso em relação ao tratamento
intravenoso vigente, controle dos riscos residuais que o
tratamento invasivo pode causar (aquisição de infecções hematogênicas, reações pirogênicas, autoimunidade) e monitoramento da qualidade de vida do paciente.
Se o tratamento de reposição de imunoglobulina não for
realizado com a periodicidade exigida, ou até mesmo se os
níveis de imunoglobulina humana recebidos não forem suficientes para as necessidades do paciente, os níveis de imunoglobulina voltarão a um nível baixo, deixando o paciente
sujeito a infecções recorrentes ou complicações clínicas adversas devido à imunidade baixa. Além disso, como as variações desta imunodeficiência são muito amplas e em geral
todos os casos relatados e encontrados na literatura de certo
modo difer­em entre si, é de fundamental importância que
o maior número de informações e esclarecimentos a respeito
da ICV sejam estudados e validados dentro da área da saúde.
Desta forma, além da contribuição para melhor compreensão
da ICV, também serão buscados novos métodos de diagnóstico e tratamento eficaz da doença, que conta atualmente com
o método de diagnóstico por exclusão e tratamento paliativo
de caráter invasivo, com risco de infecções residuais.
REFERÊNCIAS
1. Graudenz GS, Oliveira CH, Pinho Júnior AJ, Lazzarini S. Complicações graves na imunodeficiência comum variável: relato de dois casos [Severe complications in common variable immunodeficiency:
two case reports]. Revista Brasielira de Alergia e imunopatologia.
1999;22(2):63-7. Disponível em: http://www.asbai.org.br/revistas/
Vol222/imuno.htm. Acessado em 2014 (8 abr).
2. Lopes A, Barata F. A propósito de um caso de imunodeficiência
comum variável--Revisão das hipogamaglobulinemias
[About a case of common variable immunodeficiency-revision of hypogammaglobulinemias]. Rev Port Pneumol.
2006;12(3):293-301.
3. Torres J, Fortuna J, Trigo E, et al. Diarreia num doente com imunodeficiência comum variável: a propósito de um caso clínico. J
Port Gastrenterol. 2007;14(4):199-203.
4. Grumach AS, Duarte AJ, Bellinati-Pires R, et al. Brazilian report on
primary immunodeficiencies in children: 166 cases studied over a
follow-up time of 15 years. J Clin Immunol. 1997;17(4):340-5.
5. Chapel H, Cuningham-Rundles C. Update in understanding
common variable immunodeficiency disorders (CVIDs) and the
management of patients with these conditions. Br J Haematol.
2009;145(6):709-27.
6. Sneller MC, Strober W, Einsensten E, Jaffe JS, Cunningham-Ruddles C. NIH conference. New insights into common variable
immunodeficiency. Ann Inter Med. 1993;118(9):720-30.
7. Weiler CR, Bankers-Fulbright JL. Common variable immunodeficiency: test indications and interpretations. Mayo Clin Proc.
2005;80(9):1187-200.
8. International Patient Organisation for Primary Immunodeficiencies (IPOPI). Imunodeficiência comum variável. 2007. Disponível
em: http://www.ipopi.org/uploads/media/publication/IMUNODEFICIENCIA%20COMUN%20VARIAVEL_06.02.08.pdf. Acessado em 2014 (8 abr).
9. Bonilla FA, Geha RS. 2. Update on primary immunodeficiency
diseases. J Allergy Clin Immunol. 2006;117(2 Suppl MiniPrimer):S435-41.
10. Eijkhout HW, van Der Meer JW, Kallenberg CG, et al. The
effect of two different dosages on intravenous immunoglobulin on the incidence of reccurent infections in patients with primary hypogammaglobulinemia. A randomized, double-blind,
multicenter crossover trial. Ann Intern Med 2001;135(3):165-74.
11. Park MA, Li JT, Hagan JB, Maddox DE, Abraham RS. Common
variable immunodeficiency: a new look at an old disease. Lancet. 2008;372(9637):489-502.
12. Pedreschi M. Classificação de pacientes com imunodeficiência
comum variável através da identificação de subtipos de linfócitos B [dissertação]. São Paulo: Faculdade de Medicina da Universidade de São Paulo; 2011.
13. Brasil. Consulta Pública no 36, de 20 de maio de 2004. Diretrizes
para a transfusão de imunoglobulinas. Disponível em: http://
www4.anvisa.gov.br/base/visadoc/CP/CP%5B7489-5-0%5D.
PDF. Acessado em 2014 (3 mai).
14. Brasil. Portaria no 495 de 11 de setembro de 2007. Imunodeficiência primária com predominância de defeitos de anticorpos. Imunoglobulina humana. Disponível em: http://dtr2001.
Diagn Tratamento. 2014;19(3):119-24.
123
Imunodeficiência comum variável: relato de caso
saude.gov.br/sas/PORTARIAS/Port2007/PT-495.htm. Acessado em 2014 (8 abr).
15. Carvalho BTC, Condino-Neto A, Solé D, Rosário Filho N. I Consenso Brasileiro sobre o uso de imunoglobulina humana em
pacientes com imunodeficiências primárias. Revista Brasielira
de Alergia e Imunopatologia. 2010;33(3):104-16. Disponível
em: http://www.sbai.org.br/revistas/Vol333/consenso_33_3.pdf.
Acessado em 2014 (8 abr).
16. Grumach AS, Vasconcelos DM, Duarte AJS. Imunodeficiência comum variável: relato de 14 casos. Revista Brasileira de
Alergia e Imunopatologia. 2007;[abstract 001]. Disponível em:
http://www.asbai.org.br/revistas/Vol235/temas1-40.htm. Acessado em 2014 (8 abr).
124
Diagn Tratamento. 2014;19(3):119-24.
17. Collanieri AC. Imunodeficiência comum variável: distúrbio de
diferenciação dos linfócitos B ou distúrbio de ativação os linfócitos T? [tese]. São Paulo: Faculdade de Medicina da Universidade de São Paulo; 2010.
18. Nobre FA, Gonzalez IGS, Melo KM, et al. Impacto do tratamento com imunoglobulina humana intravenosa no número de
pneumonias em pacientes com deficiência de anticorpo. Rev
Bras Alergia Imunopatol. 2012;35(1):25-9.
19. Bayri J, Fournier EM, Maddur MS, et al. Intravenous immunoglobulin induces proliferation and immunoglobulin synthesis from B cells
of patients with common variable immunodeficiency: a mechanism
underlying the beneficial effect of IVIg in primary immunodeficiences. J Autoimmun. 2011;36(1):9-15.
DERMATOLOGIA
Impetigo bolhoso disseminado
Vanessa Mello TonolliI, Juliana Polizel OcanhaII, Hamilton Ometto StolfIII
Universidade Estadual Paulista Júlio de Mesquita Filho (Unesp), Faculdade de Medicina de Botucatu, São Paulo
Resumo
Contexto: O impetigo é piodermite comum da criança, de tratamento fácil, porém de diagnóstico muitas vezes desafiador, principalmente
na sua forma bolhosa, que faz diferencial com as doenças bolhosas da infância. Relato de caso: Relatam-se dois casos de impetigo bolhoso,
que foram desafiadores em termos diagnósticos, exemplificando a dificuldade no diagnóstico e terapêutica desses pacientes. Discussão:
Casos clínicos de impetigo de extensão corporal importante simulam outros diagnósticos diferenciais. A relevância deste relato é demonstrar que o diagnóstico preciso na fase inicial possibilita a terapêutica específica e evita complicações. Conclusão: O impetigo bolhoso deve
ser sempre lembrado pelo profissional médico que atende pacientes na faixa etária pré-escolar e escolar, apresentando bolhas e exulcerações com crostas pelo corpo. Este artigo objetiva atualização diagnóstica e terapêutica nesse contexto.
PALAVRAS-CHAVE: Impetigo, pele, infecção, bactérias, terapêutica
INTRODUÇÃO
O impetigo é infecção cutânea bacteriana mais frequente da infância.1 Acomete crianças, em idade pré-escolar e escolar, convivendo em aglomeração e má higiene.
Também afeta crianças predispostas com, por exemplo,
eczema atópico. O impetigo pode se apresentar classicamente sob a forma bolhosa e não bolhosa. A forma bolhosa é importante, pois tem como diagnóstico diferencial as
doenças bolhosas da infância, como pênfigo vulgar e dermatite herpetiforme, e também doenças como eritema polimorfo, síndrome da pele escaldada estafilocócica, tinha
bolhosa, alergia a picada de insetos e dermatite venenata.2
Foi realizada extensa revisão da literatura e encontrados
inúmeros relatos de caso e revisões, demonstrando a importância desta afecção dermatológica (Tabela 1).
RELATO DE CASO
Caso 1. JPPS, oito anos de idade, sexo masculino, cor
parda, procedente de Areiópolis, São Paulo. Procurou atendimento no pronto-socorro relatando que, há seis dias,
após brincar em lixão perto de sua casa, passou a apresentar prurido no abdome que evoluiu com vesículas e bolhas no local, posteriormente espalhando-se para tronco,
face, mucosa oral, membros superiores e inferiores, e febre.
Dermatologista. Autônoma (consultório particular).
Dermatologista, residente do quarto ano de Dermatologia da Faculdade de Medicina de Botucatu (Unesp).
Professor assistente doutor do Departamento de Dermatologia e Radioterapia, Faculdade de Medicina de Botucatu, Universidade Estadual Paulista (Unesp).
I
II
III
Editor responsável por esta seção:
Hamilton Ometto Stolf. Professor doutor, Faculdade de Medicina de Botucatu, Universidade Estadual Paulista.
Endereço para correspondência:
Hamilton Ometto Stolf
Caixa Postal 557
Botucatu (SP) — CEP 18618-970
Tel. (14) 3882-4922
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 8 de maio de 2014 — Última modificação: 11 de junho 2014 — Aceite: 23 de junho de 2014
Diagn Tratamento. 2014;19(3):125-8.
125
Impetigo bolhoso disseminado
Tabela 1. Resultado da busca sistematizada em bases de dados com os descritores em saúde (Decs) e Medical Subheadings
(MeSH), realizada em 6 de maio de 2014
Estratégia de busca
Artigos
encontrados
Artigos relacionados
com o caso
Search (“Impetigo”[Mesh]) AND “Staphylococcus
aureus”[Mesh] Filters: Case Reports
18
3
Lilacs (via Biblioteca Virtual em Saúde)
Search “impetigo AND staphylococcus aureus”
14
2
Embase (via Elsevier)
Search “impetigo AND staphylococcus aureus”
10
1
Base de dados
Medline (via PubMed)
Foi medicado com antialérgico (maleato de dexclorfeniramina) via oral, dexametasona e neomicina tópicos, além
de banhos com permanganato de potássio, com piora progressiva do quadro. À admissão, apresentava bolhas flácidas e vesículas de conteúdo sero-hemorrágico e exulcerações recobertas por crostas hemato-melicéricas, em todo
o corpo, de tamanhos variados (Figura 1). Apresentava
ainda exulceração na mucosa oral, de aproximadamente
0,5 cm. Realizadas as hipóteses de impetigo bolhoso e pênfigo vulgar, iniciando-se tratamento com o cefazolina endovenosa. O paciente apresentou melhora e teve alta após
nove dias de internação.
Caso 2. ABTO, três anos de idade, sexo feminino. Mãe
referia que há duas semanas a criança começou a apresentar pequenas bolhas na fossa cubital direita, que se
estenderam para a região axilar, tronco, face e membros
inferiores. Procurou o pronto-socorro de sua cidade, onde
permaneceu internada por quatro dias, em uso de eritromicina e corticoide via oral, com melhora momentânea do
quadro. Após a alta, ainda em uso das medicações, as lesões retornaram com piora importante, o que motivou o
encaminhamento ao dermatologista. Ao exame, a paciente
apresentava extensas áreas de exulceração, recobertas por
crostas hematomelicéricas nas axilas, tronco e face, muito dolorosas, além de vesículas no tronco (Figura 2). Mãe
negava febre ou outros sinais sistêmicos. Realizada hipótese diagnóstica de impetigo bolhoso, sendo suspensos a
eritromicina e o corticoide via oral e iniciada cefalexina e
cuidados locais com permanganato de potássio. No retorno, após sete dias, a criança apresentava apenas máculas
hipocrômicas nos locais das exulcerações.
A
B
DISCUSSÃO
O impetigo é a piodermite mais comum da infância, acometendo igualmente ambos os sexos, principalmente abaixo
dos seis anos de idade. Os fatores de risco são as aglomerações, higiene precária, traumas na pele e também doenças
dermatológicas que servem como portas de entrada, sendo o
maior exemplo a dermatite atópica.1
Os agentes causais são o estreptococo beta-hemolítico do grupo A e Staphylococcus aureus, mas as infecções
126
Diagn Tratamento. 2014;19(3):125-8.
Figura 1. Bolhas rotas e exulcerações por todo o tegumento
na face (A) e tronco (B) do caso 1.
Vanessa Mello Tonolli | Juliana Polizel Ocanha | Hamilton Ometto Stolf
também podem ser mistas. O impetigo pode ser de dois
tipos: bolhoso e não bolhoso, sendo este último o mais comum. O impetigo bolhoso apresenta lesões vesicobolhosas
e exulcerações recobertas por crostas hemato-melicéricas,
com aspecto circinado. O quadro geralmente não é acompanhado de sintomas sistêmicos, mas pode haver febre e
linfadenopatia. A forma bolhosa tem como diferenciais o
pênfigo vulgar e a dermatite herpetiforme, eritema polimorfo, síndrome da pele escaldada estafilocócica, tinha
bolhosa, alergia a picada de insetos e dermatite venenata
(por plantas).2 Através da busca sistematizada dos relatos
de casos clínicos semelhantes (Tabela 2), fica evidente o
desafio da diferenciação clinica inicial retardando o tratamento adequado.3-5
Nos pacientes apresentados, a manifestação clínica
ocorreu de forma disseminada, o que é incomum. Foi
inicialmente suspeitado tratar-se de doença bolhosa
A
autoimune, porém detalhes clínicos como a epidemiologia, a presença de bolhas rotas de aspecto circinado,
sintomas sistêmicos como febre, inapetência e queda do
estado geral indicaram o diagnóstico de impetigo bolhoso estafilocócico.
O tratamento é realizado com agentes tópicos e, em casos
com lesões extensas, são utilizados antibióticos sistêmicos.6
O tratamento local consiste em limpeza, emprego de permanganato de potássio (diluir meio comprimido em quatro
a cinco litros de água e fazer banhos de assento ou compressas duas a três vezes ao dia) ou água boricada a 3% ( fazer
compressas duas a três vezes ao dia).6 A antibioticoterapia
local pode ser feita com mupirocina 2% ou o ácido fusídico
e neomicina. A antibioticoterapia sistêmica com cefalexina
(40 mg/kg/dia a 50 mg/kg/dia), amoxicilina associada ao
ácido clavulânico (25 mg/kg/dia), cefaclor (20 mg/kg/dia) ou
clindamicina (15 mg/kg/dia).7 Atualmente, as penicilinas e a
eritromicina não são consideradas antibióticos de primeira
escolha, pois há possibilidade de resistência por cepas de estafilococos meticilino-resistentes.7
CONCLUSÃO
B
Figura 2. Áreas de exulceração, recobertas por crostas hematomelicéricas no tronco (A) e dorso (B), associadas a vesículas.
O impetigo é afecção dermatológica comum na faixa
etária pré-escolar e escolar, de fácil tratamento, porém seu
diagnóstico inicial muitas vezes é desafiador, principalmente na sua forma bolhosa, fazendo diagnóstico diferencial com outras doenças bolhosas da infância. Esperamos,
com este artigo, orientar o profissional médico, como pediatras, emergencistas e da saúde pública sobre a doença
e seu tratamento.
Tabela 2. Diagnóstico diferencial do impetigo bolhoso infantil
Características clínicas
Diagnóstico
Vesicobolhas e exulcerações com aspecto circinado.
Clínico e a cultura e antibiograma da secreção
das vesículas e bolhas.
Adulto jovem. Erupção simétrica e polimorfa pruriginosa,
nas faces extensoras dos membros. Lesões orais são
comuns. Todos os casos apresentam enteropatia sensível
ao glúten (doença celíaca), clínica ou subclínica.
Biópsia para anatomopatológico e
imunofluorescência direta.
Crianças menores de cinco anos com vesicobolhas aspecto
em roseta; erosões.
Biópsia para anatomopatológico e
imunofluorescência direta.
Pênfigo vulgar
Adultos com bolhas flácidas, erosões dolorosas, úmidas.
Biópsia para anatomopatológico e
imunofluorescência direta.
Eritema multiforme bolhoso
Lesões polimorfas; morfologia típica em “alvo” é mais
comum nos casos por infecções, pode apresentar lesões
nas mucosas.
Biópsia para anatomopatológico e investigação
de possíveis fatores desencadeantes (drogas,
vírus, bactérias, entre outros).
Impetigo bolhoso
Dermatite herpetiforme
Dermatose por IgA linear
IgA = imunoglobulina A.
Diagn Tratamento. 2014;19(3):125-8.
127
Impetigo bolhoso disseminado
REFERÊNCIAS
1. Azulay L, Hannauer L, Leal F, et al. Atlas de dermatologia: da
semiologia ao diagnostico. 2a ed. São Paulo: Elsevier; 2013.
2. Oliveira ZNP. Dermatologia pediátrica. Piodermites. 2a ed. São
Paulo: Manole; 2012.
3. Hubiche T, Bes M, Roudiere L, et al. Mild staphylococcal
scalded skin syndrome: an underdiagnosed clinical disorder. Br
J Dermatol. 2012;166(1):213-5.
4. Knox BL, Petska HW, DeMuri GP, Feldman KW. Staphylococcal
infection mimicking child abuse: what is the differential
128
Diagn Tratamento. 2014;19(3):125-8.
diagnosis and appropriate evaluation? Pediatr Emerg Care.
2011;27(6):547-9.
5. Sandhu K, Kanwar AJ. Generalized bullous impetigo in a
neonate. Pediatr Dermatol. 2004;21(6):667-9.
6. Bernard P. Management of common bacterial infections of the
skin. Curr Opin Infect Dis. 2008;21(2):122-8.
7. Cohen PR. Community-acquired methicillin-resistant Staphylococcus aureus skin infections: implications for patients and practitioners. Am J Clin Dermatol. 2007;8(5):259-70.
NUTROLOGIA
Efetividade e segurança do vegetal
Cissus sicyoides (“insulina vegetal”)
como fitoterápico hipoglicemiante
Hernani Pinto de Lemos JúniorI, André Luis Alves de LemosII
Pós-graduação em Medicina Interna e Terapêutica e Medicina Baseada em Evidências da Universidade Federal
de São Paulo — Escola Paulista de Medicina (Unifesp-EPM), Centro Cochrane do Brasil
Resumo
Introdução: Em algumas regiões do Brasil, a infusão de folhas da planta Cissus sicyoides (conhecida popularmente como “insulina vegetal”)
é utilizada como agente hipoglicemiante em diabéticos. Objetivo: Verificar a efetividade desse fitoterápico no tratamento do diabetes em
seres humanos. Métodos: Revisão sistematizada da literatura realizada no Centro Cochrane do Brasil. Resultados: Um estudo feito em coelhos mostrou redução significativa de 60% da glicemia. Dois estudos feitos em ratos foram controversos, um mostrando redução de 25% na
glicemia e outro mostrando resultados insignificantes. Um estudo feito em humanos mostrou resultados não satisfatórios para a efetividade
do Cissus sicyoides. Conclusão: Não existem evidências científicas que indiquem a planta Cissus sicyoides, conhecida popularmente como
insulina vegetal, no tratamento do diabetes mellitus em humanos.
PALAVRAS-CHAVE: Diabetes mellitus, cissus, hiperglicemia, flavonoides, insulina
INTRODUÇÃO
A espécie vegetal Cissus sicyoides é conhecida popularmente como “insulina vegetal” dentre outros nomes regionais
menos populares, como cortina japonesa, cipó-jucá, anil trepador, uva-brava etc.1-3 Na medicina popular, Cissus sicyoides
é utilizada na forma de chá das folhas, principalmente no
tratamento do diabetes mellitus, embora existam inúmeras
outras indicações terapêuticas.2,4-6
A atividade hipoglicemiante de Cissus sicyoides pode ser
explicada pela presença de flavonoides na planta, dentre eles
a rutina. A administração oral de rutina a ratos com diabetes induzidas por estreptozotocina reduz significativamente
os níveis plasmáticos de glicose e hemoglobina glicosilada.7
Também o alcaloide multiflorina, isolado de plantas
I
Médico, mestre e doutor em Medicina Interna e Terapêutica e Medicina Baseada em Evidências da Universidade Federal de São Paulo – Escola Paulista
de Medicina (Unifesp-EPM). Médico pesquisador do Centro de Pesquisas em Revisões Sistemáticas do Centro Cochrane do Brasil e médico assistente da
Universidade Federal de São Paulo.
II
Médico, mestre e doutorando em Medicina Interna e Terapêutica e Medicina Baseada em Evidências da Universidade Federal de São Paulo – Escola
Paulista de Medicina (Unifesp-EPM). Pesquisador colaborador do Centro Cochrane do Brasil.
Editor responsável por esta seção:
Hernani Pinto de Lemos Júnior. Médico, mestre e doutor em Medicina Interna e Terapêutica e Medicina Baseada em Evidências da Universidade Federal de
São Paulo – Escola Paulista de Medicina (Unifesp-EPM). Médico pesquisador do Centro de Pesquisas em Revisões Sistemáticas do Centro Cochrane do Brasil
e médico assistente da Universidade Federal de São Paulo.
Endereço para correspondência:
Hernani Pinto de Lemos Júnior
Centro Cochrane do Brasil — Rua Pedro de Toledo, 740 — 3o andar — Vila Clementino — São Paulo (SP) — CEP 04023-900
Tel./Fax. (11) 5575-2970/5579-0469
E-mail: [email protected] — E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 13 de maio de 2014 — Última modificação: 13 de maio de 2014 — Aceite: 3 de junho de 2014
Diagn Tratamento. 2014;19(3):129-31.
129
Efetividade e segurança do vegetal Cissus sicyoides (“insulina vegetal”) como fitoterápico hipoglicemiante
leguminosas, exerce efeito hipoglicemiante. Derivados da
criptolepina, um membro da família dos alcaloides indoloquinolinas, possuem atividade hipoglicemiante.8
OBJETIVO
Verificar a efetividade e segurança do Cissus sicyoides como
fitoterápico hipoglicemiante.
MÉTODOS
Revisão sistematizada da literatura na biblioteca Cochrane,
na Lilacs, na Medline e na PubMed.
RESULTADOS
Um estudo9 utilizou 24 coelhos divididos em quatro grupos para testar a atividade hipoglicemiante do extrato hidroalcoólico das folhas de Cissus sicyoides. No grupo 1 foram
incluídos animais com diabetes não tratados, no grupo 2,
animais sem diabetes e, nos grupos 3 e 4, animais com diabetes tratados com doses de 4,5 mg/kg e 13,5 mg/kg respectivamente. O tratamento foi realizado num período de 28 dias.
De acordo com o grupo experimental, os animais receberam
as cápsulas todos os dias no mesmo horário. Após 30 minutos da administração do medicamento, foi fornecida a porção de 120 g de ração a cada animal. A avaliação da atividade
hipoglicemiante de Cissus sicyoides foi realizada por meio
das dosagens dos parâmetros bioquímicos e hematológicos
dos coelhos com diabetes induzida por aloxano. A glicemia
teve redução de 35% com a dose de 4,5 mg/kg e de 60% com
a dose de 13,5 mg/kg. Nenhuma das doses testadas alterou
os níveis plasmáticos de insulina.
Na Faculdade de Medicina de Juazeiro do Norte, estado
do Ceará, foi estudado10 o efeito hipoglicemiante do extrato
aquoso de folhas frescas do Cissus sicyoides, no modelo de diabetes induzida por aloxano em ratazanas. Além da glicemia,
os níveis das enzimas hepáticas foram também determinados.
Os resultados mostraram que o tratamento diário dos ratos
diabéticos durante sete dias (100 mg/kg e 200 mg/kg) reduziu
significativamente os níveis de glicose no sangue em 25% e
22% respectivamente, em comparação com os mesmos grupos antes do tratamento. As enzimas hepáticas, transaminases, não se alteraram após o tratamento.
Na Universidade Federal da Paraíba, um estudo11 objetivou realizar ensaio toxicológico pré-clínico inicial para
investigar a toxicidade do Cissus sicyoides em altas doses.
Foram utilizados grupos de camundongos machos (n = 10)
submetidos a doses de 5,0 g/kg, via oral, e dose de 2,0 g/kg
por via intraperitoneal, da fração aquosa das folhas de Cissus
130
Diagn Tratamento. 2014;19(3):129-31.
sicyoides. Foi retirado sangue por meio do plexo braquial
após sete dias, para análise laboratorial de parâmetros hematológicos e bioquímicos. No estudo anatomopatológico,
os animais foram examinados macro e microscopicamente,
com ressecção de pulmão, coração, fígado e rins. Na avaliação dos parâmetros hematológicos e bioquímicos, foram detectadas alterações nas enzimas hepáticas transaminases e
na fosfatase alcalina, caracterizando as alterações hepáticas
demonstradas no estudo histopatológico. Na avaliação histológica do fígado de camundongos, evidenciou-se hepatite
reacional com portite linfocitária crônica e lobular multifocal, hiperplasia kupferiana, colapsos focais da trama reticular, ausência de fibrose portal e lobular.
Também na Universidade Federal da Paraíba, um estudo12
objetivou realizar ensaios clínicos de fase II com a infusão das
folhas de Cissus sicyoides para investigar a eficácia terapêutica desse vegetal em voluntárias intolerantes à glicose (n = 14)
e diabéticas (n = 12) entre 30 e 59 anos de idade. O chá foi
preparado com 1 g do pó das folhas secas, diluído em 150 mL
de água quente por 10 minutos (uso popular), dose única, por
um período de sete dias. Nas intolerantes a glicose, o chá das
folhas teve atividade hipoglicemiante significativa aos 120 minutos, porém, não houve aumento da insulinemia, sugerindo
que esse efeito não ocorreu por liberação ou secreção da insulina. Nas diabéticas, o chá não apresentou efeito hipoglicemiante significativo.
Na Universidade Estadual de Maringá, Paraná, um
estudo13 avaliou o efeito dos extratos hidroalcoólicos obtidos
a partir de folhas de Cissus sicyoides sobre a tolerância à
glicose em ratos tratados com dexametasona. Os resultados
mostraram que o extrato de Cissus sicyoides aumenta o grau
de intolerância à glicose promovida pela dexametasona,
sugerindo efeito diabetogênico e não antidiabético como
acredita a população usuária dessa planta. Além disso,
dois flavonoides, obtidos a partir de partes aéreas de Cissus
sicyoides, foram utilizados para o estudo da incorporação de
glicose em glicogênio no músculo dos ratos. Os resultados
mostraram que os flavonoides não tiveram efeito sobre a
síntese de glicogênio. Assim, esses dados não revelaram
atividade antidiabética de Cissus sicyoides.
DISCUSSÃO
Existem inúmeros artigos sobre o vegetal Cissus sicyoides
descrevendo seus componentes e fazendo considerações
acerca de suas numerosas propriedades terapêuticas preconizadas popularmente. O foco deste artigo é o diabetes, já
que, no Brasil, essa planta é denominada, em grande parte
do país, como “insulina vegetal” e direcionanda para o tratamento do diabetes.
Hernani Pinto de Lemos Júnior | André Luis Alves de Lemos
O diabetes é uma doença que, na sua evolução, tem complicações fatais para o ser humano, com sérias consequências
vasculares em órgãos nobres do organismo. Por essa razão,
seu tratamento tem que ser monitorado pelo médico de maneira rigorosa, tanto no aspecto alimentar quanto no uso de
drogas. Isso pode ser difícil se o paciente usar infusão de vegetais cultivado no quintal ou comprado em feiras. A dose utilizada pode variar diariamente e a sua efetividade e segurança
podem não ter, ou ter baixa evidência científica. Não cabe, no
mundo científico atual, e com tantas drogas à disposição, utilizarmos meios duvidosos, mesmo que a médio/longo prazo,
para uma doença potencialmente destrutiva.
Como podemos evidenciar nos artigos aqui demonstrados,
somente um artigo incluiu humanos para avaliação do efeito
hipoglicêmico do vegetal e os resultados foram negativos.
Dois estudos em ratos demonstraram resultados divergentes,
um diminuiu a glicemia em 25% e o outro não encontrou diferença significativa. O estudo feito em coelhos mostrou
resultado surpreendente, com redução de 60% da glicemia.
A toxicidade hepática demonstrada minuciosamente em um
estudo torna-se preocupante se pensarmos na automedicação facilitada pela fácil aquisição do vegetal.
Um ponto comum em todos os estudos é a não modificação da insulinemia. Isso torna impróprio o nome popular de
insulina vegetal e também impossível sua ação como secretagogo nas ilhotas de Langerhans.
CONCLUSÃO
Não existem evidências científicas em humanos que indiquem a planta Cissus sicyoides, conhecida popularmente
como insulina vegetal, no tratamento do diabetes mellitus.
REFERÊNCIAS
1. Oliveira AB. Cissus verticillata (VITACEAE): Informações
etnofarmacológicas e anatomia dos órgãos vegetativos
[dissertação]. Viçosa: Universidade Federal de Viçosa; 2006.
2. Barbosa WLR, Santos WRA, Pinto LN, Tavares ICC. Flavonóides
de Cissus verticillata e a atividade hipoglicemiante do chá
de suas folhas. Rev Bras Farmacogn. 2002;12(supl 1):13-15.
3. Souza VC, Lorenzi H. Botânica sistemática: guia ilustrado
para identificação das famílias de Angiospermas da flora
brasileira, baseado em APG II. Nova Odessa: Instituto
Plantarum; 2005.
4. Garcia MD, Saenz MT, Puerta R, Quilez A, Fernandez MA.
Antibacterial activity of Agave intermixta and Cissus sicyoides.
Fitoterapia.1999;70(1):71-3.
Disponível
em:
http://www.
sciencedirect.com/science/article/pii/S0367326X98000094.
Acessado em 2014 (29 mai).
5. Lans CA. Ethnomedicines used in Trinidad and Tobago for
urinary problems and diabetes mellitus. J Ethnobiol Ethnomed.
2006;2:45.
6. de Paula Ferreira M, Nishijima CM, Seito LN, et al.
Gastroprotective effect of Cissus sicyoides (Vitaceae):
involvement of microcirculation, endogenous sulfhydryls and
nitric oxide. J Ethnopharmacol. 2008;117(1):170-4.
7. Kamalakkannan N, Prince PS. Antihyperglycaemic and
antioxidant effect of rutin, a polyphenolic flavonoid, in
streptozotocin-induced diabetic wistar rats. Basic Clin
Pharmacol Toxicol. 2006;98(1):97-103.
8. Negri G. Diabetes melito: plantas e princípios ativos naturais hipoglicemiantes [Diabetes mellitus: hypoglicemic plants and natural active principles]. RBCF Rev Bras Ciênc Farm (Impr). 2005;41(2):122-42.
9. Braga TV. Avaliação da atividade farmacológica de Cissus
verticillata Nicolson & C. E. Jarvis subsp verticillata como
antioxidante, antifúngico, hipoglicemiante e cicatrizante
[dissertação]. Ouro Preto: Universidade Federal de Ouro Preto;
2008. Disponível em: http://www.tede.ufop.br/tde_busca/
arquivo.php?codArquivo=299. Acessado em 2014 (29 mai).
10. Viana GS, Medeiros AC, Lacerda AM, et al. Hypoglycemic and
anti-lipemic effects of the aqueous extract from Cissus sicyoides.
BMC Pharmacol. 2004;4:9.
11. Vasconcelos THC, Modesto-Filho J, Diniz MFFM, et al. Estudo
toxicológico pré-clínico agudo com o extrato hidroalcoólico das
folhas de Cissus sicyoides L. (Vitaceae) [Acute pre-clinical toxicological study with the hydroalcoholic extract of the leaves of Cissus
sicyoides L. (Vitaceae)]. Rev Bras Farmacogn. 2007;17(4):583-91.
12. Santos HB, Modesto-Filho J, Diniz MFFM, et al. Avaliação do
efeito hipoglicemiante de Cissus sicyoides em estudos clínicos
fase II [Evaluation of the hypoglycemic effect of Cissus sicyoides
in phase II clinical trials]. Rev Bras Farmacogn. 2008;18(1):70-6.
13. Beltrame FL, Sartoretto JL, Bazotte RB, Cuman RN, Cortez
AG. Estudo fitoquímico e avaliação do potencial antidiabético
de Cissus sicyoides L. (VITACEAE) [Phytochemical study and
evaluation of the antidiabetic potential of Cissus sicyoides L.
(VITACEAE).]. Quím Nova. 2001;24(6):783-5.
Diagn Tratamento. 2014;19(3):129-31.
131
POEMS: PATIENTS-ORIENTED EVIDENCE THAT MATTERS
Sequência de testes pode melhorar
identificação do delirium em idosos
atendidos na emergência
Autores da tradução:
Pablo Gonzáles BlascoI, Marcelo Rozenfeld LevitesII, Cauê MonacoIII
Sociedade Brasileira de Medicina de Família
QUESTÃO CLÍNICA
Uma abordagem que consiste de triagem e confirmação é
útil para identificar com precisão o delirium em pacientes idosos que se apresentam em unidade de emergência?
DESENHO DO ESTUDO
Estudo de acurácia (coorte retrospectivo).
Nível de evidência: 1b.2
RESUMO
CASUÍSTICA
Um processo de duas etapas — uma triagem rápida (cerca de 20 segundos) seguida de uma segunda série de tarefas
e perguntas para os pacientes que tiverem teste inicial positivo — é uma forma eficaz para identificar ou descartar o delirium em pacientes idosos que se apresentam em serviço de
emergência. A combinação dos testes Delirium Triage Screen
e Brief Confusion Assessment Method é igualmente eficaz se
administrada tanto por médico quanto por profissionais de
outras formações e parece ser um acréscimo simples ao fluxo
de trabalho que pode aumentar a identificação desse estado
muitas vezes negligenciado.1
Pacientes idosos atendidos em pronto-socorro por emergências clínicas.
DISCUSSÃO
Os autores desse estudo recrutaram 406 pacientes de
65 anos ou mais de idade que compareceram a um serviço
de emergência. O padrão-ouro para o diagnóstico do delirium
foi a avaliação por um psiquiatra, então somente foram incluídos pacientes nos horários em que um desses especialistas
Médico de família, doutor em Medicina, diretor científico e membro-fundador da Sociedade Brasileira de Medicina de Família (Sobramfa).
Médico de família e diretor da Sociedade Brasileira de Medicina de Família (Sobramfa).
Médico de família, professor do curso de Medicina do Centro Universitário São Camilo, membro ativo da Sociedade Brasileira de Medicina de Família (Sobramfa).
I
II
III
Editores responsáveis por esta seção:
Pablo Gonzáles Blasco. Médico de família, doutor em Medicina, diretor científico e membro-fundador da Sociedade Brasileira de Medicina de Família (Sobramfa).
Marcelo Rozenfeld Levites. Médico de família e diretor da Sociedade Brasileira de Medicina de Família (Sobramfa).
Cauê Mônaco. Médico de família, membro ativo da Sociedade Brasileira de Medicina de Família (Sobramfa).
Tradução e adaptação:
Sobramfa (Sociedade Brasileira de Medicina de Família)
Rua Sílvia, 56 — Bela Vista — São Paulo (SP) — CEP 01331-000
Tel. (11) 3253-7251/3285-3126
E-mail: [email protected] — http://www.sobramfa.com.br
Data de entrada: 11 de junho de 2014 — Última modificação: 11 de junho de 2014 — Aceite: 23 de junho de 2014
132
Diagn Tratamento. 2014;19(3):132-3.
Pablo Gonzáles Blasco | Marcelo Rozenfeld Levites | Cauê Monaco
estava disponível. Foram excluídos os pacientes que tinham
demência, não falavam inglês, estavam não responsivos ou foram incapazes de seguir comandos simples. Para o rastreamento do delirium, os pesquisadores avaliaram os pacientes com
o uso da Delirium Triage Screen, que avalia uma possível alteração do nível de consciência (pela escala Richmond de agitação e sedação) e, estando o resultado normal, avalia a atenção
com a tentativa de soletrar a palavra “LUNCH” de trás para
frente. Os pacientes que não tiveram o delirium descartado
nessa etapa foram então avaliados segundo o Brief Confusion
Assessment Method, uma curta série de observações e perguntas que avaliam a alteração no estado mental, na atenção
e no pensamento. O delirium foi diagnosticado em 12,3% dos
pacientes por um psiquiatra que não tinha ciência dos resultados obtidos nos dois testes. O Delirium Triage Screen teve 98%
de sensibilidade (intervalo de confiança, IC de 95%: 89,5%99,5%), efetivamente excluindo os pacientes sem delirium.
O Brief Confusion Assessment Method subsequente teve
95,8% de especificidade (93,2%-97,4%) e foi eficaz na detecção
do delirium. Ambos os testes foram igualmente eficazes tanto
quando administrados por médicos quanto por outros profissionais com formações clínicas variadas.
COMENTÁRIO
O delirium é uma condição comum em serviços de
emergência. Ele é associado a prognósticos indesejáveis
(aumentos de tempo de internação, complicações clínicas,
reinternações e mortalidade), mas, com muita frequência,
não é identificado.
A estratégia descrita pelo POEM se apresenta como alternativa interessante para aumentar a segurança do paciente, mas, por enquanto, sua relevância se concentra
nas implicações para a pesquisa. Os testes Delirium Triage
Screen e Brief Confusion Assessment Method ainda não
foram traduzidos para o português e validados em populações brasileiras, de maneira que sua aplicabilidade clínica
fica limitada em nosso meio.
Até o momento, a Richmond Agitation-Sedation Scale é a
única das escalas mencionadas que já foi validada no Brasil.3
REFERÊNCIAS
1. Han JH, Wilson A, Vasilevskis EE, et al. Diagnosing delirium in
older emergency department patients: validity and reliability of
the delirium triage screen and the brief confusion assessment
method. Ann Emerg Med. 2013;62(5):457-65.
2. Centre for Evidence Based Medicine. Oxford Centre for
Evidence-based Medicine - Levels of Evidence (March 2009).
Disponível
em:
http://www.cebm.net/index.aspx?o=1025.
Acessado em 2014 (11 jun).
3. Nassar Junior AP, Pires Neto RC, de Figueiredo WB, Park M.
Validity, reliability and applicability of Portuguese versions of
sedation-agitation scales among critically ill patients. Sao Paulo
Med J. 2008;126(4):215-9.
RESPONSÁVEL PELA EDIÇÃO DESTA SEÇÃO: SOBRAMFA
Diagn Tratamento. 2014;19(3):132-3.
133
POEMS: PATIENTS-ORIENTED EVIDENCE THAT MATTERS
Purulência do escarro e proteína
C-reativa são preditores de mau
prognóstico na exacerbação da
doença pulmonar obstrutiva crônica
Autores da tradução:
Pablo Gonzáles BlascoI, Marcelo Rozenfeld LevitesII, Cauê MonacoIII
Sociedade Brasileira de Medicina de Família
QUESTÃO CLÍNICA
CASUÍSTICA
É possível identificar as exacerbações da doença pulmonar
obstrutiva crônica de leve a moderada que não exigem tratamento com antibióticos?
Adultos portadores de DPOC leve a moderada tratados por
exacerbação em contexto ambulatorial.
RESUMO
Entre os pacientes com exacerbação de doença pulmonar
obstrutiva crônica (DPOC) de leve a moderada, aqueles
com proteína C-reativa (PCR) em nível superior a 40 mg/L
e aqueles com escarro purulento estão em maior risco de
falha do tratamento sem antibióticos. Os pacientes sem essas
características têm menos probabilidade de se beneficiarem
de antibióticos e são candidatos a terapia sintomática com
acompanhamento estrito.1
DESENHO DO ESTUDO
Estudo prospectivo de coorte.
Nível de evidência: 1b.2
DISCUSSÃO
Um recente ensaio clínico aleatório controlado sobre a
amoxicilina com clavulanato comparou-a com placebo em
310 pacientes com exacerbação de DPOC leve a moderada.3
Nele, a falha clínica foi definida como resolução incompleta,
persistência ou agravamento dos sintomas nos dias 9 a 11
com necessidade de tratamento adicional, sendo que 19%
do grupo do placebo e 10% do grupo dos antibióticos foram
classificados como insucessos clínicos (número necessário
para tratar = 9). Nesse estudo,1 os autores analisaram apenas
a coorte daqueles que receberam placebo (n = 152), os quais
já tinham tido aumento da dispneia, do volume escarro
e/ou da purulência do escarro como critérios de inclusão
para o ensaio. Os pacientes com aumento da dispneia e/ou
volume de expectoração tiveram taxa de falhas de 5,6%, os
Médico de família, doutor em Medicina, diretor científico e membro-fundador da Sociedade Brasileira de Medicina de Família (Sobramfa).
Médico de família e diretor da Sociedade Brasileira de Medicina de Família (Sobramfa).
Médico de família, professor do curso de Medicina do Centro Universitário São Camilo, membro ativo da Sociedade Brasileira de Medicina de Família (Sobramfa).
I
II
III
Editores responsáveis por esta seção:
Pablo Gonzáles Blasco. Médico de família, doutor em Medicina, diretor científico e membro-fundador da Sociedade Brasileira de Medicina de Família (Sobramfa).
Marcelo Rozenfeld Levites. Médico de família e diretor da Sociedade Brasileira de Medicina de Família (Sobramfa).
Cauê Mônaco. Médico de família, membro ativo da Sociedade Brasileira de Medicina de Família (Sobramfa).
Tradução e adaptação:
Sobramfa (Sociedade Brasileira de Medicina de Família)
Rua Sílvia, 56 — Bela Vista — São Paulo (SP) — CEP 01331-000
Tel. (11) 3253-7251/3285-3126
E-mail: [email protected] — http://www.sobramfa.com.br
Data de entrada: 26 de maio de 2014 — Última modificação: 26 de maio de 2014 — Aceite: 9 de junho de 2014
134
Diagn Tratamento. 2014;19(3):134-5.
Pablo Gonzáles Blasco | Marcelo Rozenfeld Levites | Cauê Monaco
que tiveram somente purulência da expectoração ou purulência associada a aumento da dispneia ou volume da expectoração tiveram taxa de falha de 20,3%, e aqueles com todos
os três sintomas tiveram taxa de fracasso de 33%. Os pacientes com níveis de PCR de menos de 40 mg/L tiveram taxa de
insucesso de 12,4%, em comparação com taxa de insucesso
de 65% para aqueles com níveis de PCR de 40 mg/L ou mais.
A análise multivariada revelou que níveis de PCR iguais ou
superiores a 40 mg/L (odds ratio [OR] = 13,4, intervalo de
confiança, IC de 95%, 4,6-39) e aumento da purulência do
escarro (OR = 6,1, IC de 95% 1,5-25) foram preditores independentes de falha do tratamento.
REFERÊNCIAS
1. Miravitlles M, Moragas A, Hernández S, Bayona C, Llor C. Is it
possible to identify exacerbations of mild to moderate COPD that
do not require antibiotic treatment? Chest. 2013;144(5):1571-7.
2. Centre for Evidence Based Medicine. Oxford Centre for
Evidence-based Medicine - Levels of Evidence (March 2009).
Disponível
em:
http://www.cebm.net/index.aspx?o=1025.
Acessado em 2014 (30 mai).
3. Llor C, Moragas A, Hernández S, Bayona C, Miravitlles M.
Efficacy of antibiotic therapy for acute exacerbations of mild to
moderate chronic obstructive pulmonary disease. Am J Respir
Crit Care Med. 2012;186(8):716-23.
Responsável pela edição desta seção: sobramfa
Diagn Tratamento. 2014;19(3):134-5.
135
LINGUAGENS
Lógicas
Alfredo José MansurI
Unidade Clínica de Ambulatório do Instituto do Coração do Hospital das Clínicas
da Faculdade de Medicina da Universidade de São Paulo
Lógica, segundo os dicionários1,2 é a parte do conhecimento
que trata das formas de pensamento em geral (dedução, indução, hipótese, inferência etc.) e das operações intelectuais que
visam à determinação do que é verdadeiro ou não. Uma das
derivações por extensão do sentido apontadas no dicionário,
entre outras, é a maneira por que necessariamente se encadeiam os acontecimentos, as coisas ou os elementos de natureza efetiva.1 O encadear cotidiano de acontecimentos, coisas
ou elementos segundo regras3 é também feito por pacientes,
médicos e profissionais de saúde e aspira a um caráter lógico.
Vivemos atualmente na era da medicina científica e tecnológica, que pode contribuir para a melhor qualidade de vida,
ressalvadas dificuldades de acesso em muitas circunstâncias.
Tal potencialidade cria expectativas, inclusive quanto a sua
lógica. Pacientes (ou meios laicos) em geral, muitas vezes,
estimulados pela propaganda, podem assumir implícito que
todos os fundamentos da medicina e da prática clínica se
assentam sobre bases científicas e lógicas solidamente assentadas, dentro dos humanos e óbvios limites, e que os profissionais da saúde em geral, e os médicos em particular, detenham
conhecimentos que permitam se situar com clareza a respeito
dos mais variados temas, por vezes até extra-médicos, às vezes
restando escasso espaço mental aos hiatos do conhecimento.
Talvez pela sua própria extensão e alcance, a lógica é
invocada, apropriadamente ou não, e exposta a apreciações pelos diferentes autores de proposições, entre eles os
pacientes, os médicos e outros profissionais de saúde de
modo geral. Essas apreciações estão voltadas para o exame
de fatos da prática clínica ou de áreas de interface. Surgem,
ocasionalmente, comentários e perguntas intelectualmente estimulantes, trazidos por pacientes e familiares, que
constituem parte da riqueza e dos desafios da prática médica. Seguem algumas delas.
Lógica de assuntos gerais:
a)café – uma das perguntas bem-humoradas desencadeadoras destas reflexões foi sobre o café – “Não compreendo
a lógica do que dizem os médicos sobre o café, deveriam
chegar a um acordo. Passaram tanto tempo a afirmar que
era prejudicial à saúde, e agora estão a dizer que é benéfico
para a saúde!”.
Nuances desse conhecimento podem escapar à lógica do
sim e do não, como tantas outras questões dentro da medicina em geral, e da prática clínica em particular, às vezes
até para irritação dos seus protagonistas. Publicações recentes aprofundaram o exame tais nuances.4-6 A natureza
dos estudos (efeito agudo, efeito no longo prazo), as diferentes substâncias químicas envolvidas, padrão da relação entre variáveis de estudo (curva em J), estudos ora sugerindo
efeito maléfico, outros sugerindo efeito benéfico, variáveis
de confusão, diferença entre associação e causalidade,5 associações inversas não lineares6 nem sempre são conceitos
rapidamente assimiláveis no curto tempo da prática, de tal
forma que podem ser percebidos como inconsistência lógica ou pelo menos, lógica que não foi explicada.
I
Livre-docente em Cardiologia pela Faculdade de Medicina da Universidade de São Paulo. Diretor da Unidade Clínica de Ambulatório do Instituto do
Coração do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo.
Endereço para correspondência:
Alfredo José Mansur
Unidade Clínica de Ambulatório do Instituto do Coração do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
Avenida Dr. Enéas de Carvalho Aguiar, 44 — São Paulo (SP) — CEP 05403-000
Tel. InCor (11) 2661-5237 — Consultório: (11) 3289-7020/3289-6889
E-mail: [email protected]
Fontes de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 12 de maio de 2014 — Última modificação: 12 de maio de 2014 — Aceite: 21 de maio de 2014
136
Diagn Tratamento. 2014;19(3):136-8.
Alfredo José Mansur
b) dieta – estatinas são recomendadas para o tratamento
de hipercolesterolemia, em geral como complemento de
adequação dietética. Estudo recente demonstrou maior
ingestão de calorias e de gorduras nos pacientes em uso
de estatinas em relação aos pacientes que não faziam uso
de estatinas.7 Uma interpretação plausível, e que talvez já
tenha sido ouvida, é que o uso dos fármacos franquearia
dieta mais liberal ou menos seletiva. Seria uma lógica que
poderíamos chamar de conveniência, não terapêutica,
livre e não profissional. Talvez não sejam mesmo novas
categorias de lógica.
c) gorduras – a redução de ingestão de gorduras saturadas
tem sido recomendada há décadas e orientou a lógica
das diretrizes de alimentação e aconselhamento de pacientes, quase como um mantra.8 Recentemente, foi publicada
uma interpretação diferente (ainda que lógica) sobre os dados a respeito do consumo de gorduras saturadas — a cultura de evitar o consumo de gorduras saturadas se associou
com o aumento da prevalência de obesidade e de diabetes
melito. Sugeriu o autor da tese que, em razão dos alimentos
se tornarem menos palatáveis pela ausência ou carência de
gorduras saturadas, há mais oferta ou maior ingestão de alimentos ricos em calorias e hidratos de carbono; o real vilão
alimentar seria o açúcar e não a gordura saturada.8 Curioso
justapor essa curiosa lógica com histórias de nosso meio,
que contam de avós nonagenários que se alimentaram de
gordura saturada preservada em grandes recipientes, e
contrapõe esse empirismo não científico e de livre lógica
em oposição a orientações terapêuticas vigentes.
Lógica da prevenção – é dos fundamentos da medicina
que é quase sempre melhor prevenir doenças do que remediá-las. A prevenção de doenças pode ser feita por meio de
cuidados de higiene, dietéticos, hábitos, condições de vida,
de exposições a serem evitadas e de vacinações, entre outros
métodos ou intervenções.
Às vezes, com o objetivo de prevenção, realiza-se o exame
clínico e exames complementares, alguns deles de tecnologia
recente e cara. Uma inferência supostamente “lógica” poderia
ser “fazer todos os exames”. Atualmente há algumas iniciativas que não referendam o desenvolvimento dessa lógica em livros de texto (Doppler de carótidas para todos?),9 publicações
(tomografia de corpo inteiro?)10 ou mesmo em instituições
com sites disponíveis na internet.11
Outras vezes a prevenção avança até a prescrição de uso diário de medicamentos, como exemplo a aspirina e vitaminas,
entre outros. O U.S. Food and Drug Administration (6 de maio
de 2014)12 reavaliou os dados disponíveis e concluiu não haver
evidência para recomendar o seu uso para prevenção primária de infarto do miocárdio e de acidente vascular cerebral.
Advertiu ainda para o maior risco de sangramento digestivo
e cerebral pelo seu uso quando não formalmente indicado.
Suplementação de vitaminas também não foi recomendada.9
Fazem parte da lógica do screening consequências não planejadas nem previstas e efeitos adversos;13 portanto screening nem
sempre é protetor. Médica experiente e professora de Medicina
lembrou que o termo profilaxia em geral é visto como algo bom,
qualificativo nem sempre verdadeiro.
Lógica científica – vivemos momento histórico no qual
a busca do conhecimento é importante motor social e econômico. Uma das dimensões atuais do conhecimento cientificamente fundamentado é a mudança de paradigmas como
resultados de novas pesquisas e novas descobertas; essas
mudanças podem ser rápidas e tal rapidez já foi qualificada
como vertiginosa. Um exemplo corriqueiro pode ser obtido
no avanço dos equipamentos eletrônicos e de comunicação,
em geral de muito sucesso e que provoca filas para aquisição
em Nova Iorque.
Ainda que não tão visível, o aprimoramento da ciência
médica, com dados obtidos em novos estudos, e as novas
descobertas modificam ou ampliam conceitos, definições,
cuidados, tratamento e prognóstico. De fato, já ensinou
grande pensador que são poucas ciências que podem chegar
a um estado permanente.3 A natureza veloz da ciência contemporânea nessas mudanças faz com que essa realidade
possa ser vivenciada por muitas pessoas no decorrer da própria existência. Assim, diagnósticos, tratamentos, técnicas e
operações que foram consideradas salvadoras há uma, duas
ou três décadas, hoje são entendidas como uma das opções
terapêuticas, não necessariamente a única e não necessariamente a melhor entre as opções hoje existentes. O resultado
de algumas terapêuticas, no início considerado superiores,
no longo prazo não logrou a superioridade esperada ou os
efeitos colaterais não se resolveram.
Tal velocidade permite que pacientes vivenciem na prática
essas mudanças, e discutam a lógica da Medicina científica,
exprimindo, poucos anos depois do tratamento, reflexões do
tipo “se fosse hoje, talvez minha operação não fosse necessária”. Nesse contexto, a rapidez da evolução do conhecimento
passa a ser percebida como uma instabilidade lógica do fundamento de algumas decisões de tratamento, particularmente as que provocam mudanças irreversíveis. Há quem recorra
até ao modismo, no sentido de tendência predominante que
todos devem seguir sob pena de serem considerados fora de
moda — “naquele tempo, a moda era essa, isso que se usava”.
Felizmente, para superar essa aparente instabilidade, há o
recurso da competente, dedicada, boa e perene clínica, que,
na prática, um dia foi até qualificada de soberana; modernamente ela dá conta com galhardia, ainda que muitas vezes
com prudência e modéstia, de compor o complexo conjunto
Diagn Tratamento. 2014;19(3):136-8.
137
Lógicas
de dados científicos disponíveis, analisá-los sob sua luz, para
que decisões diagnósticas e terapêuticas possam ser tomadas de modo apropriado para melhor servir ao paciente.
Lógica da comunicação de massa – os fatos relacionados à saúde divulgados pelos meios de comunicação de massa, particularmente a televisão, tem entre as características de
sua linguagem poderosa, a informação editada com muita rapidez, genérica, curta e parcial, isto é, superficial, de tal modo
que pode criar demanda nos espectadores mais sensíveis. Não
raro, os hiatos de conhecimentos surgem no noticiário com
acepção retrospectiva, depois que uma descoberta (ou pretensa descoberta) de grande apelo de audiência foi divulgada.
Só o resultado é passível de notoriedade e notícia, o processo
nem sempre o é. É evidente que há diferença entre divulgação
educativa, planejada e orientada e a divulgação de notícias
que ocupam espaço entre os intervalos de publicidade.
Uma inconsistência apontada nessa lógica é a veiculação de
recomendações de acesso ao sistema de saúde (por exemplo,
consultas, exames, tratamentos) que o sistema público não
consegue acolher. Cria-se uma curiosa inconsistência lógica.
Lógica da necessidade, da esperança ou da expectativa – por diferentes razões, seja necessidade, esperança
ou expectativa, pessoas sob ameaça de doenças ou doentes
podem tecer arcabouço lógico de garantias que podem nem
sempre ter guarida na dimensão do real. Nessa lógica das expectativas, podem ser associados fatos ainda não ocorridos,
mas apenas desejados, relacionados com médicos, com profissionais de saúde, com serviços ou com instituições, criando uma demanda que pode não ser atendida, ou por meio
dessa lógica, fazendo interpretações no sentido positivo ou
no sentido negativo.
Mistura – uma questão hipotética pode ser formulada sobre os objetivos e as consequências advindas quando lógicas se
mesclam — lógica híbrida, linear, fuzzy, livre, de justificação, de
ação, modal, deôntica, temporal, epistemológica, informal, paraconsistente, da intuição, antiga, dialógica, intensional, combinatória, indutiva, clássica, condicional.14 O mesmo exercício
pode ser proposto na área médica e de profissionais da saúde
ao se permear lógica geral, lógica clínica, lógica científica, lógica econômica, lógica do marketing, do poder etc.
Vastos são os domínios da lógica, das suas interfaces, da
sua aplicação e das suas consequências;14 vastíssimos são
os domínios da lógica no que diz respeito à prática clínica — vasto mundo. Irresistível parafrasear o famoso verso
drummondiano: “Mundo, mundo, vasto mundo, mais vasta
é a prática clínica”.
Concluímos, lembrando que a experiência de outros colegas pode enriquecer as reflexões ora apresentadas.
REFERÊNCIAS
1. Houaiss A, Villar MS. Dicionário Houaiss da Língua Portuguesa.
Rio de Janeiro: Objetiva; 2001.
2. Lalande A. Vocabulaire technique et critique de la philosophie.
Paris: Presses Universitaires de Fraqnce; 1926.
3. Kant I. Manual dos cursos de Lógica Geral. Trad. Castilho F. 2a
ed. Campinas: Editora da Unicamp; 2002.
4. Ludwig IA, Clifford MN, Lean ME, Ashihara H, Crozier A. Coffee:
biochemistry and potential impact on health. Food Funct. 2014.
[Epub ahead of print].
5. Je Y, Giovannucci E. Coffee consumption and total mortality: a
meta-analysis of twenty prospective cohort studies. Br J Nutr.
2014;111(7):1162-73.
6. Ding M, Bhupathiraju SN, Satija A, van Dam RM, Hu FB.
Long-term coffee consumption and risk of cardiovascular disease: a systematic review and a dose-response
meta-analysis of prospective cohort studies. Circulation.
2014;129(6):643-59.
7. Sugiyama T, Tsugawa Y, Tseng CH, Kobayashi Y, Shapiro MF. Different Time Trends of Caloric and Fat Intake Between Statin
Users and Nonusers Among US Adults: Gluttony in the Time of
Statins? JAMA Intern Med. 2014;174(7):1038-45.
138
Diagn Tratamento. 2014;19(3):136-8.
8. Malhotra A. Saturated fat is not the major issue. BMJ.
2013;347:f6340.
9. Atkins D, Barton M. The periodic health examination. In: Goldman L, Schafer AI, eds. Goldman Cecil Medicine. 24th ed. Philadelphia: Elsevier Saunders, 2012. p. 52-6.
10. Furtado CD, Aguirre DA, Sirlin CB, et al. Whole-body CT screening: spectrum of findings and recommendations in 1192 patients. Radiology. 2005;237(2):385-94.
11. Choosing wisely. An initiative of the ABIM Foundation. Advancing
Medical Professionalism to Improve Health Care. Disponível em:
http://www.choosingwisely.org/. Acessado em 2014 (13 mai).
12. U.S. Food and Drug Administration. Use of Aspirin for Primary
Prevention of Heart Attack and Stroke. Disponível em: http://
www.fda.gov/drugs/resourcesforyou/consumers/ucm390574.
htm. Acessado em 2014 (13 mai).
13. Sharma S, Estes NA 3rd, Vetter VL, Corrado D. Clinical decisions. Cardiac screening before participation in sports. N Engl J
Med. 2013;369(21):2049-53.
14. Logic. Stanford encyclopedia of phylosophy. Disponível em:
http://plato.stanford.edu/search/searcher.py?query=logic.
Acessado em 2014 (13 mai).
RESIDÊNCIA E ENSINO MÉDICO
A vocação médica e a academia
Ricardo AunI
Hospital das Cínicas da Faculdade de Medicina da Universidade de São Paulo
A medicina é uma profissão difícil. Na base desta profissão,
está a abnegação de muitos médicos, jovens e não tão jovens,
que dedicam seus dias a tratar da alma e da saúde de seus pacientes, conhecem as famílias, já trataram gerações. Exercem
a profissão com abnegação e sacrificam- se, e a seus familiares,
com longas ausências. Outros, apesar de elevado conhecimento tecnológico, provindo do aprendizado de suas especialidades, não abandonam
o aspecto humano da profissão, têm formação cultural e humanista bem formadas para tratar seus pacientes. Alguns médicos, como em todas as atividades, visam o lucro, o que não é
pecado em minha opinião, desde que respeitado o bom senso,
se bem que o que se amealha na nossa atividade é o fruto do
trabalho diário, constante e diuturno.
O maior defeito dos médicos em sua PROFISSÃO é a vaidade, é se achar acima da vida e da morte, é julgar que seu procedimento é mais importante que o resultado e seus pacientes
(coitados destes). É a busca frenética da fama, é a BUSCA DE
TÍTULOS PELOS TÍTULOS. É o SELF, a falta de respeito e o
uso de colegas para atingir seu objetivo, que é ter um nome
estrelar e vangloriar-se do conseguido.
Vocês viram que tratei a medicina como profissão, que é
o que ela realmente é. Ciência é a biologia, a farmacologia,
os ramos mais básicos do conhecimento necessário para
ser médico, tratar aqueles que precisam de nós. Neste sentido, a Coordenação de Aperfeiçoamento de Pessoal de Nível
I
Superior (Capes) e o Conselho Nacional de Desenvolvimento
Científico e Tecnológico (CNPq) distorcem a visão do médico, que é tratar, confortar, ao invés da busca desenfreada de
publicações, às vezes até artigos que ganhariam o “framboesa
de ouro” da medicina. Publicações de casos anedóticos, que
se tornam verdades absolutas, e principalmente publicar por
interesses econômicos, quase sempre de forma implícita em
seus artigos, outras vezes, explícita mesmo. Este é o maior
viés de nossa profissão (PROFISSÃO). Como sou mais velho,
permito-me comentários para vocês pensarem a respeito:
1. Muitas das revistas norte-americanas são movidas a patrocínio.
2. Quando você tiver um tema que realmente seja de interesse, publique em revista de maior abrangência, que seus
colegas irão ler.
3. Esteja aberto às críticas.
4. A maior contribuição da medicina moderna foi dada por um autor de apenas
dois trabalhos (sobre penicilina).
5. Queira ser o médico que
satisfaz seus doentes, e não outros interesses (os pessoais).
6. Assuma a responsabilidade pelo que disser, pelo que prescrever, pelo que indicar e pelo que fizer, evite o “mas”...
7. Não
sou exemplo para ninguém, escrevo este texto com o coração
aberto, sem almejar mais nada em minha carreira, a não ser o
que manda Hipócrates, que é ensinar e tratar.
8. Muito cuidado com armadilhas, dos planos de saúde, dos hospitais, dos
fornecedores, de médicos inescrupulosos.
9. Finalmente, você
um dia vai parar, mas se for um exemplo para os que lhe seguem seu nome não morrerá.
Professor associado de Cirurgia Vascular da Faculdade de Medicina da Universidade de São Paulo.
Editor responsável por essa seção:
Olavo Pires de Camargo. Professor titular e chefe do Departamento de Ortopedia e Traumatologia da Faculdade de Medicina da Universidade de São Paulo (FMUSP).
Endereço para correspondência:
Olavo Pires de Camargo
Avenida Albert Einstein 627 sala 422
Tel. (11) 2151-3109
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Data de entrada: 28 de maio de 2014 — Última modificação: 28 de maio de 2014 — Aceite: 9 de junho de 2014
Diagn Tratamento. 2014;19(3):139-40.
139
A vocação médica e a academia
Este texto não é ao acaso. Hoje vivi uma situação, paralela ao exercício da medicina, envolvendo colegas que
têm como objetivo a promoção e não o ensino, que almejam índice H altíssimo, mas que mal se portam na frente
de um paciente ou de uma situação conflituosa. Colocar
no texto o que penso a respeito é a melhor forma de ficar
mais calmo.
140
Diagn Tratamento. 2014;19(3):139-40.
Não se esqueçam, fiem-se em exemplos sérios, vocês sabem
muito bem distinguir o joio do trigo. Confiem na sua intuição.
Completando: pesquisa médica vem da busca de uma resposta a uma dúvida que você tenha, aí você pesquisa e publica.
Desta dúvida virão outras e mais outras. Que você publicará.
E assim é. Não sejam como colegas que replicam trabalhos e
até caem no ridículo, pois nem sabem o que falam e escrevem.
ELETROCARDIOGRAMA
Fibrilação atrial na síndrome de
Wolff-Parkinson-White
Antonio Américo FriedmannI
Clínica Geral do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo
(Professor Milton de Arruda Martins)
Um paciente de 54 anos de idade foi atendido no
pronto-socorro com quadro de taquicardia de início súbito
e intensa dispneia. Contou que já estava acostumado com
taquicardias, que cessavam espontaneamente após alguns
instantes, mas desta vez foi diferente, muito mais forte e persistente. Ao exame físico exibia palidez, frequência cardíaca
maior que 200 bpm, frequência respiratória de 40/min e pressão arterial 90 mmHg x 60 mmHg. Na ausculta cardíaca, além
da taquicardia, o ritmo estava muito irregular.
O eletrocardiograma realizado prontamente (Figura 1)
mostrou taquicardia de QRS alargado, ausência de onda P
e ritmo irregular. À primeira vista, com tanta aberrância do
QRS, parecia taquicardia ventricular, porém a irregularidade
do ritmo sugeria fibrilação atrial. Havia trechos do eletrocardiograma em que a frequência cardíaca atingia 300 bpm.
E como explicar o complexo QRS estreito, de condução intraventricular aparentemente normal, na metade inicial (11o batimento) do traçado?
A piora das condições hemodinâmicas do paciente interrompeu a discussão diagnóstica e os assistentes decidiram
pela cardioversão elétrica.
O procedimento foi eficaz e o eletrocardiograma registrado em seguida (Figura 2) evidenciou reversão ao ritmo
sinusal com frequência cardíaca de 56 bpm. O intervalo PR
curto (0,11 s) e a presença de pequena onda delta, alargando
a porção inicial do QRS, indicavam pré-excitação ventricular.
A alteração mais marcante estava na repolarização ventricular: infradesnivelamento difuso e acentuado do segmento ST,
I
atingindo amplitudes maiores que 5 mm em algumas derivações precordiais.
Após algumas horas, o eletrocardiograma foi repetido e as
alterações da repolarização ventricular haviam regredido.
O paciente foi encaminhado ao ambulatório de arritmias cardíacas com diagnóstico de síndrome de
Wolff-Parkinson-White.
DISCUSSÃO
A síndrome de Wolff-Parkinson-White resulta de uma via
acessória de condução que conecta os átrios diretamente aos
ventrículos, paralelamente ao nó atrioventricular e ao feixe
de His. Tal via acessória é constituída por qualquer ponto do
sulco atrioventricular que tenha permeabilidade elétrica, não
apresentando, necessariamente, expressividade anatômica.
Daí a frequente ocorrência da síndrome em indivíduos hígidos
com coração estruturalmente normal. Em ritmo sinusal,
pode ser suspeitada por alterações do eletrocardiograma
(intervalo PR curto e QRS alargado por onda delta)
consequentes à despolarização precoce da área adjacente à
via acessória, fenômeno este denominado de pré-excitação.
A presença da via acessória constitui o substrato para a
ocorrência do fenômeno de reentrada.1
Assim, os portadores da síndrome são propensos a taquicardias paroxísticas por mecanismo de reentrada. Em 90%
dos casos de taquicardia, o estímulo elétrico despolariza os
ventrículos por meio das vias normais de condução e retorna
Professor livre-docente pela Faculdade de Medicina da Universidade de São Paulo.
Endereço para correspondência:
Clínica Geral do Hospital das Clínicas da Faculdade de Medicina da Universidade de São Paulo (Professor Milton de Arruda Martins) — Prédio dos
Ambulatórios
Avenida Dr. Enéas de Carvalho Aguiar, 155 — São Paulo (SP) — CEP 05403-000
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 5 de maio de 2014 — Última modificação: 22 de maio de 2014 — Aceite: 2 de junho de 2014
Diagn Tratamento. 2014;19(3):141-3.
141
Fibrilação atrial na síndrome de Wolff-Parkinson-White
D1
aVR
V1
V4
D2
aVL
V2
V5
D3
aVF
V3
V6
Figura 1. Taquicardia com QRS alargado e ritmo irregular, com frequência cardíaca muito elevada, próxima de 300 bpm.
A aberrância do QRS simula taquicardia ventricular, mas a irregularidade do ritmo sugere fibrilação atrial. O primeiro complexo em
aVR, aVL e aVF (11o batimento do traçado) é um QRS estreito, com duração e orientação normais.
D1
aVR
V1
V4
D2
aVL
V2
V5
D3
aVF
V3
V6
Figura 2. Eletrocardiograma após cardioversão elétrica, realizado cinco minutos após o anterior. Retorno ao ritmo sinusal com
frequência cardíaca de 65 bpm e sinais de pré-excitação (PR curto e onda delta). Verifica-se infradesnivelamento do segmento ST
acentuado e difuso, na maioria das derivações.
aos átrios pela via acessória (reentrada ortodrômica). Durante
a taquicardia, o QRS é normal (estreito) enquanto que, paradoxalmente, em ritmo sinusal, o ORS é aberrante devido à
pré-excitação. Em menor porcentagem das taquicardias, a
142
Diagn Tratamento. 2014;19(3):141-3.
reentrada é antidrômica. Neste caso, o impulso elétrico despolariza os ventrículos a partir da via acessória, causando
aberrância de condução praticamente indistinguível da taquicardia ventricular.2
Antonio Américo Friedmann
A fibrilação atrial nos pacientes com Wolff-ParkinsonWhite é mais rara que as taquicardias por reentrada, mas
é mais frequente que na população em geral porque a reentrada atrioventricular pode degenerar em fibrilação atrial.
Durante a fibrilação atrial, os impulsos elétricos dos átrios
descem para os ventrículos preferencialmente pela via acessória. Como esta não possui a propriedade de diminuir a
velocidade de condução, que é característica das células do
nó atrioventricular, a frequência ventricular durante a fibrilação atrial é muito alta, causando importante repercussão
hemodinâmica, e pode levar a fibrilação ventricular e morte
súbita cardíaca. Os complexos QRS são muito aberrantes
porque os ventrículos são despolarizados a partir da via
acessória, mas ocasionalmente verificam-se QRS estreitos,
quando o estímulo passa pelo sistema normal de condução.
Pode ocorrer também passagem do estímulo simultaneamente pelas duas vias ( fenômeno de fusão) causando
batimentos com morfologia intermediária. No eletrocardiograma, a fibrilação atrial difere fundamentalmente da
taquicardia por reentrada antidrômica porque, nesta última
o ritmo é sempre regular.3
Mais rara ainda é a ocorrência de flutter atrial em portadores de Wolff-Parkinson-White, o que também determina
frequências ventriculares elevadas.
O eletrocardiograma em ritmo sinusal, após a reversão da
fibrilação atrial, mostrou profundas alterações da repolarização ventricular. As alterações do segmento ST (elevação ou
depressão) ocorrem com maior frequência na doença arterial
coro­nária. Entretanto, alterações dinâmicas do segmento ST
não são específicas de insuficiência coronária aguda e podem
ocorrer em várias outras condições. No caso apresentado,
a depressão do segmento ST, sugestiva de lesão subendocárdica, pode ser decorrência do sofrimento do miocárdio
consequente à acentuada taquicardia e hipotensão arterial.
É interessante observar que, no eletrocardiograma durante
a taquiarritmia, o 11o batimento exibiu o mesmo infradesnível em D2, que persistiu no eletrocardiograma logo após a
cardioversão.
O tratamento da fibrilação atrial no paciente com a síndrome de Wolff-Parkinson-White apresenta peculiaridades.
Medicamentos que aumentam o período refratário do nó
atrioventricular, como adenosina, verapamil, betabloqueador e digital, são contraindicados, porque favorecem a condução preferencial pela via acessória, aumentando ainda
mais a frequência cardíaca, e o risco de fibrilação ventricular.
A cardioversão elétrica imediata é o tratamento de escolha.
O tratamento definitivo pode ser obtido pela ablação da via
acessória por radiofrequência.4
CONCLUSÃO
O reconhecimento da fibrilação atrial no portador da síndrome de Wolff-Parkinson-White é de grande importância
para o clínico que atende emergências, devido à gravidade
dessa taquiarritmia e às características do seu tratamento.
Iatrogenia pode ser fatal.
REFERÊNCIAS
1. Friedmann AA, Fonseca AJ. Vias acessórias. In: Friedmann
AA, editor. Eletrocardiograma em 7 aulas: temas avançados e outros métodos. São Paulo: Editora Manole; 2010.
p. 207-12.
2. Friedmann AA, Grindler J. Taquiarritmias. In: Friedmann AA,
editor. Eletrocardiograma em 7 aulas: temas avançados e outros
métodos. São Paulo: Editora Manole; 2010. p. 57-80.
3. Friedmann AA, Nishizawa WAT, Grindler J, Oliveira CAR. Taquicardias com QRS largo. In: Friedmann AA, Grindler J, Oliveira
CAR, Fonseca AJ, editores. Diagnóstico diferencial no eletrocardiograma. 2a ed. São Paulo: Editora Manole; 2011. p. 219-35.
4. Diretriz de Fibrilação Atrial. Arq Bras Cardiol. 2003;81(suplemento VI):1-24. Disponível em: http://publicacoes.cardiol.br/
consenso/2003/site/052.pdf. Acessado em 2014 (12 mai).
Diagn Tratamento. 2014;19(3):141-3.
143
MEDICINA SEXUAL
Desejo sexual em mulheres jovens
em relacionamentos estáveis
Heloisa Junqueira FleuryI, Mirian Bernardes Lopes AlvesII, Carmita Helena Najjar AbdoIII
Programa de Estudos em Sexualidade (ProSex) do Instituto de Psiquiatria do Hospital das Clínicas da Faculdade de
Medicina da Universidade de São Paulo
Resumo
Uma das principais dificuldades sexuais femininas é a falta de interesse/desejo sexual. Entre os fatores de risco, destacam-se o tempo de
duração do relacionamento, a pouca satisfação no relacionamento afetivo, menor valorização da vida sexual, condições médicas e respectivos tratamentos. Embora a diminuição do desejo atinja todas as faixas etárias, mulheres jovens apresentam maior desconforto com essa
condição. As particularidades da função sexual feminina foram reconhecidas em modelo em que o desejo por intimidade, ao invés de um
impulso biológico, é considerado o deflagrador da resposta sexual. Esse modelo se caracteriza como circular, no qual elementos emocionais
e físicos favorecem a disponibilidade da mulher para a experiência sexual. Em mulheres jovens, falta de desejo e sofrimento sexual estão
correlacionados. Apesar das dificuldades sexuais se agravarem com a idade, o sofrimento sexual (pessoal e relacional) parece diminuir.
A duração do relacionamento está negativamente associada com a frequência de iniciativa sexual e com a satisfação da mulher e do parceiro. A manutenção do desejo é mais provável para os casais que buscam ativamente novas e positivas experiências (lazer, desenvolvimento
pessoal). Algumas mulheres atribuem o declínio do desejo sexual à institucionalização do casamento, à familiaridade excessiva com o parceiro e à dessexualização do papel de esposa, mãe e profissional. Mulheres com baixo desejo relatam incômodo, principalmente porque
percebem que esse decréscimo afeta o parceiro. Aspectos fisiológicos, emocionais, ambientais, comportamentais, socioculturais e, principalmente, os relacionais comprometem a experiência do desejo sexual na mulher jovem em relacionamentos estáveis.
PALAVRAS-CHAVE: Libido, saúde sexual, relacionamento conjugal, sexualidade, disfunções sexuais psicogênicas
INTRODUÇÃO
Dificuldades sexuais são comuns na população feminina,
sendo uma das principais a falta de interesse/desejo sexual.1
Enquanto para alguns autores a prevalência é de 33% a 43%,1,2
para outros é de 10%,2 demonstrando que a queixa varia em
diferentes populações. No Brasil, por faixa etária, é de 5,8%
entre 18 e 25 anos; 5,8% entre 26 e 40 anos; 8,6% entre 41 e
50 anos; 15,2% entre 51 e 60 anos e 19,9% acima dos 60 anos.3
A quinta edição do Manual Diagnóstico e Estatístico de
Transtornos Mentais (DSM-5)4 define as disfunções sexuais
como um grupo heterogêneo de distúrbios que provoca alteração clinicamente significante na habilidade do indivíduo
Psicóloga, mestre em Ciências pela Faculdade de Medicina da Universidade de São Paulo (FMUSP).
Psicóloga, especialista em Sexualidade Humana pela Faculdade de Medicina da Universidade de São Paulo (FMUSP).
Psiquiatra, livre-docente e professora associada do Departamento de Psiquiatria da Faculdade de Medicina da Universidade de São Paulo (FMUSP).
Fundadora e coordenadora do Programa de Estudos em Sexualidade (ProSex) do Instituto de Psiquiatria do Hospital das Clínicas da FMUSP.
I
II
III
Editor responsável por esta seção:
Carmita Helena Najjar Abdo. Psiquiatra, livre-docente e professora associada do Departamento de Psiquiatria da Faculdade de Medicina da Universidade de
São Paulo (FMUSP). Fundadora e coordenadora do Programa de Estudos em Sexualidade (ProSex) do Instituto de Psiquiatria do Hospital das Clínicas da FMUSP.
Endereço para correspondência:
Heloisa Junqueira Fleury
Rua Sergipe, 401 — cj. 309 — São Paulo (SP) — CEP 01243-906
Tel. (11) 3256-9928
E-mail: [email protected]
Fonte de fomento: nenhuma declarada — Conflito de interesse: nenhum declarado
Entrada: 12 de maio de 2014 — Última modificação: 4 de junho de 2014 — Aceite: 5 de junho de 2014
144
Diagn Tratamento. 2014;19(3):144-7.
Heloisa Junqueira Fleury | Mirian Bernardes Lopes Alves | Carmita Helena Najjar Abdo
de responder sexualmente ou experimentar prazer sexual.
O transtorno do desejo sexual hipoativo e o transtorno da excitação sexual descritos separadamente no DSM-IV-TR5 foram
combinados como transtorno do interesse/excitação sexual
feminino, sendo definido pela perda ou redução significativa
do interesse e/ou da excitação sexual. Essa revisão tem sido
contestada pela substituição do termo “desejo” por “interesse”,
o que dificulta um diagnóstico acurado, e pela ausência de alguns critérios para os transtornos da excitação sexual feminina e do desejo sexual hipoativo presentes na edição anterior.6
A 10a revisão da Classificação Internacional de Doenças e
Problemas Relacionados à Saúde (CID-10)7 considera o transtorno do desejo sexual hipoativo uma disfunção sexual não
causada por distúrbio ou doença orgânica e caracterizada
pela perda do desejo sexual.
Entre os fatores de risco para o declínio ou a ausência do
interesse/desejo sexual, acompanhado ou não de sofrimento,
destacam-se a duração do relacionamento, a pouca satisfação
afetiva e menor valorização da vida sexual.8 Condições médicas
e respectivos tratamentos também afetam o desejo sexual.2
Problemas sexuais tendem a ser mais comuns em mulheres
idosas. Contudo, fatores relacionais são mais impactantes do que
a idade ou a menopausa, sendo a diminuição do desejo mais significativa entre aquelas com relacionamentos de longa duração.8
Embora a diminuição do desejo atinja todas as faixas etárias, as mulheres jovens apresentam maior desconforto com essa condição.9
Por se tratar de transtorno de etiologia multifatorial e de
alta prevalência na população feminina, este artigo visa reflexão sobre a experiência do desejo sexual em mulheres jovens
em relacionamentos estáveis.
DESEJO SEXUAL EM MULHERES JOVENS
O modelo tradicional de resposta sexual masculina e feminina (excitação – platô – orgasmo – resolução) foi desenvolvido por Masters e Johnson,10 com enfoque prioritário sobre os
aspectos fisiológicos dessa resposta sexual. Posteriormente,
Kaplan11 defendeu o desejo como precursor necessário para
o desenvolvimento da excitação e o desencadeamento do orgasmo. Essa autora desconsiderou a fase do platô. O ciclo de
resposta sexual proposto pelo DSM-IV-TR,5 baseado nesses
modelos, considera quatro fases, a saber: desejo, excitação, orgasmo e resolução. A complexidade da função sexual feminina
foi reconhecida no início da década de 2000, quando o desejo
por intimidade, ao invés de impulso biológico, foi proposto
como deflagrador da resposta sexual.12 O resultado emocional
e físico da experiência seria responsável pela disponibilidade
da mulher para uma próxima experiência sexual, caracterizando um modelo circular, que valoriza a responsividade física e a receptividade da mulher.12
Dificuldades sexuais são frequentes e sua ocorrência aumenta com a idade tanto em homens como em mulheres.13
Porém, causar sofrimento ou dificuldades interpessoais é
critério para essas dificuldades serem diagnosticadas como
disfunções sexuais.5 Problemas relativos ao desejo sexual
ocorrem em até 64% (12%-64%) das mulheres com alguma
dificuldade sexual, porém a proporção daquelas que sofrem
com essa condição é muito menor.8
O desejo sexual feminino depende do equilíbrio entre aspectos biológicos, psicológicos e socioculturais. Fatores cognitivos, principalmente os pensamentos automáticos durante a
atividade sexual, são importantes preditores do desejo sexual.
Idade avançada, pensamentos de fracasso, distanciamento do
parceiro, assim como a ausência de fantasias eróticas durante
a atividade sexual desempenham papel importante no comprometimento do desejo.14
Observa-se também que a idade é fator relevante na
complexa relação entre a função sexual e o bem-estar
subjetivo feminino.15 Em mulheres jovens, falta de desejo
e sofrimento sexual estão correlacionados. Porém, apesar
de as dificuldades sexuais se intensificarem com a idade, o
sofrimento sexual parece diminuir, tanto numa dimensão
pessoal como relacional.16
Conflitos relacionais,8 presença de várias dificuldades
sexuais,17 depressão8 e disfunção sexual do parceiro9 tendem a aumentar o sofrimento com a atividade sexual, sendo maior a insatisfação em mulheres com baixo desejo e
sofrimento sexual.15
A experiência feminina de perda do desejo sexual influencia e é influenciada pelo parceiro, tornando essa condição uma questão do casal e não um problema individual.18
Observa-se maior compatibilidade com o parceiro em mulheres funcionais do que naquelas com disfunção ou com
sofrimento sexual.19
DESEJO SEXUAL EM
RELACIONAMENTOS ESTÁVEIS
A duração do relacionamento, mesmo com a idade controlada, está negativamente associada com a frequência de iniciativa para a atividade sexual e com a satisfação da mulher
e do parceiro,20 indicando a influência desse tempo sobre o
desejo, inclusive em mulheres jovens.21
No início do relacionamento, o desejo tende a estar mais
preservado. Entretanto, a maioria das mulheres refere diminuição progressiva do desejo sexual, com a duração do relacionamento,22 ainda que algumas possam manter os mesmos
níveis de desejo.23 A manutenção do desejo se observa principalmente entre os casais que buscam novas e positivas experiências no relacionamento (lazer, desenvolvimento pessoal).23
Diagn Tratamento. 2014;19(3):144-7.
145
Desejo sexual em mulheres jovens em relacionamentos estáveis
Estudo com alemães entre 19 e 32 anos demonstrou que
a atividade e a satisfação sexual diminuem para mulheres e
homens em relacionamentos longos, sendo que o desejo sexual declina para as mulheres enquanto a necessidade de carinho diminui para os homens e aumenta para as mulheres.22
Algumas mulheres atribuem o declínio do desejo sexual à
institucionalização do casamento, à familiaridade excessiva
com o parceiro e à dessexualização do papel de esposa, mãe
e profissional.24 Outros fatores que comprometem relacionamentos de longa duração são: diminuição do afeto em relação
ao parceiro,25 estratégias de evitação que provocam menor
possibilidade de interação sexual e ausência de receptividade
para a iniciativa masculina.26
Porcentagem significativa (58%) de mulheres refere já ter
feito sexo apenas para atender ao parceiro, excedendo em
muito os homens (27%) nessa situação. Há associação entre
sexo por obrigação, pouco reconhecimento das próprias necessidades sexuais e dificuldade de comunicação com o parceiro sobre alternativas para a satisfação sexual.27
A diminuição do desejo sexual ao longo do relacionamento ocorre a muitas mulheres, no entanto para as mais jovens
tanto a satisfação como o sofrimento não se relacionam ao
nível do desejo propriamente dito mas à intensidade que atribuem a essa diminuição.28 Aquelas com desejo elevado consideram o declínio como natural e esperado e, com essa perspectiva, não vivenciam impacto negativo na satisfação sexual
e não se preocupam com as flutuações do desejo ao longo do
relacionamento. Por outro lado, mulheres com baixo desejo
relatam sofrimento frente a esse decréscimo, que consideram
negativo porque afeta o parceiro.23
Níveis maiores de discrepâncias entre o desejo sexual
dos parceiros se correlacionam significativamente com
menor satisfação sexual em mulheres (mas não em homens) e com menor satisfação com o relacionamento em
homens (mas não em mulheres), sugerindo a importância
da interação do casal sobre a função sexual feminina.29
Essas evidências indicam que o desejo sexual feminino
pode ser percebido como problemático apenas por ser
menor do que o vivenciado pelo parceiro, o que confirma
a necessidade de abordagem terapêutica do casal jovem e
não apenas da mulher.20
CONCLUSÃO
Aspectos fisiológicos, emocionais, ambientais, comportamentais, socioculturais e principalmente relacionais comprometem a experiência do desejo sexual de mulheres jovens em
relacionamentos estáveis.
O conhecimento dos fatores de risco para essa condição contribui para o melhor manejo clínico das dificuldades do casal jovem.
Profissionais de saúde devem estar preparados para
avaliar mulheres jovens com diminuição ou ausência de
desejo sexual, no sentido de implementar tratamento adequado, preferencialmente para o casal, enquanto essa situação ainda causa sofrimento a ela, o que não mais ocorre a
partir do final da idade reprodutiva.
REFERÊNCIAS
1. Laumann EO, Glasser DB, Neves RC, Moreira ED Jr; GSSAB
Investigators’ Group. A population-based survey of sexual
activity, sexual problems and associated help-seeking behavior
patterns in mature adults in the United States of America. Int J
Impot Res. 2009;21(3):171-8.
2. Kingsberg SA, Rezaee RL. Hypoactive sexual desire in women.
Menopause. 2013;20(12):1284-300.
3. Abdo CHN. Descobrimento sexual do Brasil. São Paulo:
Summus; 2004.
4. American Psychiatric Association. Diagnostic and statistical
manual of mental disorders: DSM-V. 5th ed. Washington:
American Psychiatric Association; 2013.
5. American Psychiatric Association. Manual diagnóstico e
estatístico de transtornos mentais. Texto revisado (DSM-IV-TR).
4a ed. Porto Alegre: Artmed; 2002.
6. Clayton AH, DeRogatis RL, Rosen RC, Pyke R. Intended or
unintended consequences? The likely implications of raising
the bar for sexual dysfunction diagnosis in the proposed DSM-V
revisions: 1. For women with incomplete loss of desire or sexual
receptivity. J Sex Med. 2012;9(8):2027-39.
146
Diagn Tratamento. 2014;19(3):144-7.
7. Organização Mundial da Saúde (OMS). Classificação estatística
internacional de doenças e problemas relacionados à saúde
(CID-10). 10a ed. São Paulo: Edusp; 2011.
8. Hayes RD, Dennerstein L, Bennett CM, et al. Risk factors for
female sexual dysfunction in the general population: exploring
factors associated with low sexual function and sexual distress. J
Sex Med. 2008;5(7):1681-93.
9. Bancroft J, Loftus J, Long JS. Distress about sex: a national
survey of women in heterosexual relationships. Arch Sex Behav.
2003;32(3):193-208. 10. Masters WH, Johnson V. A resposta sexual humana. São Paulo:
Roca; 1984.
11. Kaplan HS. A nova terapia do sexo. 3a ed. Rio de Janeiro: Nova
Fronteira; 1977.
12. Basson R. Human sex-response cycles. J Sex Marital Ther.
2001;27(1):33-43.
13. Derogatis LR, Burnett AL. The epidemiology of sexual
dysfunctions. J Sex Med. 2008;5(2):289-300.
14. Carvalho J, Nobre P. Sexual desire in women: an integrative
approach regarding psychological, medical, and relationship
dimensions. J Sex Med. 2010;7(5):1807-15.
Heloisa Junqueira Fleury | Mirian Bernardes Lopes Alves | Carmita Helena Najjar Abdo
15. Rosen RC, Shifren JL, Monz BU, et al. Correlates of sexually
related personal distress in women with low sexual desire. J Sex
Med. 2009;6(6):1549-60.
16. Stephenson KR, Meston CM. The young and the restless? Age
as a moderator of the association between sexual desire and
sexual distress in women. J Sex Marital Ther. 2012;38(5): 445-57.
17. Ferenidou F, Kapoteli V, Moisidis K, et al. Presence of a sexual
problem may not affect women’s satisfaction from their sexual
function. J Sex Med. 2008;5(3):631-9.
18. Hurlbert DF, Apt C, Hurlbert MK, Pierce AP. Sexual
compatibility and the sexual desire-motivation relation
in females with hypoactive sexual desire disorder. Behav
Modif. 2000;24(3):325-47.
19. Witting K, Santtila P, Varjonen M, et al. Female sexual
dysfunction, sexual distress, and compatibility with partner. J
Sex Med. 2008;5(11):2587-99.
20. Carvalheira AA, Brotto LA, Leal I. Women’s motivations for sex:
exploring the diagnostic and statistical manual, fourth edition,
text revision criteria for hypoactive sexual desire and female
sexual arousal disorders. J Sex Med. 2010;7(4 Pt 1):1454-63.
21. Murray SH, Milhausen RR. Sexual desire and relationship
duration in young men and women. J Sex Marital Ther.
2012;38(1):28-40.
22. Klusmann D. Sexual motivation and the duration of partnership.
Arch Sex Behav. 2002;31(3):275-87.
23. Impett EA, Strachman A, Finkel EJ, Gable SL. Maintaining sexual
desire in intimate relationships: the importance of approach
goals. J Pers Soc Psychol. 2008;94(5):808-23.
24. Sims KE, Meana M. Why did passion wane? A qualitative study
of married women’s attributions for declines in sexual desire. J
Sex Marital Ther. 2010;36(4):360-80.
25. Apay SE, Nagorska M, Akpinar BA, et al. Student comparison
of sexual myths: two-country case. Sexuality and Disability.
2013;31(3):249-62. Disponível em: http://link.springer.com/
article/10.1007%2Fs11195-013-9301-0#page-1. Acessado em
2014 (13 mai).
26. Hubin A, De Sutter P, Reynaert C. Etiological factors in female
hypoactive sexual desire disorder. Sexologies. 2011;20(3):149-57.
27. Traeen B, Skogerbø A. Sex as an obligation and interpersonal
communication among Norwegian heterosexual couples.
Scand J Psychol. 2009;50(3):221-9.
28. Murray SH, Sutherland O, Milhausen RR. Young women’s
descriptions of sexual desire in long-term relationships. Sexual
and Relationship Therapy. 2012;27(1):3-16. Disponível em:
http://www.tandfonline.com/doi/pdf/10.1080/14681994.2011.6
49251. Acessado em 2014 (13 mai).
29. Mark KP, Murray SH. Gender differences in desire discrepancy
as a predictor of sexual and relationship satisfaction in a college
sample of heterosexual romantic relationships. J Sex Marital
Ther. 2012;38(2):198-215.
Diagn Tratamento. 2014;19(3):144-7.
147
DESTAQUES COCHRANE
Medicamentos orais para
o tratamento do pé de atleta
(tinea pedis)
Tradução:
Centro Cochrane do Brasil e Liga de Medicina Baseada em Evidências da Escola Paulista de Medicina —
Universidade Federal de Medicina (EPM-Unifesp)
Autora dos comentários independentes: Leontina da Conceição MargaridoI
RESUMO
Introdução: Cerca de 15% da população mundial tem
pé de atleta ( frieira, ou tinea pedis), uma infecção fúngica
do pé. Existem várias formas clínicas da doença; a tinea dos
dedos do pé, da sola (interdigital), do calcanhar e lateral do
pé (plantar) são as formas mais comuns. A tinha plantar é
conhecida como “pé em mocassim”. Uma vez adquirida, a infecção pode disseminar-se para outras áreas do pé, inclusive
para as unhas, que se tornam fonte de reinfecção. A terapia
oral é frequentemente usada para quadros crônicos de tinea
ou quando o tratamento tópico não resolveu o problema.
Objetivos: Avaliar a efetividade dos tratamentos orais para
infecções fúngicas da pele do pé (tinea pedis).
Métodos:
Métodos de busca: Para esta atualização da revisão, foram
feitas buscas nas seguintes bases de dados até julho de 2012:
Cochrane Skin Group Specialised Register, Central, Medline
(a partir de 1946), Embase (a partir de 1974), e CINAHL (a partir de 1981). Também foi feita uma busca nas referências bibliográficas citadas nos estudos encontrados e nas plataformas de registros de ensaios clínicos.
Critérios de seleção: Ensaios clínicos controlados e randomizados que avaliaram medicamentos orais para participantes com diagnóstico clínico de tinea pedis, confirmado
pela microscopia e pelo crescimento de dermatófitos ( fungos) na cultura.
Coleta de dados e análise: Dois autores da revisão realizaram a seleção de estudos, a avaliação do risco de viés e a extração de dados, de modo independente.
Principais resultados: Incluímos 15 ensaios clínicos que
envolveram 1.438 participantes. Segundo dois ensaios clínicos
(71 participantes) que compararam terbinafina versus griseofulvina, a razão de risco (RR) de cura foi de 2.26 [intervalo de
confiança de 95% (IC 95%) 1,49 a 3,44] em favor da terbinafina.
Apesar de a maioria dos estudos ser pequena, não foi detectada
I
Doutora em Dermatologia pela Faculdade de Medicina da Universidade de São Paulo (FMUSP). Professora do Centro de Ciências Biológicas e da Saúde
(CCBS), Universidade Presbiteriana Mackenzie. Presidente do Departamento de Dermatologia da Associação Paulista de Medicina (APM), Conselheira da
Sociedade Brasileira de Dermatologia.
Tradução e adaptação:
Centro Cochrane do Brasil e Liga de Medicina Baseada em Evidências da Escola Paulista de Medicina — Universidade Federal de São Paulo (EPM-Unifesp)
Rua Pedro de Toledo, 598
Vila Clementino — São Paulo (SP) — CEP 04039-001
Tel. (11) 5579-0469/5575-2970
E-mail: [email protected]
http://www.centrocochranedobrasil.org.br/
Informações:
Este é o resumo de uma revisão sistemática Cochrane publicada na Cochrane Database of Systematic Reviews (CDSR) 2012, edição 10, art. No. CD003584.
DOI: 10.1002/14651858.CD003584.pub2 (http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD003584.pub2/full). Para citação e detalhes sobre os autores,
veja referência 1.
O texto completo desta revisão está disponível em: http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD003584.pub2/pdf
O resumo desta revisão está disponível em Português, Espanhol e Chinês em: http://summaries.cochrane.org/CD003584/oral-antifungal-drugs-for-treatingathletes-foot-tinea-pedis#sthash.i0KoYuHh.dpuf
148
Diagn Tratamento. 2014;19(3):148-9.
Leontina da Conceição Margarido
nenhuma diferença significante entre terbinafina e itraconazol, nem entre fluconazol e itraconazol, ou fluconazol e cetoconazol, ou entre griseofulvina e cetoconazol. Dois ensaios clínicos mostraram que a terbinafina e o itraconazol foram mais
efetivos do que placebo: terbinafina (31 participantes, RR 24,54,
IC 95% 1,57 a 384,32) e itraconazol (72 participantes, RR 6,67,
IC 95% 2,17 a 20,48). Houve relato de efeitos adversos para todas as drogas estudadas, sendo os efeitos gastrointestinais
os mais frequentes. Dez dos ensaios clínicos foram publicados
há mais de 15 anos, portanto apresentam informações sem clara avaliação do risco de viés metodológico. Apenas um ensaio
clínico apresentou baixo risco de viés em relação a todos os critérios metodológicos avaliados. A maioria dos ensaios clínicos
restantes foi categorizada como tendo risco “incerto” de viés
metodológico devido à falta de informações claras a respeito
dos métodos de geração da sequência de randomização e de
sigilo da alocação. O número de ensaios clínicos com cegamento dos participantes e dos investigadores foi maior que o de
estudos com cegamento dos avaliadores dos desfechos, sendo
que este último parâmetro foi pouco relatado.
Conclusões dos autores: A evidência sugere que a terbinafina é mais efetiva que a griseofulvina, e que a terbinafina e
o itraconazol são mais efetivos que nenhum tratamento. Para
que se produzam dados mais confiáveis, rigorosa avaliação de
diferentes terapias com drogas orais precisa ser realizada em
amostras maiores que permitam identificar diferenças reais
ao se comparar dois tratamentos. É também importante a
continuidade do seguimento e da coleta dos dados ao longo
dos ensaios clínicos, preferencialmente por seis meses após o
fim do período de administração da intervenção, para poder
ter certeza se houve ou não recorrência da infecção.
REFERÊNCIA
1. Bell-Syer SE, Khan SM, Torgerson DJ. Oral treatments for fungal
infections of the skin of the foot. Cochrane Database Syst Rev.
2012;10:CD003584.
COMENTÁRIOS
A micose dos pés, tinea pedis ou tinha dos pés, incluindo-se
a tinea interdigital dessa região, conhecida como “pé de atleta”
é um problema muito importante além de frequente, e precisa ser tratado adequadamente. A micose das unhas, em geral, está associada e é a fonte de reinfecção ou recidiva das
tinhas, inclusive, de outras regiões do corpo. O itraconazol é
mais efetivo por eliminar dermatófitos e∕ou leveduras e também fungos filamentosos; a terbinafina é mais efetiva contra
os dermatófitos.
A tinha das regiões interdigitais provoca descamação,
fissuras ou maceração, e pode ser a porta de entrada dos
estreptococos beta-hemolíticos que causam celulite nas
pernas. Porém, o intertrigo interdigital ou outras micoses
dos pés não têm sido valorizados de modo adequado, ou
a região nem é examinada. Em 85% das culturas de material de doentes com celulite e tinea pedis, observou-se
crescimento de estreptococos beta-hemolítico, em quatro
do grupo A de Lancefield, em três do grupo B, em um do
grupo C e em nove do grupo G. E, ao contrário, no grupo
com tinea pedis, mas sem celulite, não se isolou o estreptococo beta-hemolítico nos interdígitos. O crescimento
de Staphylococcus aureus foi semelhante nos dois grupos.1
A bactéria causa celulite penetrando na pele através da maceração, das fissuras ou nas áreas com defesas diminuídas.
Essa correlação mostra que é preciso dar ênfase ao exame
dos pés e suas unhas para diagnosticar e tratar, adequadamente, as micoses da região, com o objetivo de prevenir
celulite ou suas recidivas.
REFERÊNCIA
1. Semel JD, Goldin H. Association of athlete’s foot with cellulitis
of the lower extremities: diagnostic value of bacterial cultures
of ipsilateral interdigital space samples. Clin Infect Dis.
1996;23(5):1162-4.
Diagn Tratamento. 2014;19(3):148-9.
149
DESTAQUES COCHRANE
Intervenções para a prevenção
da obesidade infantil
Tradução:
Centro Cochrane do Brasil e Liga de Medicina Baseada em Evidências da Escola Paulista de Medicina —
Universidade Federal de Medicina (EPM-Unifesp)
Autora dos comentários independentes: Angela Maria Spinola e CastroI
RESUMO
Introdução: A prevenção da obesidade infantil é prioridade internacional de saúde pública devido ao seu impacto
significante sobre doenças agudas e crônicas, sobre a saúde
geral, sobre o desenvolvimento e o bem-estar. Tem havido aumento na base de evidências internacionais sobre estratégias
que podem ser usadas por governos, comunidades e famílias
para prevenir a obesidade e promover a saúde infantil. Porém
ainda existem incertezas nessa área.
Objetivos: Esta revisão atualizou a revisão Cochrane anterior sobre prevenção da obesidade infantil e avaliou a efetividade de intervenções para prevenir a obesidade infantil medida através de mudanças no índice de massa corporal (IMC).
Como objetivos secundários, foram avaliadas as características dos programas e das estratégias para responder as perguntas “O que funciona para quem, porque e com qual custo?”
Métodos:
Métodos de busca: As buscas foram refeitas nas bases
Central, Medline, Embase PsychINFO e CINAHL em Março de
2010 e também buscamos websites relevantes. Incluímos artigos escritos em outros idiomas além do inglês e entramos em
contato com especialistas da área.
Critérios de seleção: Esta revisão incluiu estudos de prevenção da obesidade infantil que utilizaram desenho controlado (com ou sem randomização). Os estudos foram
incluídos quando avaliaram as intervenções, políticas ou
programas por pelo menos 12 semanas. Se os estudos fossem randomizados por aglomerados (clusters), pelo menos 6
clusters eram necessários.
Coleta e análise dos dados: Dois revisores extraíram os
dados e analisaram de forma independente o risco de viés
dos estudos incluídos. Foram extraídos dados sobre a implementação da intervenção, seus custos, equidade e desfechos.
Os desfechos foram agrupados quanto à mensuração de medidas de adiposidade, atividade física ou dieta. Os desfechos
adversos também foram coletados. Foi feita metanálise utilizando o IMC disponível ou valores do IMC padronizado
(zIMC), com análise de subgrupos por faixa etária entre 0-5,
6-12, 13-18 anos de idade, correspondendo aos estágios do
desenvolvimento infantil.
I
Doutora em Medicina pela Universidade Federal de São Paulo, professora adjunta do Departamento de Pediatria da Escola Paulista de Medicina,
Universidade Federal de São Paulo (EPM-Unifesp); chefe do Setor de Endocrinologia Pediátrica e Presidente do Departamento de Endocrinologia da
Associação Paulista de Medicina (APM), São Paulo, Brazil.
Tradução e adaptação:
Centro Cochrane do Brasil e Liga de Medicina Baseada em Evidências da Escola Paulista de Medicina — Universidade Federal de São Paulo (EPM-Unifesp)
Rua Pedro de Toledo, 598
Vila Clementino — São Paulo (SP) — CEP 04039-001
Tel. (11) 5579-0469/5575-2970
E-mail: [email protected]
http://www.centrocochranedobrasil.org.br/
Informações:
Este é o resumo de uma revisão sistemática Cochrane publicada na Cochrane Database of Systematic Reviews (CDSR) 2011, edição 12, art. No. CD001871.
DOI: 10.1002/14651858.CD001871.pub3 (http://onlinelibrary.wiley.com/doi/10.1002/14651858.CD001871.pub3/abstract). Para citação e detalhes sobre os
autores, veja referência 1.
O texto completo desta revisão está disponível em: http://cochrane.bvsalud.org/doc.php?db=reviews&id=CD001871&lib=COC
O resumo desta revisão está disponível em Português, Espanhol e Chinês em: http://summaries.cochrane.org/CD001871/interventions-for-preventingobesity-in-children
150
Diagn Tratamento. 2014;19(3):150-2.
Angela Maria Spinola e Castro
Resultados principais: Esta revisão incluiu um total
de 55 estudos (sendo que 36 desses estudos vieram desta
atualização). A maioria dos estudos incluiu crianças entre 6 a
12 anos. A metanálise incluiu 37 estudos com 27.946 crianças
e demonstrou que os programas eram efetivos para reduzir
a adiposidade. Porém, nem todas as intervenções foram
efetivas e a heterogeneidade foi alta (I2 = 82%). Em geral,
as crianças do grupo intervenção tiveram diferença média
padronizada da adiposidade (medida como IMC ou zIMC)
de -0.15 kg/m2 (intervalo de confiança de 95% (IC 95%): -0.21
a -0.09). Os efeitos da intervenção por subgrupos de idade foram: -0.26 kg/m2 (IC 95%: -0.53 a 0.00) para crianças de
0-5 anos, -0.15 kg/m2 (IC 95% -0.23 a -0.08) para crianças
de 6-12 anos e -0.09 kg/m2 (IC 95% -0.20 a 0.03) para crianças de 13-18 anos. A heterogeneidade foi evidente nas três
faixas etárias e não foi justificada pela presença ou ausência
de randomização ou pelo tipo, duração ou local da intervenção. Apenas oito estudos relataram efeitos adversos. As intervenções não produziram desfechos adversos como práticas alimentares não saudáveis ou aumento na prevalência
de crianças desnutridas ou com problemas de imagem
corporal. As intervenções não parecem ter aumentado desigualdades de saúde; porém este desfecho foi avaliado em
poucos estudos.
Conclusões do autor: Encontramos fortes evidências indicando efeitos benéficos dos programas de prevenção de
obesidade infantil sobre o IMC, especialmente nos programas
dirigidos a crianças de 6-12 anos de idade. Entretanto, esses
achados devem ser interpretados com cautela devido à heterogeneidade inexplicável e a probabilidade de existir viés
decorrente de estudos com pequena casuística. Os estudos
incluídos nesta revisão tinham programas com grande variedade de componentes. Apesar de não conseguirmos identificar quais dos componentes abaixo mais contribuíram para
os efeitos benéficos observados, nossa síntese indica que as
seguintes políticas e estratégias parecem ser promissoras:
• um currículo escolar que inclua alimentação saudável, atividade física e imagem corporal
• mais sessões de atividade física e de desenvolvimento
de habilidades motoras fundamentais ao longo da semana escolar
• melhora na qualidade nutricional dos alimentos fornecidos
nas escolas
• ambientes e práticas culturais que incentivem as crianças
a comerem alimentos mais saudáveis e serem fisicamente
ativas ao longo de cada dia
• apoio para os professores e outros funcionários para a implementação de estratégias e atividades de promoção de
saúde (por exemplo, atividades de desenvolvimento e capacitação profissional)
• apoio dos pais e atividades em casa que encorajem a criança a ser fisicamente ativa, a comer alimentos mais nutritivos e a gastar menos tempo com atividades em frente das
telas da televisão, do computador e de jogos eletrônicos
Porém, ainda é necessário melhorar o desenho dos estudos e das análises. Os estudos também precisam avaliar
fatores relacionados a processos e a implementação, incluir
desfechos relacionados com medidas de equidade e desfechos a longo prazo, assim como possíveis efeitos adversos
e custos das intervenções. As pesquisas sobre a prevenção
da obesidade infantil precisam progredir no sentido de
identificar como os componentes efetivos da intervenção
podem ser incorporados dentro dos sistemas de saúde, de
educação e de cuidados e como podem alcançar impactos
sustentáveis a longo prazo.
REFERÊNCIA
1. Waters E, de Silva-Sanigorski A, Burford BJ, et al. Interventions
for preventing obesity in children. Cochrane Database Syst Rev.
2011;(12):CD001871.
COMENTÁRIOS
A obesidade durante a infância e a adolescência se transformou numa questão muito preocupante nos últimos 10 anos
ao redor do mundo, independentemente de raça. Essa condição tem sido considerada uma epidemia e tem muito a ver
não apenas com questões econômicas, por meio de maior renda per capita, mas também com uma profunda mudança dos
hábitos alimentares e estilo de vida, paralelamente a redução
nas atividades físicas devido a varias razões. Apesar de toda a
preocupação com a diminuição do peso e o aparecimento de
inúmeras dietas, parece que a maioria delas tem sido ineficaz,
fazendo com que essa revisão seja muito oportuna, devido
à importância no momento atual de obtermos intervenções
que possam prevenir e tratar a obesidade infantil.
A experiência mundial nesse sentido tem sido muito ampla, envolvendo governos, comunidades, famílias, sem, no entanto, ficar evidente qual a melhor estratégia para promoção
da saúde, representada pela perda de peso.
O primeiro objetivo dessa revisão foi determinar a efetividade dos programas de intervenção feitos para prevenir a
obesidade em crianças, avaliada pelo índice de massa corpórea (IMC). Essa forma de avaliar os programas tem sensibilidade questionável em crianças, nas quais o IMC não é um
parâmetro que reflete de forma apropriada a perda de peso,
visto que, apenas pela influência do crescimento, ele pode
ser modificado, até mesmo se houver perda de peso apenas
Diagn Tratamento. 2014;19(3):150-2.
151
Intervenções para a prevenção da obesidade infantil
discreta. Essa questão torna-se mais importante durante a
puberdade. Da mesma forma, crianças e especialmente adolescentes que pratiquem esportes de impacto que exerçam
importante influência na composição corporal também terão seus resultados falseados.
O segundo objetivo pode ser resumido na avaliação das características dos programas e a qual perfil de pacientes esses
se adequam, assim como seu custo e benefício.
De acordo com os critérios estabelecidos na revisão, os estudos incluídos foram todos os que tivessem grupo controle.
No entanto, nem todos os estudos avaliados foram randomizados, o que poderia facilitar a entrada, no grupo de pacientes avaliados, de crianças e/ou famílias já motivadas a perder
peso, o que pode ter interferido com os resultados obtidos.
Os autores incluíram 37 estudos na revisão, correspondendo a 27.496 crianças com idade entre 6 e 12 anos, e a revisão
conclui pela efetividade dos programas no sentido de reduzir
a adiposidade, embora nem todas as intervenções tenham
sido efetivas. Houve grande heterogeneidade nos resultados
encontrados, o que não pôde ser adequadamente explicado
pelos autores da revisão.
Alguns dos aspectos já comentados nesse artigo, assim
como a população do estudo e a possibilidade de viés, provavelmente explicam essa heterogeneidade, incluindo a necessidade de uma avaliação melhor do comportamento dos estudos
randomizados em relação aos não randomizados. Avaliar porcentagem das crianças que não perderam peso, mas estabilizaram e das que eventualmente ganharam peso talvez ajudasse
a compreendermos melhor os resultados obtidos. Além disso,
é muito importante termos claro que a abordagem clínica dos
pacientes obesos deve ser sempre individualizada, principalmente com crianças, que estão sempre submetidas a diversas
influências, dos familiares, amigos, escola e do ambiente.
A revisão não conseguiu identificar quais aspectos
colaboraram para os resultados, mas enfatiza na discussão, que está bem redigida, a importância de melhorar
152
Diagn Tratamento. 2014;19(3):150-2.
as condições do ambiente e incentivar práticas culturais
que privilegiem a ingestão de alimentos saudáveis, sugere
a necessidade de um currículo escolar que inclua noções
de alimentação, atividade física e trabalho com a imagem
corporal, e suporte educacional para professores para atividades de promoção de saúde. Entretanto, é importante
salientar que, isoladamente e sem a adequada participação e sensibilização das famílias, será difícil que qualquer
programa funcione. Os resultados sugerem também a importância de aumentar a atividade física durante a semana
escolar, o que em determinados locais é muito difícil devido à falta de políticas públicas nesse sentido.
A revisão não acrescentou fatos novos e não indica
efetivamente qual o tipo de intervenção favorece aos melhores resultados. Conclui com aspectos já bem reconhecidos na abordagem de crianças obesas e que já fazem
parte da rotina de atendimento. Talvez o tempo de intervenção tenha sido muito curto, visto que o mínimo e de
12 semanas para inclusão no estudo pode ter sido insuficiente para promoção de mudanças no comportamento.
Por outro lado, isso torna patente a necessidade do estabelecimento de políticas públicas que permitam a professores, educadores, ensinar sobre nutrição, aumento das
atividades físicas na escola, a criação de espaços comunitários para a prática de exercícios e a ampla participação
das famílias. Talvez atualmente mais importante do que
o peso em si seja trabalhar a aderência a hábitos mais
saudáveis de alimentação e a prática de exercícios, não
apenas para perda de peso mas objetivando promoção
de saúde. A avaliação da composição corporal também
se torna mais importante do que o IMC visto de forma
isolada. Avaliações futuras precisam se concentrar na
evolução do peso após as intervenções e na manutenção
dos conhecimentos adquiridos a longo prazo, pois apenas através disso será possível capacitar-se para prevenir
as complicações da obesidade ao longo da vida.
instruções aos autores
Revista
diagnóstico
& Tratamento
Indexação e escopo
A Revista Diagnóstico & Tratamento (ISSN 1413-9979) tem por
objetivo oferecer atualização médica, baseada nas melhores evidências disponíveis, em artigos escritos por especialistas. Seus artigos são
indexados na base de dados Lilacs (Literatura Latino-Americana e do
Caribe em Ciências da Saúde). São aceitos artigos originais (ensaios
clínicos, estudos coorte, estudos caso-controle, revisões sistemáticas,
estudos transversais, avaliações econômicas), relatos de caso, revisões
narrativas da literatura (artigos de atualização) e cartas ao editor, que
devem enquadrar-se nas normas editoriais dos manuscritos submetidos a revistas biomédicas (do International Committee of Medical
Journal Editors1).
Políticas e procedimentos da revista
Após o recebimento do manuscrito pelo setor de Publicações
Científicas, os autores receberão um número de protocolo que
servirá para manter o bom entendimento entre os autores e o setor.
Em seguida, o artigo será lido pelo editor, que verificará se está de
acordo com a política e o interesse da revista. Em caso afirmativo,
o setor de Publicações Científicas vai verificar se o texto cumpre as
normas de publicação expressas nestas Instruções para Autores. Se o
texto estiver incompleto ou se não estiver organizado como exigido,
os autores deverão resolver os problemas e submetê-lo novamente.
Quando o formato estiver aceitável, o setor enviará o trabalho para
a revisão por pares, na qual os revisores não assinarão seus veredictos
e não conhecerão os nomes dos autores do trabalho. Cada manuscrito
será avaliado por dois revisores: um especialista no assunto e um
consultor ad hoc (que vai avaliar aspectos metodológicos do trabalho);
as discordâncias serão resolvidas pelos editores.
Os autores então receberão a avaliação e será solicitado que resolvam os problemas apontados. Uma vez que o setor de Publicações
Científicas receba o texto novamente, o artigo será enviado ao editor
científico e revisor de provas, que identificará problemas na construção
de frases, ortografia, gramática, referências bibliográficas e outros. Os
autores deverão providenciar todas as informações e correções solicitadas e deverão marcar , no texto, todos os pontos em que realizaram
modificações, utilizando cores diferentes ou sistemas eletrônicos de
marcação de alterações, de maneira que elas fiquem evidentes.
Quando o texto for considerado aceitável para publicação, e só
então, entrará na pauta. O setor de Publicações Científicas fornecerá
uma prova, incluindo Tabelas e Figuras, para que os autores aprovem.
Nenhum artigo é publicado sem este último procedimento.
INSTRUÇÕES PARA AUTORES
Diretriz geral: para todos os tipos de artigos
Os artigos devem ser submetidos exclusivamente pela internet para
o e-mail [email protected] e/ou [email protected].
O manuscrito deve ser submetido em português e deve conter um
resumo e cinco palavras-chave em português, que devem ser selecionadas das listas DeCS (Descritores em Ciências da Saúde), conforme
explicado em detalhes abaixo (nenhuma outra palavra-chave
será aceita).
Artigos submetidos devem ser originais e todos os autores precisam
declarar que o texto não foi e não será submetido para publicação em
outra revista. Artigos envolvendo seres humanos (individual ou coletivamente, direta ou indireta ou indiretamente, total ou parcialmente,
incluindo o gerenciamento de informações e materiais) devem ser
acompanhados de uma cópia da autorização do Comitê de Ética em
Pesquisa da instituição onde o experimento foi realizado.
Todo artigo submetido deve cumprir os padrões editoriais estabelecidos na Convenção de Vancouver (Requerimentos Uniformes para
Manuscritos Submetidos a Revistas Biomédicas),1 e as diretrizes de
qualidade para relatórios de estudos clínicos,2 revisões sistemáticas
(com ou sem metanálises)3 e estudos observacionais.4 O estilo conhecido
como “estilo Vancouver” deve ser usado não somente quanto ao formato
de referências, mas para todo o texto. Os editores recomendam que
os autores se familiarizem com esse estilo acessando www.icmje.org.
Para a classificação dos níveis de evidência e graus de recomendação
de evidências, a Revista Diagnóstico e Tratamento adota a nova classificação elaborada pelo Centro de Medicina Baseada em Evidências
de Oxford (Centre for Evidence-Based Medicine - CEBM) e disponível
em http://www.cebm.net/mod_product/design/files/CEBM-Levels-of-Evidence-2.pdf Abreviações não devem ser empregadas, mesmo as
que são de uso comum. Drogas ou medicações devem ser citadas
usando-se os nomes genéricos, evitando-se a menção desnecessária
a marcas ou nomes comerciais. Qualquer produto citado no capítulo
de Métodos, tal como equipamento diagnóstico, testes, reagentes,
instrumentos, utensílios, próteses, órteses e dispositivos intraoperatórios devem ser descritos juntamente como o nome do fabricante e
o local (cidade e país) de produção entre parênteses. Medicamentos
administrados devem ser descritos pelo nome genérico (não a marca),
seguidos da dosagem e posologia.
Para qualquer tipo de estudo, todas as afirmações no texto que não
sejam resultado da pesquisa apresentada para publicação à revista
Diagnóstico & Tratamento, mas sim dados de outras pesquisas já
publicadas em outros locais, devem ser acompanhadas de citações
da literatura pertinente.
Os relatos de caso e as revisões narrativas deverão conter uma
busca sistematizada (atenção: o que é diferente de uma revisão
sistemática) do assunto apresentado, realizada nas principais bases
de dados (Cochrane Library, Embase, Lilacs, PubMed, outras bases específicas do tema).
Bolsas, apoios e qualquer suporte financeiro a estudos devem ser
mencionados separadamente na última página. Agradecimentos, se
necessário, devem ser colocados após as referências bibliográficas.
A Diagnóstico & Tratamento apóia as políticas para registro de ensaios
clínicos da Organização Mundial da Saúde (OMS) e do International
Committee of Medical Journal Editors (ICMJE), reconhecendo a importância dessas iniciativas para o registro e divulgação internacional
de informação sobre estudos clínicos, em acesso aberto. Sendo assim,
somente serão aceitos para publicação, a partir de 2007, os artigos de
Diagn Tratamento. 2014;19(3):I-III
I
instruções aos autores
pesquisa clínicas que tenham recebido um número de identificação
em um dos Registros de Ensaios Clínicos validados pelos critérios
estabelecidos pela OMS e ICMJE, cujos endereços estão disponíveis
no site do ICMJE (http://www.icmje.org/). O número de identificação
deverá ser registrado ao final do resumo.
FORMATO
Primeira página (capa)
A primeira página deve conter:
1) classificação do artigo (original, revisão narrativa da literatura, relato
de caso e carta ao editor);
2) o título do artigo, que deverá ser conciso, mas informativo;
3) o nome de cada autor (a política editorial da revista Diagnóstico &
Tratamento é não utilizar abreviações dos nomes dos autores. Assim, solicitamos que os nomes sejam enviados completos), sua titulação acadêmica
mais alta e a instituição onde trabalha;
4) o local onde o trabalho foi desenvolvido;
Segunda página
Artigos originais: a segunda página, neste caso, deve conter um resumo5
(máximo de 250 palavras) estruturado da seguinte forma:
1) contexto e objetivo;
2) desenho e local (onde o estudo se desenvolveu);
3) métodos (descritos em detalhes);
4) resultados;
5) Discussão;
6) conclusões.
Relatos de caso: devem conter um resumo5 (máximo de 250 palavras)
estruturado da seguinte forma:
1) contexto;
2) descrição do caso;
3) discussão;
4) conclusões.
Revisão da narrativa da literatura: deve conter um resumo (máximo de
250 palavras) com formato livre.
O resumo deve conter cinco palavras-chave, que devem ser escolhidas
a partir dos Descritores em Ciências da Saúde (DeCS), desenvolvidos pela
Bireme, que estão disponíveis na internet (http://decs.bvs.br/).6
Referências
As referências bibliográficas (no estilo “Vancouver”, como indicado
pelo Comitê Internacional de Editores de Revistas Biomédicas, ICMJE)
devem ser dispostas na parte final do artigo e numeradas de acordo
com a ordem de citação. Os números das citações devem ser inseridos
após pontos finais ou vírgulas nas frases, e sobrescritos (sem parênteses
ou colchetes). Referências citadas nas legendas de Tabelas e Figuras
devem manter a sequência com as referências citadas no texto. Todos
os autores devem ser citados se houver menos de seis; se houver mais de
seis autores, os primeiros três devem ser citados seguidos de “et al.” Para
livros, a cidade de publicação e o nome da editora são indispensáveis.
Para textos publicados na internet, a fonte localizadora completa (URL)
ou endereço completo é necessário (não apenas a página principal ou
link), de maneira que, copiando o endereço completo em seus programas
para navegação na internet, os leitores possam ser levados diretamente
ao documento citado, e não a um site geral. A seguir estão dispostos
alguns exemplos dos tipos mais comuns de referências:
II
Diagn Tratamento. 2014;19(3):I-III
Artigo em periódico
• Lahita R, Kluger J, Drayer DE, Koffler D, Reidenberg MM. Antibodies
to nuclear antigens in patients treated with procainamide or
acetylprocainamide. N Engl J Med. 1979;301(25):1382-5.
Livro
• Styne DM, Brook CGD. Current concepts in pediatric endocrinology.
New York: Elsevier; 1987.
Capítulo de livro
• Reppert SM. Circadian rhythms: basic aspects and pediatric implications.
In: Styne DM, Brook CGD, editors. Current concepts in pediatric
endocrinology. New York: Elsevier; 1987. p. 91-125.
Texto na internet
• World Health Organization. WHO calls for protection of women and
girls from tobacco. Disponível em: http://www.who.int/mediacentre/
news/releases/2010/women_tobacco_20100528/en/index.html.
Acessado em 2010 (8 jun).
Dissertações e teses
• Neves SRB. Distribuição da proteína IMPACT em encéfalos de
camundongos, ratos e saguis. [tese]. São Paulo: Faculdade de Medicina
da Universidade Federal de São Paulo; 2009.
Última página
A última página deve conter:
1) a data e o local do evento no qual o artigo foi apresentado, se aplicável,
como congressos ou defesas de dissertações ou teses;
2) fontes de apoio na forma de suporte financeiro, equipamentos ou drogas
e número do protocolo;
3) descrição de qualquer conflito de interesse por parte dos autores;
4) endereço completo, e-mail e telefone do autor a ser contatado quanto
à publicação na revista.
Figuras e tabelas
As imagens devem ter boa resolução (mínimo de 300 DPI) e ser
gravadas em formato “.jpg” ou “.tif ”. Imagens não devem ser incluídas
em documentos do Microsoft PowerPoint. Se as fotografias forem
inseridas num documento Microsoft Word, as imagens também
devem ser enviadas separadamente. Gráficos devem ser preparados
com o Microsoft Excel (não devem ser enviados como imagem) e
devem ser acompanhados das tabelas de dados a partir dos quais
foram gerados. O número de ilustrações não deve exceder o número
total de páginas menos um.
Todas as figuras e tabelas devem conter legendas ou títulos que
descrevam precisamente seu conteúdo e o contexto ou amostra a
partir da qual a informação foi obtida (por exemplo, quais foram os
resultados apresentados e qual foi o tipo de amostra e local). A legenda
ou título devem ser curtos, mas compreensíveis independentemente
da leitura do artigo.
O MANUSCRITO
# Relatos de caso devem conter Introdução, Descrição do Caso,
Discussão (contendo a busca sistematizada sobre o tema) e Conclusão.
# Artigos originais e revisões narrativas devem ser estruturados de maneira que contenham as seguintes partes: Introdução, Objetivo, Método, Resultados, Discussão e Conclusão.
A Revista publica revisões narrativas desde que contenham
busca sistematizada da literatura. O texto não deve exceder
2.200 palavras (excluindo tabelas, figuras e referências), da
introdução até o final da conclusão. A estrutura do documento
deve seguir o formato abaixo:
instruções aos autores
1. Introdução: as razões para que o estudo fosse realizado devem
ser explicitadas, descrevendo-se o atual estado da arte do assunto.
Deve ser descrito o contexto, o que se sabe a respeito. Aqui não devem
ser inseridos resultados ou conclusões do estudo. No último parágrafo, deve ser especificada a principal questão do estudo e a principal
hipótese, se houver. Não se deve fazer discussões sobre a literatura
na introdução; a seção de introdução deve ser curta.
2. Objetivo: deve ser descrito o principal objetivo do estudo, brevemente. Hipóteses pré-estabelecidas devem ser descritas claramente.
De preferência deve-se estruturar a pergunta do estudo no formato
“PICO”, onde P é a população ou problema, I é intervenção ou fator
de risco, C é o grupo controle e O vem de “outcome”, ou desfecho.
3. Métodos
3.1. Tipo de estudo: deve-se descrever o desenho do estudo, adequado para responder a pergunta, e especificando, se apropriado,
o tipo de randomização, cegamento, padrões de testes diagnósticos e a direção temporal (se retrospectivo ou prospectivo). Por
exemplo: “estudo clínico randomizado”, “estudo clínico duplo-cego
controlado por placebo”, “estudo de acurácia”, “relato de caso”
3.2. Local: deve ser indicado o local onde o estudo foi desenvolvido,
o tipo de instituição: se primária ou terciária, se hospital público ou
privado. Deve-se evitar o nome da instituição onde o estudo foi desenvolvido (para cegamento do texto para revisão): apenas o tipo de
instituição deve ficar claro. Por exemplo: hospital universitário público.
3.3. Amostra, participantes ou pacientes: devem ser descritos
os critérios de elegibilidade para os participantes (de inclusão
e exclusão), as fontes e os procedimentos de seleção ou recrutamento. Em estudos de caso-controle, a lógica de distribuição de
casos como casos e controles como controles deve ser descrita,
assim como a forma de pareamento. O número de participantes
no início e no final do estudo (após exclusões) deve ficar claro.
3.4. Tamanho de amostra e análise estatística: descrever o cálculo do
tamanho da amostra, a análise estatística planejada, os testes utilizados e
o nível de significância, e também qualquer análise post hoc. Descrever os
métodos usados para o controle de variáveis e fatores de confusão, como
se lidou com dados faltantes (“missing data”) e como se lidou com casos
cujo acompanhamento foi perdido (“loss from follow-up”).
3.5. Randomização: descrever qual foi o método usado para
implementação da alocação de sequência aleatória (por exemplo,
“envelopes selados contendo sequências aleatórias de números
gerados por computador”). Adicionalmente, descrever quem gerou a sequência aleatória, quem alocou participantes nos grupos
(no caso de estudos controlados) e quem os recrutou.
3.6. Procedimentos de intervenção, teste diagnóstico ou exposição: descrever quais as principais características da intervenção,
incluindo o método, o período e a duração de sua administração
ou de coleta de dados. Descrever as diferenças nas intervenções
administradas a cada grupo (se a pesquisa é controlada).
3.7. Principais medidas, variáveis e desfecho: descrever o método de
medida do principal resultado, da maneira pela qual foi planejado
antes da coleta de dados. Afirmar quais são os desfechos primário
e secundário esperados. Para cada variável de interesse, detalhar os
métodos de avaliação. Se a hipótese do estudo foi formulada durante ou
após a coleta de dados (não antes), isso deve ser declarado. Descrever
os métodos utilizados para melhorar a qualidade das medidas (por
exemplo, múltiplos observadores, treinamento etc.). Explicar como
se lidou com as variáveis quantitativas na análise.
4. Resultados: descrever os principais achados. Se possível,
estes devem conter os intervalos de confiança de 95% e o exato
nível de significância estatística. Para estudos comparativos, o
intervalo de confiança para as diferenças deve ser afirmado.
4.1. Fluxo de participantes: descreva o fluxo dos participantes em
cada fase do estudo (inclusões e exclusões), o período de acompanhamento e o número de participantes que concluiu o estudo (ou
com acompanhamento perdido). Considerar usar um fluxograma.
Se houver análise do tipo “intenção de tratar”, esta deve ser descrita.
4.2. Desvios: se houve qualquer desvio do protocolo, fora do que
foi inicialmente planejado, ele deve ser descrito, assim como as
razões para o acontecimento.
4.3. Efeitos adversos: devem ser descritos quaisquer efeitos ou
eventos adversos ou complicações.
5. Discussão: deve seguir a sequência: começar com um resumo
dos objetivos e das conclusões mais relevantes; comparar métodos e
resultados com a literatura; enfatizar os pontos fortes da metodologia
aplicada; explicar possíveis pontos fracos e vieses; incluir implicações
para a prática clínica e implicações para pesquisas futuras.
6. Conclusões: especificar apenas as conclusões que podem
ser sustentadas, junto com a significância clínica (evitando excessiva generalização). Tirar conclusões baseadas nos objetivos
e hipóteses do estudo. A mesma ênfase deve ser dada a estudos
com resultados negativos ou positivos.
CARTAS AO EDITOR
É uma parte da revista destinada à recepção de comentários e
críticas e/ou sugestões sobre assuntos abordados na revista ou
outros que mereçam destaque. Tem formato livre e não segue as
recomendações anteriores destinadas aos artigos originais, relatos
de casos e revisão da literatura.
Documentos citados
1. International Committee of Medical Journal Editors. Uniform requirements for manuscripts submitted to biomedical journals.
Disponível em: http://www.icmje.org/urm_main.html. Acessado
em 2010 (7 jun).
2. CONSORT Transparent Reporting of Trials. Welcome to the
CONSORT statement website. Disponível em: http://www.consort-statement.org. Acessado em 2010 (7 jun).
3. Moher D, Cook DJ, Eastwood S, Olkin I, Rennie D, Stroup DF.
Improving the quality of reports of meta-analyses of randomised
controlled trials: the QUOROM statement. Quality of Reporting of
Meta-analyses. Lancet. 1999;354(9193):1896-900.
4.STROBE Statement Strengthening the reporting of observational studies in epidemiology. Checklist on items that should
be included in reports of observational studies. Disponível
em:
http://www.strobe-statement.org/index.php?eID=tx_
nawsecuredl&u=0&file=fileadmin/Strobe/uploads/checklists/
STROBE_checklist_v4_combined.pdf&t=1257007091&hash=771
3ea8f7f2662b288689b3dab40c1cb. Acessado em 2010 (7 jun).
5. Haynes RB, Mulrow CD, Huth EJ, Altman DG, Gardner MJ. More informative abstracts revisited. Ann Intern Med. 1990;113(1):69-76.
6. BVS Biblioteca Virtual em Saúde. Descritores em Ciências da Saúde.
Disponível em:: http://decs.bvs.br/. Acessado em 2010 (7 jun).
Diagn Tratamento. 2014;19(3):I-III
III
A combinação perfeita
entre a natureza e o lazer
está no Clube de Campo!
Curta com a família momentos
inesquecíveis diante da belíssima natureza
que o Clube de Campo oferece!
São ótimas opções de lazer
para todas as idades: piscinas climatizadas
com toboágua, quadras poliesportiva e de tênis,
campo de futebol, pesca esportiva, playground,
escola de equitação, camping,
área para churrasqueira
e muito mais!
O Clube de Campo da APM está esperando por você.
Venha dividir seus momentos de alegria com a gente!
Faça já sua reserva:
Telefones: (11) 4899-3535 / 3518
E-mail: [email protected]
Horário de atendimento: 9h às 18h
Endereço: Estrada de Santa Inês, Km 10, Caieiras / SP
Médico: o que você está esperando para cuidar
ainda mais de sua saúde por até metade do preço?
Só a parceria da APM com a Qualicorp proporciona
acesso aos melhores planos de saúde, com inúmeras
vantagens para você, Médico.
• Rede com os melhores hospitais, laboratórios e médicos do Brasil.1
• Livre escolha de prestadores médico-hospitalares com reembolso.2
• Confira as possibilidades de redução de carências.3
Ligue e aproveite:
0800 799 3003
De segunda a sexta, das 9 às 21h, e aos sábados, das 10 às 16h.
www.economizecomaqualicorp.com.br
Metade do preço: em comparação a produtos similares no mercado de planos de saúde individuais (tabela de junho/2014 – Omint). ¹ De acordo com a disponibilidade da rede médica da operadora escolhida e do
plano contratado. ² Conforme condições contratuais. 3 A disponibilidade e as características desse benefício especial podem variar conforme a operadora escolhida e o plano contratado.
Planos de saúde coletivos por adesão, conforme as regras da ANS. Informações resumidas. A comercialização dos planos respeita a área de abrangência das respectivas operadoras. Os preços e as redes estão
sujeitos a alterações, por parte das respectivas operadoras, respeitadas as disposições contratuais e legais (Lei no 9.656/98). Condições contratuais disponíveis para análise. Julho/2014.
Amil:
ANS nº 326305
Bradesco Saúde:
ANS nº 005711
Omint:
ANS nº 359661
SulAmérica:
Qualicorp
Adm. de Benefícios:
ANS nº 417173


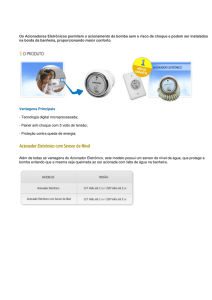


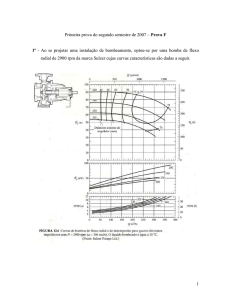
![[Wilson Jacob Filho] Desafios](http://s1.studylibpt.com/store/data/005403888_1-37e729ebc4743a519f99366f501ce250-300x300.png)