DETERMINAÇÃO DE MERCÚRIO TOTAL E METIL-MERCÚRIO EM AMOSTRAS
DE PEIXES MAIS CONSUMIDAS NA COMUNIDADE BARREIRAS, MUNICÍPIO DE
ITAITUBA – ESTADO DO PARÁ.
(1)
Kleber Raimundo Freitas Faial; (2)Kelson do Carmo Freitas Faial; (3) Mônia Maria
Carvalho da Silva ; (4) Thiago Lobato da Rocha; (5) Simonny de Deus; (6) Ricardo Jorge
Amorim de Deus; (7) Iracina Maura de Jesus; (8) Davi Brasil
(1)
Pesquisador em Saúde Pública, Seção de Meio Ambiente; Instituto Evandro Chagas, BR-316, Km 07,
Levilândia, S/N, Ananindeua, Pará, [email protected]; (2) Pesquisador em Saúde Pública, Seção de Meio
Ambiente, Instituto Evandro Chagas, BR-316, Km 07, Levilândia, S/N, Ananindeua, Pará,
[email protected]; (3) Pesquisador Colaborador, Seção de Meio Ambiente; Instituto Evandro Chagas; BR316, Km 07, Levilândia, S/N, Ananindeua, Pará, [email protected] 4) Assistente Técnico, Seção de Meio
Ambiente; Instituto Evandro Chagas; BR-316, Km 07, Levilândia, S/N, Ananindeua, Pará,
[email protected]; (5) Pesquisador Colaborador, Instituto de Química; UFPA; Belém, Pará,
[email protected] (6) Professor Adjunto, Instituto de Química; Belém, Pará, [email protected] (7) Pesquisador em
Saúde Pública, Seção de Meio Ambiente; Instituto Evandro Chagas; BR-316, Km 07, Levilândia, S/N,
Ananindeua, Pará, [email protected] (8) Professor Adjunto, Instituto de Química; Belém, Pará,
[email protected].
RESUMO
Os compostos mercuriais não estão somente relacionados com a
contaminação direta dos indivíduos expostos, também com a liberação inadequada
dos rejeitos das áreas de garimpo ao meio ambiente que pode acarretar
conseqüências danosas à saúde humana. Sabendo que o pescado é aprincipal
fonte protéica das comunidades ribeirinhas, torna-se importante a necessidade de
estudos de se avaliar os níveis de contaminantes como o mercúrio e seus
compostos principalmente o metil-mercúrio dessa população. O atual estudo está
situado no Estado do Pará, município de Itaituba (comunidade Barreiras). A
comunidade Barreiras está localizada às margens do rio Tapajós, onde na década
de 80 ocorreu uma intensa atividade garimpeira, produzindo toneladas de mercúrio
que foram despejadas diretamente no leito do rio, vindo a contaminar as espécies
biotas e abióticas principalmente o pescado. O objetivo principal deste trabalho é
determinar os teores de mercúrio total (HgT) e metil-mercúrio (CH3Hg) em amostras
de peixes. Foram coletadas 127 amostras de peixes. A técnica de Espectrometria de
Absorção Atômica vapor frio foi utilizada para análise de mercúrio total em peixes,
para determinar metil-mercúrio foi utilizada o método de Cromatografia gasosa. A
média de Hg total nas espécies peixes com hábito carnívoro foi de 0.70g/g,
enquanto que nas espécies não carnívoras a média foi de 0.07g/g, a concentração
média de metil-mercúrio nas espécies carnívoras foi de 0.65g/g e as não carnívoras
de 0.06 g/g.
Palavras-chaves: Mercúrio total, Metil-mercúrio, Peixes e Comunidade Barreiras.
INTRODUÇÃO
A contaminação de águas por metais pesados vem recebendo grande
atenção dos ambientalistas no que diz respeito a sua toxicidade em relação ao meio
aquático e à vida humana (TOREM & CASQUEIRA, 2003). Devido ao crescimento
populacional e à intensificação de atividades humanas que envolvem estes
elementos, a concentração de metais pesados tem aumentado de forma
generalizada nos corpos d’água em níveis que ameaçam não somente a biota
aquática, mas também os organismos terrestres, incluindo o homem (HUNN et al.,
1987; PEÁLEZ-RODRIGUEZ et al., 2002).
Dentre os diversos contaminantes presentes no ambiente pode-se mencionar
o mercúrio. O mercúrio (Hg) é um metal pesado de aspecto argênteo, inodoro, cujo
símbolo Hg deriva do latim hydrargyrum que, normalmente, é encontrado em dois
estados de oxidação. Na sua forma elementar, é um líquido denso, prateado, nas
condições normais de temperatura e pressão. Pertence à família química dos metais
do grupo II B, da tabela periódica, juntamente com o cádmio e o zinco. As formas
nas quais pode ser encontrado, além da elementar, são: mercúrio metálico (Hg 0),
mercúrio I e mercúrio II, onde os átomos perdem um ou dois elétrons,
respectivamente, formando mercúrio mercuroso (Hg2++) e o mercúrio mercúrico
(Hg++) (ATSDR ,1999).
As diferentes formas químicas e físicas do mercúrio têm suas propriedades
tóxicas intrínsecas e diferentes aplicações na indústria, na agricultura, e na
medicina. O mercúrio volátil é altamente tóxico. Porém, é na forma catiônica e
também quando ligados a cadeias curtas de átomos de carbono que está sua forma
mais tóxica. O mecanismo de ação tóxica deriva da forte afinidade dos cátions pelo
enxofre. Assim, os grupos sulfidrila – SH, que ocorrem nas enzimas que controlam a
velocidade das reações metabólicas de importância crítica no corpo humano, ligamse rapidamente aos cátions de metais pesados como o mercúrio, afetando a ação da
enzima como um todo, não podendo atuar com normalidade e em conseqüência
atua negativamente para a saúde humana, a principal forma química que pode se
acumular em peixes é a metilada, denominada de metil-mercúrio (MeHg) (MICARINI
et al. 2000; COLIN, 2004).
O metilmercúrio constitui mais de 90% (BLOOM et al., 1992; BRANCO et al.,
2007) de mercúrio no músculo de peixe, onde é ligado a grupos tiol na cisteína (Cys)
(HARRIS et al., 2003). Uma vez ingerido, é hidrolisado formando o complexo
metilmercúrio-Cys onde é absorvido na parede do intestino (CLARKSON E MAGOS,
2006). Este é um processo altamente eficaz, com mais de 95% de metilmercúrio a
ser absorvido no trato intestinal (MAGOS, 1997). Isto acontece porque o complexo
de metilmercúrio-Cys tem uma estrutura semelhante à do aminoácido metionina
(Met), que lhe permite, por homologia molecular, utilizar a transportadora de
aminoácido neutro (LAT) (CLARKSON E MAGOS, 2006; ROOS et al, 2010;.
SIMMONS-WILLIS et al, 2002).
Os dados disponíveis sobre os níveis de mercúrio em populações
potencialmente expostas aos riscos de intoxicação em áreas impactadas pela
garimpagem, através da ingestão de peixes ainda não são suficientes para traçar um
perfil do comportamento desse agente nas comunidades envolvidas, sobretudo
ribeirinhas, que também encontram-se submetidas aos agravos tradicionais
representados pelas endemias locais, e com as quais será necessário estabelecer
diagnósticos diferenciais nos casos em que exista a suspeita de intoxicação por Hg
(SANTOS et al. 2000).
MATERIAIS E MÉTODOS
Para análise de mercúrio total (HgT) e metil-mercúrio (CH3Hg) foram amostrados
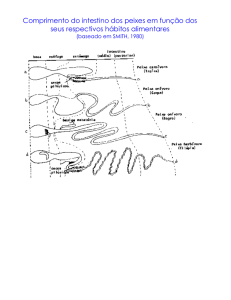
127 espécimes de peixes de 07 espécies diferentes (sendo 04 de hábito alimentar carnívoro
e 03 não carnívoros). As amostras foram adquiridas junto aos pescadores locais.
No momento da coleta os espécimes foram identificados e preenchida uma ficha de
campo onde foram registradas informações detalhadas do local da coleta que inclui Estado,
Cidade, Bacia hidrográfica e suas principais características, local da pesca (procedência do
pescado), caracterização de consumo e hábito alimentar. Neste procedimento deve-se evitar
adquirir espécimes no mercado. O pescado comercializado nestes locais são de diferentes
procedências. As amostras foram pesadas, medidas, dissecadas, separadas as vísceras e
músculos e transportados para o laboratório sede, onde foram mantidas sob refrigeração
(<4ºC), e posteriormente encaminhadas ao laboratório acondicionadas em caixas
isotérmicas para os procedimentos analíticos.
As amostras de peixe ao chegarem no laboratório foram descongeladas à
temperatura ambiente sendo retirada em seguida a epiderme superficial e acondicionadas
em vidro âmbar, onde foram homogeneizados e identificadas. Para análise de mercúrio
total foi utilizada uma balança analítica (modelo JK 200, marca chyo) onde foi pesado (0,5 –
1g) em balões volumétricos de 50 mL e submetidos aos procedimentos analíticos, através
do método proposto pôr Akagi (AKAGI, NISHIMURA, 1990; AKAGI et al.,1995) que será
descrito abaixo.
A abertura das amostras foi realizada adicionando os seguintes reagentes 2 mL da
solução de HNO3 – HClO4 (1:1), 5 mL de H2SO4 e 1 mL de H2O Milli-Q. Os balões
volumétricos contendo as amostras foram deixados por um período de 12 horas, onde
posteriormente foram colocados a uma chapa aquecedora (marca theemolyne, modelo type
2200) à uma temperatura de 220 0C pelo tempo de 20 minutos. Após o esfriamento à
temperatura ambiente, os balões foram aferidos ao volume de 50 mL com água Milli-Q e
homogeneizados. O mercúrio nestas condições está disponível em solução na forma iônica.
As determinações de mercúrio total nas amostras de peixes, foram realizadas por
Espectrometria de Absorção Atômica com sistema para geração de vapor frio de mercúrio,
sendo utilizado o modelo Mercury Analyzer Hg–201. As determinações de mercúrio total
foram registradas através de um registrador modelo 3102111, fabricante YOKOGAWA.
Para determinar metil-mercúrio, em uma balança analítica utilizando um tubo cônico
de centrifuga foi pesada uma quantidade em torno de 0,2 -0,5 g em peso úmido da amostra,
em seguida foram adicionados: 10 mL de etanol – KOH 1N. Fechado e aquecido em um
banho térmico a 100°C durante uma hora, agitando suavemente. Deixou-se esfriar,
adicionando-se 10 mL de HCl 1N e 5 mL de hexano em seqüência, agitando-se por 3
minutos em agitador de sentido recíproco, em seguida foi centrifugado a 2500 rpm por 3
minutos, onde foi retirado e descartado a fase de hexano (fase superior) para remover
materiais gordurosos. Adicionou-se 2 mL de EDTA 20% e 5 ml de ditizona – tolueno 0,01%
purificada.
Agitou-se por 3 minutos para extrair metilmercúrio com o seu ditizonato (complexo)
na fase de tolueno, em seguida foi descartada a fase aquosa (fase mais baixa). Centrifugouse a 2.500 rpm durante 3 minutos, sendo descartado o máximo possível da fase aquosa
restante. Adicionou-se 3 mL de NaOH 1N à fase de tolueno e agitou-se durante três minutos
para lavar e remover o excesso de ditizona. Deixar separar as fases. Descartar a fase
aquosa (fase mais baixa). Centrifugar a 2.500 rpm por 3 minutos para obter uma fase clara
de tolueno. Transferir um volume fixo (normalmente 3 mL) da fase de tolueno para um tubo
cônico de centrifuga de 10 mL com rolha de vidro. Adicionou-se 2 mL da solução alcalina de
sulfeto de sódio e agitou-se por 3 minutos para extrair de volta o metilmercúrio na fase
aquosa.
Centrifugou-se a 1.200 rpm por 3 minutos, tampado com a rolha de vidro, em
seguida foi retirado e descartado cuidadosamente a fase de tolueno (fase superior).
Adicionou-se 2 mL de tolueno a fase aquosa e agitou-se por 3 minutos para lavar a fase
aquosa. Centrifugou-se novamente a 1.200 rpm por 3 minutos, tampado com rolha de vidro.
Foi retirado e descartado a fase de tolueno (fase superior). Adicionou-se HCl 1N (3-5 gotas)
para tornar a solução ligeiramente ácida. Com uma pipeta Pasteur aerar a solução com gás
N2 através de um medidor de fluxo por 3 minutos (50 mL/min) para expelir o excesso de íons
sulfeto como o gás sulfídrico. Subsequentemente, adicionou-se 2 mL da solução tampão
Walpole’s lavando a extremidade da pipeta Pasteur.
Misturar bem com um misturador de vórtice, em seguida foi adicionado 0,5 mL de
ditizona-tolueno 0,01% purificada e agitar para extrair o metilmercúrio. Centrifugou-se a
1.200 rpm por 3 minutos tampado com a rolha de vidro. Retirar e descartar a fase aquosa
(fase mais baixa). Acrescentar 3 mL de NaOH 1N à fase de tolueno e agitar por 3 minutos
para lavar e remover o excesso de ditizona. Deixar separar as fases. Descartar a fase
aquosa (fase mais baixa). Acidificar a solução acrescentando 2 gotas de HCl 1N a fase de
tolueno e misture bem com um misturador vórtice. Centrifugar a 1.200 rpm por 3 minutos,
tampado com a rolha de vidro. Retirar e descartar a fase clorídrica ácida (fase mais baixa).
Usar a solução resultante como a solução amostra. (Fonte: Akagi et al, 1995). As
determinações de metil-mercúrio, foram realizadas por Cromatografia Gasosa com detector
de captura de elétrons.
RESULTADOS E DISCUSSÃO
Para melhor entendimento, as amostras de peixes foram divididas em dois
grupos em função dos hábitos alimentares: carnívoros e não carnívoros. O primeiro
grupo representado por 04 espécies totalizou 71 espécimes (56%) e o segundo com
03 espécies totalizando 56 amostras correspondendo a (44%) do total de amostras.
As Tabelas de 01 a 04 mostram os resultados das análises de mercúrio total e metilmercúrio nos peixes carnívoros e não carnívoros, respectivamente.
Tabela 01: Concentração média de mercúrio total em peixes carnívoros mais
consumidos da comunidade Barreiras/Itaituba.
Nome
Popular
Nome Científico
N
Média
(g/g)
Desvio
Padrão
(g/g)
Mínimo
(g/g)
Máximo
(g/g)
Filhote
Brachyplatystoma
filamentosum
07
0,93
0,32
0,50
1,35
Plagisocion squamosissimus
40
0,80
0,34
0,44
2,33
Calophysus macropterus
Cichla sp.
-
12
12
71
0,63
0,68
-
0,24
0,33
-
0,40
0,42
0,96
1,37
Pescada
Branca
Piranambu
Tucunaré
Total
Tabela 02: Concentração média de metil-mercúrio em peixes carnívoros mais
consumidos da comunidade Barreiras/Itaituba.
Nome
Popular
Filhote
Pescada
Branca
Piranambu
Tucunaré
Total
Nome Científico
Brachyplatystoma
filamentosum
Plagisocion
squamosissimus
Calophysus macropterus
Cichla sp.
-
N
Média
(g/g)
Desvio
Padrão
(g/g)
Mínimo
(g/g)
Máximo
(g/g)
07
0,79
0,30
0,41
1,12
40
0,66
0,31
0,29
1,98
12
12
71
0,45
0,51
-
0,23
0,27
-
0,20
0,26
0,78
1,01
Tabela 03: Concentração média dos resultados de Hg T nas espécies de peixes não
carnívoros mais consumidos da comunidade Barreiras/Itaituba.
Nome
Popular
Aracu
Caratinga
Pacu
Total
Nome
Científico
Leporinus sp.
Eugerus
brasiliensis.
Mylossoma spp
-
Hábito
Alimentar
Onívoro
Detritívoro
Onívoro
N
Média
(g/g)
Desvio
Padrão
(g/g)
Mínimo
(g/g)
Máximo
(g/g)
20
0,13
0,04
0,10
0,19
14
0,14
0,04
0,10
0,26
22
56
0,06
0,01
0,04
0,09
Tabela 04: Média dos resultados de Metil-mercúrio nas espécies de peixes não
carnívoros mais consumidos da comunidade Barreiras/Itaituba.
Nome
Popular
Aracu
Caratinga
Pacu
Total
Nome
Científico
Leporinus sp.
Eugerus
brasiliensis.
Mylossoma
spp
-
Hábito
Alimentar
Onívoro
Detritívoro
Onívoro
N
Média
(g/g)
Desvio
Padrão
(g/g)
Mínimo
(g/g)
Máximo
(g/g)
20
0,08
0,15
0,06
0,09
14
0,11
0,03
0,07
0,14
22
0,03
0,01
0,01
0,06
56
As concentrações de Hg total nas espécies carnívoras apresentaram média
de 0,76 g/g, acima do permitido pela ANVISA (0,5g/g) e abaixo do preconizado
pela OMS (1g/g), com variação de 0,40 a 2,33g/g, enquanto que as espécies não
carnívoras apresentaram valores abaixo dos índices preconizados pela OMS
(0,5g/g) com média de 0,10 g/g, variando entre 0,04 e 0,26 g/g. Das espécies de
peixes carnívoras estudadas 10 espécimes em torno de 14%, apresentaram teores
de Hg T acima do que é preconizado pela OMS.
Do grupo das espécies não carnívoras as referidas pela população como
mais consumidas foram: aracu (36,0%), caratinga (23,8%), pacu (27,8%) e outros
12,4%. Neste estudo, as espécies de peixes, classificadas genericamente como não
carnívoros, apresentaram diferenças significativas nos teores de HgT no tecido
muscular, sendo inferiores quando comparados com as espécies de peixes
carnívoros.
Quando comparado a concentração média de metil-mercúrio em relação a
mercúrio total foi obtido um valor de 78,72%.
A metodologia apresentou também excelente reprodutibilidade e a sua
recuperação analítica foi de 93,68% para a amostra de peixe de referência
certificada DORM 2, conforme Tabela 05.
Tabela 05 - Recuperação analítica para determinação de mercúrio em peixes de
barreiras a partir de amostra de referência certificada DORM 2.
Referência
Certificada
Concentração
Certificada
N
Recuperação
(%)
Desvio
Padrão
DORM 2
2,91 g/g de Hg
14
93,68
0,15
CONCLUSÕES
Os resultados obtidos neste estudo, apesar de não serem conclusivos,
indicam que a população pesquisada da comunidade Barreiras, município de
Itaituba/PA, encontra-se seriamente exposta a elevadas concentrações de Hg total e
metil-mercúrio pelo consumo de peixes.
O uso do mercúrio na atividade garimpeira deve ser controlado, de forma
que se evite a sua emissão para o ambiente. Campanhas de saúde pública podem
providenciar orientação às populações quanto ao consumo de pescado, de acordo
com os níveis de concentração de mercúrio nas diferentes espécies ictiológicas.
Contudo, apesar do pescado amazônida apresentar teores significativos de
mercúrio total, não foram registrados sinais ou sintomas de distúrbio neurológicos
relacionados ao metal pesado e sua forma orgânica (metilmercúrio). Com isso, são
necessários mais estudos e monitoramento das áreas impactadas ou sem registro
de emissão mercurial, objetivando se estabelecer valores de concentração mercurial
considerados “normais” para a região Amazônica (FAIAL, 2005).
REFERÊNCIAS BIBLIOGRÁFICAS
AGENCY FOR TOXIC SUBSTANCES AND DISEASES REGISTRY (ATSDR).
Toxicological profile for selenium. U.S. Department of Health and Human Services.
Atlanta; 2003. 457 pp.
AHLMARK, A. 1948. Poisoning by Methyl Mercury Compounds. Brit J Ind Med 5,
117-119.
AKAGI, H.; MALM, O.; BRANCHES, F. J. P. Human exposure to mercury due to gold
mining in the Tapajós river basin, Amazon, Brazil: Speciation of mercury in human
hair, blood and urine. Water air and soil pollution, v. 80, p. 85-94, 1995.
AKAGI, H. (1998). Studies on mercury pollution in the Amazon, Brazil. Global
Environmental Research. 2(2):193-202.
ATSDR – Agency for Toxic Substances and Disease Registry. Toxicological profile
for mercury. Março-1999.
BARTELL, S.M., PONCE, R.A., SANGA, R.N. AND FAUSTMAN, E.M. 2000. Human
Variability in Mercury Toxicokinetics and Steady State Biomarker Ratios. Environ Res
84, 127–132.
BLOOM, N.S., 1992. On the chemical form of mercury in edible fish and marine
invertebrate tissue. Can J Fish Aquat Sci 49, 1010-1017.
BRABO, E. S.; SANTOS, E. C. O.; JESUS, I. M.; MASCARENHAS, A. F. S.; FAIAL,
K. R. F. Mercury contamination of fish and exposure of an indigenous community in
Pará state - Brazil. Environmental Research, Maryland, v. 84, p. 197-203. 2000.
BRANCO, V.R.V.N., 2012. In vivo Mercury Interaction with the Thioredoxin System.
Tese de Doutorado. Faculdade de Farmácia – Universidade de Lisboa.
BRANCO, V., VALE, C., CANÁRIO, J. AND SANTOS, M.N. 2007. Mercury and
Selenium in Blue Shark (Prionace glauca, L.1758) and Swordfish (Xiphias gladius,
L.1758) from two areas of the Atlantic Ocean. Environ Pollut 150, 373-380.
CLARKSON, T.W. AND MAGOS, L. 2006. The Toxicology of Mercury and Its
Chemical Compounds. Crit Rev Toxicol 36, 609-662.
CLARKSON, T.W. VYAS, J.B. AND BALLATORI, N. 2007. Mechanisms of Mercury
Disposition in the Body. Am J Ind Med 50, 757–764.
CONSELHO NACIONAL DE SAÚDE (CNS) Resolução nº 196 de 10 de Outubro de
1996.
DOI, R. AND TAGAWA, M. 1983. A Study on the Biochemical and Biological
Behavior of Methylmercury. Toxicol Appl Pharm 69, 407–416.
FAIAL, K.R.F.; SANTOS, E.C.O.; BRABO, E.S.; SÁ, G.C.; JESUS, I.R.M.; LIMA,
M.O.; MENDES, R.A.; MASCARENHAS, A.F.S. Mercure levels in fish of Trombetas
river in low Amazon área and área out of the influence of gold mining. Cadernos
Saúde Coletiva, v.13, n. 1, p. 237-248, Rio de Janeiro, 2005.
IBGE, Biblioteca. Itaituba– Pará (PA). Documentação Territorial do Brasil. 2014.
MICARINI, R. C. C. M.; BUENO, M. I. M. S., JARDIM, W.F. Compostos de mercúrio.
Revisão de métodos de determinação, tratamento e descarte. Química Nova, São
Paulo, v. 23, n.4, p. 487 – 495, 2000.
NAGAMUNA, A., ISHII, Y. AND IMURA, N. 1984. Effect of Administration Sequence
of Mercury Chloride and Sodium Selenite on their Fates and Toxicities in Mice.
Ecotox Environ Safe 8, 572-580.
ROOS, D.H, ROBSON LUIZ PUNTEL, R.L., LUGOKENSKI,, T.H., INEU, R.P.,
BOHRER, D., BURGER, M.E., FRANCO, J.L., FARINA, M., ASCHNER, M., ROCHA,
J.B.T. AND BARBOSA, N.B.V. 2010. Complex Methylmercury–Cysteine Alters
Mercury Accumulationin Different Tissues of Mice. Basic Clin Pharmacol 107, 789792.
SANTOS, E. C. O. Enquêtes sanitaites et contaminations mercurielles en Amazonie
brésilienne In: CARMOUZE, J; LUCOTTE, M.; BOUDOU, A. (Coord.). Le Mercure
en Amazonie. Paris : Institut de Recherche pour le Développement (IRD), p.
347-372. 2001.
SANTOS, E. C. O.; JESUS, I. M.; BRABO, E. S.; LOUREIRO, E. C. B.;
MASCARENHAS, A. F. S.; WEIRICH, J.; CÂMARA, V. M.; CLEARY, D. Mercury
exposure in riverside Amazon communities in Pará, Brazil. Environmental
Research, Meryland, v. 84, p. 100-107. 2000.
SATOH, H. 2000. Occupational and Environmental Toxicology of Mercury and its
Compounds. Ind Health 38, 153-164.
STATISTIC, Release 7.0 for windows, Tulsa, Usa, 2004.
TENUTA-FILHO, A.; NASCIMENTO, E.S. Review: Mercury in shark. Occurrence and
possibility of removal. Brazilian Journal of Food Technology, Campinas, v.10, n.2,
p.78-85, 2007.
WHO (1976). Environmental Health Criteria 1: Mercury - Geneva, World Health
Organization. p132.
WHO (1989). Environmental Health Criteria 86: Mercury - Environmental Aspects,
Geneva, World Health Organization. 150p.