Daniela Mota Gonçalves
Doença Inflamatória Intestinal crônica:
relato de caso
Niterói/RJ
2013
Daniela Mota Gonçalves
Doença Inflamatória Intestinal crônica:
relato de caso
Monografia apresentada como requisito final à obtenção do
Título de Especialista no Curso de Pós-Graduação,
Especialização em Clínica e Cirurgia de Pequenos Animais,
da Equalis, orientada pela Prof. MSc. Sylvia Cristina Silva
de Azevedo.
Niterói/RJ
2013
Daniela Mota Gonçalves
Doença Inflamatória Intestinal crônica:
relato de caso
Monografia apresentada como requisito final à obtenção do
Título de Especialista no Curso de Pós-Graduação,
Especialização em Clínica e Cirurgia de Pequenos Animais,
da Equalis, orientada pela Prof. MSc. Sylvia Cristina Silva
de Azevedo.
Niterói/RJ, 11 de junho de 2013
_______________________________________
- Sylvia Cristina Silva de Azevedo -
Niterói/RJ
2013
Dedicatória
Aos meus pais e irmãs por tudo que sou hoje.
Ao meu marido pela compreensão, paciência e apoio.
Agradecimentos
Agradeço à minha família, por tudo que sou. Não tenho palavras pra descrever o
quanto sou grata por tudo. Nos momentos mais difíceis a nossa união nos deu a força de
continuar em frente. E vocês sempre me mostram o caminho!
Ao Carlos, que teve a grande compreensão pela minha ausência nos finais de semana
de pós-graduação. TE AMO!!!
Aos meus amigos e padrinhos Marcela e Pedro que também compreenderam a minha
ausência. Em especial a Nina, que nos trará eterna alegria.
A minha Orientadora, Sylvia pelos ensinamentos, pela paciência, companheirismo e
mais do que tudo, pela amizade. Ao Mauricio, obrigada por fazer minha amiga feliz.
Obrigada por existirem!
A toda Equipe da Animália que acreditou em mim desde o início. Em especial,
obrigada aos padrinhos Jaqueline, Renato e Ana Carolina por tudo!
A amiga Priscila, sempre presente e que me incentivou a ingressar nessa jornada.
A Duda e a Tchatcha, que contribuem diariamente na minha formação profissional e
me fazem entender o que é ser proprietária.
A Raquel, por me ajudar nessa jornada.
A todos os amigos que fazem parte da minha vida e me mostram que nada é por acaso!
“Toda grande caminhada começa com um primeiro
passo. Então, não espere um momento ideal, uma
pessoa ideal, um local ideal, uma ferramenta ideal ou
uma ideia ideal para começar sua caminhada (seu
trabalho). As ferramentas são muitos úteis, contudo,
quando damos mais ênfase às ferramentas, acabamos
perdendo o foco, o objetivo da caminhada. Logo,
antes de sair de casa tenha em mente um objetivo
claro e um plano bem definido. Contudo, pode ser que
seu objetivo e consequentemente seu plano mude.
Entretanto, perceba que eles nunca deixam de existir
nas caminhadas bem sucedidas.”
Robson Feitosa
Resumo
A doença inflamatória intestinal crônica é uma patologia imunomediada que pode
causar diarreia, vômitos, perda de peso e hematoquezia por mais de 3 a 4 semanas. Seu
diagnóstico é feito através da histopatologia de fragmentos de estômago e intestino, que
podem ser coletados por endoscopia ou por laparotomia exploratória. O objetivo deste
trabalho foi relatar o caso de um cão, fêmea, Labrador Retriever, 8 anos com gastrite
linfocítico-plasmocitária cujos sintomas de vômito e diarreia persistentes, anorexia, perda
progressiva de peso e hematoquezia persistiam cerca de 8 meses. O paciente foi submetido à
corticoterapia já que não teve boa resposta a outros imunossupressores.
Palavras-chave: vômito, diarreia, histopatologia.
Lista de Ilustrações
Figura 1 – Segmento intestinal com arquitetura ultrassonográfica normal (seta
preta). Segmento intestinal com discreto espessamento em submucosa e discreta
perda de definição de arquitetura parietal (seta branca).
7
Figura 2 – Segmento intestinal com paredes muito espessas, hipoecoicas, com perda
de arquitetura. Segmento intestinal com moderado espessamento em camada
muscular (seta branca).
7
Figura 3 – Visão endoscópica do estômago: A e B, evidenciando coloração e
aspecto normais de mucosa. C, D, E e F, evidenciando mucosa de aspecto
hiperêmico e com pontos de hematina (seta branca).
8
Figura 4 – Visão endoscópica do duodeno: A, evidenciando coloração e aspecto
normais de mucosa. B e C, evidenciando mucosa de aspecto granuloso e
hiperêmico (seta branca).
9
Sumário
Introdução .........................................................................................................................
1 Revisão de literatura .....................................................................................................
1.1 Etiopatogenia ..........................................................................................................
1.2 Classificação ...........................................................................................................
1.3 Sinais clínicos .........................................................................................................
1.4 Diagnóstico .............................................................................................................
1.4.1 Exames laboratoriais ......................................................................................
1.4.2 Exame coproprasitológico ..............................................................................
1.4.3 Ultrassonografia .............................................................................................
1.4.4 Endoscopia .....................................................................................................
1.4.5 Histopatologia ................................................................................................
1.4.6 Radiologia ......................................................................................................
1.5 Diagnóstico diferencial ...........................................................................................
1.6 Tratamento ..............................................................................................................
1.7 Prognóstico .............................................................................................................
2 Relato de caso ...............................................................................................................
3 Resultados e Discussão .................................................................................................
Conclusão ..........................................................................................................................
Referências bibliográficas .................................................................................................
1
2
2
3
4
5
5
5
6
8
9
10
10
10
14
15
16
17
19
1
INTRODUÇÃO
A Doença inflamatória intestinal crônica é um distúrbio gastroentérico
caracterizado pela infiltração de células inflamatórias (linfócitos e plasmócitos) na mucosa o
trato gastrointestinal (GUILFORD, 1996; JERGENS, 1996). Os sinais clínicos mais
frequentes são vômitos e diarreia crônica, perda de peso, anorexia, alterações no apetite e
hematoquezia. (RICART, 2012; TAMS, 2005). Consideram-se como sinais crônicos aqueles
que persistem por mais de três semanas (CLASCON, 2011).
A sua etiologia ainda é desconhecida, mas acredita-se que ocorre uma complexa
interrupção na homeostasia do microambiente da mucosa intestinal em indivíduos
geneticamente predispostos, ocasionando uma resposta imune agressiva (linfócitos T) as
bactérias existentes no trato gastrointestinal (BALFOUR, 2006) .
O diagnóstico da enfermidade é realizado com base na exclusão de todas as outras
causas possíveis de infiltração inflamatória na mucosa intestinal.
Por isso torna-se
indispensável uma anamnese criteriosa do paciente, observando atentamente a alimentação e
o uso de medicamentos já administrados (MAGALHÃES, 2008). Excluídas as causas, o
diagnóstico histopatológico é essencial e seus fragmentos podem ser obtidos através de
endoscopia ou laparotomia exploratória (JERGENS et al, 2003)
O presente estudo tem como objetivo relatar o caso de um cão com doença
inflamatória gastrointestinal crônica já que seus sinais clínicos são rotineiramente observados
na clínica médica de pequenos animais, fato que reforça a necessidade de um diagnóstico
preciso e tratamento eficiente.
2
1 REVISÃO DE LITERATURA
1.1 Etiopatogenia
A DIIC é um grupo de afecções gastrointestinais crônicas e idiopáticas,
determinadas pela presença de infiltrados difusos de células inflamatórias na mucosa do trato
gastrointestinal. Trata-se de uma síndrome caracterizada pela resposta exacerbada e
descontrolada do trato digestório a uma estimulação antigênica normal, e deve ser
diferenciada do processo inflamatório normal em consequência à exposição excessiva a
antígenos. Sugere-se que seja resultante de uma resposta imunológica citopática, devido a um
desafio antigênico crônico (JUNIOR, 2003).
Ainda não se elucidou uma etiologia definitiva para a DIIC, portanto, é
considerada como um processo de origem não determinado (JUNIOR, 2003).
As teorias sobre as causas potenciais incluem doença imunomediada, defeitos de
permeabilidade do trato gastroentérico (TGI), intolerância ou alergia dietética, influência
genética, influência psicológica e doença infecciosa segundo Crystal (2006). E de acordo com
Junior (2003) os fatores predisponentes da DIIC incluem infecções bacterianas
(Campylobacter sp.), quadros parasitários (Giardia sp.), neoplasias (linfoma), e quadros
alérgicos ou de intolerância alimentar sitiados no TGI, bem como, pancreatite, colangiohepatite e hipertireoidismo.
A resposta a esses estímulos antigênicos ocorre mediante um influxo de células
inflamatórias (linfócitos, plasmócitos, macrófagos, neutrófilos ou eosinófilos) na mucosa,
cuja gravidade e extensão podem variar consideravelmente, o que explica as diferentes
manifestações clínicas. As camadas muscular e serosa não apresentam envolvimento
significante na maioria das vezes (JUNIOR, 2003).
Pesquisadores identificaram um desequilíbrio no perfil normal de citocinas em
pacientes afetados com DIIC e especulam que este desequilíbrio pode contribuir com a
patologia da mesma. A motilidade intestinal seria afetada pela inflamação, uma vez que
citocinas liberadas dos imunócitos poderiam alterar a função neural ou do músculo liso
entérico, resultando em motilidade anormal (KRECIC, 2001). Existem indícios de que seja
uma afecção causada pelo próprio sistema imunológico, que se torna a principal causa dos
danos teciduais observados nesses pacientes. Essa afirmativa tem como base a falta de
3
detecção de agentes infecciosos na etiologia desses processos, bem como, uma boa resposta
terapêutica às drogas anti-inflamatórias e imunossupressoras (JUNIOR, 2003).
Segundo Junior (2003) os processos inflamatórios situados nas alças tornam-se
permanentes através da perda de integridade da mucosa, com consequente alteração de
permeabilidade, o que permite que microrganismos da própria microbiota entérica e antígenos
(proteínas da dieta) adentrem a lâmina própria, estimulando e intensificando as respostas
imunes já iniciadas.
Para Crystal (2006) a síndrome clínica da DIIC possui sinais do TGI persistentes
(com mais de três semanas de duração), respostas incompletas aos ensaios dietéticos ou
terapêuticos empíricos de rotina, incapacidade de encontrar outras causas para a inflamação
do TGI, lesões histológicas de inflamação da mucosa, e responsividade geral à intervenção
imunoterapêutica.
A DIIC é descrita principalmente em animais de meia idade a avançada, mas pode
afetar também cães e gatos jovens (LEICONDRE, 2004).
1.2 Classificação
A DIIC é classificada segundo Crystal (2006) de acordo com o tipo de infiltrado
celular inflamatória na parede intestinal. O tipo mais comum é a gastroenterite e/ou a colite
linfocítico-plasmocítica. Outras formas menos comuns de DIIC incluem gastroenterite e/ou
colite eosinofílica, granulomatosa, supurativa (neutrofílica) e histiocítica.
Para os gatos o segundo tipo mais importante de DIIC é a enterite eosinofílica.
Nestes animais, as células inflamatórias localizadas dentro da lâmina própria do intestino são
os eosinófilos. Pressupõe que isso pode ser resultado de reação imunológica a parasitas ou a
dieta. A síndrome hipereosinofílica é uma enfermidade rara em gatos, e designa uma situação
hematológica inespecífica que se caracteriza por eosinofilia acentuada persistente. Essa
condição sanguínea acarreta em doença sistêmica concomitante e está associada a
parasitismo, doenças fúngicas, reações de hipersensibilidade e neoplasias (FIGHERA, 2004).
É necessária confirmação histopatológica para diferenciá-las. A histopatologia
também determinará a gravidade das lesões através da intensidade do infiltrado celular; tipo
de epitélio do segmento envolvido; arquitetura de vilosidades, criptas e glândulas; além de
outras alterações inflamatórias observadas no tecido (JUNIOR, 2003).
4
1.3 Sinais Clínicos
A DIIC pode apresentar diversos sinais clínicos, sendo o mais comum o vômito
intermitente crônico. Outros sinais observados incluem perda de peso, anorexia e diarreia.
Alguns animais podem apresentar início súbito dos sinais clínicos; os quadros eméticos são
normalmente intermitentes, com evolução de semanas, meses ou anos. Na medida em que o
quadro progride, a frequência dos episódios aumenta e outras manifestações clínicas passam a
ser notadas. Ressalta-se que não há correlação entre vômito e o momento da ingestão de
alimento e/ou água. (FEIJÓ, 2008)
Quando há comprometimento do cólon, a hematoquezia, tenesmo, presença de
material sólido e muco nas fezes são sinais encontrados com frequência. Outros sinais ainda
podem ser observados como flatulência, borborigmos, halitose, poliúria, polidpsia e mudanças
de comportamento como excitação, agressividade, ansiedade e defecação em locais não usuais
(JUNIOR, 2003).
No exame físico a palpação as alças intestinais podem estar espessadas e a diarreia
ocorre com mais frequência, em fases mais tardias da doença, podendo manifestar-se de
forma aguda ou crônica, sendo a última intermitente ou intratável. As características das fezes
são normalmente de processos que ocorrem no intestino delgado, variando de macias a
aquosas, podendo haver esteatorreia.(WASHABAU, 2010).
O apetite nesses pacientes é bem variável e pode não haver nenhum tipo de
alteração, porém, extremos podem ser observados, como anorexia ou polifagia. Quando se
observa, num mesmo paciente, a concomitância de polifagia, perda de peso e diarreia,
primeiramente deve-se realizar o diagnóstico diferencial entre DIIC, hipertireoidismo e
insuficiência pancreática exócrina, sendo esse último pouco frequente em felinos (JUNIOR,
2003).
Gatos com síndrome hipereosinofílica podem manifestar mal-estar, diarreia
sanguinolenta, tosse e anormalidades dermatológicas (BURROWS et al., 1997).
5
1.4 Diagnóstico
1.4.1 Exames Laboratoriais
Os exames laboratoriais (hematologia, bioquímica sérica e urinálise) raramente
tem alterações que apontem um diagnóstico, mas podem oferecer indicação da gravidade do
processo patológico. Achados como eosinofilia podem estar relacionados com parasitismo e a
hipoalbuminemia pode indicar perda desta protreína pelo lúmen intestinal (BURROWS et al.,
1997).
Os dados laboratoriais irão auxiliar na exclusão de alguns diagnósticos
diferencias, por exemplo, diabetes mellitus, onde é comum observar hiperglicemia, glicosúria
e densidade urinária baixa; doenças hepáticas, as quais cursam com hiperbilirrubinemia,
redução dos níveis séricos de uréia, aumento da atividade sérica das enzimas hepáticas e
bilirrubinúria; doença renal crônica, caracterizada pelo nitrogênio urêico plasmático e
creatinina elevados e densidade urinária baixa; e também pelo hipertireoidismo, na qual a
tiroxina total, ALT e/ou FA séricas estão elevadas, leve aumento no hematócrito e densidade
urinária baixa (CRYSTAL, 2006).
1.4.2 Exame coproparasitológico:
O exame fecal é parte importante no diagnóstico de afecção intestinal, devendo
ser rotineiro em qualquer paciente com distúrbios do TGI (BURROWS et al., 2004).
Porém, como esses exames nem sempre podem detectar parasitas, se recomenda o
tratamento empírico contra esses agentes. (GERMAN, 2005)
Um exame coproparasitológico deve ser realizado para a exclusão da presença de
possíveis parasitas. As amostras fecais podem ser enviadas para cultura de Salmonella sp.,
Campylobacter sp. e teste de sensibilidade,
principalmente nos gatos com diarreia. As
amostras devem ser submetidas em meio especial (meio de selenito ou tetrationato), pois os
altos números de bactérias entéricas normais presentes nas fezes tendem a crescer
excessivamente e mascarar o crescimento da Salmonella sp. e do Campylobacter sp.
(CRYSTAL, 2006).
6
1.4.3 Ultrassonografia
O exame ultrassonográfico pode indicar se há ou não a presença de alteração do
TGI, se essa alteração é localizada ou difusa, além de descartar outras doenças que causem
sinais digestivos.
A ecogenicidade e a linfonodomegalia são mais importantes que o
espessamento da mucosa intestinal para indicar inflamação (RICART, 2012).
A aparência ultrassonográfica das doenças inflamatórias gastrointestinais varia
com o tipo, duração e extensão do processo. O espessamento da parede do TGI é o achado
sonográfico mais frequente. O estudo da distribuição, simetria, extensão e arquitetura das
camadas parietais nas lesões é um critério útil na diferenciação entre processos inflamatórios e
neoplásicos (FROES, 2004).
A inflamação tem sido caracterizada por um espessamento mais extenso, com a
estratificação das camadas parietais preservadas, ou seja, as camadas apresentam-se bem
diferenciadas, com nítido predomínio da visualização da camada submucosa. Nas neoplasias o
espessamento tende a ser localizado, com marcante perda da estratificação das camadas
(FROES, 2004).
Nas enterites, a grande importância e indicação do exame ultrassonográfico esta
na exclusão dos processos neoplásicos, uma vez que os sinais clínicos nas duas enfermidades
são muitos semelhantes. As enterites inflamatórias, como as enterites linfocíticasplasmocíticas, caracterizam-se sonograficamente por espessamento leve (4 a 5mm) e muitas
vezes difuso. Quando só alguns segmentos estão afetados, apresentam-se com hipomotilidade,
rígidos e com uma pequena dilatação fluida ou alimentar, pode ocorrer evidenciação da
camada submucosa decorrente de fibrose (FROES, 2004).
7
Figura 1: Segmento intestinal com arquitetura ultrassonográfica normal (seta preta).
Segmento intestinal com discreto espessamento em submucosa e discreta perda de definição
de arquitetura parietal (seta branca).
(Fonte: IEMEV)
Figura 2 : Segmento intestinal com paredes muito espessas, hipoecoicas, com perda de
arquitetura. Segmento intestinal com moderado espessamento em camada muscular (seta
branca).
(Fonte: IEMEV)
De acordo com Froes (2004), deve-se considerar a importância de se realizar o
exame ultrassonográfico em animais de meia-idade com histórico de hiporexia, vômitos e/ou
diarreia crônicos; sendo que o objetivo principal do exame nesses pacientes não é evidenciar
8
as alterações sonográficas de processos inflamatórios gastroentéricos e sim descartar os
processos neoplásicos.
1.4.4 Endoscopia
A possibilidade de observação direta juntamente com a obtenção de amostras
teciduais de esôfago, estômago e trato intestinal, de maneira minimamente invasiva,
incrementou o diagnóstico clínico e aumentou a precisão do tratamento das doenças do
sistema digestivo (TAMS, 1999).
A laparotomia exploratória é indicada quando não há o alcance do endoscópio
para obter amostras da região intestinal atingida (WASHABAU, 2010).
Figura 1: Visão endoscópica do estômago: A e B, evidenciando coloração e aspecto normais
de mucosa. C, D, E e F, evidenciando mucosa de aspecto hiperêmico e com pontos de
hematina (seta branca).
PEQUENA CURVATURA
PREGAS GÁSTRICAS
PEQUENA CURVATURA
hematina
B
A
C
CORPO GÁSTRICO
PILORO
CORPO GÁSTRICO
Erosões / edema
Edema
D
Hematina
E
F
(Fonte: Ana Lúcia)
9
Figura 2: Visão endoscópica do duodeno: A, evidenciando coloração e aspecto normais de
mucosa. B e C, evidenciando mucosa de aspecto granuloso e hiperêmico (seta branca).
DUODENO
DUODENO
DUODENO
aspecto granuloso
hiperemia
A
B
C
(Fonte: Ana Lúcia)
1.4.5 Histopatologia
O diagnóstico definitivo somente pode ser determinado por meio de exames
histopatológicos e/ou citopatológicos de fragmentos intestinais obtidos por biópsia. As
biópsias podem ser coletadas por meio de endoscopia, laparotomia exploratória ou, no caso de
espessamento intestinal focal ou difuso maior do que 2 a 3cm guiadas por ultrassom. A
histopatologia pode revelar DIIC, linfoma alimentar, Cryptosporidium sp. e/ou gastrite por
Helicobacter sp.. O linfoma alimentar só pode ser diferenciado da DIIC por meio de
histopatologia, uma vez que os sinais clínicos são idênticos (CRYSTAL, 2006)
Segundo Wilson (2008) é importante ressaltar que os fragmentos de biópsia
devem ser colhidos, preferencialmente, por laparotomia exploratória, pois tal método permite
a colheita de todas as camadas do órgão envolvido. Os outros métodos de colheita de biópsia,
como endoscopia e/ou guiado por ultrassom não são capazes de coletar todas as camadas,
sendo que o linfoma pode estar presente em qualquer camada intestinal.
As alterações encontradas no exame histopatológico são: número aumentado de
células inflamatórias na lâmina própria, número aumentado de linfócitos intraepiteliais,
estrutura alterada da mucosa como fusões das vilosidades ou atrofia, edema e fibrose. A
submucosa não é frequentemente afetada nesta patologia, exceto em casos agressivos como
enterites eosinofílica e granulomatosa (KRECIC, 2001).
10
1.4.6 Radiologia
As radiografias contrastadas de trato GI raramente são úteis para o diagnóstico das
doenças crônicas do TGI. Elas consomem bastante tempo, são difíceis de serem realizadas e
interpretadas e raramente revelam um diagnóstico. Mesmo quando existem lesões, a biópsia
do TGI e a histopatologia são necessárias para um diagnóstico preciso (CRYSTAL, 2006).
Os achados radiográficos não são específicos para DIIC, mas são de grande valia
para descartar processos obstrutivos e alterações na motilidade (JUNIOR, 2003).
1.5 Diagnóstico diferencial
Todos os diagnósticos diferenciais devem ser excluídos antes de se fazer um
diagnóstico de DIIC. Muitas outras doenças são semelhantes clinicamente à esta enfermidade,
e pelo fato do TGI responder aos insultos de diversas causas por meio de inflamação, uma
biópsia sem a exclusão de outros diagnósticos diferenciais não constitui um diagnóstico de
DIIC. Para realização de um diagnóstico preciso de DIIC, todos os diagnósticos diferenciais
devem ser excluídos e as células inflamatórias devem ser observadas no interior da mucosa do
TGI, por meio do exame histopatológico dos fragmentos obtidos. Outras alterações
histopatológicas, como por exemplo, atrofia ou fusão das vilosidades, separação das criptas
com edema, fibrose ou necrose da mucosa,achatamento epitelial e vasos linfáticos dilatados
ajudam a apoiar o diagnóstico de DIIC (CRYSTAL, 2006).
1.6 Tratamento
A doença intestinal inflamatória crônica na sua terapêutica inclui o controle
dietético, a suplementação com fibras e a administração de drogas anti-inflamatórias e
imunossupressoras. É importante que a escolha da terapêutica a ser aplicada no paciente seja
individual, com base na correlação entre os sinais clínicos apresentados, achados
laboratoriais, alterações histológicas, resposta à terapia escolhida, bem como gravidade e
variedade dos efeitos colaterais das drogas, aceitabilidade das mesmas pelo paciente,
cooperação do proprietário e custos gerais do tratamento (JUNIOR, 2003).
Para maximizar a resposta clínica do paciente devemos associar à terapia
farmacológica com a mudança da dieta, pois desta forma, minimizamos a ação do sistema
imune sobre o trato digestório, e simultaneamente reduzimos sua exposição a antígenos,
11
interrompendo a amplificação e a sequência da doença inflamatória. A grande maioria dos
felinos apresenta uma boa resposta terapêutica a esse sinergismo, e uma vez em remissão, a
doença pode ser controlada através da dieta, o que faz com que o tratamento de manutenção
seja de grande importância (BRIDGEFORD, 2008).
O manejo dietético é bastante favorável. Animais com quadros de enterite
requerem dietas hipoalergências ou de eliminação. Tendo em vista, além da oferta de
nutrientes, reduzir a carga de alérgenos no alimento (componentes nutricionais e/ou aditivos),
a fim de minimizar a estimulação antigênica nas alças já inflamadas (JUNIOR, 2003).
A dieta é uma parte importante da terapêutica em todas as formas de DIIC. Deve
ser estabelecida uma dieta altamente digerível, facilmente assimilável e reduzida em conteúdo
de gordura. As dietas à base de uma fonte de proteínas diferentes ou parcialmente hidrolisadas
e a inclusão de fibras fermentáveis (frutooligossacarídeos) também podem trazer beneficio
para alguns pacientes (MANSIFIELD, 2011).
De acordo com Junior (2003) dietas caseiras de eliminação podem ser compostas
de carne de carneiro, cabrito, coelho ou frango, queijo cottage, arroz, batata e/ou macarrão,
com adição de óleo vegetal, vitaminas de complexo B, vitamina K, fosfato dicálcico e taurina
(200 a 500mg por refeição). Caso o animal permaneça se alimentado de dieta caseira, a
mesma deve ser formulada pelo veterinário.
A suplementação com ácidos graxos do tipo ômega-3 é benéfica, pois tais ácidos
graxos possuem efeitos anti-inflamatórios sobre o TGI (CRYSTAL, 2006).
Nos casos de colite, os gatos apresentam boa resposta terapêutica à administração
de fibras insolúveis. O papel das fibras na dieta é a normalização da motilidade. Caso o
animal rejeite rações com alto teor de fibras, pode-se administrar uma dieta hipoalergênica
com suplementação de Psyllium plantago, na dose de duas colheres de chá por refeição, ou
ainda farelo de aveia na dose de uma colher de sobremesa por refeição (JUNIOR, 2003).
Segundo Crystal (2006) abóbora enlatada também pode ser fonte de fibra,
administrada por via oral misturada ao alimento, na quantidade de 1 a 2 colheres de chá a
cada 12 a 24 horas.
O segredo para o manejo alimentar é a flexibilidade e persistência, já que algumas
vezes, várias dietas tenham sido testadas. O paciente deve ser submetido a uma dieta
específica, sem a oferta de qualquer outro item alimentar, por um período mínimo de seis a
nove semanas, para se verificar os resultados. Devido ao alto custo das formulações
12
comerciais, os proprietários preferem adotar a dieta caseira, sobretudo, na maioria das vezes,
estas possuem um balanceamento desfavorável sendo incompletas nutricionalmente
(JUNIOR, 2003).
Os principais fármacos utilizados atualmente são os salicilatos, os corticosteróides
e os antibióticos com efeito anti-inflamatório, como metronidazol e tilosina. Nas enterites ou
enterocolitesplasmocitárias, linfocitárias ou eosinofílicas com intenso infiltrado celular, por
vezes torna-se necessária a associação de fármacos imunossupressores, como a azatioprina,
em combinação com os corticosteróides e antibióticos (ANDRADE, 2008).
O manejo do paciente com DIIC e as combinações de fármacos a serem
empregadas, assim como suas dosagens, devem sempre ser individualizados de acordo com a
gravidade da doença e dos sinais clínicos, a tolerância do paciente e a resposta ao tratamento
(ANDRADE, 2008).
A prednisolona ou prednisona tem sido o fármaco de eleição no tratamento inicial
da DIIC e sua a dose inicial é 1-2mg/Kg a cada 12 horas, com redução da mesma a cada duas
a quatro semanas. Em alguns pacientes a redução pode chegar a uma manutenção terapêutica
a cada 48 horas, ou até a eliminação total da medicação(RICART, 2012). Gatos que não
respondem adequadamente a doses crescentes da prednisolona podem ser tratados com
dexametasona na dose de 0,3 a 0,5mg/kg/dia por via oral. O acetato de metilprednisolona na
dosagem de 20mg/gato por via subcutânea ou intramuscular pode ser usado em gatos a cada
15 a 30 dias como terapêutica de manutenção ou quando o proprietário não consegue medicar
o animal de maneira adequada. Porém, não é uma boa alternativa como terapêutica única em
animais com grave inflamação (ANDRADE, 2008).
Sinais iatrogênicos de hiperadrenocorticismo podem ocorrer em muitas ocasiões,
mas cessam com a diminuição da dose do corticosteróide (MANSFIELD, 2011).
A budesonida, um corticosteróide administrado por via oral e fracamente
absorvido sistemicamente, pode ser usado na dose de 1mg/gato a cada 12 a 24 horas, porém
existem apenas relatos informais sobre a eficácia deste em pacientes felinos, sendo
necessários estudos adicionais para determinar a eficácia da dose (CRYSTAL, 2006).
De forma geral, os corticosteróides diminuem a exsudação que resulta em perda
de proteínas para o lúmen intestinal e melhoram a circulação e absorção nos enterócitos,
reduzindo essas perdas. Além disso, tendem a melhorar o apetite do animal e fazer com que
ele se sinta melhor. Os corticosteróides devem sempre ser usados com cautela, buscando-se a
13
menor dose eficaz e a associação com outros fármacos que permitam o controle dos sinais
clínicos por longos períodos com menor risco ao paciente (ANDRADE, 2008).
Segundo Junior (2003), há de se fazer algumas observações quanto à
corticoterapia. Apesar dos bons resultados observados, não se recomenda sua instituição
previamente à biópsia, uma vez que pode vir a conduzir o clínico a alguns erros de
abordagem. O primeiro deles se refere ao fato de que os linfomas alimentares são sensíveis
aos corticosteróides, e iniciando sua administração precocemente, podemos determinar uma
resistência tumoral a uma das principais drogas envolvidas em seu protocolo terapêutico.
A Sulfasalazina é o medicamento de escolha para a colite linfocíticoplasmocitária. Libera ácido 5-aminosalicílico no cólon provocando efeitoanti-inflamatório
local. Inicia-se a sulfasalazina na dose de 15mg/kg, via oral a cada 24h, durante 3 semanas.
Em seguida, reduzir a dose para 7,5mg/kg, via oral a cada 24h, durante 1 mês e, depois
suspender a medicação se a remissão clínica ocorrer. Se os sinais clínicos recorrerem após a
interrupção do tratamento, deve-se manter o gato na menor dose eficaz durante 2 meses e
tentar suspender a terapêutica novamente. Alternativamente, a preparação de olsalazina pode
ser usada na dose de 5-10mg/kg a cada 24h, sendo a duração e redução iguais às da
sulfasalazina (CRYSTAL, 2006).
De acordo com Andrade (2008), os gatos usualmenterespondem bem ao
tratamento com corticosteróides, sendo o uso da sulfasalazina nessa espécie reservado aos
casos refratários.
Segundo Junior (2003) os derivados do ácido acetilsalicílico, como sulfasalazina
ou mesalazina apresentam efeito anti-inflamatório bastante potente, em decorrência da
inibição dos leucotrienos, com a vantagem de serem específicos para afecções localizadas no
intestino grosso, por sua degradação exclusiva pela microbiota local. No entanto, os animais
podem apresentar sinais de intoxicação pelo salicilato. Há indicação de seu uso terapêutico
quando houver intenso infiltrado neutrofílico no exame histopatológico ou quando todas as
outras possibilidades terapêuticas tenham fracassado. Os efeitos colaterais mais comumente
observados são anorexia, vômito, anemia e ceratoconjuntivite seca.
Agentes imunossupressores podem ser úteis nos casos refratários de DIIC. Podem
ser usadas as seguintes medicações: clorambucila, na dose de 2mg/m² ou 0,01 a 0,2mg/kg, via
oral, a cada 48h; azatioprina, 1-2mg/kg, via oral, a cada 24 h; ou ciclofosfamida, 50mg/m²,
via oral durante 4 dias e suspender durante 3 dias. Tais medicações devem ser usadas durante
14
4 a 6 meses, quando então são reduzidas em 25 a 50% da dose inicial por mais 2 a 4 meses. A
contagem de neutrófilos deve ser semanalmente monitorada durante o primeiro mês de
tratamento e, depois desse período, a cada 2 a 4 semanas, enquanto o gato estiver em
tratamento. A terapêutica deve ser suspensa ou reduzida se a contagem de neutrófilos estiver
abaixo de 3.000/µL (CRYSTAL, 2006).
A terapêutica com metronidazol, juntamente com os protocolos descritos
anteriormente, pode auxiliar no manejo da DIIC, como resultado de seus efeitos
antimicrobianos. Descreveu-se também que o metronidazol inibe a imunidade mediada por
células, embora este fato não tenha sido demonstrado em gatos. A dose é de 10mg/kg, via
oral, a cada 12h durante 4 a 6 semanas (RICART, 2012).
Segundo Junior (2003), animais cujo diagnóstico envolva a presença de
espiroquetas (Campylobactersp. ou Helicobacter sp.), devem ser submetidos ao tratamento
triplo específico com amoxicilina, na dosagem de 20mg/kg, a cada 12h; metronidazol, na
dosagem de 10 a 20mg/kg, a cada 12h; e sucralfato 2,5ml/cão a cada 12 horas.
Segundo Andrade (2008), se indica o subsalicilato ou citrato de bismuto como
adjuvante no tratamento das infecções por Helicobactersp.. Aqueles pacientes que apresentam
quadros eméticos requerem administração de cloridrato demetoclopramida, na dosagem de
0,3 a 0,5mg/kg, a cada 8 a 12h (JUNIOR, 2003).
A maioria dos gatos com DIIC responsiva demonstra sinais de melhora clínica
dentro de uma semana do início do tratamento (CRYSTAL, 2006).
1.7 Prognóstico
Com a terapêutica dietética e medicamentosa adequada, a DIIC linfocíticoplasmocitária frequentemente é controlável, mas raramente curável. O envolvimento
pancreático e/ou hepático simultâneo e significativo pode levar a um prognóstico menos
favorável. A colite linfocítico-plasmocitária geralmente é controlada com a terapêutica
dietética isolada. De forma diferente da doença dos cães, a enterocolite eosinofílica em gatos
é agressiva e tem uma natureza quase neoplásica, em geral infiltrando-se em outros órgãos,
inclusive medula óssea (CRYSTAL, 2006).
15
O proprietário deve ser notificado de que a resposta terapêutica não significa cura
do animal. Normalmente, obtém-se um bom controle do quadro mórbido, porém com grande
possibilidade de recidiva (JUNIOR, 2003).
Pacientes imunossuprimidos podem apresentar complicações e agravamento do
estado geral em decorrência do tratamento farmacológico. Deve-se sempre ponderar com o
proprietário todos os riscos envolvidos para o tratamento desses animais (JUNIOR, 2003).
Segundo Junior (2003), como a maior parte dos felinos com DIIC apresenta
infiltrados linfocitários, o prognóstico é bom resultando em melhora da qualidade de vida,
uma vez que o paciente seja periodicamente reavaliado pelo clínico e o proprietário seja
cooperativo.
Em humanos existe uma associação entre DIIC e aparecimento tardio de neoplasia
intestinal, tanto na Doença de Crohn de cólon como na colite ulcerativa (RIBEIRO, 1996;
VAN HOGEZAND, 2002), mas essa ocorrência ainda não foi estudada em cães. Em contraste
com humanos, existe pouca informação na literatura veterinária tratando o desenvolvimento
de neoplasia a longo prazo (CHURCHER; WATSON,1997; STOKES, 2001).
2 RELATO DE CASO
Foi atendido um cão da raça Labrador, fêmea, 8 anos, 35kg em um consultório
veterinário situado no bairro de Copacabana - RJ com histórico de vômito e diarreia
persistentes, anorexia, perda progressiva de peso e hematoquezia há cerca de 8 meses.
O animal já havia sido tratado por outros veterinários com terapêuticas baseadas
nos sintomas e não houve mudança ou melhora no quadro. Também realizaram hemograma
completo, ureia, creatinina e fosfatase alcalina e todos os valores estavam dentro da
normalidade. Na ultrassonografia foram visualizadas alterações sugestivas de gastrite e
enterite.
O tratamento inicialmente instituído foi metronidazol 25mg/kg + sulfadimetoxina
25mg/kg a cada 12 horas, por vi oraldurante 15 dias,omeprazol 1mg/kg a cada 24 horas por
via oral durante 30 dias e ondansetrona 0,5 mg/kg a cada 8 horas por via oral por 10 dias.
Após o termino desse tratamento, foi prescrito também febenzadole 50mg/kg a cada 24 horas,
16
por 3 dias consecutivos e essa dose foi repetida após 15 dias. A alimentação do paciente foi
modificada para a Royal Canin Hipoalergênica®.
Após a realização de todo o tratamento, o animal foi submetido a novo exame
ultrassonográfico no qual observou-se imagens sugestivas de gastrite e duodenite. O estudo
radiográfico contrastado revelou que animal apresentava hipomotilidade do trânsito
gastrointestinal. Nova amostra de sangue foi colhida para realização de hemograma completo,
dosagens séricas de proteína total e frações, bilirrubinas, e Gama GT e mais uma vez não foi
constatada nenhuma alteração. Diante dos sinais clínicos inespecíficos relacionados ao TGI e
a ausência de conclusão diagnóstica pelos exames de imagem anteriores sugeriu-se ao
proprietário do animal a realização de endoscopia com biópsia gástrica. A cadela foi então
submetida à anestesia para a realização do procedimento endoscópico. Para a indução
anestésica, administrou-se 5mg/kg de fentanil via endovenosa e 5mg mg/kg de
propofoltambém por via endovenosa. O animal foi mantido anestesiado com isofluorano em
vaporizador universal. Na endoscopia encontraram-se edema e hiperemia em pregas de terço
proximal de corpo gástrico, pontos de hematina em canal antral que sugerem gastrite
enentemática, ou seja, gastrite com lesões na mucosa gástrica.
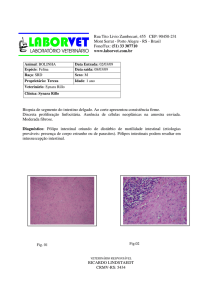
O exame histopatológico dos fragmentos do estômago revelou infiltrado
linfoplasmocitário em glândulas gástricas, edema e congestão, sugerindo como diagnóstico
gastritelinfoplasmocitária.
O tratamento consistiu na administração de prednisona na dosagem de 2,2 mg/kg
por via oral, a cada 12 horas durante 20 dias e essa dose foi sendo diminuída gradativamente
até atingir a dosagem de 0,2 mg/kg a cada 48 horas por uso contínuo, uma vez que o animal
não tolerou a retirada completa da medicação. Tentou-se também a utilização de budesonida
na dosagem de 1mg/kg a cada 12 horas via oral como forma de tratamento única, mas animal
continuava apresentando os sinais clínicos. O paciente também manifestou intolerância ao uso
da azatioprina na dosagem de 2,2 mg/kg via oral a cada 24 horas.
3 RESULTADO E DISCUSSÃO
A doença inflamatória intestinal crônica é uma patologia de grande importância na
rotina da clínica de pequenos animais, já que se confunde com diversas patologias
gastrointestinais.
17
Conforme descritos por Feijó (2008) e Junior(2013)os sinais clínicos relatados
pelo proprietário do animal também eram vômito e diarreia crônicos, anorexia, perda
progressiva de peso e hematoquezia.
Os exames laboratoriais não tiveram nenhuma alteração relevante, como foi descrito por
BURROWS (1997) e Ricart (2012).
O manejo alimentar do paciente foi modificado instituído com base em proteína
hipoalergênica, seguindo as mesmas orientações relatadas por Junior(2003) e Ricart(2012).
O animal também foi tratado concomitantemente com febendazol para descartar a
possibilidade de endoparasitas corroborando com German (2005).
A ultrassonografia foi solicitada para descartar processos neoplásicos e delimitar a
extensão das lesões, sendo escolhido a endoscopia como método de investigação e colheita de
amostras a serem enviadas para realização de exame histopatológico, assim como indicado
por Froes (2008).
Conforme Tams (2005) a endoscopia foi o método escolhido por ser menos
invasivo e pelas lesões estarem ao alcance do endoscópio.
O tratamento prednisona foi instituído na dose de 2,2mg/ Kg a cada 12 horas,
segundo relatado por Andrade(2008). A dose também fora reduzida em 20 dias, até ser
encontrada a menor dose tolerada pelo animal (0,2mg/kg por via oral a cada 48 horas).
A azatioprina citada por Crystal(2006) também foi administrada,mas animal
apresentou novamente os sintomas. Neste paciente o mesmo ocorreu com a tentativa do uso
da budesonida.
CONCLUSÃO
A Doença inflamatória intestinal crônica pode se confundir com outras doenças
digestivas ou sistêmicas devido a inespecificidade dos sinais clínicos apresentados, devendose sempre descartá-la inicialmente através da mudança alimentar, uso de antiparasitários
gastrointestinais e realização de exames laboratoriais e de imagem.
18
O diagnóstico definitivo da doença consiste na execução de exame
histopatológico de mucosa gastrointestinal cujas amostras podem ser obtidas por endoscopia
ou laparotomia exploratória.
Devido à complexidade do diagnóstico e do tratamento da enfermidade, o Médico
Veterinário precisa orientar e conscientizar o proprietário quanto às complicações esperadas,
recidivas, fracassos das terapêuticas e do prognóstico avaliando individualmente cada caso e
cada paciente.
19
REFERÊNCIAS BIBLIOGRÁFICAS
ANDRADE, S.F., Manual de Terapêutica Veterinária. 3ª ed. São Paulo: Roca Ltda., 2008.
BALFOUR, S.R. Mechanisms of disease: pathogenesis of Crohn’s disease and colitis
ulcerative. Nature Clinical Practice Gastroenterology & Hepatology. v.3, n. 7, p. 390-407,
2006.
BRIDGEFORD, E.C.; MARINI, R. P.; FENG, Y.; PARRY N.M.A; RICKMAN, B.; FOX
J.G. Gastric Helicobacter species as a cause of feline gastric lymphoma: as viable hypothesis.
Veterinary Immunology and immunopathology, v.123, n 1-2, p.106-113, 2008.
CHURCHER, R. K.; WATSON, A.D. Canine histiocytic ulcerative colitis. Australian
Veterinary Journal, v. 75, p. 710-713, 1997.
CRYSTAL, M. A. Doença Intestinal Inflamatória. In:___NORSWORTHY, G. D. O Paciente
Felino – Tópicos Essenciais de Diagnóstico e Tratamento, 3ª ed. São Paulo: Manole, 2006. p
174-177.
CRYSTAL, M. A. Linfoma. In:___NORSWORTHY, G. D. O Paciente Felino – Tópicos
Essenciais de Diagnóstico e Tratamento, 3ª ed. São Paulo: Manole, 2006. p 186-188
BURROWS, C. F.; BATT, R. M.; SHERDING, R.G. Tratado de Medicina Interna
Veterinária. Moléstias do cão e do gato. 5ª ed. Rio de Janeiro: Guanabara Koogan, v.2,
p.1618-1705, 2004.
FEIJÓ, S. Inflammatory bowel disease. Diagnostic with path and treatment. Differential
diagnosis and therapeutical management of vomiting patients. In:___Latin American
Veterinary Conference, 2008, Lima, Peru. Proceedings… Lima: LAVC, 2008.
FIGHERA, R. A. Síndrome hipereosinofílica idiopática associada à doença eosinofílica
disseminada em cães e gatos. Revista Ciência Rural, v. 34, n. 3, p. 939-942, 2004.
20
FROES, T. R. Ultrassonografia do trato gastrointestinal. In:___CARVALHO, C. F.,
Ultrassonografia em Pequenos Animais. 1ª ed. São Paulo: Roca, 2004. p. 147-162.
GERMAN, A. J. Uptade on Inflammatory bpwel disease. In:___North American Veterinary
Conference, 2005, Orlando, Flórida, p. 335-356
GUILFORD W. G. Idiopathic inflammatory bowel diseases. In:___STROMBECK D.R.
Small Animal Gastroenterology. 3ª ed. Philadelphia: WB Saunders, 1996. p.451–486.
JERGENS A. E. Inflammatory bowel disease: Current perspectives. Veterinary Clinics of
North America: Small Animal Practice, v.29, p.501–521, 1999.
JERGENS A.E.; SCHREINER C.A.; FRANK D.E.; NIYO, Y.; AHRENS, F.E;
ECKERSALL, P.D.; BENSON, T.J.; EVANS, R.A. A scoring index for disease activity in
canine inflammatory bowel disease. Journal of Veterinary Internal Medicine; v. 17, p. 291–
297, 2003.
JUNIOR, A. R. Doença Intestinal Inflamatória Crônica. In:___SOUZA, H. J. Coletâneas em
Medicina e Cirurgia Felina, Rio de Janeiro: LF Livros de Veterinária, 2003. p. 155 -164.
KRECIC, M. R. Feline inflammatory bowel disease: pathogenesis, diagnosis and relationship
to lymphossarcoma. Compendium on continuing education for the practicing veterinarian, v.
23, n. 11, p. 951 – 961, 2001.
LEICONDRE, P. Enfermidades inflamatorias crónicas intestinales. Enciclopedia Veterinaria,
3ª. edição. Philadelphia: Editora Whaltam Focus, p. 1-15, 2004.
MAGALHÃES, T. L. P. Enterite linfoplasmocítica canina. Dissertação de Mestrado.
Universidade Técnica de Lisboa. Faculdade de Medicina Veterinária, Lisboa, 2008.
MANSFIELD, C. Management of feline inflammatory bowel disease. In: World Small
Veterinary Congress, 36,2011, Jeju, Korea, Proceedings… Jeju: WSAVA, 2011.
21
RIBEIRO, M. B.; GREENSTEIN, A. J.; SACHAR, D. B.; BARTH, J. ;
BALASUBRAMANIAN, S.; HARPAZ, N.; HEIMANN, T. M.; AUFSES, A. H. JR.;
Colorectal adenocarcinoma in Crohn Disease. Annals of Surgery, 223, p. 186-193. 1996.
RICART, M.C., FEIJÓ, S.M., GÓMES, N.V., Doença intestinal inflamatória – atualização.
Revista Clínica Veterinária, 2012; n.101, 44-54.
TAMS, T. R. Gastroscopy. In:___Small Animal Endoscopy. TAMS, T. R. Missouri: Mosby,
1999. p.107-111.
VAN HOGEZAND, R. A., EICCHORN, R. F., CHOUDRY, A.; VEENENDAAL, R. A.;
LAMERS, C. B. Malignancies in inflammatory bowel disease: fact or fiction? Scandinavian
Journal of Gastroenterology, 236, p. 48-53, 2002.
WASHBAU, R. J. ; WILLARD, M. D.; HALL, E J .; JERGENS, A. E.; MANSELL, J.;
MINAMI, T; BILZER, T.W. Endoscopic, biopsy, and histopathologic guidelines for de
evaluation of gastrointestinal inflammation in companion animals. Journal of Veterinary
Internal Medicine, v.24, n.1, p.10 -26, 2010.
WILLARD, M. D. Feline inflammatory bowel disease: a review. Journal of Feline Medicine
and Surgery, v. 1, n. 3, p. 155-164, 1999.