1.
Definição: Doença desmielinizante do SNC, de mecanismo
inflamatórioauto-imune, acometendo, sob a fonna de placas, a
substânciabranca do cérebro, tronco encefálico, cerebelo, medulaespinhal e nervo óptico.
Fisiopatoloeia: Agressão inflamatória auto-imune (dependente de linfócitos T) da bainha de mielina dos axônios do SNC e
dosoligodendrócitos (células produtoras de mielina no SNC).
Epidemiologia: Apresentação na faixa etária de 35-50 anos. Mais
comum em mulheres (2:1).
Ouadro Clínico: A doença geralmente tem um curso de exacerbaçõese remissões (tipo mais comum), cada surto apresentando-sede forma aguda ou subaguda com a instalação de algumdéficitneurológico focal. Os sintomas iniciais mais comuns
são(1)paresia (monoparesia ou hemiparesia), (2) déficit sensoriallocalizado (hipoestesia), (3) neurite óptica - dor ocular
associadaa perda da acuidade visual ou amaurose fugaz e a um
achadofundoscópico semelhante ao edema de papila. Outras
apresentaçõescomuns são: parestesias, diplopia (oftalmoplegia
intemuc1ear
- perda da adução de um ou ambos os olhos), ataxia,
vertigens,disfunção vesical. Dois ou mais déficits provenientes
de diferentesáreas do SNC são comuns, especialmente com o
aparecimentodos próximos surtos. É freqüente o acúmulo de
déficitsneurológicos parciais irreversíveis após os surtos. Uma
formaevolutiva menos comum é a fonna progressiva (piora
paulatinados sintomas, sem surtos), que pode ser secundária
(apósum período de surtos) ou primária. Deve-se ressaltar: o
déficitda esc1erosemúltipla piora caracteristicamente com o
aumentoda temperatura corporal (febre, clima quente) e melhoracoma sua redução. A doença evolui inexoravelmente para
a disfunçãomatara grave, em um período médio de 15 anos.
Dia~nóstico: É feito pelo quadro clínico, complementado pela
RNMe pela punção lombar. Para estabelecer o diagnóstico, são
utilizadoscritérios clínico-laboratoriais. Os principais critérios
clínicossão: (1) envolvimento de 2 ou mais áreas do SNC, (2)
envolvimentoda substância branca (tratopiramidal, feixe espinotalâmico,cordão posterior da medula, vias cerebelares, fascículo longitudinalmedial do tronco - oftalmoplegia internuclear,
41
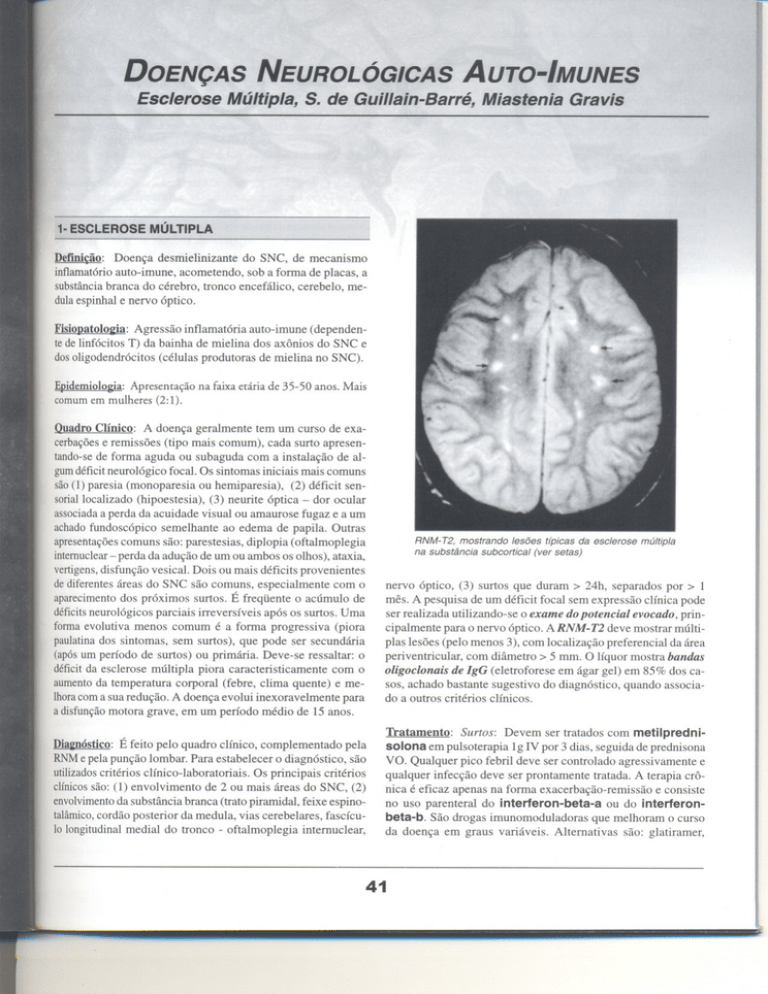
RNM- T2, mostrando lesões típicas da esclerose múltipla
na substância subcortical (ver setas)
nervo óptico, (3) surtos que duram> 24h, separados por> 1
mês. A pesquisa de um déficit focal sem expressão clínica pode
ser realizada utilizando-se o exame do potencial evocado, principalmente para o nervo óptico. A RNM- T2 deve mostrar múltiplas lesões (pelo menos 3), com localização preferencial da área
periventricular, com diâmetro> 5 mm. O líquor mostra bandas
oligoclonais de IgG (eletroforese em ágar gel) em 85% dos casos, achado bastante sugestivo do diagnóstico, quando associado a outros critérios clínicos.
Tratamento: Surtos: Devem ser tratados com metilpredni8010na em pulsoterapia 1g IV por 3 dias, seguida de prednisona
VO. Qualquer pico febril deve ser controlado agressivamente e
qualquer infecção deve ser prontamente tratada. A terapia crônica é eficaz apenas na forma exacerbação-remissão e consiste
no uso parenteral do interferon-beta-a
ou do interferonbeta-b. São drogas imunomoduladoras que melhoram o curso
da doença em graus variáveis. Alternativas são: glatiramer,
r-42
MEDCURSO
- "Do
INTERNATO À RESIDÊNCIA"
mitoxantrona, metotrexate, azatioprina, ciclofosfamida e imunoglobulina.
lidade é de 5%. Cerca de 85% dos pacientes apresenta boa recuperação dos movimentos durante os próximos meses.
2- SíNDROME DE GUILLAIN-BARRÉ
Polineuropatia Desmielinizante Inflamatória Crônica (PDIC)
Defini~ão: Polirediculoneuropatia inflamatória aguda auto-limitada, na maioria das vezes do tipo desmielinizante, de mecanismo auto-imune pós-infeccioso.
Definição: É a versão crônica da 8GB.
Fisiopatologia: Fenômeno auto-imune desencadeado por uma
infecção respiratória ou gastrointestinal.O agenteinfeccioso mais
relacionado é o Campylobacter jejuni. Em cerca de 75% dos
casos, pode-se detectar a infecção 1-3 semanas precedendo a
doença. A imunopatogênese é dependente de linfócitos T, porém, em cerca de 20-50% dos casos podem ser detectados autoanticorpos anti-GMl (anti-glicofosfolipídeo 1).
Quadro Clínico: A doença tem uma instalação hiperaguda (horas ou dias). Inicia-se com uma lombalgia associada a disestesias
nas extremidades dos membros inferiores, que logo tomam-se
paréticos ou plégicos. Portanto, ocorre uma paraparesia ou
paraplegia, que sempre é do tipo flácida e arreflexa. Nos dias
subseqüentes, o comprometimento neurológico ascende para os
membros superiores que, inicialmente, ficam arreflexos e então
podem tomar-se paréticos ou plágicos também. Em 50% dos
casos, a evolução pode acometer a face e a função bulbar, levando à disparesia facial periférica, disfagia, disfonia e disartria.
Em 30% dos casos, há paresia da musculatura respiratória,
suficiente para necessitar de suporte ventilatório. O exame físico é característico: paresia ou plegia + arreflexia + flacidez do
tipo simétrico. A sensibilidade térmica e dolorosa geralmente
está preservada, mas não a proprioceptiva e a vibratória. Na
maioria das vezes, não há distúrbio vesical nem nível sensitivo.
A presença destes achados sugere síndrome de compressão medular ou mielite transversa. A variante de Miller-Fisher manifesta-se com oftalmoplegia, ataxia e arreflesia generalizada.
Ouadro Clínico: O paciente vai lentamente evoluindo com piora da força muscular, com períodos de exacerbação e remissão.
O exame físico é igual À 8GB, exceto por um comprometimento maior da sensibilidade e menor simetria. Esta pode ser uma
síndrome paraneoplásica (principal: CA broncogênico oat cell)
ou pode estar associada a uma gamopatia monoclonal de significado indeterminado.
Tratamento: É diferente ao da 8GB. Baseia-se no uso do
corticóide: pulsos de metilprednisolona
6/6 semanas ou
prednisona em doses imunossupressoras.
Opções são:
plasmaferese e imunoglobulina IV.
3- MIASTENIA GRAVIS
Diagnóstico: É dado principalmente pelo quadro clínico, às
vezes necessitando da exclusão de uma síndrome medular pelo
exame de imagem. O exame de líquor apresenta uma alteração
característica após a 1a semana da doença: dissociação albumino-
citológica (aumento da proteína sem pleocitose ou aumento da
celularidade). Quando a 8GB está associada à infecção pelo HIV,
pode haver pleocitose com hiperproteinorraquia.
A
eletroneuromiografia mostra uma polineuroradiculopatia com
padrão desmielinizante na maioria dos casos.
Tratamento: O paciente deve estar internado, de preferência
no CTI (pelo risco de insuficiência ventilatória e arritmias). A
causa mais comum de óbito atualmente é a morte súbita arrítmica.
O tratamento específico deve ser iniciado com uma das seguintes opções: (1) plasmaferese; (2) imunoglobulina IV.A morta-
A sí
pela
mus
rênc
da.!
(prit
ça di
Definição: Doença auto-imune da placa motora neuro-muscular (anticorpos anti-AchR - receptor pós-sináptico de
aceti1colina), caracterizada por fraqueza e fadigabilidade muscular.
Epidemiologia:
Acomete mais o sexo feminino (3:2). Apresen-
ta-se geralmente na faixa etária de 20-30 anos (mulheres) e de
40-50 anos (homens).
Fisiopatologia: Fenômeno auto-imune, com surgimento de
anticorpos anti-AchR. A destruição destes receptores e da membrana pós-sináptica da junção neuro-muscular leva à fraqueza
do músculo. À medida que a aceti1colina das vesículas présinápticas vão sendo liberadas e consumidas, a fraqueza vai pi-
Nos pacientes mais graves, instala-se a insuficiência ventilatória
e a disautonomia, levando a arritmias cardíacas, sudorese e picos hipertensivos.
Dia
dia!
acel
da s
(5 n
dod
braç
um2
haja
coliI
do t
conJ
dect
anfi,
tóra
hipe
orando (fadigabilidade). Com o repouso muscular, os estoques
são repostos. A reação auto-imune provavelmente depende do
timo, uma vez que existe uma grande associação entre MG e
hiperplasia tímica ou timoma.
Trai
anti
pirid
prog
form
oper
co. )
mais
50m.
DeVE
amiIJ
fenol
curat
Crisl
asso(
nado
Ouadro Clínico: Os dois mais importantes marcos da doença plan
são: (1) comprometimento preferencial da musculatura ocular, antic
(2) fadigabilidade - a fraqueza do músculo piora após a sua diagt
utilização repetida. As queixas iniciais são ptose e diplopia, mas!
que pioram com o passar do dia. A fraqueza da musculatura
bulbar leva à disartria, fala anasalada e disfagia. O comprometimento facialleva à dificuldade de expressar um sorriso. Com sue;
o passar dos meses, a doença evolui com fraqueza muscular
proximal nos membros. A história natural da doença costuma 1. I
~
respeitar esta ordem: musculatura ocular - bulbar - membros
J
proximais. A doença pode seguir um curso de exacerbação e
~
remissão. Os sintomas sempre são piores no fim do dia. Existe 2.
umaformamaisbrandada doença,que acometeapenasa musculatura ocular.
~
=
CAPíTULO
Diagnóstico: O teste do edrofônio é o primeiro passo para o
diagnóstico. O edrofônio é um anticolinesterásico (inibe a
aceti1colinesterase,enzima que cataboliza a acetilcolina da fendasináptica)de ação imediata (30 seg) e meia-vida muito curta
(5min).O médico centraliza a sua atenção para um determinadodéficitmuscular (ex.: ptose palpebral, fraqueza proximal dos
braços,voz anasalada) e faz 2mg de edrofônio IV. Se houver
umamelhora nítida, o teste é considerado positivo. Caso não
hajaresposta,repete-se o teste com 8mg IV.Os efeitos colaterais
colinérgicospodem ser revertidos com atropina. A positividade
do teste deve ser complementada com mais dois exames para
confirmaro diagnóstico: eletromiografia (mostra uma resposta
decrementaldos potenciais de ação muscular) e dosagem do
anticorpoanti-AchR (presente em 80% dos casos). A TC de
tórax deve ser solicitada visando à pesquisa de timoma ou
hiperplasiatírnica.
3.
4.
5.
6.
7.
8.
9.
Asíndrome de Eaton-Lambert deve ser diferenciada da MG
pelaeletromiografia(respostaincremental dos potenciais de ação
musculares).O quadro clínico é semelhante, exceto pela preferênciapela musculatura dos membros e pela idade mais avançada.Na maioria das vezes, esta é uma síndrome paraneoplásica
(principal:CA broncogênico oat celi) e está associada a presençade auto anticorpos anti-canal de cálcio pré-sináptico.
Tratamento: O tratamento deve ser iniciado com drogas
anticolinesterásicas,
sendo a mais utilizada o brometo de
piridostigmina60-120mg VO 3-5 xldia. A timectomia deve ser
programadaem todos os casos de timoma e nos pacientes com a
formageneralizada. A plasmaferese deve ser realizada no préoperatórionos pacientes de maior comprometimento e alto risco.A terapia imunossupressora é recomendada para os casos
maisgraves e refratários. Pode ser feito com prednisona 1550mg/diacom ou sem azatioprina.
ser evitadas as seguintes drogas no paciente miastênico:
aminoglicosídeos, beta-bloqueadores, procainamida, quinidina,
fenotiazinas, lítio, magnésio venoso, tetraciclinas, polimixina,
curare (exceto a succini1colina).
Devem
CriseMiastênica: Definida como uma piora aguda do quadro
associadaà insuficiência ventilatória. O paciente deve ser internadono CTI, intubado e ventilado. O tratamento de escolha é a
plamaferese. Uma alternativa é a imunoglobulina
IV. O
anticolinesterásicodeve ser retirado à princípio, para se fazer o
diagnósticodiferencial com a crise colinérgica (sinais e sintomassemelhantes à crise rniastênica).
10.
11.
12.
NEUROLÓGICAS
AUTO-IMUNES
43
Trapp, BO, Peterson, J, Ransohoff, RM, et ai. Axonal transection
in the lesions of multiple sclerosis. N Engl J Med 1998; 338:278.
Newcombe, J, Hawkins, Cp, Henderson, CL, et ai. Histopathology of multiple sclerosis lesions detected by magnetic resonance
imaging in unfixed postmottem central nervous system tissue. Brain
1991; 114 (Pt 2):1013.
Offenbacher,H, Fazekas, F,Schmidt, R, et ai. Assessment of MRI
criteriafor a diagnosis of MS. Neurology 1993; 43:905.
Kidd, O, Thorpe, JIN, Thompson, AJ, et ai. Spinal cord MRI using
multi-arraycoils and fast spin echo. 11.Findingsin multiplesclerosisoNeurology 1993; 43:2632.
Paty, OIN,Oger, JJ, Kastrukoff, LF,et ai. MRI in the diagnosis of
MS: a prospective study with comparison of clinicalevaluation,
evoked potentials, oligoclonalbanding, and CT. Neurology 1988;
38:180.
Lee, KH, Hashimoto, SA, Hooge, Jp, et ai. Magnetic resonance
imaging of the head in the diagnosis of multiple sclerosis: a prospective 2-year fol/ow-up with comparison of clinicalevaluation,
evoked potentials, oligoclonalbanding, and CT. Neurology 1991;
41:657.
Morrissey, SP, Mil/er,OH, Kendal/, BE, et ai. The significance of
brain magnetic resonance imaging abnormalities at presentation
with clinical/y isolated syndromes suggestive of multiple sclerosiso A 5-year fol/ow-up study. Brain 1993; 116 (Pt 1):135.
Brex, PA, Miszkiel, KA, O'Riordan, JI, et ai. Assessing the risk of
early multiple sclerosis
in patients
with clinically
isolated
syndromes:
The role of a fol/ow up MRI. J Neurol Neurosurg
Psychiatry 2001; 70:390.
Filippi, M, Horsfield, MA, Morrissey, Sp, et ai. Quantitative brain
MRllesion load predicts the course of clinical/y isolated syndromes
suggestive of multiple sclerosis. Neurology 1994; 44:635.
Miller, OH, Barkhof, F, Nauta, JJ. Gadolinium enhancement in-
creases the sensitivity of MRI in detecting disease activity in multiple sclerosis. Brain 1993; 116 (Pt 5):1077.
13. Tottorel/a, C, Codel/a, M, Rocca, MA, et ai. Oisease activity in
multiple
sclerosis
studied by weekly triple-dose
magnetic
resonance imaging. J Neuro11999; 246:689.
14. Arnold, OL, Riess, GT, Matthews, PM, et ai. Use of proton magnetic resonance spectroscopy for monitoring disease progression
in multiple sclerosis. Ann Neuro11994; 36:76.
15. Rudick, RA, Whitaker, JN. Cerebrospinal fIuid tests for multiple
sclerosis. In P. Scheinberg (Ed.), Neurology/neurosurgery
update
series, Vol. 7, CPEC, Princeton, NJ, 1987; P 1.
16. McLean, BN, Luxton, RIN, Thompson, EJ. A study of immunoglobulin G in the cerebrospinal fIuid of 1007 patients with suspected
neurological disease using isoelectric focusing and the Log IgGIndex. A comparison and diagnostic applications. Brain 1990; 113
( Pt 5):1269.
17. Rudick, RA, Whitaker, JN. Cerebrospinal fIuid tests for multiple
sclerosis. In Scheinberg, P (Ed). Neurology/neurosurgery
update
series, Vol. 7, CPEC. Princeton, NJ 1987; 1.
18. McLean, BN, Luxton, RIN, Thompson, EJ. A study of immunoglobulin G in the cerebrospinal fIuid of 1007 patients with suspected
neurological disease using i$oelectric focusing and the Log IgGIndex. A comparison and diagnostic applications. Brain 1990; 113
( pt 5):1269.
19. Avasarala,
JR, Cross, AH, Trotter, JL. Oligoclonal band number
as a marker for prognosis in multiple sclerosis. Arch Neurol 2001;
58:2044.
20.
SUGESTÕES BIBLIOGRÁFICAS
1. Poser, CM, Paty, OIN, Scheinberg, L, et ai. New diagnostic criteria
formultiple sclerosis: guidelines for research protocols. Ann Neurol
1983; 13:227.
2. McOonald, WI, Compston, A, Edan, G, et ai. Recommended diagnostic criteria for multiple sclerosis: guidelines from the InternationalPanel on the diagnosis of multiple sclerosis. Ann Neurol200 1;
50:121.
5 - DOENÇAS
21.
22.
23.
Gronseth, GS, Ashman, EJ. Practice parameter: the usefulness
of evoked potentials in identifying clinical/y silent lesions in patients with suspected multiple sclerosis (an evidence-based
review): Repott of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2000; 54:1720.
Hahn, AF. The Guillain-Barré syndrome. Lancet 1998; 352:635.
Beghi, E, Kurland, LT, Mulder, OIN, Wiederholt, WC. Guillain-Barre
syndrome. Clinicoepidemiologic
features and effect of influenza
vaccine. Arch Neuro11985;
42:1053.
Olive, JM, Castillo, C, Castro, RG, de Quadros, CA. Epidemiologic
study of Guillain-Barre
syndrome
in children &It; 15 years of age in
Latin America. J Infect Ois 1997; 175 SuppI1:S160.