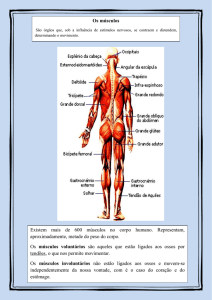
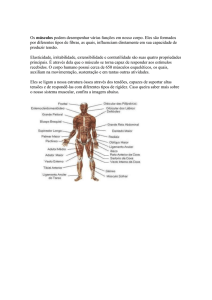
14
1 INTRODUÇÃO
Espondilite Anquilosante (EA), para Buss et al (2000), é a mais comum disfunção
do
grupo
das
espondiloartropatias,
caracterizada
por
associação
do
HLA-B27
histocompatibilidade complexa, propensão à inflamação das ênteses, das articulações
sinoviais e cartilagem articular. O marco radiográfico é a anquilose, principalmente na coluna
e articulação sacroilíaca.
Segundo Sampaio Barros et al (1999), o acometimento pulmonar na EA foi
inicialmente descrito em 1941, considerando uma manifestação extra-articular da doença,
tendo como achado a fibrose apical. Dentre as hipóteses sugeridas para explicar esta fibrose,
pode-se incluir o distúrbio da ventilação apical, devido a marcante restrição da
expansibilidade torácica causada pela anquilose das articulações costovertebrais.
A avaliação da função pulmonar na EA tem relevado elevada prevalência de
defeito ventilatório restritivo segundo muitos autores, caracterizado pela diminuição da
capacidade vital forçada, geralmente correlacionado à diminuição da expansibilidade torácica.
A existência da vida animal segundo Ficher (2002) é caracterizada pelo
deslocamento corporal, ou movimento físico, dependente do fornecimento contínuo de
energia. Em consequência da capacidade pulmonar diminuída, esses pacientes podem vir a ter
reserva metabólica diminuída para realizar os exercícios.
Eles são menos ativos por causa da dor que ocorre com o movimento. Resultando
15
em um descondicionamento cárdio-respiratório para realizar suas tarefas cotidianas. E, devido
o comprometimento postural, esses pacientes tem um maior gasto energético para realizar
suas atividades do que os indivíduos sadios.
O desejo de buscar maior compreensão a respeito dos efeitos do treinamento
aquático sobre a função pulmonar desses pacientes foi o que impulsionou a idéia desta
pesquisa com o intuito de o conhecimento obtido possa indicar para a formulação de
tratamento fisioterápico que reduza o acometimento da doença, melhorando a qualidade de
vida.
Em geral esses pacientes estão interessados em tratamento terapêutico,
especialmente o exercício, capazes de ajudá-los a controlar sua doença e reduzir seus níveis
de incapacidade. A escolha do treinamento aquático foi devido ao fato de que na água, há
pouca ou nenhuma sustentação de peso sobre a coluna, e também é menos doloroso segundo o
relato dos pacientes.
Neste estudo, o objetivo geral é avaliar o efeito do treinamento aquático sobre as
capacidades e volumes pulmonares, assim como a força muscular ventilatória após
treinamento aquático no pacientes com EA. Já nos objetivos específicos: avaliar a capacidade
vital forçada (CVF); avaliar a capacidade pulmonar total (CPT); avaliar a capacidade residual
funcional (CRF); avaliar o volume expiratório forçado no primeiro segundo (VEF1); avaliar o
fluxo expiratório forçado entre 25% e 75% da capacidade vital (FEF25-75%); avaliar o pico de
fluxo expiratório (PFE); avaliar o índice de Tiffenau (VEF1/CVF); avaliar a capacidade
muscular inspiratória máxima através da pressão inspiratória máxima (PImáx).; avaliar a
capacidade muscular expiratória máxima através da pressão expiratória máxima (PE máx).
Esta pesquisa em seu sentido estrutural divide-se em cinco capítulos.
No primeiro capítulo há uma breve introdução sobre o trabalho, o segundo contém
uma revisão bibliográfica abordando os principais assuntos do trabalho, falando sobre
espondilite anquilosante, função pulmonar, treinamento aquático, avaliação funcional
16
pulmonar. No terceiro capítulo temos o delineamento da pesquisa, onde a pesquisa
caracteriza-se como exploratória, sendo um estudo multi-caso.
No quarto capítulo foram analisados e discutidos os dados, apresentados em forma
de gráficos e tabelas, e por fim, no quinto capítulo as considerações finais.
17
2 EFEITOS DO TREINAMENTO AQUÁTCO NA FUNÇÃO PULMONAR DE
PACIENTES COM ESPONDILITE ANQUILOSANTE
2.1 Espondilite anquilosante
2.1.1 Definição
Inicialmente será feita uma breve definição de Espondilite Anquilosante, segundo
alguns autores.
Para a Sociedade Brasileira de Reumatologia (2004), a Espondilite Anquilosante
(EA) é uma doença inflamatória crônica que acomete preferencialmente a coluna vertebral,
podendo evoluir com rigidez e limitação funcional progressiva do esqueleto axial. Geralmente
inicia-se no adulto jovem, preferencialmente no sexo masculino, da cor branca e em
indivíduos HLA – B 27 positivos.
“A EA diferencia-se da artrite reumatóide que ataca a membrana sinovial, pois ela
acomete o sítio de inserção dos tendões, ligamentos, fáscia e cápsulas fibrosas articulares
(ênteses)” (BUSS et al 2000).
Golding (1999), define a EA, como uma condição, não rara que afeta
principalmente adultos jovens do sexo masculino. Seu quadro completo se caracteriza por
18
anquilose das articulações sinoviais da coluna, e ossificação dos ligamentos espinhais. Por
vezes acomete as articulações periféricas, e produz irite a aortite.
É a mais comum disfunção do grupo das espondiloartropatias soronegativas,
caracterizada por associação com HLA-B27, histocompatibilidade complexa, propensão à
inflamação das ênteses, das articulações sinoviais e cartilagem articular.
“Sabe-se atualmente que a EA é quase tão comum quanto a artrite reumatóide e
também que as mulheres jovens são afetadas quase tão frequentemente quanto os homens
jovens.” (SALTER, 2001, p. 131).
2.1.2 Etiopatogenia
Segundo a Sociedade Brasileira de Reumatologia (2004), é freqüente a associação
com o HLA-B27 faz com que a doença seja mais comum em populações brancas, onde a
prevalência do HLA–B27 é significativamente maior. Por sua vez, a positividade do HLA –
B27 nos pacientes espondilíticos pode variar entre 80 a 98% sendo mais elevadas nas
populações brancas não miscigenadas do norte da Europa. Devido à extrema raridade do HLA
– B27 em populações negras africanas, a doença é muito pouco frequente em negros; no
Brasil, país de intensa miscigenação racial, a EA, costuma ser encontrada em mulatos (devido
à influência da ascendência genética branca), mas é bastante rara em negros não
miscigenados.
Essa predisposição genética está ligada direta ou indiretamente ao gene HLA-B27
do complexo maior de histocompatibilidade humano. Assim enquanto 6 a 8% da população
branca normal apresenta o referido gene, cerca de 90 % dos pacientes espondilíticos brancos
são HLA-B27 positivos, (MEIRELES ; KITIDAI, 1999).
Segundo Cruz Filho (1980) do ponto de vista etiopatogênico, admite-se hoje que
19
fatores precipitantes como a colite ulcerativa ou outras doenças associadas, tais como
infecções urogenitais ou mesmo reumatismos e exposições climáticas desfavoráveis possam
precipitar o aparecimento da EA em indivíduos geneticamente predispostos, marcados com
HLA-B27. A doença poderia então ser perpetuada por alguma forma de mecanismo
imunológico não identificado. “A grande maioria dos pacientes desenvolve os sintomas entre
os 20 e 35 anos de idade.”(BUSS et al, 2000).
2.1.3 Incidência
Para Ghosh (2003), a EA costuma surgir na terceira década de vida sendo a
relação de homens e mulheres de 3:1. Segundo Meirelles e Kitidai (2001), a EA apresenta
uma forte agregação familiar, de tal forma que parentes de primeiro grau de pacientes
espondilíticos apresentam um risco cerca de 20 vezes maior de vir manifestá-la, quando
comparados à população em geral.
Acomete principalmente indivíduos caucasianos, possivelmente pela maior
incidência de HLA-B27 nesta amostragem, e é enfermidade relativamente mais
comum, ocorrendo em cerca de 0,1 a 0,2 % da população geral. Entretanto, se forem
consideradas as populações em que a incidência do HLA-B27 é mais alta, como na
Finlândia, a prevalência da doença chega de 0,5 a 1,0 % da população geral.
Observa-se também que a enfermidade é muito mais freqüente entre parentes de 1º
grau HLA-B27 positivos de pacientes portadores de Espondilite Anquilosante e,
também portadores do antígeno HLA-B27. (MOREIRA; CARVALHO, 2001, p.
405).
Segundo Sampaio Barros et al (2003), após estudos com 80 pacientes portadores
de espondiloartropatias observou que o gene HLA-B27 foi observado em 92,5% dos pacientes
com EA, sendo esse estudo o primeiro realizado em uma população espondilítica brasileira,
onde há uma grande variedade racial e étnica.
Para Buss et al (2000), as mulheres com EA carregam grande hereditariedade do que
20
os homens, enquanto estes têm maior carreamento a psoríase (quando EA presente).
Entretanto essa susceptibilidade não afeta a severidade da doença.
2.1.4 Evolução
Para a maioria dos autores a doença segue de uma maneira lenta e progressiva.
Segundo Cruz Filho (1980), a doença começa sempre nas articulações sacroilíacas, onde
normalmente estende-se para cima envolvendo a coluna lombar torácica e frequentemente a
cervical. Ocasionalmente os quadris e os ombros também são afetados. A cartilagem articular
sinóvial e ligamentos apresentam alterações inflamatórias e eventualmente tornam-se
ossificados. Após vários anos o processo inflamatório torna-se quiescente.
Para Sampaio Barros et al (2003), a presença do HLA-B27 é um importante fator
de evolução da doença após dois anos de segmento se comparado com pacientes que não
apresentam. Esse resultado representa um importante fator prognóstico, indicando um começo
cedo e mais agressivo da doença.
2.1.5 Diagnóstico
“O diagnóstico da EA será baseado, fundamentalmente, em três pilares: a
sintomatologia clínica, as alterações radiológicas e a determinação do HLA-B27.”
(GOLDING, 1999, p. 126).
Para Buss et al (2000), a EA é uma doença de caráter sistêmico. Os sintomas
ocorrem nos períodos de maior atividade da doença ou nas fases iniciais e consistem de
astenia, fadiga, hiporexia, emagrecimento leve e febrícula.
21
“O diagnóstico de certeza da EA envolve achados clínicos de história ou exame
físico, laboratorial e de métodos de imagem.” (MEIRELES; KITIDAI, 1999). Os critérios
originais de Nova Iorque de 1996, (descritos no quadro 1) ainda são utilizados em função de
apresentarem maior grau de especificidade.
A. Diagnóstico Clínico
1. Limitação da mobilidade lombar nos 3 planos: flexão, inclinação e extensão.
2. História ou presença de dor na junção dorsolombar ou na coluna lombar.
3. Limitação da expansibilidade torácica para 1cm ou menos no nível do 4º espaço
intercostal.
B. Graduação Radiográfica das Sacroilíacas
Grau 0 – Ausência de sacroileíte.
Grau 1 – Ausência de sacroileíte (pseudo-alargamento articular).
Grau 2 – sacroileíte leve (esclerose periarticular).
Grau 3 – sacroileíte moderada (erosão periarticular).
Grau 4 – sacroileíte grave (anquilose articular).
Espondilite Anquilosante Definida
Sacroileíte bilateral grau 3 ou 4, e no mínimo 1 critério clínico.
Sacroileíte unilateral grau 3 ou 4, ou sacroileíte bilateral grau 2 com critério clínico 1 ou
ambos critérios clínicos 2 e 3.
Espondilite Anquilosante Provável
Sacroileíte bilateral grau 3 ou 4, sem outro critério clínico.
Quadro 1: Critérios de Nova Iorque para EA.
Fonte: MEIRELLES e KITIDAI 1999 apud TAYLOR.
2.1.6 Prognóstico
Segundo Cruz Filho (1980), a doença cessa de progredir após dez ou quinze anos,
deixando rigidez permanente, cuja magnitude varia para cada paciente. As complicações
22
incluem deformidade em flexão fixa da coluna infecções respiratórias intercorrentes e
iridocidite que em casos graves pode causar cegueira.
Nas formas mais graves de EA a coluna vertebral se torna progressivamente rígida
(poder back); ela também tende a tornar-se progressivamente fletida (rocker back).
Além disso, esta progressiva deformidade em flexão da coluna pode ser
drasticamente acelerada por uma série de fraturas patológicas de insuficiência,
resultantes do traumatismo trivial. Eventualmente o paciente é incapaz de visão
horizontal, incapacidade perigosa e embaraçosa. (BUSS et al, 2000).
2.1.7 Manifestações osteo-articulares
“Pacientes com EA geralmente desenvolvem osteoporose, particularmente no
esqueleto axial, podendo contribuir para a deformidade espinhal e dor óssea.”(BUSS et al,
2000).”
São próprias da enfermidade. Segundo Serra Gabriel, Pett e Carril (2001),
acometem principalmente a coluna (em todos os seus níveis), no tórax e articulações
sacroilíacas este comprometimento pode ser periférico e do tipo assimétrico, com preferência
pela localização proximal antes da distal, isto é serão mais afetados os quadris e os ombros e,
em menor grau, joelhos, tornozelos e pés.
Dentre as características do comprimento axial, temos as sinovites de repetição, que
darão lugar à formação de um tecido de granulação que se estenderá, originando
sindesmófitos, em direção vertical, as quais unirão uma vértebra a outra, isto, junto
com a calcificação dos ligamentos, dará lugar à rigidez. (SERRA GABRIEL; PETT;
CARRIL 2001, p. 351).
2.1.7.1 Comprometimento vertebral
O comprometimento da cervical geralmente se instalará tardiamente, ainda que
23
possam haver exceções em que possam haver maior rigidez cervical em relação ao restante da
coluna.
Segundo Serra Gabriel, Pett e Carril (2001), os movimentos comprometidos em
primeiro lugar são as inclinações laterais, seguidas de flexão e extensão; as rotações serão
mantidas por um maior tempo em virtude das articulações atlaidontóideos e atlodaxóideas que
habitualmente se comprometem num estágio mais avançado da doença. Mas, na fase
avançada da doença, poderá ocorrer a perda total da mobilidade articular. Como resultado
ocorrerá a projeção do pescoço para frente (Figura 1).
Figura 1 – Anquilose cervical com retificação da
lordose fisiológica, calcificação ligamentar e
fusão das articulações interapofisárias.
Fonte: Espondiloartropatias (2006).
Serão comprometidas segundo Serra Gabriel, Pett e Carril (2001) as articulações
costovertebrais, costotransversais e condrosternais, o que dará uma limitação da expansão
torácica e uma diminuição dos diâmetros ântero-posterior e transverso do tórax, até o ponto
em que, nas fases avançadas da enfermidade, a ventilação terá lugar unicamente a custa do
diâmetro vertical, por descida do diafragma. “Nesses casos em que a respiração é totalmente
diafragmática geralmente observamos uma protusão abdominal.”(BUSS et al, 2000).
24
Em conseqüência disto haverá perda do movimento de rotação e instalação de
uma deformidade em cifose fixa (Figura 2).
Figura 2 – Cifose fixa.
Fonte: Espondilite anquilosante (2006).
A retifição da lordose presente no estágio inicial da doença, que na fase avançada
da doença segundo Serra Gabriel, Pett e Carril (2001), ocorrerá uma anquilose total do
segmento (com ausência de cifose lombar na flexão de tronco. Também surgirão contratura e
retração dos músculos espinhais e paravertebrais e uma diminuição ou perda dos movimentos
laterais de rotação.
A manifestação mais comum é a dor nas articulações sacroilíacas e/ou lombar,
segundo Bus set al (2000), a dor tem início geralmente na segunda década de vida e de modo
insidioso.
Serra Gabriel, Pett e Carril (2001), afirmam que geralmente a primeira
manifestação da EA será uma sacroileíte. Todos os pacientes portadores de EA apresentam,
na evolução da história natural da doença, acometimento do esqueleto axial, sendo
característico o envolvimento e bilateral e precoce das articulações sacroilíacas (sacroileíte)
(Figura 3).
25
Figura 3 – Sacroileíte bilateral.
Fonte: Espondiloartropatias (2006).
Golding (1999), descreve que na articulação sacroilíaca, de início ocorre sinovite
e infiltração celular como na artrite reumatóide (porém sem necrose da camada superficial da
membrana sinovial. Posteriormente, destruição da cartilagem, causando um estreitamento das
articulações e destruição do osso justa-articular, cursando esclerose, ao final anquilose óssea.
Nos quadris, segundo Serra Gabriel, Pett e Carril (2001), acontecerá uma coxite
que evoluirá com limitação importante de todos os movimentos e contratura e retração de
flexores e adutores. A deformidade se instalará em forma de contratura em flexão, que
associada à rigidez vertebral, dará lugar a uma atitude de flexão e uma grande dificuldade
para a marcha. A solução cirúrgica será a artroplastia total de quadril, que em algum casos
terá que ser bilateral, para devolução da funcionalidade daquela articulação permitindo uma
reintegração à atividade profissional.
O comprometimento escapuloumeral estará associado a um comprometimento
acromioclavicular e esterno clavicular, existindo uma limitação importante de todos os
movimentos que causará uma incapacidade para as atividades de vida diária de moderada a
grave.
Já o comprometimento dos joelhos é menos freqüente, e em geral se manifesta em
formas de artrites transitórias, as quais normalmente não deixam sequelas, salvo uma
26
moderada contratura em flexão que somada à do quadril (mais severa) e à rigidez vertebral
obrigará o paciente a uma postura como de um esquiador.
Nos tornozelos e pés, podem acontecer artrites transitórias pouco frequentes.
2.1.8 Manifestações extra articulares
A EA é uma doença de caráter sistêmico, segundo Buss et al (2000), os sintomas
ocorrem nos períodos de maior atividade da doença ou nas fases iniciais e consistem de
astenia, fadiga, hiporexia, emagrecimento leve e febrícula. Para Moreira e Carvalho (2001), os
olhos são acometidos em cerca de 20 a 30% dos pacientes, ocorrendo uma uveíte anterior
aguda (iridociclite), não granulomatosa, unilateral e recidivante, acontece uma hiperemia
ocular intensa, visão borrada, dor, fotofobia e lacrijamento, de início súbito geralmente
durando dias a semanas.
No aparelho geniturinário, a manifestação mais comum é a prostatite,
representada clinicamente por uma piúria estéril. De descrição mais recente, a nefropatia
mesengial por depósitos de IgA tem tradução clínica à custa de hematúria microscópica e as
vezes macroscópica, podendo ou não ser acompanhada por proteinúria.
A síndrome da cauda eqüina é complicação rara, possivelmente secundária a uma
aracnoidite, e se traduz por um quadro insidioso de dor nas nádegas e nas faces internas das
coxas e pernas, com alterações sensoriais e motoras.
Para Serra Gabriel, Pett e Carril (2001), a fibrose pulmonar é bem mais rara,
porém pode revestir-se de gravidade se associada ao processo restritivo consequente da pouca
elasticidade do tórax.
27
Para Moreira e Carvalho (2001) as manifestações cardio-respiratórias são os
distúrbios de condução do ritmo cardíaco, insuficiência aórtica, pericardite, miocardite e uma
fibrose pulmonar apical que, com a evolução da doença, torna-se bilateral.
“A árvore respiratória é atingida, indiretamente, por três fatores: pela rigidez
cervical, hipercifose dorsal, pela redução da expansibilidade torácica e pela dos quadris.”
(CRUZ FILHO 1980, p. 277). Devido à deformidade postural, que leva uma anquilose das
articulações vertebrais desses pacientes, sua árvore respiratória poderá ser atingida em alguns
casos.
Segundo Shneerson (1993), As alterações típicas do volume pulmonar ocorrem na
forma de uma queda discreta da capacidade pulmonar total e da capacidade vital e um
aumento do volume residual e capacidade residual funcional. A queda da capacidade vital é
proporcional ao grau de anquilose vertebral e a queda da complacência pulmonar, porém não
se relaciona ao grau de cifose ou duração da doença.
Sampaio Barros et al (1999), afirma que a diminuição de difusão CO2 e o
diâmetro torácico diminuído na EA estão associados ao acometimento da coluna dorsal,
doença tardia e disfunção pulmonar restritiva crônica, frequentemente pior em tabagistas.
A contração diafragmática é relativamente mais importante do que os músculos
intercostais acessórios na Espondilite Anquilosante, comparando com a de
indivíduos normais. Ela compensa em grande parte a incapacidade de expansão do
gradil costal e minimiza as alterações dos volumes pulmonares. O volume minuto
encontra-se até menos anormal que a capacidade vital, provavelmente porque o
diafragma permite a utilização de uma proporção incomumente elevada da
capacidade vital. As resposta ventilatórias aos exercícios são notavelmente normais
e são habitualmente limitadas por fatores circulatórios. (SHNEERSON, 1993, p.
187).
2.1.9 Achados radiológicos
O diagnóstico feito por imagem radiográfica, segundo estudos de Meireles e
28
Ktadai (2001), baseia-se no achado de alterações do esqueleto axial tais como sacroileíte, em
regra bilateral e simétrica, quadratização vertebral, anquilose das articulações interfacetárias
vertebrais, presença de sindesmófitos vertebrais e ossificação do ligamento longitudinal
anterior da coluna vertebral.
Segundo Meireles e Ktadai (2001), a investigação radiográfica completa do
esqueleto axial e justaaxial na EA compreende as radiografias de bacia em ântero-posterior ou
na posição de Fergunson, radiografias da coluna lombar, dorsal e cervical em ântero-posterior
e oblíquas. O grau de intensidade das alterações radiográficas das articulações sacroilíacas
pode ser avaliado segundo a escala quantitativa de Nova Iorque (Quadro 1).
Segundo Greenspan (2001), o formato quadrado da borda anterior das vértebras
torácicas inferiores e lombares é um dos primeiros aspectos radiológicos da EA, que é melhor
demonstrado da radiografia lateral de coluna. À medida que a condição progride, formam-se
sindesmófitos, unindo os corpos vertebrais. O aspecto delicado destes crescimentos e sua
orientação vertical, e não horizontal, os distinguem de osteófitos da doença vertebral
degenerativa. As ossificações paravertebrais são comuns na EA. Quando
as
articulações
apofisárias e os corpos vertebrais se fundem mais tarde na evolução da doença, pode ser
observada uma característica radiológica deste distúrbio, a coluna em “bambu”, as
articulações sacroilíacas são também são invariavelmente afetadas neste processo. Nas
articulações periféricas para, Greenspan (2001), as alterações inflamatórias podem ser
indistinguíveis das observadas na artrite reumatóide.
Segundo Buss et al (2000), o aspecto da coluna em “bambu”, no sexo feminino,
está ausente nos achados radiológicos.
29
2.1.10 Tratamento
O tratamento da EA envolve medidas educacionais, farmacológicas, físicas ou
reabilitacionais, radioterápicas e cirúrgicas, devendo, portanto, idealmente ser multidisciplinar
e multiprofissional, envolvendo médicos especialistas em reumatologia, ortopedia e fisiatria,
fisioterapeuta, terapeuta ocupacional, enfermeira, psicóloga e assistente social (MEIRELES ;
KITIDAI, 2001).
Os principais objetivos do tratamento estão relacionados à redução da dor controle
inflamatório, redução da rigidez articular e da sua conseqüente incapacidade funcional,
através da prevenção das deformidades osteoarticulares, principalmente coluna vertebral e
quadris. Visa paralelamente, reabilitação pisicossocial e profissional do paciente
(MEIRELES; KITIDAI, 2001).
2.1.10.1 Tratamento medicamentoso
Segundo Meirelles e Kitadai (2001), o tratamento medicamentoso visa o controle
da inflamação articular, com conseqüente alívio da dor e rigidez articular. Pode ser
sintomático ou de ação rápida e potencialmente indutor de remissão ou de ação lenta.
Segundo o mesmo autor, os analgésicos mais utilizados são parecetamol e os
opiódes morfínicos leves, como codeína, o profenol e, ou, com menor freqüência os opióides
morfínicos potentes agonistas completos ou parciais
30
2.1.10.2 Tratamento cirúrgico
A intervenção cirúrgica mais comum é a prótese de quadril. Um número menor de
pacientes pode se beneficiar de correção cirúrgica de deformidades em flexão na coluna ou
em casos de subluxação atlanto-axial (SKARE, 1999).
2.1.10.3 Tratamento fisioterapêutico
Linden, Tubergen e Hidding (2006), afirmam que o tratamento fisioterapêutico
tradicionalmente visa a manutenção da função músculo-esquelética.
Segundo Bus set al (2000), a fisioterapia é amplamente reconhecida como a
estratégia de maior relevância no tratamento da EA. A reabilitação física desses pacientes
deve ser dirigida para os aparelhos locomotor e respiratório.
No que se refere à função respiratória Gabriel (2001), devido a diminuição da
mobilidade do tórax (pela perda da expansão torácica se faz necessário a manutenção da
função respiratória através de exercícios respiratórios.
Outro ponto importante à mobilidade do aparelho locomotor, que segundo Gabriel
(2001), seria o objetivo prioritário que dele dependerá, unicamente a não instalação da
anquilose óssea. Este compreende exercícios de flexibilização de todos os segmentos
vertebrais.
Para Henderson (2003), o treinamento dos indivíduos portadores de EA, mostra
uma redução da dor minimizando a perda funcional e melhorando a qualidade de vida.
Uma importante revisão sobre o metabolismo energético humano se faz
necessário. Pois muitos pacientes com EA queixam-se sobre a capacidade reduzida do
31
exercício quando são atendidos pela fisioterapia.
No contexto biológico, energia química (potencial) dos alimentos e a energia
mecânica (cinética) do trabalho muscular (W) expressam-se fisicamente como calor
(Q), sendo regidas, portanto pelas leis básicas da termodinâmica. Em poucas
palavras a primeira lei da termodinâmica estabelece o princípio universal da energia,
ou seja, energia não é criada, nem destruída e sim transformada. (NEDER; NERY
2003, p. 35).
O exercício é um processo que depende da transformação de energia bioquímica
dos alimentos ingeridos em energia mecânica para contração muscular.
“A função primordial dos sistemas respiratório e cardiovascular é manter a troca
gasosa celular dentro dos limites compatíveis com as demandas energético metabólicas e o
equilíbrio ácido-básico.” (NEDER; NERY 2003, p. 36). Durante o esforço físico, o aumento
da atividade contrátil do músculo estriado induz consideráveis incrementos no consumo
celular de oxigênio (QO2) e na liberação celular de dióxido de carbono (QCO2), e por
conseguinte a sobrecarga dos sistemas de suporte ao exercício (Figura 4).
Figura 4 – “Engrenagem” dos sistemas respiratório e cardiovascular.
Fonte: Neder; Nery 2003, p.36.
Para os mesmos autores, o fundamental para a manutenção do exercício é o
transporte de oxigênio para as células e a remoção de gás carbônico dos tecidos, e, para
satisfazer o aumento da demanda de trocas entre a atmosfera e as células durante o exercício,
32
a ventilação e a circulação têm que se elevar conjunta e adequadamente para se acoplar às
demandas do metabolismo.
“Entretanto as anormalidades destas respostas, eventualmente não detectadas no
repouso, podem ser identificadas no exercício, quando os sistemas cardiovascular e pulmonar
encontram-se em sobrecarga funcional.”(NEDER; NERY 2003, p. 9).
Muitos estudos mostram, segundo Ficher (2002), que os pacientes com AO, AR,
SFM, exibem funções neuromuscular e cardio-respiratória mais baixas, assim como seu
condicionamento físico (flexibilidade, desempenho funcional), essa espiral descendente
(perda de reserva fisiológica) progressiva, a não ser que sejam administrados tratamentos
apropriados. Tendo essas funções diminuídas, haverá então um maior gasto energético para
realizar os exercícios.
O aspecto mais notável da transição repouso-exercício diz respeito ao paradoxo
entre as necessidades imediatas de energia e a natureza progressiva dos processos
mitocondriais oxigênios-dependentes (aeróbios), seja por limitação enzimática ou por
verdadeira deficiência local de O2.
Segundo Ficher (2002), muitos programas de exercícios diferentes foram
estudados nesses grupos de pacientes, a maioria concentrou-se nos exercícios aeróbico,
exercício de resistência ou protocolo de condicionamento geral. Em geral eles foram bem
sucedidos no sentido de induzir algum nível de aprimoramento da flexibilidade, na função
neuromuscular, na função cardiovascular, no desempenho funcional, na dor, na
sintomatologia da doença, na auto eficácia com os exercícios e na função psicológica.
Segundo Neder e Nery (2003), o metabolismo dos chamados substratos
energéticos- proveniente dos alimentos fornece importante energia química potencial. Esta,
portanto, é primeiramente armazenada na porção terminal da molécula de adenosina trifosfato
(ATP) sob a ligação de fosfato de alta energia, que é a moeda energética orgânica.
“Embora essas reservas corporais de ATP sejam razoavelmente vasta (80-100g)
33
sua mobilidade é extremamente restrita; disto decorre que, somente a ATP disponível no sítio
de contração pode ser utilizada”.(NEDER; NERY 2003, p.37).
Segundo Neder e Nery (2003), outro ponto importante á a eficiência desse
fornecimento de energia, e quanto da energia disponível nos alimentos, o músculo consegue
realmente utilizar para gerar trabalho, que é cerca de 50 a 55%. Isso que dizer que 45-50% da
energia total contida no substrato está perdida. Por outro lado, a quantidade de trabalho
realizada pelo músculo, como resultado da transferência de energia, das ligações de fosfato de
alta energia para as proteínas musculares depende da eficiência contrátil.
É importante que o terapeuta determine com exatidão a função fisiológica e o
desempenho funcional no paciente com EA para poder prescrever uma progressão do
exercício que se concentre na redução das limitações fisiológicas e funcionais do paciente.
Ao prescrever exercícios para os pacientes com EA é essencial avaliar com
extremo
cuidado
a
capacidade
basal
de
realizar
exercícios
(cárdio-respiratório,
neuromuscular, flexibilidade, etc.) e o desempenho e estado funcional a fim de prescrever
individualmente, o programa mais benéfico para cada paciente. Os programas progressivos
prescritos individualmente com base nos déficits fisiológicos funcionais, são necessários para
garantir que o paciente não falhe nos estágios iniciais de um programa de exercícios.
2.2 Função pulmonar
Segundo Silveira (2000), a função respiratória fisiológica se dá quando o ar
atmosférico penetra nos pulmões se houver um gradiente de pressão entre a atmosfera e o
alvéolo. E a criação desse gradiente só poderá ser possível por dois modos: ou criando uma
pressão subatmosférica dentro do tórax ou aumentando a pressão no ar ambiente (pressão
positiva). Para haver uma respiração normal, os músculos inspiratórios fazem aumentar os
34
diâmetros do fole torácico; a ampliação torácica cria uma pressão atmosférica intrapleural, e
esta atrai o pulmão distendendo-o.
2.2.1 Mecânica da ventilação
Para West (1996), na respiração corrente normal, o nível do diafragma move-se
cerca de um centímetro mais ou menos, mas na inspiração e expiração forçadas pode ocorrer
uma excursão total de até dez centímetros. Na inspiração o diafragma move-se para cima
porque a pressão intratorácica cai. Isto é conhecido como movimento paradoxal.
Para Kapandji (2000), a mecânica respiratória acontece da seguinte maneira:
inspiração a contração do diafragma faz o centro frênico baixar, que aumenta o diâmetro
vertical do tórax; porém em seguida, a resistência ao alongamento dos elementos verticais do
mediastino se contrapõem assim como a resistência das massas viscerais abdominais.
Com isso a pressão atmosférica é superior a pressão interior, fazendo com que o ar
entre. Já na expiração o diafragma se relaxa, e a contração dos músculos abdominais faz
baixar o orifício inferior ao tórax, diminuindo simultaneamente os diâmetros transversal e
ântero-posterior ao tórax, aumentando a pressão intra-torácica fazendo com que ar seja
expulso (Figura 5).
Figura 5 - Mecânica da ventilação.
Fonte: Kapandji, 2000.
35
2.2.2 Complacência pulmonar
Para Shneerson (1993), a análise da expansão do gradil costal é complexa, por
causa da multiplicidade de músculos que se insere no gradil costal e na coluna vertebral e das
diferenças de comprimento, obliquidade e tipos de articulações e costelas. Quando o gradil
costal se espande, ele é deformado pela força dos músculos. Sua forma não segue o padrão
que seria possível apenas com base em suas propriedades elásticas. A extensão dessa
deformação varia com o padrão de atividade dos músculos inspiratórios e o volume pulmonar.
A expansão pode ocorrer nos diâmetros longitudinal, ântero-posterior e transverso. O
comprimento do gradil costal aumenta através da elevação da primeira costela, extensão da
coluna e descida do diafragma.
Kapandji (2000), a noção de distembilidade está diretamente relacionada com a
elasticidade dos elementos anatômicos do tórax e dos pulmões. Durante a expiração normal, o
tórax e os pulmões tomam uma posição de equilíbrio comparável a de uma mola que não
esteja nem comprimida nem esticada. Existe então um equilíbrio de pressão entre o ar intra
alveolar e o ar atmosférico.
2.2.3 Capacidades pulmonares
Silva; Rubin e Silva (2000), definem que ao final de uma inspiração máxima, a
quantidade de ar contida nos pulmões denomina-se capacidade pulmonar total (CPT), esta
compreende algumas divisões e subdivisões, sendo que a capacidade vital (CV) é quantidade
máxima de ar que pode ser expirada a partir da capacidade pulmonar total (CPT). A
capacidade residual funcional (CRF) é a quantidade de ar nos pulmões ao final de uma
36
expiração normal. A capacidade residual funcional (CRF) possui dois componentes: o volume
de reserva expiratório (VRE), sendo o volume máximo que pode ser eliminado a partir da
CRF, e o volume residual (VR), quantidade de ar que não pode ser eliminada dos pulmões
após uma expiração máxima.
2.2.4 Músculos ventilatórios
A classificação dos músculos responsáveis pela respiração do homem sofre
algumas alterações de autor para autor, mas alguns aspectos básicos são inconfundíveis, como
é o caso dos músculos primários e músculos acessórios da respiração.
Segundo Costa (2004), os músculos que desempenham papel indispensável na
respiração normal são o diafragma e os músculos intercostais externos, para expiração
normal, basta o relaxamento desses músculos, pois a própria elasticidade do parênquima,
somada aos gradientes intratorácico e intrapulmonar, é suficiente para produzir o mecanismo
da expiração.
Na expiração mais profunda, ou simplesmente na tosse, há necessidade de um
trabalho muscular, onde exige a ação dos músculos da parede abdominal.
Costa (2004), afirma que a classificação dos músculos intercostais internos e
externos, como respectivamente expiradores e inspiradores, tem sido contestada por
investigações eletromiográficas, nas quais foi detectada tanto a ação dos internos como
externos durante a fase inspiratória, quando analisados próximo ao osso externo, durante a
fase expiratória, quando analisados próximos das vértebras.
37
2.2.4.1 Propriedades contráteis
Segundo Shneerson (1993), a contração dos músculos ventilatórios fornece
energia para a expansão do pulmão. Em comum com todos os outros músculos esqueléticos,
eles são compostos de fibras musculares alinhadas longitudinalmente, em meio ao tecido
conjuntivo. As fibras são ativadas quando um impulso alcança a junção neuromuscular e
libera acetilcolina da membrana pré-sináptica. Esta despolariza a membrana da fibra
muscular, com perda de seu potencial negativo em cerca de 75 mV.
O grupo de fibras musculares inervados por um axônio constitui uma unidade
motora. Todas as fibras dentro de uma unidade motora contraem-se
simultaneamente. As fibras dentro de uma unidade motora são todas do mesmo tipo,
apesar de poderem estar espalhadas pelo músculo. O número de fibras que
compreende uma unidade motora de modo geral é maior, se as fibras forem de
contração rápida, e menor se forem de contração lenta. São atividade é controlada
não apenas pelos motoneurônios alfa, porem também por retroalimentação
provenientes dos fusos musculares. (SHNEERSON, 1993, p. 15).
2.2.4.2 Tipos de fibras musculares
Para Shneerson (1993) fibras dentro de cada músculo possuem diferentes
propriedades estruturais, histoquímicas e contráteis. Reconhece-se dois tipos principais. O
tipo 1 (vermelho) possui um diâmetro menor, mais enzimas oxidativas, uma menor atividade
da fosforilase, mais mitocôndrias e enzimas lipídicas e um maior conteúdo de mioglobina que
as fibras do tipo 2. as fibras do tipo 2 foram subdivididas em 2a e 2b; as fibras 2a são
intermediarias entre as fibras de tipo 1 e 2b.
38
2.2.4.3 Massa contrátil
Segundo Shneerson (1993), força desenvolvida pelo músculo depende de sua
massa ou área de secção transversal e da porção de fibras que foram ativadas. Os músculos
esqueléticos podem hipertrofiar-se e aumentar sua força com esquemas de treinamento
adequado. A massa é influenciada também pelo estado nutricional, idade (que está
relacionada à perda de motoneurônios alfa e de unidades motoras) e a distúrbios patológicos
dos músculos. A massa de músculo que se contrai empregada em determinada carga pode ser
aumentada através do recrutamento de novos grupos musculares. Isto possibilita a diminuição
da freqüência de descarga dos motoneurônios, o que impede ou alivia a fadiga muscular. A
incapacidade de recrutar músculos pode ser devida à falta de motivação ou a um
comprometimento do controle respiratório. A força de contração pode ser aumentada também
através do recrutamento de unidades motoras extras.
Para Shneerson (1993), tensão desenvolvida durante uma contração muscular
isolada é menor do que a observada na estimulação repetida rápida. Após uma estimulação
isolada, a fibra muscular relaxa-se antes que suas propriedades elásticas permitam que atinja a
tensão máxima: esta é a base de relação freqüência-força. A relação exata entre freqüência
força de contração muscular depende do tipo de composição, em termos de fibras, do músculo
e de fatores que afetam a contratilidade, como por exemplo a fadiga. De modo geral, a força
desenvolvida é de aproximadamente 25% do máximo a uma freqüência de estimulação de
10Hz, 70% do máximo a 20 Hz, 95% do máximo a 50 Hz e máxima 100 Hz.
As fibras musculares adaptam-se prontamente a alterações de seu comprimento,
geralmente, a não ser que o músculo seja hiper-estendido, quanto maior for o comprimento
inicial, tanto maior será a força que ele consegue desenvolver durante estimulação tetânica.
39
O comprimento muscular segundo Shneerson (1993), constitui importante fator na
determinação de força gerada pelos músculos respiratórios. Os músculos inspiratórios são
mais eficazes quando próximos ao VR, visto que apresentam o comprimento máximo, e os
músculos expiratórios são mais eficazes na CPT, quando se encontram distendidos. O volume
dos pulmões, entretanto, constitui um guia grosseiro para o comprimento dos músculos. Em
qualquer volume pulmonar, a configuração do gradil costal depende da quantidade de
deformação causada pela contração muscular a partir de sua forma o prevista com base em
suas propriedades elásticas. O comprimento dos músculos respiratórios pode variar, assim, de
um ciclo respiratório para outro, mesmo com o mesmo volume pulmonar.
Quando as fibras musculares são ativadas, o músculo pode encurtar (contração
isotônica) ou pode haver desenvolvimento de tensão (contração isométrica). Quanto
mais rápido for o encurtamento muscular, menor a tensão que pode ser mantida. Há
mais necessidade de mais energia muscular, se o músculo encurtar rapidamente, do
que quando seu comprimento permanece constante. A velocidade de encurtamento
dos músculos respiratório é difícil de ser analisada em pormenores, porém, mostrouse que a fadiga muscular é mais provável se a velocidade de fluxo inspiratória for
rápida. (SHNEERSON, 1993, p. 17).
Para Shneerson (1993), fraqueza de um músculo é a incapacidade de gerar força
esperada, porem a fadiga é a incapacidade de manter uma força. É o oposto da resistência
muscular e pode ser considerada como desenvolvimento de fraqueza durante contrações
mantidas ou repetidas. Quando se desenvolve fadiga muscular, ocorre normalmente um
aumento compensatório da freqüência de descargas e do número de motoneurônios ativos que
suprem o músculo.
2.3 Treinamento aquático
Primeiramente se abordará uma breve revisão dos benefícios do exercício
40
realizado na água. A fim de compreender os princípios do treinamento aquático, através do
conhecimento das propriedades da água.
2.3.1 Água aquecida
“A água aquecida (temperatura variando entre 30ºC e 34ºC) diminui a tensão e
dores musculares, proporcionando um ambiente confortável e relaxante para o exercício
terapêutico precoce.” (KOURY, 2000 p. 3). Ainda para Koury (2000), a redução da
espasticidade muscular pode melhorar a amplitude de movimento, e a redução da dor pode
beneficiar psicologicamente o paciente.
O calor da água durante o treinamento aquático diminui a sensibilidade da fibra
nervosa rápida (tato) e a exposição prolongada diminui a sensibilidade da fibra nervosa lenta
(dor).
Quando as articulações são mobilizadas, a amplitude do movimento aumenta mais
facilmente, indicando mais vantagens para o uso da água aquecida como meio terapêutico
(DEGANI, 1998, p. 99).
Exaustão muito mais cedo durante a execução do exercício físico intenso no calor
porque o sangue, além de carregar oxigênio para o músculo em exercício, também
precisa carregar calor do interior do corpo para a pele. Isso representa uma carga
extra para o coração, que tem que bombear mais fortemente. (ASTRAND e
RODAHL apud KOURY, 2000).
Segundo Koury (2000), o estresse por calor durante a atividade física
(basicamente do tipo condicionamento físico) aumente a frequência cardíaca a uma
determinada carga de trabalho, sendo que ao reduzir o estresse e aumentar o calor no
condicionamento físico podemos ser capazes de diminuir a frequência cardíaca no exercício a
uma determinada carga de trabalho, aumentando dessa forma a tolerância ao exercício.
41
2.3.2 Flutuação
A flutuação é a força ascendente vertical sobre um corpo que esteja submerso ou
flutuando em um fluido. A quantidade de força direta ascendente exercida sobre o
corpo será equivalente ao peso do volume do fluido deslocado pela fração do corpo
que esta abaixo da superfície da piscina. (KOURY, 2000, p. 14).
Isso significa que, para Koury (2000), quanto maior a porcentagem do corpo que
está embaixo da água, maior será a força de flutuação que estará agindo sobre o corpo. Um
corpo flutuando na água está apenas deslocando uma quantidade suficiente de líquido para
equilibrar seu peso. A quantidade de força de flutuação experimentada por um corpo será
determinada pela densidade do líquido no qual está submerso.
Para Degani (1998), o peso corporal dentro da água é reduzido em quase 90%, as
articulações ficam livres de atrito e há uma diminuição de riscos de lesões. Com isso há uma
maior facilidade na realização dos movimentos.
2.3.3 Gravidade específica
Segundo Astrand e Rodall apud Koury (2000), o peso submerso do corpo humano
na água é reduzido a poucos quilogramas, uma vez que a gravidade específica do corpo não é
muito diferente daquela da água.
A gravidade específica do corpo humano varia ligeiramente acima ou abaixo de
1,0. A da piscina tem uma gravidade de 1,0.
42
2.3.4 Pressão hidrostática
Segundo a Lei de Pascal, a PH é a pressão que o líquido exerce igualmente sobre
cada partícula da superfície de um corpo imerso em repouso, a uma dada
profundidade. É exercida igualmente em todas as direções e aumenta de acordo com
a densidade do líquido. (DEGANI, 1998, p. 97).
Ainda para Degani (1998), essa pressão exercida em toda a superfície do corpo
oferece estabilização articular auxiliando o trabalho dos músculos enfraquecidos e sua ação
nas faces do tórax promove resistência à expansão, solicitando um maior trabalho da
musculatura inspiratória e favorecendo a expiração.
2.4 Avaliação da função pulmonar
2.4.1 Espirometria
Com a espirometria segundo Silva; Rubin e Silva (2000), basicamente são
medidos volumes e fluxos aéreos. Pode ser realizada tanto com tradicionais espirômetros de
campânula, como modernos aparelhos computadorizados que fornecem adicionalmente à
curva volume-tempo, os fluxos instantâneos em cada volume pulmonar, compondo-se a curva
fluxo-volume.
Esse volume de gás dentro dos pulmões pode ser subdividido em volumes e
capacidades pulmonares tais como as descritas a seguir:
•
Capacidade residual funcional (CRF): volume de ar nos pulmões após uma expiração
normal: CRF = VR +VRE.
•
Volume residual (VR): volume retido nos pulmões após uma expiração máxima.
43
•
Volume de reserva expiatória (VRE): volume máximo que pode ser expirado após o final
de uma expiração normal.
•
Volume corrente (VC): volume expirado ou inspirado durante cada movimento
respiratório, em repouso.
•
Volume de reserva inspiratória (VRI): volume máximo que pode ser inspirado a partir do
final de uma inspiração de repouso.
•
Capacidade inspiratória (CI): volume máximo que pode ser inspirado a partir do final de
uma expiração normal; CI= VRI = VC.
•
Capacidade vital (VC): volume máximo que pode ser expirado após a inspiração máxima:
CV= VRE + VC + VRI.
•
Capacidade pulmonar total (CPT): volume de ar nos pulmões após uma inspiração
máxima: CPT = CV + VR.
Segundo Silva, Rubin e Silva (2000), os espirômetros modernos fornecem a curva
fluxo-volume para a análise gráfica do fluxo gerado durante a manobra da capacidade vital
forçada (CVF), plotando o volume e fluxo. Para se obter os dados necessários, o paciente
realiza a seguinte manobra: inspira até a CPT e, após expira de maneira forçada e rápida até o
VR; após inspira rapidamente do VR até a CPT. No início do movimento expiratório, o fluxo
chega rapidamente ao máximo possível – este é pico de fluxo expiratório – e a seguir, ocorre
redução progressiva à medida que se aproxima do VR. Considerando a curva expiratória, a
partir dos seus primeiros 30%, o fluxo torna-se independente do esforço.
2.4.2 Manovacuometria
O desempenho ventilatório depende não apenas das propriedades mecânicas dos
44
pulmões (vias aéreas e parênquima) e da parede torácica, mas também da ação dos músculos
respiratórios. Segundo Silva, Rubin e Silva (2000), enquanto a avaliação dos músculos, dos
membros pode ser feita diretamente através da força que eles podem desenvolver no
levantamento de pesos, em contraste, a avaliação dos músculos respiratórios só pode ser
determinada indiretamente pela medida das pressões exercidas contra uma via aérea ocluída.
A manovacuometria é um teste relativamente simples realizado com o esforço
voluntário, com a utilização de um manovacuômetro arenóide a vácuo.
A PImáx é o índice da força diafragmática, e a PEmáx mede a força da musculatura
abdominal e intercostal.
O teste deve ser repetido pelo menos três vezes, sendo que os dois melhores
resultados podem diferir no máximo em 10%, sendo escolhido o de maior valor. O resultado é
dado em cmH2O, sendo que a PImáx expressa com sinal negativo e a PEmáx, com valor
positivo. Valores abaixo de 60%, segundo Silva; Rubin e Silva (2000), são considerados
anormais, indicando alteração na força muscular respiratória.
45
3 DELINEAMENTO DA PESQUISA
O delineamento da pesquisa, segundo Gil (1996, p. 70), “refere-se ao
planejamento da mesma em sua dimensão mais ampla.” Neste momento, o investigador
estabelece os meios técnicos da investigação, prevendo-se os instrumentos e os procedimentos
necessários utilizados para a coleta de dados.
3.1 Tipo de pesquisa
Essa pesquisa pode ser classificada quanto ao nível como exploratória, quanto
abordagem quantitativa e quanto ao procedimento estudo multi-caso.
3.1.1 Tipo de pesquisa quanto ao nível
Essa pesquisa tem caráter de pesquisa exploratória. Segundo Heerdt e Leonel (2005), o
principal objetivo da pesquisa exploratória é proporcionar maior familiaridade com o objeto
de estudo. Ou seja, neste caso, é necessário “[...] desencadear um processo de investigação
que identifica a natureza do fenômeno e aponte as características essenciais das variáveis que
46
se quer estudar [...]” (KOCHE apud HEERDT; LEONEL, 2005).
3.1.2 Tipo de pesquisa quanto à abordagem
A pesquisa tem caráter quantitativa, sendo que é objetiva e analisa números. Para,
Richardson (1989), a pesquisa é quantitativa porque emprega técnicas, estatísticas como
média.
3.1.3 Tipo de pesquisa quanto ao procedimento utilizado na coleta de dados
A pesquisa quanto ao procedimento é um multi-caso, para Rauen (2002) é uma
análise profunda e exaustiva de um ou mais objetos de estudo de modo a permitir o seu amplo
e detalhado conhecimento. Tem como vantagens o estímulo a novas descobertas, a ênfase na
totalidade e na simplicidade dos procedimentos.Tendo como objetivo geral avaliar a função
pulmonar de pacientes com EA, os objetivos específicos indicam exatamente os dados que se
pretende obter.
Como as variáveis nesse estudo não são passiveis de observação imediata, foi
necessário operacionalizar esses conceitos ou variáveis, ou seja, torná-los passível de
observação empírica e de mensuração.
3.2 População/ amostra
A pesquisa tem caráter acidental não probabilística, segundo Rauen (2002), elas
47
caracterizam-se por não permitir iguais oportunidades, para todos os elementos participarem
da seleção amostral, elas podem ser: acidentais, por quotas ou intencionais.
A pesquisa é do tipo amostra acidental, foi utilizado os pacientes que procuraram
os atendimentos da clínica escola de fisioterapia da Unisul, atingindo determinado
tamanho.“Amostra é conjunto de elementos de uma população, que é escolhido de acordo
com uma regra ou plano para representá-la, em função de alguma característica sob estudo.”
(RAUEN, 2002, p.120)
Foram estudados três pacientes adultos do sexo masculino com EA em diferentes
estágios da doença (utilizando critérios do American College of Rheumatology, Nova Iorque,
1990, quadro 2), através da radiografia da articulação sacroilíaca realizada na avaliação.
A. Diagnóstico Clínico
1. Limitação da mobilidade lombar nos 3 planos: flexão, inclinação e extensão.
2. História ou presença de dor na junção dorsolombar ou na coluna lombar.
3. Limitação da expansibilidade torácica para 1cm ou menos no nível do 4º espaço
intercostal.
B. Graduação Radiográfica das Sacroilíacas
Grau 0 – Ausência de sacroileíte.
Grau 1 – Ausência de sacroileíte (pseudo-alargamento articular).
Grau 2 – sacroileíte leve (esclerose periarticular).
Grau 3 – sacroileíte moderada (erosão periarticular).
Grau 4 – sacroileíte grave (anquilose articular).
Espondilite Anquilosante Definida
Sacroileíte bilateral grau 3 ou 4, e no mínimo 1 critério clínico.
Sacroileíte unilateral grau 3 ou 4, ou sacroileíte bilateral grau 2 com critério clínico 1 ou
ambos critérios clínicos 2 e 3.
Espondilite Anquilosante Provável
Sacroileíte bilateral grau 3 ou 4, sem outro critério clínico.
Quadro 2: Critérios de Nova Iorque para EA.
Fonte: TAYLOR apud MEIRELLES e KITIDAI 1999.
ID 1: Indivíduo com 39 anos de idade, massa 57Kg, 174 centímetros de altura,
IMC = 0,19 Kg/m2, fazendo o uso de antiinflamatórios no período de exacerbação da doença.
48
Figura 6: Radiografia da articulação
sacroilíaca do indivíduo 1.
ID 2: Indivíduo com 44 anos de idade, massa 83 Kg, 156 centímetros de altura,
IMC = 0,34 Kg/m2, apresentando grau de acometimento avançado da articulação sacroilíaca
fazendo o uso de medicações constantes.
Figura 7: Radiografia da articulação
sacroilíaca do indivíduo 2.
ID 3: Indivíduo com 47 anos de idade, massa 80 Kg, 160 centímetros de altura,
IMC = 0,31 Kg/m2, não fazendo uso de medicações.
Figura 8: Radiografia da articulação
sacroilíaca do indivíduo 3.
49
3.3 Protocolo de treinamento
O programa de treinamento consistiu em 12 semanas, de exercícios na piscina,
com a altura da água no processo xifóide, aquecida a 33ºC a 35ºC, três vezes por semana,
sempre no período matutino, 60 minutos por dia, de acordo com os critérios do American
College of Sports Medicine (2002).
Cada sessão era composta por exercícios de aquecimento, alongamento global,
fortalecimento de membros superiores e tronco associados a padrão respiratório
diafragmático, condicionamento aeróbico, e alongamento.
Ao início da sessão era realizado a aquecimento sendo cinco minutos de
caminhada em ritmo moderado. Após eram realizados alongamento global de membros
inferiores, superiores e tronco.
O condicionamento aeróbico era realizado caminhadas (Figura 9.1-a) em
intensidade moderada, marcha lateral para ambos os lados (Figuras 9.1-b 9.1–c) e marcha
para trás (Figura 9.1-d), compondo 20 minutos nas primeiras 4 semanas de atendimento,
progredindo para 25 minutos e utilização de carga de 1Kg na extremidade dos membros
inferiores dos indivíduos I e III, o indivíduo II, não utilizava carga em virtude do
comprometimento avançado da articulação sacroilíaca, nas quatro semanas seguintes e após
trinta minutos.
Figura 9.1-a
Figura 9.1-b
50
Figura 9.1-c
Figura 9 – Aquecimento.
Figura 9.1-d
No fortalecimento de membros superiores e tronco, eram realizados exercícios de
flexão de ombro (Figura 10.2-a) e rotação de tronco com abdução horizontal de ombro
(Figura 10.2-b) e flexão de 90º graus ombro, com auxílio de bastões, associados ao padrão
respiratório diafragmático, com duração de cinco minutos cada um, eram realizados
exercícios de e abdução de ombros com alteres de espuma (Figura 10.2-c), arremesso de bola
com todos os pacientes (Figura 10.2-d) todos os exercícios com água acima do nível dos
ombros.
Figura 10.2-a
Figura 10.2-b
Figura 10.2-c
Figura 10.2-d
Figuras 10 – Fortalecimento de membros superiores e tronco.
51
Ao final era realizado novamente o alongamento global dos pacientes de membros
inferiores (Figuras 11.3-a, 11.3-b), membros superiores e tronco (Figura 11.3-c e 11.3-d).
Figura 11.3-a
Figura 11.3-b
Figura 11.3-c
Figura 11.3-d
Figuras 11 - Alongamento de membros superiores e inferiores.
Durante as sessões o Indivíduo II, apresentava exarcebação das dores na região
sacroilíaca, portanto tinha necessidade de parar algumas vezes para descanso. Os Indivíduos I
e III não tiveram dificuldades na realização do treinamento.
3.4 Instrumentos utilizados para a coleta de dados
Para a pesquisa foram utilizados os seguintes instrumentos o para a coleta de
dados:
•
Manovacuômetro.
52
Para mensuração da força muscular ventilatória foi utilizado o manovacuômetro
da marca Gerar® (MVC300) aparelho que mede as pressões inspiratórias e expiratórias
máximas, sendo quantificadas em centímetros d’água. Avaliando-se o conjunto dos músculos
inspiratórios e expiratórios.
Figura 12 – Manovacuômetro.
•
Espirômetro
Para a mensuração das capacidades pulmonares foi utilizado o Espirômetro da
marca Multispiro™., aparelho que mede o fluxo de ar nas vias aéreas ou brônquios, que
compara os resultados obtidos com pessoas da mesma idade, altura, sexo, raça e etnia:
•
Capacidade pulmonar vital (CPV);
•
Capacidade vital forçada (CVF);
•
Volume expiatório forçado no primeiro segundo (VEF1);
•
Fluxo expiratório forçado entre 25 e 75% da capacidade vital (FEF25-75%);
•
Pico de fluxo expiratório (PFE);
•
Índice de Tiffeneau (VEF1/CVF).
53
Figura 13 – Espirômetro.
3.5 Procedimentos para a coleta de dados
A coleta de dados foi realizada no período de agosto a novembro de 2005, na
Clínica Escola de Fisioterapia da UNISUL – campus Tubarão/SC.
Primeiramente todo o procedimento da coleta de dados foi explicada aos
indivíduos da pesquisa. No mesmo dia foi iniciada a coleta de dados através da avaliação
fisioterapêutica.
A coleta de dados compreendeu uma consulta inicial denominada avaliação,
realizadas um dia antes aos procedimentos terapêuticos, equivalentes há doze semanas. Os
indivíduos realizaram um programa de exercícios aquáticos seguindo os critérios do American
College of Sports Medicine (ACSM) (2002), três vezes por semana, com duração de sessenta
minutos cada atendimento. Concluído o período de exercícios aquáticos foi realizada a
reavaliação quarenta e oito horas após o término dos exercícios. Totalizando quarenta e oito
atendimentos, um para avaliação, quarenta e seis de abordagem terapêutica e um para
reavaliação.
3.5.1 Procedimentos utilizados na avaliação
54
Os procedimentos descritos a seguir foram utilizados para realização da avaliação
e reavaliação, consistem em verificação da estatura e massa corpórea, espirometria,
manovacuometria.
A radiografia da coluna foi aplicada na avaliação com objetivo de
identificar o grau de acometimento da doença, através da análise da articulação sacroilíaca.
3.5.1.2 Verificação da estatura e massa corpórea
A mensuração da estatura e massa corpórea foi obtida através da balança
antropométrica da marca Welmy, com carga máxima de 150 Kg, esses dados foram
necessários para a utilização do programa que realiza os gráficos da espirometria.
Para a verificação da massa e estatura, o indivíduo foi posicionado na balança
antropométrica, sendo orientado a retirar os calçados, permanecendo com vestimenta leve. O
mesmo foi instruído a permanecer na posição ortostática, com os membros superiores
(MMSS) junto ao corpo e olhar voltado para o horizonte, aferindo assim a sua estatura e
massa corpórea.
A importância de se verificar estatura e massa corpórea seria porque para
utilização do programa do aparelho espirômetro se faz necessária para correlacionar com as
variáveis antropométricas e clínicas.
Foi avaliado o índice de massa corporal (IMC), calculado pela fórmula peso/altura
ao quadrado (KG/M2), de acordo com Zanchet, Viegas e Lima (2004), utilizado para
diagnóstico nutricional, de acordo com a World Healt Organization: magreza (IMC< 18,5),
eutrofia (IMC entre 18,5 e 24,9), pré-obesidade (IMC entre 25 e 29,9), obesidade grau I (IMC
entre 30 e 30,9) obesidade grau II (IMC entre 35 e 39,9) e obesidade grau III (IMC>40).
55
3.5.1.2 Manovacuometria
As pressões inspiratória e expiratória máxima (PImáx e PEmáx): a pressão
inspiratória máxima foi aferida após o paciente expirar da capacidade pulmonar total (CPT)
até o volume residual (VR) com subseqüente esforço inspiratório máximo contra uma válvula
ocluída. A PEmáx foi obtida após o paciente inspirar do VR até a CPT e subseqüente esforço
expiratório máximo contra uma válvula ocluída. Sendo os valores quantificados em
centímetros d’ água.
O protocolo realizado para avaliação das pressões inspiratórias e expiratórias
máximas (PImáx e PEmáx) compreendeu as seguintes etapas:
1- O paciente foi colocado na posição sentada.
2- Os lábios do paciente eram pressionados contra um largo bocal achatado de borracha, o
qual pôr conveniência é conectado a uma válvula tridimensional estrangulável. Segundo
Azeredo (1999), o uso de um tubo de borracha tem sido interpretado por diversos
estudiosos como causa de altas pressões, quando comparada a peça de bocal rígida
colocada no interior dos lábios, podendo ocorrer em razão das propriedades elásticas da
bochechas.
3- Foram fixados clipes nasais ao nariz do paciente para evitar vazamentos.
4- O paciente foi orientado a realizar uma ou mais respirações profundas quando a válvula é
aberta e quando expira completamente o volume residual.
5- O paciente foi solicitado a inspirar e mais profundo e rápido possível, para atingir sua
PImáx e mantê-la pôr mais de um segundo, através de estímulo verbal.
6- O procedimento foi realizado não mais de três vezes com cada paciente, permitindo-se um
minuto de repouso entre os esforços.
56
7- O teste foi realizado também para avaliar a PEmáx, com a mesma rotina sendo realizado a
partir da capacidade pulmonar total.
8- Nesse teste, foram acompanhados pelo fisioterapeuta onde não se permite escape de ar
pressionando suas bochechas, e permitir o mínimo de pressão em torno da cavidade oral.
3.5.1.3 Espirometria
A espirometria foi quantificada através do aparelho espirômetro, para verificar as
capacidades pulmonares, como a capacidade pulmonar total (CPT), capacidade vital forçada
(CVF), volume expiratório forçado no primeiro segundo (VEF1), fluxo expiratório forçado
entre 25 e 75% da capacidade vital (FEF25-75%), pico de fluxo expiratório (PFE), e índice de
Tiffeneau (VEF1/CVF).
Para a realização do testes espirométricos, primeiramente foi realizada uma
demonstração para o indivíduo das manobras e movimentos respiratórios que ele deveria
realizar durante o exame, para que ficasse mais fácil o entendimento.
•
Primeiramente o paciente foi instruído a sentar-se;
•
Foi orientada a colocação de um clipe nasal e aclopamento dos lábios ao bocal do
espirômetro hermeticamente;
•
Foi instruído então a realizar uma respiração normal, logo após que ao final da expiração
realizasse inspiração forçada máxima, seguida sem interrupção, de expiração rápida e
forçada durante um mínimo de seis segundos. Ao final da inspiração máxima que precede
a expiração forçada, pausa inspiratória de no máximo três segundos;
57
•
O teste foi realizado até serem obtidas três curvas reprodutíveis, considerando satisfatório
quando a curva foi adequada, ou seja, pico de fluxo expiatório inicial o mais elevado o
possível, seguido de queda homogênea dos fluxos e semelhantes nas manobras sucessivas,
e quando os valores da VEF1 e CVF não diferiam mais de 5 %.
•
O teste foi realizado algumas vezes até conseguir a curva adequada, respeitando o limite
de tentativas, que eram oito.
3.6 Procedimentos para a análise e interpretação de dados
Após a coleta dos dados realizada durante a avaliação dos indivíduos onde foram
expostos em forma de tabelas utilizando-se o Microsoft Excel. As variáveis foram descritas
em média ± erro padrão médio, o método estatístico utilizado foi o teste de distribuição The
Stundent pareado (p< 0,05).
Segundo Ander Egg apud Rauen (2002), uma tabela tem a função de auxiliar o
investigador, permitindo que ele “distinga semelhanças e diferenças em relações mediante a
clareza e o relevo que a distribuição lógica presta a classificação.” Tem a função de
simplificar os dados para melhor compreensão.
Os gráficos serão utilizados assim como as tabelas para todos os dados coletados
“[...] por vezes, os dados apresentados em tabelas são de difícil interpretação e a
representação pictórica é mais acessível.” (RAUEN, 2002, p. 139), o gráfico utilizado foi o
histograma de colunas.
58
4 ANÁLISE E DISCUSÃO DOS DADOS
4.1 Resultados
Os resultados foram expressos em tabelas, (Tabela 1) foram representados os
valores referentes aos efeitos do treinamento sobre as capacidades pulmonares dos pacientes
com EA.
Pela avaliação espirométrica as variáveis apresentaram os valores com média ±
EPM (erro padrão médio): CVF (3,8 l ± 0,7l antes e 3,9 ± 0,6 l depois); VEF1 (antes 3,2 l ±
0,7 e 3,1 ± 0,8 após); VEF1 % (antes 83,2± 3,1% e após 78,7 ± 6,7%); FEF25-75%, (antes 3,4 ±
1,0 l e após 3,1 ± 1,4 l); PFE (antes 8,8 ± 1,5 l e após 8,3 ± 1,5 l); portanto, não
apresentaram diferenças significativas após o período de treinamento (Tabela 1). Um paciente
apresentou distúrbio ventilatório restritivo leve, devido à redução da CVF e VEF1 e índice de
Tiffeneau normal (Tabela 1).
59
Tabela 1 – Efeitos do treinamento sobre as capacidades pulmonares de pacientes com
EA. Os valores estão expressos em média ± de erro padrão médio. NS para p> 0,05 e S
<0,05.
Capacidades
Antes
Depois
Significância
CVF ¹
3,8 l ± 0,7
3,9 ± 0,6
NS
VEF1 ¹
3,2 ± 0,7
3,1 ± 0,8
NS
VEF1 ³ %
83,2%± 3,1
78,7% ± 6,7
NS
FEF25-75%¹,
3,4 ± 1,0
3,1 ± 1,4
NS
PFE ²
8,8 ± 1,5
8,3 ± 1,5
NS
¹ - Valores em litros; ² - Valor em l/min; -³Valor em porcentagem.
Na tabela 2, foram representados os valores dos efeitos do treinamento sobre os
músculos ventilatórios dos pacientes com EA.
Já na manovacuometria, pode-se constatar que houve um aumento significativo de
15% na PEmáx, entre o início do treinamento (160,0±15,3cmH2O) e o final (183,3±16,7
cmH2O), melhorando a mecânica respiratória quanto a funções de tosse e expectoração.
Entretanto a PImáx manteve-se inalterada, sendo no início do treinamento (183,3± 34,8
cmH2O) e o final (180,0±40,4 cmH2O) tabela 2.
Tabela 2 – Efeitos do treinamento sobre os músculos ventilatórios de pacientes com EA. Os
valores estão expressos em media ± de erro padrão médio. NS para p> 0,05 e S <0,05.
Força Muscular
Antes
Depois
PImáx ¹
183,3± 34,8
180,0±40,4
NS
PEmáx ¹
160,0± 15,3
183,3±16,7
S
Significância
1 – Valores em cmH2O
Após a reavaliação do IMC os pacientes não apresentaram diferença significativa
na massa corporal, após 12 semanas de exercícios na piscina.
60
4.2 Discussão
Para Dagfinrund (2004), após uma meta-análise constatou que existe uma
tendência favorável sobre os efeitos positivos da fisioterapia na manutenção da EA, e os
novos exames dirigem outras intervenções terapêuticas das geralmente usadas na clínica.
Segundo Peralta (2004), uma das principais intervenções no tratamento da EA,
seria a manutenção da mobilidade torácica e expansão da caixa torácica que compromete
muitas vezes a função pulmonar desses pacientes, assim como a excussão de exercícios
respiratórios para a função dos músculos paravertebrais envolvidos na respiração, mantendo
assim uma melhor função respiratória.
O treinamento em ambiente aquático foi benéfico, devido às propriedades físicas
da água, facilitando a realização do treinamento. Para Hernandes et al (2005), após
treinamento aquático com quatro indivíduos com EA durante dez semanas, observou uma
melhora qualidade de vida e capacidade funcional desses indivíduos.
A diminuição da função pulmonar está freqüentemente relacionada com a
diminuição da expansibilidade torácica para muitos autores, entretanto após estudos Sampaio
Barros et al (1999), observou que defeito ventilatório restritivo não estava associado à
restrição volumétrica causada pela anquilose das articulações costovertebrais, em pacientes de
longa duração.
Na avaliação da função pulmonar dos indivíduos da pesquisa pode-se constar um
padrão ventilatório restritivo leve em um dos indivíduos, após a análise dos valores de VEF1 e
CVF, que seria 4,15 e 5,2
(valores aproximados) respectivamente, sendo menor que 80%
do predito. Segundo Pereira (1996), os resultados de VEF1 e CVF devem diferir menos de 0,2
. Após estudos, Sampaio (1999), avaliou a função pulmonar de 27 pacientes com EA,
encontrou alteração em 81% dos pacientes, sendo o defeito restritivo encontrado em 48% dos
61
pacientes.
A análise da função pulmonar através da espirometria não apresentou valores
significativos após o período de treinamento aquático. A CPT, CRF, CI (Gráfico 1) no geral
estavam dentro dos valores preditos, esse fato seria explicado segundo Seckin et al (2002),
porque a função pulmonar dos pacientes com EA, estaria sendo mantida pela compensação
diafragmática, devido a diminuição da complacência torácica.
Gráfico 1 – Capacidades pulmonares em litros pré e pós treinamento aquático em pacientes
com EA
Henderson (2003), após um estudo de caso com um paciente com EA observou
que expansão pulmonar na inspiração apresentou-se diminuída e a inspiração forçada estava
acompanhada de um audível estridor.
Entretanto pode-se observar que VEF1 encontrava-se um pouco diminuída em
relação ao predito antes e após o treinamento aquático, mas com diferenças não significantes.
Hernandes (2004), que após treinamento aquático em 10 semanas, observou uma redução da
VEF1 em metade dos indivíduos e aumento na outra metade, diminuindo na reavaliação.
A CVF encontrava-se um pouco diminuída relacionada ao previsto, mantendo o
mesmo valor na reavaliação isto sugere que o treinamento diminuiu a progressão da doença
62
no que se refere à função pulmonar. (Gráfico 1). Esse resultado corrobora com os estudos de
Seckin et al (2002), em que demonstrou que a capacidade do exercício do pacientes com EA,
não está influenciada pela diminuição da complacência torácica e sim devido à falta de
manutenção de uma atividade física moderada, junto com estilo de vida ativo.
Foi possível observar uma diminuição após o treinamento aquático da FEF25-75%,
mantendo-se ainda dentro dos valores preditos segundo Pereira (1996), a redução do FEF2575%,
após estudos comparativos com análises anátomo-fisiológicos, seria em conseqüência de
uma alteração histológica nas vias áreas periféricas. Esses resultados sugerem que não
haveria, acometimento no que se refere à fibrose apical, geralmente assintomática, e, segundo
Sampaio et al (1999), comum em doenças e longa duração, relacionada com a restrição da
expansibilidade torácica (Gráfico 2).
Segundo Pereira (1996), o PFE é um parâmetro expiratório esforço-dependente
que reflete o calibre das vias aéreas proximais e ele pode ser usado como índice da capacidade
de tossir. O PFE encontrava-se diminuído após o treinamento aquático com valores não
significantes (como visto anteriormente no item 4.1), como podemos observar no Gráfico 2.
Gráfico 2 – Valores espirométricos em litros por segundo pré e pós treinamento aquático em
paciente com EA.
63
Seckin (2002), afirma que a pressão expiratória máxima (PEmáx) e a pressão
inspiratória máxima (PImáx), estão correlacionadas com a expansão da caixa torácica.
Vaderchuerem et al (1999), observaram que a força muscular respiratória estava preservada
nos pacientes com EA devido à manutenção da força da musculatura intercostal.
Após a avaliação da força muscular respiratória pode-se constar uma diminuição
da PImáx não significante, diferentemente do resultado encontrado por Hernandes (2004), que
após o treinamento observou um aumento da PImáx, após o treinamento de 37% em três dos
quatro indivíduos treinados. Assim como nos estudos de Carter et al (1999), onde se constou
um valor mais elevado na pressão inspiratória máxima (PImáx) no grupo com EA, comparado
ao controle, o que significa que os pacientes com EA tiveram uma força muscular maior do
que o grupo controle. Esses achados seriam devido à compensação diafragmática.
Esses achados corroboram com os estudos de Souza Jr (2001), onde avaliou 17
pacientes com EA através da tomografia computadorizada e observou que não houve
correlação entre alterações pleuropulmonares e grau de acometimento da coluna, entretanto
observou redução da mobilidade parietal dos campos médio e superior, com aumento da
mobilidade diafragmática.
Na PEmáx foi possível observar um aumento significativo de 15% entre o início do
treinamento e o final (Gráfico 3), sugerindo uma melhora nas funções de tosse e expectoração
desses pacientes. Em virtude disso, para Carter et al (1999), concluíram em seus estudos que
não há nenhuma correlação significativa entre a expansão da caixa torácica, função pulmonar
e capacidade do exercício. Neste estudo concluíram que a força dos músculos periféricos era
determinantemente mais importante, sugerindo então que o descondicionamento era o fator
principal na capacidade reduzida do exercício, os músculos periféricos, explicariam 53% da
capacidade do exercício.
64
Gráfico 3 – Valores da manovacuometria em centímetros d’ água pré e pós treinamento
aquático em pacientes com EA.
Segundo estudos de Zanchet; Viegas; Lima; (2004), após 12 semanas de
exercícios aquáticos de pacientes com doença pulmonar obstrutiva crônica (DPOC) ocorreu
uma aumento da PImáx, que seria decorrente ao condicionamento geral do paciente, uma vez
que não realizado treino da musculatura respiratória e também não houve alteração no IMC.
Foi observado que os exercícios aquáticos minimizaram a progressão da doença
no que se refere à função pulmonar, isso seria confirmado também por Seckin et al (2002),
onde neste estudo demonstrou que a função pulmonar dos pacientes não está influenciada
somente pela limitação caixa torácica, mas sim devido a não manutenção de atividade física
moderada junto com um estilo de vida ativo. Este estudo corrobora com os estudos de Chouri
e Driusso (2004), onde após cinco meses de treinamento em solo e água de pacientes com EA
observou, uma melhora na função pulmonar e qualidade de vida dos indivíduos pesquisados.
Este trabalho confirma a importância do treinamento físico desses indivíduos.
Esses achados são confirmados por Ghosh (2003), onde ele afirma que o tratamento
fisioterápico para EA seria melhorar a mobilidade e vigor físico, prevenindo a redução da
curvatura vertebral anormal. O tratamento físico deve incluir fisioterapia e exercícios
65
regulares contribuindo para diminuição da progressão da EA, mas não substitui o tratamento
farmacológico. Para o autor o exercício físico é impossível com dor e infamação não
controladas, entretanto a rigidez e a deformidade postural não são prevenidas apenas com
drogas.
.
.
66
5 CONSIDERAÇÕES FINAIS
•
Após a análise dos valores espirométricos pode-se verificar neste estudo que apesar da
diminuição da complacência torácica causada pela doença, capacidade vital forçada
(CVF) encontrava-se pouco diminuída, manteve-se no mesmo valor após o treinamento
aquático, provavelmente devido à compensação diafragmática.
•
As capacidades pulmonar total e residual funcional (CPT) e (CRF) assim como
capacidade inspiratória (CI) estavam dentro do previsto e permaneceram após o
treinamento com valores não significantes.
•
O volume expiratório forçado no primeiro segundo (VEF1) em apenas um indivíduo
encontrou-se diminuído antes e após o treinamento aquático em relação predito. Esse
resultado provavelmente devido a o padrão pulmonar restritivo de acometimento da
patologia.
•
O índice Tiffenau (VEF1/CVF) apresentou-se dentro dos níveis normais e permaneceu
inalterada após o treinamento.
•
O fluxo expiratório forçado entre 25 e 75% da capacidade vital (FEF25-75%) encontrou-se
dentro do predito, sugerindo não acometimento anátomo-funcional de vias aéreas
periféricas, permanecendo o mesmo após o treinamento.
•
A pressão inspiratória máxima (PImáx), mostrou alterações não significantes. Devido à
rigidez da caixa torácica desses pacientes, haveria um aumento da função do músculo
67
principal da inspiração o diafragma, para compensar a pouca mobilidade do gradil costal,
fator importante para a mecânica da ventilação.
•
Após o treinamento aquático pode-se constar um aumento significativo na PE máx
sugerindo que o descondicionamento seria então um fator importante para a capacidade
cardio-respiratória desses pacientes. Esse resultado ressalta a importância de um programa
de treinamento para os indivíduos portadores de EA, para diminuir a progressão da doença
não só no acometimento músculo-esquelético, mas também uma melhora da função
pulmonar.
68
REFERÊNCIAS
AZEREDO, Carlos Alberto Caetano. Fisioterapia respiratória moderna. 3 ed. São Paulo:
Manole. 1999.
BUSS, Daniela Cristina, et al. Conceitos avaliação e tratamento da espondilite
anquilosante: uma revisão de literatura. UNISUL, Tubarão – SC. 2000.
CARTER, R; RIANTAWAN, P. An investigation of factors limiting aerobic capacity in
patients with ankylosing spondylits. Respiratory Medicine. 1999. Oct. 700-8.
CHOURI, Tatiane Melloni; DRIUSSO, Patrícia. Tratamento fisioterapêutico de pacientes
com espondilite anquilosante. 2004. UMESP. Disponível em: <http//www.usp.br>. Acesso
em: fev. 2005.
COBRA, Castor; COBRA, Alessandra. Espondilite anquilosante. 2006. Disponível em:
<http//www.reumatismo.med.br/espnd.anq.>. Acesso em 25 abr de 2006.
COSTA, Dirceu. Fisioterapia respiratória básica. São Paulo: Livraria Atheneu, 2004.
CRUZ FILHO, Achiles. Clínica reumatológica. Rio de Janeiro: Guanabara Koogan, 1980.
DAGFINRUD H., et all. Physiotherapy interventions for ankylosing, agos. 2004.
Disponível em: <http://www.cochrane.com >. Acesso em: 15 de mar. 2006.
DEGANI, Adriana Menezes. Hidroterapia: os efeitos físicos, fisiológicos e terapêuticos da
água. Fisioterapia em movimento, set 1998. v 10. nº 1.
69
ESPONDILOARTROPATIAS. Departamento de clínica médica da USP. 2006. Disponível
em:http// <www. fm.usp.br/departamento/cli.med/reumatologia.espond.pbp>. Acesso em 25
abr de 2006.
FISCHER, Nadine M. Fisiologia clínica do exercício: pesquisa do ACSM. Osteoartrite,
artrite reumatóide e fibromialgia. 2002. Rio de janeiro: Guanabara Coogan.
GABRIEL, Mª Serra. Fisioterapia em traumatologia ortopedia e reumatologia. Rio de
Janeiro: Revinter, 2001.
GIL, Antonio Carlos. Como elaborar projetos de pesquisa. 3. ed. São Paulo: Atlas, 1996.
GHOSH A. et al. Treatment of ankylosing spondylitis with special reference to biologics
single center experience. J Indian Rheumatology Assoc. n 12. 2003. Disponível em:
<www.cochrane.com>. Acesso em 20 de març. 2006.
GOLDING, Douglas N. Reumatologia em medicina e reabilitação. São Paulo: Livraria
Atheneu, 1999. Tradução: Ciro Lobato de Carvalho.
GREENSPAN, Adam. Radiologia ortopédica. Rio de Janeiro: Guanabara Koogan. 2001.
HEERDT, Mauri Luiz; LEONEL, Vilson. Metodologia científica: disciplina na modalidade à
distância. 2. ed. Palhoça: UnisulVirtual, 2005.
HENDERSON, Shawn et all. Rehabilitation techniques in ankylosing spondylitis
management: a case report. J Can. Chiropr. Assoc.n 47. 2003.
HERNANDES, Nídia Aparecida; IDE, Maiza Ritomy; CAROMANO, Fátima Aparecida.
Fisioterapia Aquática na qualidade de vida e capacidade funcional de pacientes com
espondilite anquilosante. Fisioterapia Brasil. v. 6, n. 1, p. 75-78, jan./fev. 2005.
HERNANDES, Nídia Aparecida. Influência da fisioterapia aquática na função pulmonar
de pacientes com espondilite anquilosante: série de casos. UNIOESTE. Cascavel-PR. 2004.
KAPANDJI, A. I.. Fisiologia articular: esquemas comentados de mecânica humana. 5. ed.
São Paulo: Panamericana; Rio de Janeiro: Guanabara Koogan, 2000. v. 3. Tradução: Editorial
medica panamericana.
70
KOURY, Joanne M. Programa de fisioterapia aquática: um guia para a reabilitação
ortopédica. São Paulo: Manole, 2000. Tradução: Solange Pessini Sieprusk.
LINDEN, S. van der; TUBERGEN A. van; HIDDING, A. Physiotherapy in Ankylosing
spondylitis: What is the evidence?. Disponível em: <www.cochrane.com>. Acesso em: 15
març. 2006.
MEIRELLES, Eduardo de Souza; KITADAI, Fabio. Aspectos clínicos e epidemiológicos da
espondilite anquilosante. Revista Brasileira de Reumatologia, mar-abr, 1999. Disponível em
<http//: www.bireme.com.br>. Acesso em: 25 abr. 2005.
MEIRELLES, Eduardo de Souza; KITADAI, Fabio. Conceituação e atualização no
tratamento da espondilite anquilosante. Revista brasileira de reumatologia, mar./abr, 2001.
v.4. Disponível em: <http//: www.bireme.br/cgi-bin/wxislind.exe/iah/online/>, Acesso em: 15
mar. 2006.
MOREIRA, Caio; CARVALHO, Marco Antônio P. Reumatologia: diagnóstico e tratamento.
2 ed. Rio de Janeiro: MEDSI, 2001.
NEDER, Alberto J.; NERY, Luiz Eduardo. Clínica do exercício: teoria e prática. [S.I.]: Artes
Médicas, 2003.
PERALTA, Gustavo Bocca. Rehabilitación en espondilitis anquilosante. Monografía. Revista
mexicana de medicina física y rehabilitación. n. 16. 2004.
PEREIRA, Carlos Alberto de Castro (coord.). I CONSENSO BRASILIEIRO SOBRE
ESPIROMETRIA. Corrd. Carlos Alberto de Castro Pereira. Jornal de pneumologia. Maio/
jun.1996.
RAUEN, Fábio José. Roteiros de investigação científica. Tubarão: Ed. UNISUL, 2002.
RICHARDSON, Roberto Jarry. Pesquisa social: métodos e técnicas. 2 ed. São Paulo: Atlas,
1989.
SALTER, Robert B. Distúrbios e lesões do sistema músculo esquelético. 3 ed. Rio de
janeiro: Manole. 2001. Tradução: Luis Américo Leão Bicalho.
SAMPAIO BARROS, Percival D., et al. Função pulmonar na espondilite anquilosante.
Revista Brasileira de Reumatologia, mar-abr, 1999. v 39. Disponível em: <http//:
www.bireme.com.br>. Acesso em: 25 abr. 2005.
71
SAMPAIO BARROS, Percival D., et al. Undifferentiated spondyloarthropathies in Brazilians:
Importance of HLA-B27- CREG Alleles in characterization and disease progression. The
Journal of rheumatology, 2003.
SECKIN et al. Relationship between pulmonary function and exercise tolerance in
patients with ankylosing spondylitis. Clinical and Experimental Rheumatology, 2002. p
503-506.
SERRA GABRIEL, Mª R.; DÍAZ PETIT, J.; SANDE CARRIL, Mª L.. Fisioterapia em
traumatologia, ortopedia e reumatologia. Rio de Janeiro: Revinter, 2001.
SHNEERSON, John. Distúrbios da ventilação. Rio de Janeiro: Revinter, 1993. Tradutor:
Ivan Mário Brun.
SILVA, Luiz Carlos Corrêa da; RUBIN, Adalberto Sperb; SILVA, Luciano Müller Corrêa da.
Avaliação funcional pulmonar: incluindo questões de auto-avaliação e respostas
comentadas. Rio de Janeiro: Revinter, 2000.
SILVERIA, Ismar Chaves da. O pulmão na prática médica. 4 ed. Rio de Janeiro: Ed. de
Publicações Biomédicas, 2000. v. 2.
SKARE, T. L. Reumatologia: Princípios e prática. 1 ed. Rio de Janeiro: Guanabara Koogan.
1999.
SOCIEDADE BRASILEIRA de Reumatologia. Projeto diretrizes. Espondiloartropatias:
Espondilite anquilosante e artrite psoriásica, jun. 2004.
SOUZA JUNIOR, Arthur Soares. Espondilite anquilosante: avaliação pulmonar pela
tomografia computadorizada de alta resolução e mobilidade das paredes torácicas. Tese de
doutorado.Revista Brasileira de Pneumologia. v. 34, n. 4. São Paulo. Jul./ago. 2001.
VANDERCHUEREM et al. Pulmonary function and maximal transrespiratory pressures in
ankylosing spondylitis. Department of Internal Medicine, K U Leuven, Belgium. Aug;
1999.
WEST, John B. Fisiologia respiratória moderna. 5. ed. São Paulo: Manole, 1996. Tradução:
Nelson Gomes de Oliveira.
72
ZANCHET, Renata Claudia; VIEGAS, Alberto de Assis; LIMA, Terezinha. A eficácia da
reabilitação pulmonar na capacidade de exercício, força da musculatura inspiratória e
qualidade de vida de portadores de doença pulmonar obstrutiva crônica. Universidade
Católica de Brasília, DF, 2004.
73
APÊNDICE
74
APÊNDICE A
Termo de consentimento
75
UNIVERSIDADE DO SUL DE SANTA CATARINA – UNISUL
CURSO DE FISIOTERAPIA
TRABALHO DE CONCLUSÃO DE CURSO
TERMO DE CONSENTIMENTO
Eu, ________________________________________, RG._________________, declaro que
aceito os procedimentos a que serei submetido, conforme explicações que foram a mim
passadas pelo responsável da pesquisa, sendo que os dados obtidos serão utilizados somente
para o desenvolvimento da pesquisa, mantendo assim minha identidade no anonimato. Assim
informo que estou ciente dos procedimentos que serei submetido, concordando com os
mesmos e que posso abandonar.
Tubarão (SC) em ____/____/____
Assinatura do avaliado:__________________________________________________
Assinatura do avaliador:____________________________________________________