Eventos hepáticos no estudo pivotal Fase III VEG1051925,6
• O estudo VEG105192 incluiu pacientes com RCC metastático recebendo Votrient
800 mg/dia via oral (n=290) ou placebo (n=145).5
Tabela 1
Eventos hepáticos no estudo piloto Fase III VEG1051925,6
®
• Elevações nas transaminases séricas (ALT e AST) e na bilirrubina foram observadas
com Votrient® (Tabela 1).5
• Elevações nas transaminases ocorreram no início do curso de tratamento (92,5% de
todas as elevações nas transaminases de qualquer grau ocorreram nas primeiras 18
semanas).4,5
• Na maioria dos casos, elevações isoladas da ALT e AST foram relatadas,
sem elevações concomitantes de fosfatase alcalina (FA) ou de bilirrubina.5
• Elevações da ALT ≥ 3x o limite superior da normalidade (valor de referência)
ocorreram em 52 pacientes tratados com Votrient® (18%); elevação de ALT retornou
para Grau 1 ou menos, após a alteração da dose, interrupção ou descontinuação
em 45 pacientes (87%), enquanto os sete pacientes restantes (13%) não tinham
dados suficientes de acompanhamento para avaliar a recuperação.
• A função hepática (ALT, AST, FA e bilirrubina total) deve ser monitorada antes do
início do tratamento, pelo menos uma vez a cada 4 semanas nos primeiros 4 meses
de tratamento e, a partir de então, mensalmente, ou conforme indicação clínica.5
• A dose de Votrient® deve ser descontinuada se as alterações na função hepática forem graves, e os pacientes não devem ser tratados novamente com essa medicação.5
Resumo das alterações laboratoriais hepáticas
em pacientes no estudo VEG 1051926
• A segurança e a farmacocinética do pazopanibe não foram completamente estabelecidas em
pacientes com insuficiência hepática preexistente.
• O uso de Votrient® em paciente com insuficiência hepática leve ou moderada deve ser conduzido
com cautela e monitorado de perto.
• É recomendado que os pacientes com alterações leves nos parâmetros hepáticos
sejam tratados inicialmente com 800 mg de pazopanibe uma vez ao dia.
• Uma dose reduzida de pazopanibe de 200 mg uma vez ao dia é recomendada para pacientes
com insuficiência hepática moderada.
• Votrient® é contraindicado em pacientes com insuficiência hepática grave.
Votrient® (n=290) n (%)
Qualquer
grau
Grau 3
Grau 4
Qualquer
grau
Grau 3
Grau 4
Aumento da ALT
152 (53)
30 (10)
5 (2)
32 (22)
2 (1)
0 (0)
Aumento da AST
152 (53)
21 (7)
2 (<1)
27 (19)
1 (<1)
0 (0)
Aumento da BT
102 (36)
7 (3)
2 (<1)
15 (10)
2 (1)
1 (<1)
Alterações
laboratoriais hepáticas
Parâmetros bioquímicos
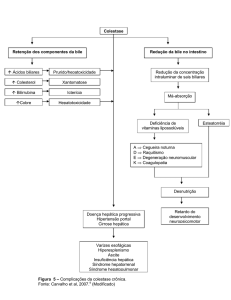
Figura 1. Recomendações da GlaxoSmithKline para o gerenciamento
da hepatotoxicidade no tratamento com Votrient®4,5
ANTES DO TRATAMENTO
COM VOTRIENT®
Placebo (n=145) n (%)
ALT= Alanina animo transaminase; AST= aspartato animo transaminase; BT= bilirrubina total
Monitore os testes
hepáticos séricos
Referências
DEPOIS DO TRATAMENTO
COM VOTRIENT®
1. SONPAVDE, G. et al. Pazopanib: a novel multitargeted tyrosine kinase inhibitor. Curr Oncol Rep, 9: 115-9, 2007.
Monitore pelo menos uma vez a cada
4 semanas durante 4 meses e, a partir
de então, periodicamente
Níveis isolados
de transaminases ≤8X
(UNL ou LSN)
Níveis de transaminases >3X
(UNL ou LSN)
E BT >2X (UNL)
2. KUMAR, R. et al. Myelosuppression and kinase selectivity of multikinase angiogenesis inhibitors. Br J Cancer, 101(10): 1717-23, 2009.
Níveis de
transaminases >8X
(UNL)
3. SONPAVDE, G. et al. Pazopanib, a potent orally administered small-molecule multitargeted tyrosine kinase inhibitor for renal cell carcinoma.
Expert Opin Investig Drugs, 17(2): 253-61, 2008.
4. VOTRIENT® (pazopanib hydrochloride). UK prescribing information.Disponível em: <http://www.medicines.org.uk/emc/medicine/23148/SPC/votrient20200%20mg%20and%20400%20mg%20film%20coated%20tablets/>. Acesso em: 10 abr. 2012.
5. VOTRIENT® (cloridrato de pazopanibe). Bula do produto.
• Não há consenso publicado sobre os critérios de suspensão em caso de alterações
bioquímicas hepáticas nos estudos clínicos.9
• Com base nas diretrizes propostas pela FDA para a indústria10, a GlaxoSmithKline
desenvolveu recomendações de gerenciamento para a hepatotoxicidade que foram
usadas em estudos clínicos de RCC metastático e/ou avançado (Figura 1).5
• Os pacientes devem ser alertados de que a hepatotoxicidade ocorreu com o uso de
Votrient® e pode, em casos raros, ser fatal. Com base em dados do estudo pivotal, a
hepatotoxicidade é listada como um efeito colateral no Resumo das Características
do Produto.5
Interrompa o Votrient até que os
níveis de transaminases voltem
ao Grau 1 ou do período basal
®
Continue o tratamento
Realize o fracionamento da bilirrubina
6. STERNBERG, CN. et al. Pazopanib in locally advanced or metastatic renal cell carcinoma: results of a randomized Phase III trial. J Clin Oncol, 28(6):
1061-68, 2010.
7. LAUNAY-VACHER, V. et al. Hypertension and proteinuria: a class-effect of antiangiogenic therapies. Anticancer Drugs, 20: 81–82, 2009.
Monitore a função hepática semanalmente até que
os níveis das transaminases retornem ao Grau 1
ou do período basal
Bilirrubina Direta >35% do total
SIM
NÃO
Descontinue o
tratamento
Continue o
tratamento
*BT= bilirrubina total; UNL = Limite Superior da Normalidade
Reintroduza Votrient®, se justificar,
em doses menores e avalie as
enzimas hepáticas séricas
semanalmente durante 8 semanas.
Descontinue o tratamento se
os níveis de transaminases >3X
(UNL) ocorrerem novamente
Adaptado a partir da referência 5.
8. MANCIA, G. et al. Guidelines for the management of arterial hypertension: The task force for the management of arterial hypertension of the
european society of hypertension (ESH) and of the european society of cardiology (ESC). Eur Heart J, 25: 1105–1187, 2007.
9. HAWKINS, RE. et al. An open-label extension study to evaluate safety and efficacy of pazopanib in patients with advanced renal cell carcinoma
(RCC). J Clin Oncol, 27(15S): abs. 5110, 2009.
Segurança Hepática e Tratamento com
Votrient® (cloridrato de pazopanibe)
Votrient® (cloridrato de pazopanibe) é um inibidor oral da tirosina quinase (TKI) seletivo que
exibe inibição potente do receptor do fator de crescimento endotelial vascular (VEGFR)-21,
o principal mediador da angiogênese mediada pelo fator de crescimento endotelial vascular
(VEGF), mas também objetiva o VEGFR-1 e 3, receptores α e β dos fatores de crescimento
derivados de plaqueta e c-kit.1-3
Votrient® foi aprovado pela Food and Drug Administration (FDA) dos EUA, pela European
Commission e pela ANVISA para o tratamento do carcinoma de células renais avançado
(RCC).4,5 No Brasil, Votrient® é indicado para o tratamento de carcinoma de células renais
(RCC) avançado e/ou metastático.5
O estudo pivotal de Fase III VEG105192 foi desenhado para avaliar a eficácia e a segurança
de Votrient® em comparação com o placebo em pacientes portadores de RCC avançado sem
exposição prévia ao tratamento e tratados previamente com citocinas.5,6 O estudo demonstrou que Votrient® proporcionou melhora significativa na Sobrevida Livre de Progressão na
população geral do estudo (n=435; mediana, 9,2 meses versus a 4,2 meses; p <0,0001), os
pacientes sem exposição prévia ao tratamento (n=233; mediana, 11,1 meses versus a 2,8
meses; p <0,0001) e pacientes tratados previamente com citocinas (n=202; mediana, 7,4
meses versus a 4,2 meses; p<0,001) com RCC metastático e/ou avançado, em comparação
com placebo.6 De forma semelhante, as taxas de resposta tumoral foram maiores com
Votrient® comparado ao placebo na população geral (30% versus a 3%; p<0,001), nas
populações sem exposição prévia ao tratamento (32% versus a 4%) e com tratamento prévio
com citocinas (29% versus a 3%).6
A hepatotoxicidade está sendo cada vez mais reconhecida como um efeito de classe que
está associado a algumas TKIs, independentemente do alvo molecular.7,8 Em estudos clínicos com Votrient®, observou-se hepatotoxicidade, a qual se manifesta como o aumento das
transaminases séricas (alanina aminotransferase [ALT] e aspartato aminotransferase [AST])
e bilirrubina.5,6 A hepatotoxicidade pode, em casos raros, ser grave e fatal. Elevações nas
transaminases ocorrem no início do curso de tratamento (92,5% de todas as elevações nas
transaminases de qualquer grau ocorreram nas primeiras 18 semanas).4,5
Recomendações específicas para o gerenciamento da hepatotoxicidade com a terapia com
Votrient® foram desenvolvidas pela GlaxoSmithKline (Figura 1).
Votrient® (cloridrato de pazopanibe). APRESENTAÇÃO: Comprimidos revestidos de 200 mg e 400 mg, para uso oral, em cartuchos com 30 e 90 comprimidos (200 mg) e 30 e 60 comprimidos (400 mg). Mantenha
o produto na embalagem original e em temperatura ambiente (entre 15°C e 30°C). INDICAÇÕES: Votrient® é indicado para o tratamento de carcinoma de células renais (RCC) avançado e/ou metastático.
CONTRAINDICAÇÕES: Votrient® é contraindicado a pacientes com hipersensibilidade a qualquer um dos componentes da formulação. Não existem contraindicações relativas à faixa etária. Entretanto,
Votrient® não foi suficientemente estudado em pacientes com menos de 18 anos de idade. POSOLOGIA: A dose recomendada é de 800 mg uma vez ao dia, por via oral. Votrient® deve ser ingerido sem
alimentos, pelo menos uma hora antes ou duas horas após uma refeição. Os comprimidos de Votrient® devem ser tomados inteiros, com água, e não devem ser partidos nem esmagados. As alterações de
dosagem devem ocorrer em incrementos de 200 mg, de modo gradativo e com base na tolerabilidade individual, com a finalidade de controlar reações adversas. A dose de Votrient® não deve ser superior a
800 mg. O uso concomitante de inibidores fortes de CYP3A4 pode aumentar as concentrações de pazopanibe e deve ser evitado. Caso se justifique a administração concomitante de um inibidor forte de
CYP3A4, recomenda-se, com base em estudos farmacocinéticos, reduzir a dose de Votrient® para 400 mg. Prevê-se que esta dose ajuste a AUC do pazopanibe para a faixa observada sem o uso desses
inibidores (ver Interações). Não há, contudo, dados clínicos sobre essa alteração de dose em pacientes tratados com inibidores fortes de CYP3A4. É pouco provável que a insuficiência renal exerça um efeito
clínico relevante sobre a farmacocinética do pazopanibe, dada a baixa excreção renal de pazopanibe e metabólitos, não havendo necessidade de alterações na dose. ADVERTÊNCIAS E PRECAUÇÕES: Efeitos
hepáticos: Foram relatados casos de insuficiência hepática, inclusive fatais, durante o uso de Votrient®. Em ensaios clínicos com Votrient® observaram-se aumentos das transaminases séricas (ALT, AST) e
da bilirrubina (ver Reações Adversas). Na maioria dos casos foram relatados aumentos isolados dos valores de ALT e AST, sem elevações concomitantes da fosfatase alcalina ou da bilirrubina. Recomendase a monitorização da função hepática antes de iniciar o tratamento com Votrient® e pelo menos uma vez a cada quatro semanas durante os primeiros quatro meses de tratamento, bem como quando
clinicamente indicado. Depois disso, realizar monitorização periódica. Pacientes com elevações isoladas da ALT entre 3 x LSN e 8 x LSN podem continuar o tratamento com Votrient®, mediante monitorização
semanal das funções hepáticas, até que a ALT volte ao Grau 1 ou ao valor basal. Pacientes com ALT > 8 x LSN devem descontinuar o uso de Votrient® até que os níveis retornem ao Grau 1 ou aos basais. Se
os efeitos benéficos do reinício do tratamento com Votrient® superarem os riscos de hepatotoxicidade, reintroduzir o medicamento com dose reduzida de 400mg uma vez ao dia e verificar a função hepática
semanalmente durante oito semanas (ver Posologia). Após a reintrodução de Votrient®, se elevações de ALT > 3 x LSN se repetirem, interromper o tratamento com Votrient®. Se elevações de ALT > 3 x LSN
coincidirem com elevações de bilirrubina > 2 x LSN, interromper permanentemente o tratamento com Votrient®. Os pacientes devem ser monitorados até a volta ao grau 1 ou aos valores basais. Votrient®
age como inibidor da UGT1A1. Pode-se observar hiperbilirrubina leve e indireta (não conjugada) em pacientes com síndrome de Gilbert. Aqueles que apresentarem apenas hiperbilirrubina leve e indireta,
síndrome de Gilbert suspeita ou confirmada e elevação da ALT >3 x LSN devem ser tratados conforme as recomendações para elevações da ALT. Além da recomendação de que os pacientes com insuficiência
hepática leve sejam tratados com 800 mg de Votrient® uma vez ao dia, e que pacientes com insuficiência hepática moderada reduzam a dose inicial para 200 mg ao dia, nenhuma modificação adicional na
administração das doses, baseando-se nos resultados de testes laboratoriais hepáticos, foi estabelecida para pacientes com insuficiência hepática preexistente. O tratamento com Votrient® não é
recomendado em pacientes com insuficiência hepática. Hipertensão: Em estudos clínicos ocorreram eventos de hipertensão, incluindo crises hipertensivas. Aferir cuidadosamente a pressão arterial antes
de iniciar o tratamento com Votrient®. Os pacientes devem ser monitorizados quanto à hipertensão e tratados conforme necessário por meio de terapia anti-hipertensiva padrão . A hipertensão surge logo
no início do tratamento (39% do casos ocorrem no nono dia e em 88% dos casos, nas primeiras 18 semanas).Se ocorrer hipertensão persistente a despeito de terapia anti-hipertensiva, a dose de Votrient®
pode ser reduzida. O tratamento com Votrient® deve ser interrompido caso o paciente apresente crise hipertensiva ou hipertensão grave ou persistente mesmo com a terapia anti-hipertensiva e a redução
da dose de Votrient®. Prolongamento do intervalo QT e Torsades de pointes: Em estudos clínicos com Votrient® ocorreram eventos de aumento do QT e torsades de pointes. Votrient® deve ser usado com
cautela em pacientes com histórico de prolongamento do QT, em pacientes sob tratamento com antiarrítmicos ou outros medicamentos com potencial de aumentar o QT e em pacientes com doença cardíaca
preexistente relevante. Durante a administração de Votrient® recomenda-se realizar a monitorização periódica de eletrocardiogramas e manter os eletrólitos (cálcio, magnésio, potássio) dentro dos limites
normais. Eventos trombóticos arteriais: Em estudos clínicos com Votrient® observou-se a ocorrência de infarto do miocárdio, angina, acidente vascular cerebral isquêmico e ataque isquêmico transitório.
Houve eventos fatais. O medicamento deve ser usado com cautela em pacientes com alto risco desses eventos ou que possuem antecedentes desses. A decisão sobre o tratamento deve ser tomada com
base na avaliação dos benefícios/riscos individuais para o paciente. Eventos hemorrágicos: Em estudos clínicos com Votrient® foram relatados eventos hemorrágicos. Houve eventos hemorrágicos fatais.
Votrient® não é recomendado para pacientes com histórico de hemoptise ou de hemorragia cerebral ou gastrintestinal clinicamente significativas nos últimos seis meses. Votrient® deve ser usado com
cautela em pacientes com risco significativo de hemorragia. Perfurações e fístulas gastrintestinais: Em estudos clínicos com Votrient® ocorreram eventos de perfuração ou fístula gastrintestinal (GI). Houve
eventos de perfuração fatais. Votrient® deve ser usado com cautela em pacientes com risco de perfuração ou fístula gastrintestinal. Cicatrização de feridas: Não foram conduzidos estudos formais sobre o
efeito de Votrient® na cicatrização de feridas. Uma vez que os inibidores do fator de crescimento vascular endotelial (VEGF) podem dificultar a cicatrização de feridas, o uso de Votrient® deve ser interrompido
pelo menos sete dias antes da data da cirurgia. A decisão de reiniciar o tratamento com Votrient® após a cirurgia deve se basear no julgamento clínico da capacidade de cicatrização. O uso de Votrient®
deve ser interrompido em pacientes com deiscência de ferida cirúrgica. Hipotireoidismo: Em estudos clínicos com Votrient®, ocorreram eventos de hipotireoidismo. Recomenda-se realizar a monitorização
pró ativa da função tireoidiana. Proteinúria: Existem relatos de proteinúria em estudos clínicos com pazopanibe. Recomendam-se exames de urina no início do tratamento, com monitoramento periódico dos
pacientes quanto ao agravamento da proteinúria. Votrient® deve ser suspenso se o paciente desenvolver síndrome nefrótica. GRAVIDEZ: Categoria D de risco na gravidez. Não há dados adequados sobre o
uso de Votrient® em mulheres grávidas. Votrient® pode prejudicar a fertilidade de homens e mulheres. Em estudos sobre a toxicidade reprodutiva feminina realizados com ratos, observou-se a diminuição
da fertilidade feminina.Estudos realizados com animais demonstraram toxicidade reprodutiva, isto é, o uso de pazopanibe em animais foi teratogênico, embriotóxico, fetotóxico e abortivo. O risco potencial em
seres humanos é desconhecido. Votrient® não deve ser usado durante a gravidez, a não ser que a condição clínica da mulher requeira o tratamento com Votrient®. Se for usado durante a gravidez ou se a
paciente ficar grávida no decorrer do tratamento com Votrient®, deve-se informar à paciente os riscos potenciais ao feto. As mulheres com potencial de ter filhos devem ser avisadas da necessidade de usar
a contracepção adequada e de evitar a gravidez durante o tratamento. LACTAÇÃO: O uso seguro de Votrient® durante a lactação não foi estabelecido. Não se sabe se o pazopanibe é excretado pelo leite
humano. A amamentação deve ser interrompida durante o tratamento com Votrient®. Votrient® pode prejudicar a fertilidade de homens e mulheres. Em estudos sobre a toxicidade reprodutiva feminina
realizados com ratos, observou-se a diminuição da fertilidade feminina. Efeitos sobre a capacidade de dirigir veículos e operar máquinas: Não há estudos sobre os efeitos de Votrient® sobre o desempenho
ao dirigir veículos ou sobre a capacidade de operar máquinas. O estado clínico do paciente e o perfil do evento adverso de Votrient® devem ser levados em consideração ao se avaliar a capacidade do
paciente de desempenhar tarefas que requeiram discernimento e habilidades motoras e cognitivas. INTERAÇÕES MEDICAMENTOSAS/ALIMENTARES: os inibidores e indutores do CYP3A4 podem modificar
o metabolismo do Pazopanibe. Recomenda-se a seleção de um medicamento alternativo para uso concomitante que tenha pouco ou nenhum potencial de inibição da CYP3A4, glicoproteína P ou BCRP. A
coadministração de Votrient® com inibidores fortes da família CYP3A4 (p. ex. itraconazol, claritromicina, atazanavir, indinavir, nefazodona, nelfinavir, ritonavir, saquinavir, telitromicina, voriconazol) pode
aumentar as concentrações de pazopanibe. O suco de toranja também pode aumentar as concentrações plasmáticas do pazopanibe. Uma redução de dose para 400mg de pazopanibe uma vez ao dia, na
presença de um inibidor forte de CYP3A4 resulta, na maioria dos pacientes, numa exposição sistêmica similar àquela observada após a administração de 800mg de pazopanibe em monoterapia uma vez ao
dia. Alguns pacientes, no entanto, podem apresentar uma exposição sistêmica de pazopanibe maior que a observada após a administração de 800mg de pazopanibe em monoterapia. A combinação com
inibidores fortes de glicoproteína P ou BCRP deve, portanto, ser evitada, recomendando-se a seleção de um medicamento alternativo para uso concomitante que tenha pouco ou nenhum potencial de inibição.
Se não tiver disponível uma medicação alternativa aceitável para o inibidor forte da família CYP 3A4, a dose de pazopanibe deve ser reduzida para 400 mg/dia durante a administração concomitante.
Uma maior redução de dose pode ser considerada se possíveis eventos adversos forem observados. Indutores de CYP3A4, como a rifampicina, podem diminuir as concentrações plasmáticas de pazopanibe.
Recomenda-se selecionar uma medicação concomitante alternativa cujo potencial de indução de enzima seja inexistente ou mínimo. Estudos in vitro com microssomos do fígado humano demonstraram que
o pazopanibe inibiu as enzimas CYP 1A2, 3A4, 2B6, 2C8, 2C9, 2C19 e 2E1. O pazopanibe pode aumentar as concentrações das drogas que são eliminadas, principalmente, através da UGT1A1 e OATP1B1. Efeito
do uso concomitante de Votrient® com sinvastatina: o uso concomitante de Votrient® com sinvastatina aumenta a incidência de elevações de ALT. Em estudos de monoterapia com Votrient®, ALT > 3 x LSN
foi relatado em 126 dos 895 pacientes (14%) que não usaram estatinas, comparado com os 11 dos 41 pacientes (27%) que fizeram uso concomitante de sinvastatina (p=0,038). Caso um paciente recebendo
sinvastatina simultaneamente desenvolva elevações de ALT, siga as orientações da posologia de Votrient® e interrompa o uso de sinvastatina. Não existem dados suficientes disponíveis para avaliar o risco
da administração concomitante de estatinas alternativas e Votrient®.Efeito dos alimentos sobre Votrient®. A administração de Votrient® junto com uma refeição rica ou pobre em gordura resulta em aumento
praticamente duplicado de AUC e Cmáx. Por isso, Votrient® deve ser administrado no mínino uma hora antes de uma refeição ou duas horas depois (ver Posologia). REAÇÕES ADVERSAS: A segurança e a
eficácia de Votrient® sobre o carcinoma de células renais (RCC) foram avaliadas em um estudo multicêntrico, randômico, duplo-cego e controlado com placebo. Muito comuns (>1/10): anorexia, dor de
cabeça, hipertensão, diarreia, náuseas, vômito, dor abdominal, alaninaminotransferase aumentada, aspartatoaminotransferase aumentada, despigmentação capilar, fadiga, astenia, dor torácica, bradicardia
assintomática. Comuns (>1/100 e <1/10): trombocitopenia, neutropenia, hipotireoidismo, perda de peso, ataque isquêmico transitório, isquemia miocárdica, prolongamento do QT, epistaxe, hematúria, disgeusia,
dispepsia, função hepática anormal, hiperbilirrubinemia, rash cutâneo, alopecia, despigmentação cutânea, síndrome da eritrodisestesia palmoplantar (síndrome mão-pé), proteinúria, elevação da lípase.
Incomuns (>1/1000 e < 1/100): Ataque isquêmico, Torsades de Pointes (Arritmia Cardíaca), hemorragia pulmonar, hemorragia gastrintestinal, hemorragia cerebral, perfuração gastrintestinal, fístulas
gastrintestinais, disfunção cardíaca (redução da fração ejeção e insuficiência cardíaca congestiva), infarto do miocárdio. Anormalidades laboratoriais selecionadas em ≥ 15% dos pacientes que receberam
Votrient® e as apresentaram mais comumente que os do grupo de placebo: leucopenia, neutropenia, trombocitopenia, ALT e AST aumentadas, bilirrubina total aumentada, fósforo reduzido, magnésio
reduzido, glicose reduzida. SUPERDOSE: Doses de Votrient® de até 2.000 mg foram avaliadas em ensaios clínicos. A toxicidade limitante de dose (fadiga grau 3) e hipertensão grau 3 foram observadas em 1
de 3 pacientes medicados com 2.000 mg/dia e 1.000mg/dia, respectivamente. A experiência atual com superdosagem de Votrient® é limitada. Não se espera que a hemodiálise acentue a eliminação
do pazopanibe, uma vez que a excreção do pazopanibe por via renal não é significativa e está fortemente ligada às proteínas de plasma. M.S: 1.0107. 0280. USO RESTRITO A HOSPITAIS. VENDA SOB
PRESCRIÇÃO MÉDICA. mBL_Votrient_com_rev_GDS07IPI07N05_VPS. A bula completa do medicamento e outras informações estão à disposição, sob solicitação ao Serviço de Informação Médica (0800 701
22 33 ou http://www.sim-gsk.com.br).
Votrient® é contraindicado a pacientes com hipersensibilidade a qualquer um dos componentes da formulação.
A coadministração de Votrient® com inibidores de CYP3A4 pode aumentar as concentrações de pazopanibe.
Estrada dos Bandeirantes, 8464
Jacarepaguá - Rio de Janeiro/RJ
CEP 22783-110 - CNPJ 33247743/0001-10
Material de distribuição exclusiva para profissionais de saúde habilitados a prescrever ou dispensar medicamentos. Recomenda-se a leitura da bula e da monografia do produto, antes da prescrição de
qualquer medicamento. Mais informações à disposição, sob solicitação a o Serviço de Informação Médica (0800 701 2233) ou http://www.sim-gsk.com.br).
FEVEREIRO 2012 BR/PAZ/0058/11(1473697)
Segurança
Hepática
e Tratamento
com Votrient®
(cloridrato de pazopanibe)