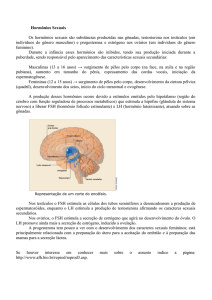
Ciclo menstrual normal
A menstruação é um sangramento genital periódico e temporário que manifestase aproximadamente a cada mês, iniciando-se com a menarca e terminando com a
menopausa.
Ciclo menstrual: é o conjunto de eventos endócrinos interdependentes do
Sistema Hipotálamo-Hipófise-Ovário (SHHO) e as modificações fisiológicas no
organismo que são conseqüentes a esses eventos, visando a preparação para o coito e a
gravidez.
Dois processos reprodutivos principais ocorrem durante cada ciclo:
- 1) Maturação e liberação de um óvulo
- 2) preparação do útero para receber um embrião, caso haja fertilização.
Características e terminologia do sangramento menstrual
O fluxo menstrual é composto por sangue proveniente dos capilares e arteríolas,
e também da camada funcional do endométrio. Não há formação de coágulos, porque
esse sangue não contém fibrinogênio. Os “coágulos” informados pelas pacientes são
agregados de hemácias, substância mucóide, mucoproteínas e glicogênio, formados na
vagina (NÃO HÁ DEPÓSITOS DE FIBRINA).
A duração do ciclo é determinada pela velocidade e qualidade do crescimento e
desenvolvimento folicular e varia entre uma mulher e outra e entre um ciclo e outro.
Média: - sangramento menstrual de 3 a 7 dias. Volume: 30 a 80 mL por dia.
- intervalo entre ciclos: 24 a 35 dias.
Um ciclo nesse padrão é chamado normal ou eumenorréico.
Variações:
- hipermenorréia: sangramento prolongado ( + que 8 dias)
- menorragia: sangramento em quantidade excessiva ( + que 80mL)
- hipomenorréia: duração < 3 dias e/ou volume < 30mL.
- polimenorréia: ciclos curtos ( freqüência < 24 dias)
- oligomenorréia: ciclos longos ( intervalos > 35 dias).
Componentes funcionais do ciclo menstrual
Interação hipotálamo- hipófise- ovário e útero.
O ovário é responsável pela ritmicidade do ciclo – relação de feedback entre
secreção ovariana e o eixo hipotálamo- hipófise.
Hipotálamo:
Os núcleos arcuados no hipotálamo médio-basal são os principais reguladores do
ciclo. Seus neurônios produzem o Hormônio Liberador de Gonadotrofinas (GnRH), que
tem meia-vida curta, é imediatamente transportado para a hipófise anterior e exerce
papel obrigatório no controle da secreção de gonadotrofinas.
O hipotálamo é influenciado por sinais extrínsecos e intrínsecos ao SNC e está
sujeito ao controle do ovário ( feedback ou retroação). O próprio GnRH controla sua
produção agindo no hipotálamo através da retroação de alça ultracurta.
Hipófise:
O GnRH age nas células gonadotróficas basofílicas da hipófise anterior,
estimulando-as a sintetizar e secretar Hormônio Luteinizante (LH) e Hormônio Folículo
Estimulante (FSH).
Os hormônios esteróides, como o estradiol e a progesterona, ou fatores ovarianos
não- esteróides, como a inibina, são moduladores da secreção de LH e FSH. A secreção
de LH é essencialmente caracterizada por um pico no meio do ciclo menstrual. A
secreção de FSH caracteriza-se por aumento na fase folicular inicial, platô na fase lútea
e acentuada elevação na fase lútea tardia.
As gonadotrofinas (LH e FSH) são secretadas de forma pulsátil ( devido a
secreção pulsátil de GnRH), com freqüência e amplitude que variam de acordo com a
fase do ciclo (em resposta ao feedback dos esteróides no hipotálamo e hipófise).
As gonadotrofinas exercem retrocontrole sobre a produção do GnRH pelo
hipotálamo – feedback em alça curta:
- gonadotrofina ↑ = ↓ inibe produção de GnRH (feedback - )
- gonadotrofina ↓ = ↑ hipotálamo (feedback +)
Ovários:
Os ovários têm duplo papel, produzir gametas e secretar hormônios, que é
desenvolvido pelo folículo de Graaf, unidade funcional básica do ovário.
Os principais hormônios ovarianos são: estradiol, estrona, androsteneriona,
testosterona e progesterona, alem dos peptídeos gonadais.
O estradiol e a progesterona (principais hormônios esteróides) se ligam a
receptores específicos no núcleo de células-alvo principalmente nos ovários, no útero,
na vagina e nas mamas.
Estradiol: tem ação no desenvolvimento endometrial e folicular, além da
promoção do pico de LH no meio do ciclo.
Progesterona: ação na manutenção do arcabouço endometrial e retroação
negativa sobre a secreção hormonal hipotalâmica.
A secreção ovariana exerce influência sobre a secreção de gonadotrofinas,
através de feedback sobre hipófise e hipotálamo (retroação de alça longa), que ocorre da
seguinte maneira:
- estrogênio: até determinados níveis inibe a produção de FSH e LH na hipófise
(feedback neg.). Em níveis mais elevados, passa a estimular a produção de GnRH pelo
hipotálamo e a hipófise, que produz o pico de LH (feedback pos.). A transição de
supressão para estimulação à produção de LH ocorre enquanto os níveis de estradiol se
elevam durante o meio da fase folicular.
- progesterona: tem ação inibitória no hipotálamo e ação positiva na hipófise.
- inibina: ação inibitória sobre o hipotálamo, em associação ao estrogênio,
suprimindo a produção de FSH. É o feedback negativo.
Útero:
A parede uterina tem 3 camadas: a serosa (+ externa), o miométrio e o
endométrio ( + interna e que possui 2 componentes anatômicos: o estroma e as
glândulas).
Histologicamente, há 3 camadas no endométrio:
-profunda ou basal: não responde aos hormônios ovarianos
-média ou esponjosa: é a maior e reage intensamente aos estímulos hormonais
-superficial ou compacta: inclui o colo das glândulas e o epitélio superficial.
As alterações produzidas pelos hormônios manifestam-se nas camadas esponjosa
e compacta, que são eliminadas na menstruação, e por isso são chamadas funcionais. A
camada basal não é eliminada e garante a renovação do endométrio para o próximo
ciclo.
As fases do ciclo ovariano:
O ciclo menstrual é dividido em 3 fases: a fase folicular, a ovulação e a fase
lútea.
FASE FOLICULAR:
Estende-se do 1° dia da menstruação até o dia do pico de LH, no meio do ciclo
(entre o 10° e 14° dia), inclusive. Também chamada de fase proliferativa, seu resultado
final é o desenvolvimento folicular e, comumente, um único folículo maduro viável.
Fases do crescimento folicular:
Folículo primordial: primeiro estágio do desenvolvimento folicular, consiste em
um oócito paralisado na prófase meiótica, envolto por uma camada única de células da
granulosa. Eles crescem e sofrem atresia durante toda vida da mulher, inclusive na
gravidez, infância, perimenopausa ou períodos de anovulação.
A fase inicial do crescimento folicular envolve respostas que não dependem da
regulação hormonal e sim de um mecanismo próprio do ovário. Ao final deste estágio, o
oócito apresenta plena capacidade de completar a meiose. Além disso, as células da
granulosa tornam-se cubóides e formam junções com o oócito que permitem a troca de
nutrientes.
Folículo primário: com a multiplicação das células da granulosa o folículo
primordial torna-se primário. Ocorre a diferenciação, independente da estimulação
hormonal, das células do estroma em teca interna e teca externa. Nesta fase, o folículo
tem padrão de crescimento limitado e pode sofrer rápida atresia a menos que o grupo de
folículos responda a uma elevação do FSH, impulsionando seu crescimento. O declínio
na produção de estradiol e inibina, que ocorre na fase lútea do ciclo anterior, permite a
elevação do FSH.
Folículo pré-antral: com o crescimento acelerado pelo FSH, o folículo tem um
oócito maior, envolto por uma membrana, a zona pelúcida. A partir dessa fase o
crescimento passa ser dependente das gonadotrofinas hipofisárias. As células da
granulosa passam a produzir estrogênio e pouco androgênio (que é substrato para a
produção de estrogênio) e progestagênio. Tanto a produção de estrogênio quanto a
proliferação das células da granulosa e o crescimento folicular são estimulados pelo
FSH. Para ter sucesso no desenvolvimento, o folículo precisa ser capaz de converter o
androgênio em estrogênio, pois em um microambiente muito androgênico, o folículo
sofre atresia.
Folículo antral: a presença de estrogênio e FSH ocasionam a produção e
acúmulo de líquido folicular nos espaços intercelulares da granulosa, formando uma
cavidade e dando origem ao folículo antral. Na presença de FSH, o estrogênio (que
promove proliferação granulosa e crescimento do oócito) predomina nesse líquido e ,
na ausência de FSH, predomina o androgênio ( que promove degeneração do oócito).
Sistema de duas células, duas gonadotrofinas: nos folículos pré-antrais e antrais,
os receptores para o LH estão presentes apenas nas células da teca e os receptores para o
FSH apenas nas células da granulosa. Em resposta ao LH, as células da teca produzem
androgênio, a partir do colesterol. O androgênio é transportado às células da granulosa e
lá é convertido em estrogênio, através da aromatização induzida pelo FSH. A granulosa
é incapaz de produzir androgênio. A resultante conversão de um microambiente
androgênico em estrogênico, essencial ao desenvolvimento folicular, é dependente da
crescente sensibilidade do folículo ao FSH, mediada pelo próprio FSH e pela crescente
influência do estrogênio.
A seleção do folículo dominante: a conversão em um folículo com
microambiente estrogênico seleciona este folículo e o destina a ovular. Esta seleção
ocorre entre o 5° e o 7° dia do ciclo e é resultado de duas ações estrogênicas: 1)
interação local com o FSH, exercendo influência positiva em sua ação; 2) e retroação
negativa em nível de hipotálamo-hipófise na produção de FSH, que serve para remover
o suporte de gonadotrofinas dos outros folículos. A diminuição da produção de FSH na
hipófise leva À diminuição da ação desse hormônio nos outros folículos e conseqüente
formação de um microambiente androgênico em cada um deles. Ou seja, a retroação
negativa do estrogênio sobre o FSH serve para inibir o desenvolvimento de todos,
menos do folículo dominante. O desenvolvimento desse folículo continua dependente
do FSH e por isso ele possui maior numero de receptores para FSH e maior ação local
do FSH que os outros folículos, uma maneira de compensar os níveis decrescentes de
FSH no plasma. Além disso, a vascularização da teca aumenta a medida que o folículo
dominante cresce.
No final do desenvolvimento antral, o FSH induz o aparecimento de receptores
de LH nas células da granulosa para que o folículo responda melhor ao pico de LH no
meio do ciclo, responsável pela ovulação.
Inibina e ativina: são peptídeos sintetizados pelas células da granulosa, em
resposta ao FSH. A primeira é um importante inibidor da secreção de FSH. Já a ativina
estimula a liberação do FSH pela hipófise e aumenta sua ação no ovário.
Folículo pré-ovulatório: nessa fase, as células da granulosa tornam-se maiores e
as da teca muito vascularizadas. O oócito prossegue na meiose, quase completando a
divisão reducional. Há uma produção cada vez maior de estrogênio, atingindo seu pico
cerca de 3 dias antes da ovulação. O pico de LH ocorre um dia depois do pico de
estradiol. O LH promove luteinização das células da granulosa no folículo dominante,
levando à produção de progesterona. A progesterona age positivamente na hipófise,
contribuindo para a elevação do FSH e do LH observada no meio do ciclo.
As células de teca dos folículos em atresia, sob ação do LH, aumentam a
produção de androgênio, que em concentrações elevadas no plasma, estimula a libido da
mulher, aumentando a freqüência de relações sexuais no período pré-ovulatório.
FASE OVULATÓRIA:
Somente o folículo que atinge seu estágio final de maturação é capaz de se romper.
O marcador fisiológico mais importante da aproximação da ovulação é o pico de
LH do meio do ciclo, que ocorre de 32 a 36 horas antes da ovulação e é precedido por
um aumento acelerado do nível de estradiol (que é produzido pelo folículo préovulatório). Dessa maneira, o folículo produz seu próprio estímulo ovulatório (↑
estradiol → ↑LH → ovulação).
No momento da ovulação, dentro do folículo dominante ocorre 3 fenômenos
principais:
Recomeço da meiose I: o oócito permanece no estagio diplóteno da meiose I até
a onda de LH, quando é retomada a meiose e ele se torna apto para a fertilização. O
oócito passa da prófase I para a metáfase I e ocorre a extrusão do primeiro corpúsculo
polar na metáfase II. A meiose só se completa após a penetração do espermatozóide e a
liberação do segundo corpúsculo polar.
Luteinização: um pequeno aumento da produção de progesterona ocorre 12 a 24
horas antes da ovulação. Ele induz a onda de FSH e LH pelo aumento do feedback
positivo do estradiol na ação desses hormônios. Sem o aumento pré-ovulatório de
progesterona não há pico de FSH e LH. Porém, com sua elevação progressiva, a
progesterona passa a exercer feedback negativo sobre o LH, terminando com o seu pico.
Além disso, ela também aumenta a distensibilidade da parede folicular.
Ovulação: desde a fase folicular há um acúmulo de prostaglandinas E e F e
produção de plasminogênio que ativam colagenases que irão digerir o colágeno da
parede do folículo, facilitando a liberação do oócito. As Plg E e F , junto com o LH,
também promovem a contração das células musculares da parede folicular, já
enfraquecida, levando à extrusão do oócito (ovulação). Além disso, ocorrem alterações
importantes no fluxo sangüíneo do ovário. Vários mediadores produzidos e liberados o
ovário promovem o aumento do fluxo sangüíneo intrafolicular e da permeabilidade
capilar. Após a rotura folicular o óvulo é apreendido pelas fimbrias tubárias.
FASE LÚTEA:
Uma vez liberado o oócito, a estrutura dominante passa a se chamar corpo lúteo.
As células da granulosa aumentam de tamanho que acumulam em vacúolos um
pigmento amarelado chamado luteína. O incremento vascular local favorece o aporte de
LDL colesterol, substrato na síntese de progesterona. É conhecida a necessidade de
estrogênio para a síntese de receptores de progesterona no endométrio. O estrogênio da
fase lútea é necessário para que ocorra as alterações induzidas pela progesterona no
endométrio após a ovulação ( fundamentais para a implantação do embrião). A cada
pulso de LH existe um aumento da concentração de progesterona. Esses pulsos de LH
são maiores no inicio da fase lútea e diminuem gradativamente., favorecendo a atuação
de fatores que levam a luteólise, na fase lútea tardia. Se a gravidez acontece, o HCG
mantém o funcionamento do corpo lúteo até que ocorra a esteroidogênese placentária.
No período lúteo intermediário, a inibina faz um pico na circulação e suprime a
secreção de FSH pela hipófise, quando são atingidas os níveis mais baixos desse
hormônio.
Ao final da fase lútea, a regressão do corpo lúteo leva à queda do estradiol,
progesterona e inibina, o que permite a elevação do GnRH e do FSH, recomeçando
todo o processo.
AS FASES DO CICLO ENDOMETRIAL
Na fase folicular ou proliferativa do ciclo, o aumento de estrogênio provoca a
reconstrução e o crescimento do endométrio. (Na fase anterior, a descamação menstrual
provocou a perda tecidual que será reconstituída). As glândulas são a porção do
endométrio mais responsiva ao estrogênio. De estreitas e tubulares, com epitélio colunar
baixo, elas passam a alongadas e pouco tortuosas, com pseudo-estratificação do epitélio.
O componente estromal evolui de celular denso para breve período de edema e,
finalmente, um sincício frouxo. Todos os componentes tissulares (glândulas, estroma e
endotélio) têm pico de proliferação do 8° ao 10° dia do ciclo. Há aumento de mitoses e
o endométrio passa de 0,5 para 3,5 a 5 mm. Isso ocorre principalmente na camada
funcional do endométrio. Nessa fase de crescimento endometrial há ainda o aumento de
células ciliadas e microvilosas, responsáveis pela mobilização e distribuição de
secreções endometriais durante a fase secretória.
No inicio da fase lútea a taxa de crescimento endometrial diminui e o
endométrio atinge a espessura máxima (8 a 10 mm). O numero de receptores de
progesterona está alto graças ao estímulo estrogênico, e ela (progesterona) provocará
modificações no endométrio, produzindo uma resposta secretora. As glândulas
endometriais tornam-se tortuosas e aumentam seu lúmen, passando a secretar grande
quantidade de muco nutritivo e preparando-se para a implantação.
Na fase lútea tardia, o estroma desenvolve características de reação decidual prémenstrual, com grande infiltrado de linfócitos e aspecto edematoso.