Carboidratos em
Bioquímica Clínica
•
•
•
•
Carboidratos
biomoléculas mais abundantes na terra.
são poliidroxialdeídos ou poliidroxicetonas
cíclicos, ou substâncias que liberam estes
compostos por hidrólise
o açúcar e o amido são a base da dieta.
A oxidação dos carboidratos é a principal via
metabólica fornecedora de energia para a maioria
das células não-fotossintéticas
Os carboidratos são divididos em três classes
principais:
- Monossacarídeos - açúcares simples –
consistem em uma única unidade de
poliidroxialdeído ou cetona
Mais abundante na natureza: glicose
Gliceraldeído
Diidroxicetona
Oligossacarídeos – são compostos por cadeias curtas de
unidades de monossacarídeos unidas por ligações
glicosídicas.
• Mais abundantes: dissacarídeo – sacarose
• Oligossacarídeos com três ou mais unidades – unidas a
moléculas de não açúcares – glicoconjugados
Polissacarídeos – polímeros de açúcar com mais de 20
unidades.
• Mais abundantes: celulose, amido e glicogênio
• Celulose e amido – unidades repetitivas de glicose, com
ligações glicosídicas diferentes – propriedades e funções
diferentes
• Obs: oligo e polissacarídeos são hidrolisados em
monossacarídeos
Digestão e absorção de carboidratos
• principais carboidratos da alimentação são:
Amido, sacarose e lactose
• α-amilase salivar (ptialina): digestão do
amido inicia-se na mastigação
• α-amilase pancreática: amido e glicogênio
são hidrolisados no duodeno por ela,
produzindo maltose e dextrinas.
Enzimas da superfície intestinal
•
•
•
•
•
Maltase
Maltose + H2O
2-D-glicose
Dextrinase
Dextrina + H2O
n D-glicose
Isomaltase
Isomaltose + H2O
2 D-glicose
Sacarase
Sacarose + H2O
D-frutose + D-glicose
Lactose + H2O Lactase
D-galactose + D-glicose
A Glicose
•
é o principal combustível da maioria dos
organismos
•
é o carboidrato mais importante, é degradada,
armazenada ou formada por diferentes vias:
1.
2.
3.
4.
5.
Glicólise
Gliconeogênese
Glicogênese
Glicogenólise
Via das Pentoses
Glicólise - Do grego glykys - doce, lysis –
quebra
Gliconeogênese
É a formação de novas moléculas de glicose a
partir de precursores não carboidratos
Glicogênese - É a síntese intracelular de
glicogênio
Glicogenólise – é a quebra do glicogênio em
moléculas de glicose.
hexoquinase
Fofoexose isomerase
Fosfofrutoquinase-1
Fase
preparatória
aldolase
isomerase
Gliceraldeídp 3-fosfato
desidrogenase
Fosfoglicerato
quinase
Fosfoglicerato
mutase
enolase
Piruvato quinase
Fase de
pagamento
Em condições normais a glicemia é mantida em
valores normais por mecanismos regulatórios.
Após uma refeição...
- Liberação de insulina - captação por tecidos energia
- 70% fígado – glicogênio – combustível
- Excesso – ác. graxos – VLDL – tec. Adiposo
Valores normais de glicemia: 70 – 99 mg/dL
Intolerância à glicose – 100 – 125 mg/dL
Diabetes – acima de 126 mg/dL
Acima dos valores de referência – hiperglicemia
- Abaixo dos valores de referência – hipoglicemia
- Glicose filtrada e reabsorvida até 180 mg/dL –
após glicosúria
-
Regulação da Glicemia
Concentração de glicose no sangue do indivíduo
Jejum
80 a 90 mg/100 ml de sangue
Inanição
Primeira hora após uma refeição
120 a 140 mg/100 ml de sangue
Sistemas de feedback
(controle da glicemia)
Rápido retorno da
Gliconeogênese do fígado
concentração de glicose aos níveis
fornece a glicose necessária
de controle (dentro de duas horas
para manter o nível de
após a última absorção de
glicemia
carboidratos)
1 dL = 100 mL
Mecanismos de Regulação da
Glicemia
Fígado
Insulina
Glucagon
Importante sistema
tampão da glicemia
Importantes sistemas
de controle por
feedback
Manter a
concentração normal
de glicose no sangue
Mecanismos de Ação da Insulina
• Insulina:
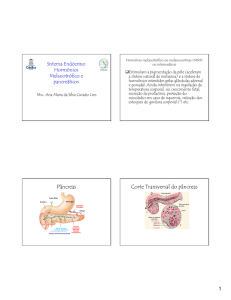
– Produzida pelas células beta das ilhotas de Langerhans
– Compreende cerca de 1% da massa celular do pâncreas
– Um dos mais importantes hormônios que coordenam a
utilização de combustíveis pelos tecidos
– Efeitos metabólicos anabólicos
síntese de
glicogênio, triacilgliceróis e proteínas
– Efeito sobre o metabolismo da glicose:
• Fígado
inibe a gliconeogênese e glicogenólise
• Fígado e músculo
aumenta a glicogênese
Músculo e tecido adiposo
aumenta o
número de transportadores de glicose na membrana
celular
aumenta a captação de glicose
Glucagon
• Age nas mesmas células que a insulina;
• Mobiliza as reservas energéticas para a manutenção da
glicemia entre as refeições;
• No fígado estimula a glicogenólise;
• No tecido adiposo estimula a lipólise, liberando ácidos
graxos;
• Estimula a gliconeogênese e a cetogênese;
• Liga-se a um receptor específico de membrana.
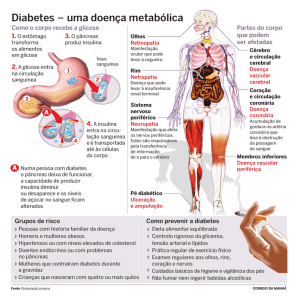
Diabetes Melitus
Síndrome de comprometimento do metabolismo dos
carboidratos, das gorduras e das proteínas
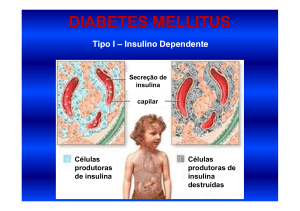
Diabetes melitus tipo I
Diabetes melitus tipo II
(DMID)
(DMNID)
Falta de secreção de insulina
Resistência à insulina
Alteração do metabolismo de todos os principais alimentos
Fisiopatologia
Ausência de insulina
Resistência à insulina
Deficiência no metabolismo da
glicose
Impedir a sua captação eficiente pela
maioria das células do corpo
Menor utilização de glicose
pelas células
Aumento da utilização de
gorduras e proteínas
Diabete Melito Tipo I (DMID)
• 10% a 20% dos diabéticos
• Diabetes melitus juvenil
Observado
com menos de 20 anos de idade
Deficiência absoluta
de insulina
em
indivíduos
Relativa excreção
excessiva de glucagon
Lesão das células beta pancreáticas
Infecções virais ou
doenças auto-imunes
Tendência hereditária
à degeneração
Sintomatologia
80% a 90% das células
beta destruídas
Sintomas abruptos
Hiperglicemia
Utilização aumentada de
gorduras para a
obtenção de energia
Cetoacidose
Depleção das proteínas
do organismo
Utilização periférica de
glicose diminuída
Gliconeogênese (aumento na
produção hepática de glicose)
Hiperglicemia
Glicosúria (excreção
de glicose em excesso
na urina)
Diurese osmótica
Poliúria (excreção
excessiva de urina)
Glicosilação
de proteínas
Desidratação celular
Polidipsia (sede
excessiva)
Lesão tecidual
Aumento da lipólise para produzir
energia (através da oxidação de
ácidos graxos)
Perda de peso,
fadiga e
fraqueza
Cetoacidose
+
Desidratação celular
Polifagia
(fome intensa)
Cetogênese acelerada
(síntese hepática de
corpos cetônicos)
Cetonúria
(excreção de
corpos cetônicos
na urina)
Acidose grave
Morte
Hálito cetônico
(eliminação de corpos
cetônicos no ar expirado)
Muitos ácidos graxos
Fígado
Triacilgliceróis
Lipoproteínas plasmáticas
(VLDL)
Glucagon – aumenta
a lipólise
Sangue
Aumento do
colesterol
Arteriosclerose e outras
lesões vasculares
Incapacidade de utilizar glicose
como fonte de energia
Maior utilização e armazenamento
diminuído de proteínas
Depleção de proteínas do
organismo
Morte
Diabetes Melitus Tipo II (DMNID)
• 80% a 90% dos diabéticos
• Diabetes melitus de início adulto
Ocorre
depois
dos 40 anos de idade, freqüentemente entre 50 e 60 anos
• Desenvolve-se de modo gradual, sem sintomas óbvios
Redução da sensibilidade dos
tecidos-alvo aos efeitos
metabólicos da insulina
=
Resistência à insulina
Fatores
Genéticos
Secundária à
obesidade
Diabético não-insulinodependente
Células beta
funcionalmente ativas
Diminuição da utilização e
armazenamento de carboidratos
Hiperglicemia
Secreção de insulina
Aumento da concentração
plasmática de insulina
Regulação normal
da glicose
Diabetes melitus tipo II
Secundária à obesidade
Menor número de
receptores de insulina
Pessoas
Obesas
Resistência à insulina
Anormalidades das vias
de sinalização
Sintomatologia
Estágios avançados
Ingestão de carboidratos
Células beta disfuncionais
Hiperglicemia leve
Hiperglicemia acentuada
Mesmos efeitos observados no diabetes melitus tipo I
• Poliúria e polidipsia (durante várias semanas), e polifagia
(menos comum)
Diagnóstico
• O diagnóstico de diabetes baseiam-se em diversos testes
químicos da urina e do sangue:
– Glicose urinária
normal
– Níveis de glicemia
80 a 90 mg/100 ml
anormal
Diabete melito
tipo I
Muito baixos ou
indetectáveis
Diabete melito
tipo II
Muito altos
ou normal
Acima de 110 mg/100 ml
Níveis plasmáticos
de insulina
Exames Laboratoriais
Testes que servem para o diagnóstico e acompanhamento
do diabetes.
GLICEMIA DE JEJUM
• Após 8 horas de jejum;
• Glicemia plasmática (mg/dl)
Normal até 99mg/dl
Pré-diabete 100 a 125mg/dl
Diabete 126mg/dl e acima, deve ser confirmado com novo
teste em outro dia.
• A amostra usada para o exame é plasma ou soro, mas
também pode ser feita com LCR e urina;
Exames Laboratoriais
•
•
•
•
GLICEMIA PÓS-PRANDIAL
Teste controle;
Concentração da glicemia 2h após ingestão de 75g de
glicose em solução aquosa a 25%;
Concentração da glicose tende a retornar ao normal após
2h;
Valor desejado para glicemia capilar até 180 mg/dl.
TESTE ORAL DE TOLERÂNCIA À GLICOSE
(TOTG)
• Teste diagnóstico para diabetes;
• Medidas seriadas de glicose nos tempos 0, 30, 60, 90, 120
min após ingestão de 75 g glicose anidra em 300 ml de
água;
• Teste realizado pela manhã, jejum de 8-10h;
• Teste mais sensível que a glicemia de jejum, mas é afetado
por vários fatores.
TESTE ORAL DE TOLERÂNCIA À GLICOSE (TOTG)
Indicações:
• Diagnóstico DM Gestacional;
• Diagnóstico tolerância à glicose diminuída;
• Avaliação de pacientes com nefropatia, neuropatia, ou
retinopatia não explicada e com glicemia em jejum abaixo
de 126 mg/dl.
Cuidados antes do teste:
• Ingestão de pelo menos 150 g de carboidratos, nos 3 dias
anteriores;
TESTE ORAL DE TOLERÂNCIA À GLICOSE (TOTG)
• Atividades físicas, hábitos alimentares normais;
• Durante o teste, não fumar e permanecer em repouso;
• Não usar medicação que interfira no metabolismo dos
carboidratos.
Valores:
• Normal - 139 mg/dl e abaixo;
• Pré-diabetes - 140 a 199 mg/dl
• Diabetes – 200 mg/dl e acima.
• Na amostra de 120 min, valor acima de 200 mg/dl é
indicativo de diabetes, mesmo que os níveis de glicose de
jejum estejam normais.
– Teste de tolerância à glicose:
HEMOGLOBINA GLICADA
• Teste controle;
• A hemoglobina liga-se à glicose, quanto maior for a taxa
de glicemia, maior a síntese de hemoglobina glicada;
• Indica o controle metabólico nas 8 a 10 semanas
precedentes ao teste, é o tempo médio de vida dos glóbulos
vermelhos;
• Não é indicado para pacientes com hemoglobinopatias,
pois há redução na meia-vida das hemácias e da exposição
da hemoglobina às variações da glicose;
• Diabéticos estáveis 3 a 4 meses;
• Diabéticos sem controle glicêmico 1 a 2 meses;
• Valores estão entre 5 a 8% da HbA total em indivíduos
normais e 8 a 30% em pacientes diabéticos;
• O valor mantido abaixo de 7% promove proteção contra o
surgimento e a progressão das complicações
microvasculares do diabetes.
Hipoglicemia
• Diminuição da taxa de glicose no sangue;
Causas são:
• Consumo de álcool (mais freqüente);
• Jejum: alimentação insuficiente ou que não fornece
carboidratos em quantidades suficientes;
• Esforço físico: o funcionamento dos músculos pode ter
consumido a glicose disponível no sangue e o corpo pode
não ter tido tempo de liberar suas reservas, é temporário
em indivíduos saudáveis;
• Consumo de medicamentos: como o caso de medicamentos
antidiabéticos. Também pode ser causada por aspirina,
AINEs, beta-bloqueadores não-cardiosseletivos.
Sinais da hipoglicemia:
• Tremor, ansiedade, nervosismo, palpitações, taquicardia,
sudorese, calor, palidez, frio, pupilas dilatadas;
• Fome, borborigma (“ronco” na barriga), náusea, vômito,
desconforto abdominal.
Sinais da hipoglicemia produzidos no cérebro:
• prejuízo de suas funções (neuroglicopenia), causando
enxaqueca, confusão, letargia, perda da consciência e
vários outros sintomas. Esses desajustes podem ir desde
um mal estar até um coma.
• Glicemia abaixo de 65 mg/dl - eficiência mental diminui;
• Glicemia abaixo de 40 mg/dl - limitação de ações e
julgamento;
• Glicemia mais baixa podem ocorrer convulsões;
• Glicemia próxima ou abaixo de 10 mg/dl - neurônios ficam
eletricamente desligados, resultando no coma.
• Nem todas manifestações ocorrem, nem há uma ordem de
ocorrência;
• Manifestações específicas variam de acordo com a idade e
a severidade da hipoglicemia;
• Hipoglicemia severa pode resultar em morte ou dano
cerebral;
• Muitas pessoas podem eventualmente ter níveis
gllicêmicos na faixa de hipoglicemia sem ter sintomas ou
distúrbios, entretanto níveis de glicose plasmática abaixo
de 70 mg/dl são considerados hipoglicêmicos;
• A hipoglicemia é a complicação mais comum do diabetes,
que ocorre quando há rompimento entre a dose de insulina,
o suprimento de glicose e as refeições e atividade física.
Tratamento
• Diabete melito tipo I:
Administração de insulina
Metabolismo dos carboidratos, das gorduras e
das proteínas mais normal possível
Regular
Ação de 3
a 8 horas
Doses adicionais
(refeições)
Insulina
Precipitada com zinco ou
com derivados protéicos
Ação de 10
a 48 horas
Dose única
• Diabete melito tipo II:
Dietas e prática de
exercícios físicos
Perda de peso
Tiazolidinedionas
e a metformina
Fármacos
Sulfoniluréias
Estágios mais tardios
Diminuir a resistência
à insulina
Aumentar a sensibilidade
à insulina
Estimular a produção
aumentada de insulina
pelo pâncreas
Administração de insulina
Questões:
1) Quais são as principais classes de carboidratos?
2) Quais são os valores de referência de glicemia?
3) Quais são os principais mecanismos de regulação de
glicemia no organismo humano?
4) A doença na qual o indivíduo apresenta deficiência de
insulina é chamada ................
5) Quais são os tipos de Diabetes e qual a diferença entre eles?
6) Como a deficiência de insulina pode levar ao coma?
7) O que significa polidipsia, polifagia e poliúria?
8) Quais são os testes usados para diagnóstico e
acompanhamento do diabetes?
9) Para que serve o teste da Hemoglobina Glicada?
10) O que significa hipoglicemia e quais são seus sintomas?