1780 : química orgânica
química inorgânica
TEORIA DO VITALISMO
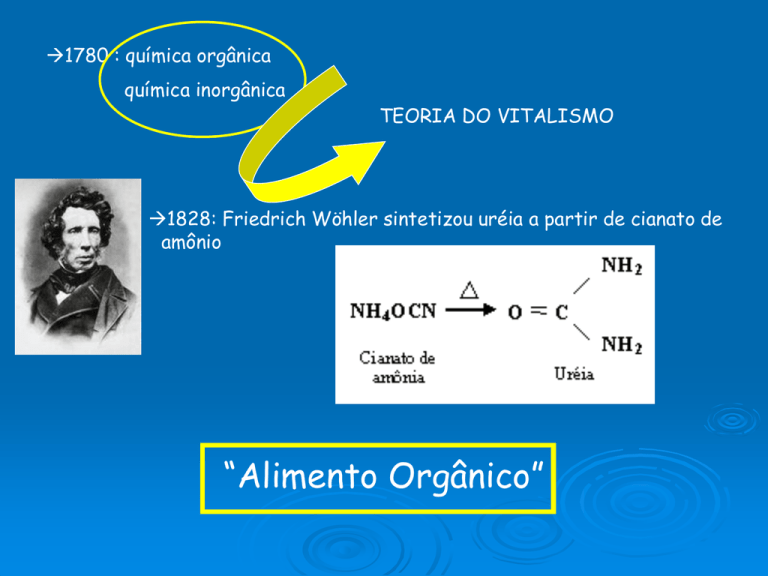
1828: Friedrich Wöhler sintetizou uréia a partir de cianato de
amônio
“Alimento Orgânico”
Regra do Octeto
Um átomo estará estável quando sua camada de valência possuir 8e-,
assemelhando-se à configuração eletrônica de um gás nobre (exceção H e
He - 2e-)
- Ligações iônicas
- Ligações covalentes
- Ligações dativas
Carbono
É a base da química orgânica: os compostos orgânicos são formados
basicamente de carbono ligado a outros elementos: H, N, O,S, Cl, etc
Nos compostos orgânicos os átomos podem formar um número fixo de
ligações; a medida dessa habilidade é chamada valência. O CARBONO é
tetravalente.
Tipos de ligações do carbono
Saturado
x insaturado;
Normal x ramificada;
Cadeia aberta x cadeia fechada
Homogênea x heterogênea;
Alicíclica
x aromática
Geometria molecular
O arranjo tri-dimensional dos átomos em
uma molécula geometria molecular
A teoria da repulsão dos pares de elétrons
(ligantes e não-ligantes) procura explicar o
arranjo dos átomos numa molécula.
Teoria da repulsão dos elétrons
Electrons são cargas carregadas negativamente,
portanto se repelem mutuamente.
Os elétrons ocuparão posições tais que minimizem
os efeitos de suas repulsões (ocupando regiões o
mais afastado possível uns dos outros).
Num
átomo os elétrons ocupam determinados
espaços chamados orbitais (máximo 2e num orbital).
Tipos de orbitais mais comuns: orbitais s ; p ;
Orbitais
Hibridizações
Hibridização
sp3
2p
hibridação
2s
H
H
H
H
sp3
Hibridização
sp2
2p
2p
hibridação
sp2
2s
H
H
C
C
H
H
Hibridização
sp
2p
2p
hibridação
sp
2s
Cl
Cl
Funções Químicas
Alcanos,
alcenos, alcinos, alcadienos;
Cicloalcanos,
ciclenos, ciclodienos;
Funções Químicas
Alcool,fenol,
Aldeído,
cetona;
ac. carboxílico, éster
Funções Químicas
Aminas
Éter
e amidas;
Isomeria
Isomerismo ou Isomeria (iso = mesmo , meros =
partes) é o fenômeno caracterizado pela existência de duas
ou mais substâncias diferentes que apresentam fórmulas
químicas idênticas, porém diferentes fórmulas estruturais.
Isomeria
constitucional
Isomeria espacial
Isomeria constitucional
- De posição
- De função
- De cadeia
Isomeria constitucional
- De compensação ou metameria
- Tautomeria
Isomeria espacial
- geométrica
Cis = do mesmo lado
Trans = de lados opostos
Mistura Quiral =
- óptica
Destrógiros (D) = desviam a luz
plano- polarizada para a direita
Levógiros (L) = desviam para a
esquerda




![Roteiro Mensal [1ª série] – Biologia – Química – Empreendedorismo](http://s1.studylibpt.com/store/data/002323123_1-73e0a36762e852c083cac33c9b995a74-300x300.png)