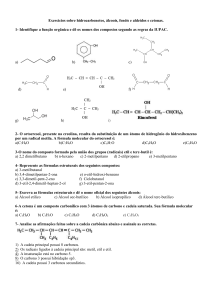
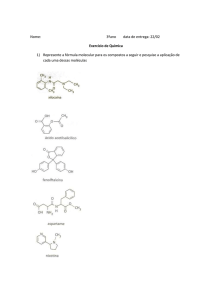
Monossacáridos
• açúcares simples
• Não podem ser hidrolisados em componentes
mais simples
• Polihidroxicetonas ou Polihidroxialdeidos
Estrutura (I)
• Possuem uma cadeia
central de carbonos
ligados por ligações
covalentes simples
• Possuem pelo menos
um grupo hidroxilo
• O número de carbonos
varia geralmente entre
3e7
Estrutura (II)
• A partir de 4 carbonos há
tendência de formação de
estruturas cíclicas em
solução aquosa
• Estrutura química geral (CH2O)n
Famílias de Monossacáridos
• Aldoses
– Possuem um grupo
funcional Aldeído num
carbono terminal
• Cetoses
– Possuem um grupo
funcional Cetona num
carbono não terminal
Isomeria
Enantiómeros
Epímeros
Anómeros
Enantiómeros
• Isómeros ópticos
• Existe devido à
quiralidade (assimetria)
dos carbonos
• Regra geral, para uma nose existem (n-2)
carbonos quirais
• Para n carbonos quirais
existem 2^n isómeros
possíveis
• Predominância de
Hexoses D na natureza
Epímeros
• 2 açúcares que diferem apenas na configuração em
redor de um carbono só
Isómeros - II
• Anómeros – formas
isoméricas que diferem
na configuração no
carbono anomérico
– Alfa
– Beta – meter imagem
• Mutarrotação
– interconversão de alfa beta
Derivados de Monossacáridos
• Açúcar + Álcool
– Falta de um aldeido ou cetona (ex. Ribitol)
• Açúcar + Ácido
– Oxidação do aldeído em C1 ou do grupo hidroxilo no carbono
terminal em ácido carboxilico. (ex, ácido glucónico e ácido
glucuronico)
• N-acetilneuraminato (ácido sialico)
– Geralmente resíduo terminal de uma cadeia olicossacárida nas glicoproteinas.
– Partilha de carga negativa nas glicoproteinas devido à dissociação de um
protão do grupo carboxilo ao pH fisiológico
• Amino + Açúcar
– Substituição de um grupo hidroxilo por um grupo amina. O
grupo amina pode ser acetilado. (ex. Glucosamina)
Derivados de Monossacáridos
Açúcares mais comuns:
Reacções de Monoglicéritos
• Formação de cadeias cíclicas em solução
aquosa
• Reacção com alcoois (formação de hemicetais
e hemiacetais)
• Monossacáridos enquanto açúcares redutores
açúcares em água Formação de estruturas cíclicas
• Em solução aquosa, aldotetroses e
monossacáridos com 5 ou mais
carbonos na estrutura central
adquirem uma estrutura cíclica
• O grupo carbonil forma uma
ligação covalente com o oxigénio
de um grupo hidroxil da cadeia
• Formação de derivados quando
em reacção com álcool –
hemiacetais (aldeidos) ou
hemicetais (cetonas)
Formação de
estruturas cíclicas
• Piranose – anéis com 6
elementos
• Furanose – aneís com 5
elementos
• 2 formas estáveis de anel da
D-glicose
– Alfa-D-Glicopiranose
– Beta-D-glicopiranose
• Apenas aldoses com 5 ou mais
carbonos conseguem
conseguem formar aneis de
piranose
Glicose Em Solução Aquosa
Formas da glicose em solução aquosa
•
•
•
•
33 % alfa-D-glicose (piranose)
66% beta-D-glicose (piranose)
<1% glicose linear
<1% glicofuranose
Hemicetais e Hemiacetais
• Formação de hemiacetais e hemicetais.
– Um aldeído ou uma cetona podem reagir com um alcool com formação de
hemiacetal ou hemicetal.
– Criação de um novo centro quiral
– A substituiçao de uma segunda molécula de alcool leva a que um acetal ou cetona
seja produzidos
– Quando o segundo alcool é parte de outro açúcar, forma-se uma ligação glicosídica
Monossacáridos – açúcares redutores
• Todos os monossacáridos são açúcares
redutores
• Monossacáridos oxidam-se por agentes
oxidantes como Fe3+ ou Cu2+
• O carbono carbonil é oxidado num grupo
carboxilo.
• Base da reacção de Fehling – teste qualitativo
para presença de açúcares redutores.
Monossacáridos - agentes redutores
•
A) - oxidação do carbono
anomérico – base da reacção de
Fehling
– O carbono C-1 da glucose na forma
cíclica não é oxidado
– A forma de cadeia aberta em
equilíbrio com a forma cíclica permite
a reacção com o Cu2+ levando à
reduçao e formaçao de D-Gliconato
•
B) - Medição da concentração de
Glicose no sangue
– Medição do H2O2 produzidos pela
reacção catalizada pela glicose
oxidase
– Degradação do H202 por uma
peroxidase num composto colorido
– Medição espectrofotométrica da
quantidade de composto
Dissacáridos
cadeias orgânicas constituidas por 2
unidades de monossacáridos unidos por
uma ligação glicosídica.
Redutores
Não Redutores
Ligação glicosídica
Ligação química covalente resultante da reacção de condensação entre 2
carbohidratos. Resulta da reacção do grupo hidroxilo de um com o
carbono anomérico de outro carbohidrato, libertando-se
consequentemente água.
H20
A ligação é alpha ou beta consoante a posição em baixo ou em cima
do grupo hidroxilo do carbono 1 respectivamente
-redutores:
funcão semiacetálica do carbono 1 de uma das oses forma uma
ligação com o grupo hidroxilo ligado a um carbono de outra ose.
O dissacárido mantém 1 carbono anomérico, logo
mantém características de redutor
Exemplo: Maltose, Lactose
-não redutores:
Exemplo: Sacarose
2 oses ligadas pelas funções semiacetálicas. Logo
o dissacárido não possui carácter redutor.
Oligossacáridos
Formados por cadeias curtas de monossacáridos ligados através de ligações
glicosídicas. Por hidrólise completa libertam apenas unidades de monossacáridos,
em número reduzido por molécula ( dissacáridos por exemplo).
Polissacáridos
São constituídos por grande número de moléculas. Da mesma ose
– homopoliósidos ou de oses diferentes – heteropoliósidos.
Apresentam elevado grau de polimerização.
Homopolissacáridos:
-amido
Constituído apenas por unidades de D-glucose. Cadeia linear é amilose ou
amilopectina. Forma de reserva glicídica nos vegetais.
-glicogénio
Semelhante ao amido, apresentando contudo mais ramificações. Forma de reserva
glícidica nos animais.
-celulose
Composto mais abundante da bioesfera. Cadeia muito longa formada por unidades de
D-glucose. Responsável pela estrutura das paredes celulares dos vegetais. Não é
hidrolisável pelas enzimas presentes no aparelho digestivo do homem pois não
dispõem de celulases. Entre as cadeias e também dentro da própria cadeia pode
haver associações através de pontes de hidrogénio o que confere uma complexidade
muito grande tornando a celulose praticamente insolúvel.
Outros exemplos: Dextranas,quitina,pectina
heteropolissacáridos
Na hidrólise pode libertar além de monossacarídeos neutros, ácidos
urónicos, osaminas, ácidos siálicos
-hemicelulose
Na sua constituição estão polímeros de hexoses, pentoses e ácidos urónicos.
Possui contudo um peso molecular relativamente baixo.
Funções celulares
- reserva energética:
-função estrutural:
Amido, glicogénio
Celulose, quitina, ácido hialurónico
Quitina:
Ácido hialurónico:
•Exoesqueletos;
•Preenche os espaços
intercelulares;
•Primeira camada de conchas ou
carapaças;
•Diminui com o aumento da idades
(aparecimento de rugas).
Na cadeia linear os monossacáridos podem estar ligados por diferentes tipos
de ligação comparativamente á ligação aos ramos. Os ângulos ( n sei que) que se
formam definem as conformação e consequentemente a função das biomolêculas.
(Em bioquímica a estrutura determina a função)
Amido ( e glicogénio):
Celulose
Ligações beta conferem às cadeias “lineares” resistência tênsil,
enquanto que as ligações alpha formam hélices abertas, sendo
adequado como fontes de glucose pois são facilmente acessíveis.
Estrutura em
hélice
Derivados
Heteródios: reacção de uma ose através do grupo
semiacetálico com um composto não glucídico
-Glicoproteínas
(parte glucídica é um glicano)
glicoaminoácidos
glicopéptidos
Exe: elastina,reticulina,colagénio,presentes na
saliva,leite e urina
-Glicolípidos
A existência destes compostos na natureza é muito importante pois
permite combinar as funções dos diferentes compostos permitindo
uma utilização e acção maior.
Glícidos Conjugados
São oligossacarídios ligados covalentemente a
outras biomoléculas (proteínas e lípidos).
Existem 3 tipos:
• Proteoglicanos;
• Glicoproteínas;
• Glicolípidos.
Proteoglicanos
•Síntese
Formam-se através de uma ligação covalente indirecta entre
o glicoseaminoglicano e um resíduo de serotonina da cadeia
peptídica.
É indirecta porque é feita através
de uma ponte de trissacáridos:
1. o resíduo de serotonina
liga-se a um dos terminais da ponte
2. o glicoseaminoglicano
liga-se ao outro terminal
Proteoglicanos
• Glicoseaminoglicanos mais comuns:
– Sulfato de Condroitina;
– Sulfato de Heparano;
– Heparina;
– Sulfato de Queratano.
Proteoglicanos
•Síntese
Agregados: conjuntos de proteoglicanos que se ligam a uma
molécula gigante de hialuronato.
Proteoglicanos
•Localização
- matriz extracelular, para onde são secretados e são mais
abundantes;
ou
- membrana celular, quando o glicoseaminoglicano se liga as
proteínas intrínsecas.
Proteoglicanos
•Funções
Têm variadas funções determinadas pelos
glicoseaminoglicanos que estão ligados à proteína.
Podem influenciar:
- a coagulação sanguínea;
- a organização dos tecidos;
- as trocas de informação inter celulares.
Os proteoglicanos agregados podem reagir com o colagénio do
espaço extracelular da cartilagem, contribuindo para a tensão e
resistência deste tecido.
Proteoglicanos
•Funções
O motivo porque os proteoglicanos podem assumir várias
funções é o facto dos glicoseaminoglicanos terem domínios
(sequências de monómeros alterados) que servem de local de
ligação com ligandos que influenciem a função da molécula.
Proteoglicanos
• Exemplos de interacções com os domínios :
Glicoproteínas
•Síntese
O oligossacarídeo liga-se pelo carbono anomérico a um
resíduo da proteína.
Podem haver 2 tipos de ligações:
- ligação ao terminal OH do resíduo (SER ou THR)
ou
- ligação ao terminal amida do resíduo (ASN)
Glicoproteínas
• Esquema dos 2 tipos de ligação:
Glicoproteínas
•Localização
Podem ser encontradas nos meios:
- intracelular: no complexo de golgi, no retículo
endoplasmático (onde se formam), nos lisossomas e em glândulas
secretórias;
- extracelular: na folha externa da membrana, no sangue e na
matriz extracelular.
Glicoproteínas
•(principais) Funções
- receptores e identificadores celulares;
- resposta imunológica;
Os açúcares auxiliam no enrolamento e estabilidade das
proteínas a que se ligam.
Glicoproteínas
• Principais elementos identificados pelos receptores:
Glicoproteínas
• Imunoglobulina:
Glicoproteínas
• Tabela-resumo de exemplos e funções associadas:
Glicoproteína
Função
Colagénio
Estrutural
Mucinas
Lubrificante, Protecção
Transferrina, Ceroplasmina
Transporte
Imunoglobulina, Agentes de
Histocompatibilidade
Resposta imunológica
Gonadotropina Coriónica, TSH
Hormonal
Fosfatase Alcalina (ex.)
Enzimática
Glicoproteínas
Glicoproteína
Função
Várias
Identificadores celulares
Existem em alguns peixes
Anticongelante
Várias
Receptores
Calnexina, Calreticulina
Enrolamento proteico
Notch (e correlacionados)
Reguladores de
diferenciação
Constituintes das plaquetas
Hemostasia
Glicolípidos
•Síntese
Oligossacarídeos ligados covalentemente à cabeça polar de
um fosfolípido.
•Localização
Folha externa da membrana celular.
•Função
- Reconhecimento e contacto entre as células;
- Manutenção do equilíbrio da estrutura.
Glicolípidos
• Localização na membrana celular:
Glicolípidos
Esfingolípidos
Galactolípidos ou
Sulfolípidos
Glicolípidos
• Estrutura dos antigenes (determinantes do grupo
sanguíneo):