Capítulo 2
James Joule
2.1
2.2
2.3
2.4
2.5
2.6
2.7
(1818-1889)
Calor e Energia Interna
Calor Específico e Calorimetria
Calor Latente
Trabalho e Calor em Processos Termodinâmicos
Primeiro Princípio da Termodinâmica
Algumas Aplicações do Primeiro Princípio da Termodinâmica
Mecanismos de Transferência de Energia em Processos Térmicos
1
2.1 Calor e Energia Interna
Até ~1850, os campos da termodinâmica e da mecânica eram considerados dois
ramos distintos da Ciência
Experimentos realizados em meados do século XIX pelo físico inglês James Joule
e outros cientistas, demonstraram que a energia pode entrar num sistema (ou
abandoná-lo), através do calor e do trabalho
Hoje a energia interna é tratada como uma forma de energia que pode ser
transformada em energia mecânica e vice-versa
Energia interna e calor
A energia interna, U é a energia associada aos componentes microscópicos de um
sistema – átomos e moléculas
As partículas no modelo de gás ideal são pontuais. Para estas partículas a U está associada
somente a energia cinética traslacional total dos átomos – depende da temperatura
Calor, Q é um mecanismo pelo qual a energia é transferida entre um sistema e
seu ambiente por causa da diferença de temperatura entre eles
Um sistema não tem calor assim como não tem trabalho
2
Unidades de calor
Antes dos cientistas reconhecerem que havia uma ligação entre a termodinâmica e
a mecânica, o calor era definido em termos das variações de temperatura que ele
produzia num corpo, e utilizava-se uma unidade separada de energia, a caloria,
para o calor.
A caloria (cal) era definida como o calor necessário para elevar a temperatura de
1g de água de 14.5 o C para 15.5 o C
Em 1948, os cientistas concordaram que, como o calor (assim como o trabalho)
é uma medida da transferência de energia, e sua unidade no SI deveria ser o
joule
Equivalente mecânico de calor
1 cal 4.186 J
Dispositivo de Joule para determinar a relação da caloria e joule
O trabalho realizado sobre a água pelos pesos em queda (em
joules), rodam as pás produzindo um aumento de temperatura,
equivalente à absorção, pela água, de uma determinada
quantidade de calor (em calorias)
3
2.2 Calor Específico e Calorimetria
O calor específico c de um substância é c
Q
mT
Q é a energia transferida para a massa m de uma substância, fazendo com que a
sua temperatura varie de T
As unidades do calor específico são J/kg·C
A energia Q transferida do meio para um sistema de massa m varia a sua
temperatura de T
Q mcT
O calor específico elevado da água comparado com a maioria das outras
substâncias comuns (Tabela) é responsável pelas temperaturas moderadas
nas regiões próximas de grandes volumes de água
4
A Tabela mostra os calores específicos de algumas substâncias a 25 C e pressão
atmosférica
5
O ar mais frio empurra o ar quente (menos denso) mais para cima, de acordo com
o princípio de Arquimedes
6
Calorimetria
Técnica para medir o calor específico de um sólido ou de um líquido
O princípio de conservação de energia para esse sistema isolado requer que a energia que
sai pelo calor da substância mais quente (de calor específico desconhecido) se iguale à
energia que entra na água. Logo, podemos escrever
Qfrio Qquente
7
Qfrio Qquente
Água de massa M (ma)
Corpo de massa m (mx)
ma ca T Ta mx cx T Tx
ca - calor específico da água
Ta - temperatura inicial da água
cx - calor específico do corpo
Tx - temperatura inicial do corpo
T – temperatura de equilíbrio final após a água e a substância se combinarem
Obtemos o calor específico do corpo
ma ca T Ta
cx
mx Tx T
Para medidas mais precisas é necessário levar em conta o calorímetro
8
2.3 Calor Latente
Em algumas situações a transferência de energia para uma substância resulta
em mudança de fase
Durante a mudança de fase a temperatura permanece constante
As mudanças de fase comuns são de sólido para líquido (fusão), líquido para gás
(evaporação)
9
A transferência de energia necessária para a mudança de fase de uma dada
substância de massa m de uma substância pura é
Q mL
L - calor latente da substância
depende da natureza da mudança de
fase e da substância
O calor latente de fusão é a energia necessária para romper todas as ligações
intermoleculares num quilograma de uma substância de maneira a converter a
fase sólida em fase líquida.
fusão ou congelamento
calor de fusão
Lf
O calor latente de vaporização é a energia que deve ser adicionada a um
quilograma da fase líquida de uma substância para romper todas as ligações
de maneira a formar um gás
evaporação ou condensação
calor de evaporação
Lv
10
A Tabela mostra os calores latentes de diferentes substâncias
O calor latente de evaporação para uma dada substância é geralmente muito
maior do que o calor latente de fusão
11
• Na mudança da fase sólida para a fase líquida, as ligações entre as moléculas
são transformadas em ligações mais fracas
• Na mudança da fase líquida para a fase gasosa, as ligações são rompidas,
criando uma situação na qual as moléculas de gás não têm essencialmente
ligação alguma entre si
12
Temperatura versus energia fornecida, quando 1 g de gelo inicialmente a – 30.0 C
é convertido em vapor a 120.0 C.
13
2.4 Trabalho e Calor em Processos Termodinâmicos
Variáveis de estado – pressão, volume, temperatura e energia interna
O estado macroscópico de um sistema pode ser especificado apenas se o sistema estiver
em equilíbrio térmico interno
Variáveis de transferência – trabalho e calor
Essas variáveis só têm valor diferente de zero se
ocorrer um processo no qual a energia é transferida
através da fronteira do sistema
• Trabalho realizado por um sistema deformável
– o gás
O gás ocupa um volume V e exerce uma pressão P
nas paredes do cilindro e no pistão
O gás é expandido quasi-estaticamente, isto é,
devagar o suficiente para permitir que o sistema se
mantenha em equilíbrio térmico em todos os
instantes
dW F dr Fj dyj Fdy PAdy
porque
F
P
A
dW PdV
14
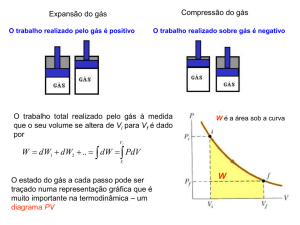
Compressão do gás
Expansão do gás
O trabalho realizado pelo gás é positivo
O trabalho realizado pelo gás é negativo
O trabalho total realizado pelo gás à medida
que o seu volume se altera de Vi para Vf é dado
por
W é a área sob a curva
Vf
W PdV
Vi
O estado do gás a cada passo pode ser
traçado numa representação gráfica que é
muito importante na termodinâmica – um
diagrama PV
W
15
O trabalho realizado pelo gás depende da trajectória seguida entre os estados inicial
e final
W2
W3
W1
W1 Pf V f Vi
W2 Pi V f Vi
Vf
W3 PdV
Vi
Para determinar o trabalho W3 é preciso conhecer a função P(V)
W1 W3 W2
16
• Calor em processos termodinâmicos
De maneira semelhante, também se descobre que a energia transferida pelo calor
para dentro ou para fora do gás depende do processo pelo qual é transferido
a) Um gás à temperatura Ti se expande
lentamente absorvendo energia de um
reservatório à mesma temperatura
b) Um gás expande rapidamente numa
região onde se fez vácuo depois que
uma membrana é rompida
Em cada caso o gás tem
o mesmo volume,
temperatura e pressão
iniciais e é considerado
ideal
Portanto concluímos que a transferência de energia pelo calor, assim como o trabalho
realizado, depende do processo seguido entre os estados inicial e final do sistema
17
2.5 Primeiro Princípio da Termodinâmica
Caso especial do princípio da conservação de energia: a única variação na
energia dum sistema é a variação na sua energia interna U, e os únicos
mecanismos de transferência de energia são o calor Q e o trabalho W
Primeiro princípio da termodinâmica
U Q W
Q é a energia transferida para o gás
W é o trabalho realizado pelo gás
Significa que a variação da energia interna de um sistema, U é
igual à soma da energia transferida através da fronteira do sistema
pelo calor e a energia transferida pelo trabalho
Quando um sistema é submetido a uma mudança infinitesimal em seu
estado, tal que uma pequena quantidade de energia dQ transferida pelo
calor e uma pequena quantidade de trabalho dW realizado pelo sistema,
a energia interna também varia de uma quantidade pequena dU
U dQ dW
18
2.6 Algumas Aplicações do Primeiro Princípio da
Termodinâmica
Processos termodinâmicos: adiabático, isométrico (ou isocórico), isotérmico
e o cíclico
Processo adiabático
Todas as superfícies do pistão são isolantes perfeitos, de maneira que a
transferência de energia pelo calor não existe
Q=0
Aplicando o primeiro princípio da termodinâmica
U Q W 0 W
U W
O trabalho realizado pelo gás é negativo, representando a
transferência de energia para dentro do sistema, de maneira que a
energia interna aumenta. E quando o gás se expande
adiabaticamente, U é negativo
A expansão livre é um processo adiabático único, em que nenhum trabalho é
realizado sobre o gás. Como Q=0 e W=0 obtemos
.
U 0 U f U i 0 U f U i
Não há variação na temperatura
19
durante uma expansão livre adiabática
Processo isobárico
Processo que ocorre a uma pressão constante
W PV f Vi
Aplicando o primeiro princípio da termodinâmica
U Q W
Processo isométrico (ou isocórico)
No processo isométrico, o volume é
constante e é criado segurando-se o
pistão de maneira que ele não se mova
W=0
Aplicando o primeiro
termodinâmica
U Q W Q 0
princípio
da
U Q
Toda a energia adicionada ao sistema por meio
do calor, vai para o aumento da energia interna
do sistema
20
Processo isotérmico
Isoterma
Num processo isotérmico a temperatura é constante
U 0
Aplicando o primeiro princípio da termodinâmica
U Q W 0 Q W W Q
A energia que entra no gás por meio do trabalho sai
do gás por meio do calor, de modo que a energia
interna permanece fixa
PV nRT P
Vf
nRT
V
Vf
Vf
nRT
1
Vf
W PdV
dV nRT dV nRT ln V V
i
V
V
Vi
Vi
Vi
nRT ln V f ln Vi
ou
Vf
W nRT ln
Vi
21
Processo cíclico
O sistema não isolado começa e termina no
mesmo estado
U 0
Aplicando o primeiro princípio da termodinâmica
U Q W 0 Q W
Q W
A energia adicionada ao sistema na forma de calor, deve ser igual ao trabalho
realizado sobre o sistema durante o ciclo
Os processos cíclicos são muito importantes na descrição das máquinas térmicas
22
2.7
Mecanismos de Transferência de Energia
em Processos Térmicos
Condução
Em escala atómica há uma troca
de
energia
cinética
entre
moléculas, na qual as moléculas
menos
energéticas
ganham
energia colidindo com moléculas
mais energéticas
- Antes de se inserir a barra na chama, os átomos estão vibrando em torno de suas posições
de equilíbrio
- À medida que a chama fornece energia à barra, os átomos próximos à chama começam
a vibrar com amplitudes cada vez maiores
- Colidem com seus vizinhos e transferem um pouco de sua energia nas colisões
O aumento da vibração das moléculas representa uma elevação de
temperatura do metal
A taxa de condução depende das propriedades da substância
23
Considere um bloco cujo material tem espessura x e uma secção de área A,
cujas faces opostas têm temperaturas T1 e T2, onde T2> T1
Taxa de transferência de energia pelo calor
T2
T2
T1
T1
H Q / t (Watts)
H é a potência
Q
T
H
A
t
x
Para um bloco de espessura infinitesimal dx e diferença de temperatura dT,
podemos escrever a lei da condução como
dT
H kA
dx
k é chamada de condutividade térmica do material
dT / dx
é o gradiente de temperatura (variação da
temperatura com a posição)
24
Suponha que uma substância esteja na forma de uma barra longa e uniforme e de
comprimento L
T2
T1
Está isolada de modo que a energia não
possa escapar pelo calor a partir da sua
superfície excepto nas extremidades, que
estão
em
contacto
térmico
com
reservatórios que têm temperaturas T1 e T2
No estado estacionário a temperatura em cada ponto ao longo da barra é
constante no tempo
dT T2 T1
dx
L
A taxa de transferência de
energia pelo calor será
H kA
T2 T1
L
k é a condutividade térmica
25
A Tabela mostra a condutividade térmica de diferentes substâncias
26
Convecção
A energia é transferida pelo movimento de um fluido
Se não fosse pelas correntes de convecção, seria muito difícil ferver a água
À medida que a água é aquecida numa panela, as camadas
inferiores são aquecidas primeiras.
Essas regiões se expandem e sobem porque tem uma densidade
menor que a da água fria. Ao mesmo tempo, a água mais fria e
mais densa vai para o fundo da panela e aí pode ser aquecida.
O mesmo processo ocorre numa
sala aquecida por um aquecedor
27
Radiação
A energia é transferida pela radiação electromagnética
A origem da radiação electromagnética é a aceleração de cargas eléctricas
Qualquer corpo emite radiação electromagnética devido ao movimento térmico de suas
moléculas
A potência irradiada pelo corpo em Watts
Constante de Stefan-Boltzmann:
H AeT 4
5.6696 108
W/m2K4
A é a área da superfície do
corpo em metros quadrados
e
é uma constante chamada
emissividade
T é a temperatura da superfície
do corpo em kelvins
28