Bioenergética e Reacções RedoxMitocondriais
Respiração Celular
Respiração Celular
Constituintes e caracterização da cadeia mitocondrial de transporte de electrões de transporte de electrões
Cadeia Respiratória
Mecanismos de transporte de electrões na Mitocôndria
Mecanismos
de transporte de electrões na Mitocôndria
Fosforilação oxidativa
Oxi‐reduções com e sem oxigénio
Formas activas de oxigénio Sistema de protecção celular anti‐oxidante
Realizado no âmbito da unidade curricular de Metabolismo e Endocrinologia do Curso de MEBM (2Ano)por: Grupo 2
André Zamith, nº58556
Eduardo Bicacro, nº58615
Pedro teixeira , nº58482
• As células do organismo humano necessitam de g
energia para realizar as funções que permitem a sustentabilidade da vida.
• A fosforilação oxidativa é o culminar de um processo de obtenção de energia realizado pelos organismos ‐ a respiração celular aeróbia.
• A fosforilação oxidativa tem lugar na matriz mitocondrial.
Mitocôndria
É na matriz que ocorre o Ciclo de Krebs em eucariotas.
| Membrana externa permeável à maioria das pequenas moléculas e iões.
iõ
| Membrana interna pouco permeável (canais
permeável (canais transportadores específicos).
|
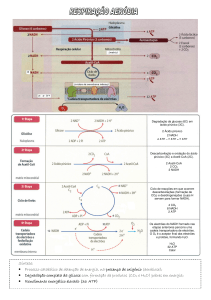
Resumo dos eventos até à esu o dos e e tos até à
conclusão da fosforilação oxidativa
Moléculas altamente energéticas (passíveis de serem oxidadas)
Fluxo de electrões na cadeia mitocondrial
(reacções redox)
Liberta
(r. exergónica)
ENERGIA
Energia armazenada sob a forma de potencial electroquímico
Síntese ATP
Movimento de protões através da membrana interna
membrana interna mitocondrial
É consumida
(r. endergónica)
(Teoria quimiosmótica Peter Mitchell, 1961)
Constituintes da Cadeia Mitocondrial de transporte de Electrões
Desidrogenase
g
• É uma Oxirredutase.
É
O i d t
• Enzima
Enzima que oxida um substrato, transferindo um que oxida um substrato transferindo um
ou mais protões e um par de electrões para um aceitador.
Desidrogenase
2e‐ + H
+ H+
• Existem diferentes tipos de molécula aceitadora que intervêm neste tipo de reacção, que seguidamente se apresentam
seguidamente se apresentam.
NAD+ e NADP +
• NAD
NAD – Nicotinamida
Nicotinamida‐adenina‐dinucleótido
adenina dinucleótido
(estrutra com 2 nucleótidos – nicotinamida e adenina).
adenina)
• São coenzimas de desidrogenases.
(Grupo fosfato no caso de NADP+) FMN e FAD
• Dá‐se o nome de Flavoproteínas às desidrogenases com coenzima
i FAD ou FMN
FAD
FMN
• FMN – flavina‐mononucleótido
• FAD – flavina‐adenina‐dinucleótido
Ribitol FMN
FAD
Centro reactivo
FAD + 2H++ 2e‐FADH2
• O potencial de redução padrão do p
nucleótido de flavina depende da proteína a que está associado. (interacções que este estabelece com ela)
(interacções que este estabelece com ela)
Coenzima Q10 10
• ÉÉ uma benzoquinona solúvel em lípidos (consegue movimentar‐se no interior da bicamada
no interior da bicamada
fosfolipídica).
• Pode aceitar um electrão, Pode aceitar um electrão
tornando‐se o radical semiquinona.
• Se aceitar outro, denomina‐se ubiquinol.
• Consegue transportar protões e electrões.
Citocromo
•
•
•
•
Proteína com um grupo prostéticoheme (com Fe).
Estado Oxidado – Fe3+ ; Estado Reduzido – Fe2+
Mitocôndrias têm 3 tipos de citocromo: a, b e c.
Os diferentes tipos são distinguidos tendo em conta os comprimentos de onda de máxima absorção de luz.
i
d
d d
á i
b
ã d l
• O
Os grupos heme
h
a e b estão fortemente ligados à parte b ã f
li d à
proteica do citocromo. • O heme
O heme c, está ligado covalentemente
c está ligado covalentemente através de dois através de dois
resíduos de Cisteína.
• 4 anéis azotados numa estrutura cíclica ‐
4 éi
t d
t t
í li
porfirina
fi i
Proteínas Fe S
Proteínas Fe‐S
• O ferro surge associado a proteínas, mas não em grupos g
p
,
g p
heme. • A associação é feita através de átomos de enxofre orgânicos, inorgânicos ou através de ambos os tipos.
• Como os citocromos, participam em transferências de apenas um electrão.
Complexosda Cadeia Mitocondrial
de transporte de Electrões
(changepresenter)
Cadeia Respiratória:
Cadeia Respiratória:
Cadeiade transporte de electrões na C d i d t
t d l tõ
Mitocôndria
FosforilaçãoOxidativa
ç
Cadeia de transporte de electrões na Mitocôndria
•
A transferência de electrões da molécula dadora (NADH) até à aceitadora (O
A
f ê i d l
õ d
lé l d d
(NADH) é à
i d
(O2), )
é um processo globalmente exergónico que ocorre através de uma série de reacções redox intermédias. Este facto revela‐se muito favorável do ponto de vista energético.
Potenciais de Redução Padrão dos Transportadores Electrónicos
(determinados experimentalmente)
Balanços Energéticos
NADH
E’O=‐0.320V
O2
E’O=0.8166V
Electrões no sentido de potenciais crescentes
ΔG’0 = ‐nFΔE’0
ΔE’0 =1.1366
Representação esquemática da p
ç
q
cadeia de transporte electrónico UQ – Ubiquinona
Cytc – Citocromo C
IMM – Membrana Mitocondrial Interna
Setas pretas são as transferências de electrões
Elementos dadoresde electrões com alta energia
Relembrar Ciclo de Krebs...
NADH
Cadeia de transporte de electrões para o oxigénio
Complexo I ‐
p
NADH: quinona‐oxidorredutase
(EC 1.6.5.3) ; 850kDa ; 43 subunidades proteicas Complexo I
p
Catalisa a oxidação do NADH e a redução da coenzima Q a Ubquinol.
Componentes:
• Flavoproteína‐FMN.
Fl
t í FMN
• Minimo 6 centros Fe‐S
•
Reacções Exergónicas:
•
Reacção Endergónica:
4H+ in→ 4H+out
•
Reacção total do complexo I
NADH + CoQ + 5H+ in→ NAD+ + CoQH2 + 4H+out
Vias de redução da Ubiquinona
ç
q
Complexo II ‐ succinatodesidrogenase
(EC 1.3.5.1) ; 140 kDa ; 4 subunidades proteicas Complexo II
p
Catalisa a oxidação do Succinato e a redução da coenzima Q.
Componentes:
• Flavoproteina‐FAD ;
• Subunidades C e D são proteínas integradas com neste complexo
ggrupos heme;
pNão ocorre bombeamento Protónico
;
• Proteinas de Fe‐S
•
ç
g
Reacções Exergónicas:
•
Reacção total do complexo II
+ CoQ → Fumarato + CoQH
→ Fumarato + CoQH2
Succinato + CoQ
Complexo III – ubiquinona:citocromocoxirredutase
(EC 1.10.2.2) ; 250 kDa ; 11 subunidades proteicas Complexo III
p
Catalisa a oxidação doUbiquinole a Catalisa
a oxidação doUbiquinole a
redução do Citocromoc.
Componentes:
• Citocromob e c1
• Grupos heme
• Proteínas Fe‐S
Proteínas Fe S
•
Reacções Exergónicas:
ç
g
•
Reacção Endergónica:
•
Reacção total do complexo I
4H+ in→ 4H+out
QH2 + 2 cytochrome c1 (FeIII) + 2 H+in → Q + 2 cytochrome c1 (FeII) + 4 H+out
Complexo IV ‐ citocromocoxidase
(EC 1.9.3.1) ; 160kDa ; 13 subunidades proteicas
Complexo IV
p
Catalisa a oxidação do citocromoc
Catalisa
a oxidação do citocromoc e e
a redução do Oxigénio a Água.
Componentes:
• CuA (centro binuclear de Cu)
(centro binuclear de Cu)
• Citocromo a
• Centro binuclear Citocromo a3‐CuB
•
Reacções Exergónicas:
•
R
Reacção Endergónica:
ã E d ó i
•
4H+in→ 4 H+out
Reacção total do complexo I
4 Cit‐c (reduzido) + 8 H+in+ O2 → 4 Cit‐c (oxidado) + 2 H2O + 4 H+out
Quanta energia se conseguiu armazenar?
g
g
ΔG’0 = ‐nFΔE’0=‐220kJ/mol (de NADH)
Força motriz protónica
ç
p
devido ao gradiente de concentração e potencial da membrana.
= 20kJ/mol (de H+)
200kJ/10mol (de H+)
Grande parte da energia foi armazenada. Permite a sintese de ATP
FosforilaçãoOxidativa
ATP Sintase
q
ATPases – enzimas que efectuam transporte activo
(com gasto de ATP);
Quando funcionam de forma inversa são denominadas ATP
inversa são denominadas ATP sintases;
Domínios: F0 e F1
Porção integrada
Subunidades:
a;b;c
a ; b ; c
Porção periférica
Subunidades:
α;β;γ;δ
α ; β ; γ
FosforilaçãoOxidativa
ATP Sintase
Como é realizada a síntese?
Junto à superfície da porção F1 a reação ADP+P ocorre a reação ADP+P ocorre
quase espontaneamente.
•O que requere energia é a O
i é
quebra da ligação que se estabelece entre a enzima e a ATP formada
ATP formada.
•O mecanismo funciona por mudanças conformacionais
das subunidades β. (changepresenter)
Transporte de Electões (Grande Eficácia)
Contudo há uma percentagem que não se liga premanentemente ao Oxigénio
Contudo há uma percentagem que não se liga premanentemente
ao Oxigénio
Resulta na formação de formas activas de oxigénio
F
Formas activas de oxigénio
ti
d
i é i
Sistema de protecção celular anti‐oxidante
Formas Activas de oxigénio
g
(Reactive oxygenspecies – ROS)
OxigénioMolecular (Grande Poder Oxidante)
Ideal Aceitador de Electrões para a Cadeia • Embora:
Transferência de 4 electrões e 4 protões reduza o oxigénio em água (Inofensivo)
• Durante esse processo ocorre:
Transferência de 1 ou 2 electrões para produzir um superóxido e peróxido, respectivamente (Potencialmente perigoso)
Estas espécies reactivas de oxigénio e os seus produtos de reacção (Ex:radical Hidroxilo), são muito perigosas para as celulas.
Estas lesões celulares podem contribuir para o desencadear de doenças
Estas lesões celulares podem contribuir para o desencadear de doenças.
Formas activas de oxigénio
Formas activas de oxigénio
ROS
ROS
• iões de oxigénio
• radicais livres • peróxidos
Geralmente pequenas moléculas altamente reactivas devido à presença de pares de electrões de valência desemparelhados.
p
Formação das ROS
ç
•
As formas activas de oxigénio são formadas por :
‐ interacção de radiação ionizada com moléculas
‐ enzimas específicas para o efeito em células fagocíticas
íf
f
él l f
í
(
(por ex.: macrófagos)
óf
)
‐ produto indesejado da respiração celular.
•
1‐4% do oxigénio que reage com a cadeia respiratória sofre uma redução incompleta, 1
4% do oxigénio que reage com a cadeia respiratória sofre uma redução incompleta
originando ROS;
•
A mitocôndria é o principal produtor de ROS; •
O ião superóxido é frequentemente formado quando uma molécula de O2 é prematura e incompletamente reduzida .
As zonas mais vulneráveis são o complexo I e complexo III
A
i
l á i ã
l
I
l
III
Todo o Ciclo Q é também uma das principais fontes de ROS (Complexo I)
Superóxido
HO2 (forma especialmente reactiva)
(forma especialmente reactiva)
Efeitos prejudiciais das ROS
e tos p ejud c a s das OS
‐ Danos no DNA
Danos no DNA
‐ Oxidações de ácidos gordos poli insaturados
‐ Oxidações de aminoácidos em proteínas.
‐ Oxidação de co
Oxidação de co‐factores
factores
‐ Esta, além de produtora, é um alvo destes mesmo ROS’s que vão interferir no mDNA.
Sistemas de Protecção Celular
ç
• As
As células apresentam uma variedade de defesas contra os células apresentam uma variedade de defesas contra os
efeitos nocivos das ROS.
Reagem com oxidantes no
oxidantes no citoplasma e plasma sanguíneo
Enzimas :
Superóxidodismutase
‐Superóxidodismutase
(SOD)
‐Catalase
‐Ascorbatoperoxidase
p
Antioxidantes :
‐Vitamina C
‐Ácido úrico
‐Glutatião
‐Vitamina E
‐Ubiquinol
Hidrófilo
Hidrofóbico
Protecção das membranas celulares da peroxidação lipídica
Acção Enzimática
SuperóxidoDismutase
M(n+1)+ − SOD + O2− → Mn+ − SOD + O2
Mn+ − SOD + O2− + 2H+ → M(n+1)+ − SOD + H2O2
M = Cu (n=1) ; Mn (n=2) ; Fe (n=2) ; Ni (n=2) – Consoante o tipo de Dismutase
Catalase
2 H2O2 → 2 H2O + O2
A característica importante a reter – elevada velocidade de conversão
Acção Antioxidante
• Capaz de atrasar ou prevenir a oxidação de outras moléculas
• Remoção de radicais livres e inibição de oxidações oxidando‐se a si próprio.
Vitamina C (ascorbato)
É a coenzima da ascorbatoperoxidase.
A
Ascorbate
b t + Hydrogenperoxide
+H d
id → Dehydroascorbate
→D h d
b t + Water
+W t
C6H8O6 + H2O2 → C6H6O6 + 2 H2O
Á id Ú i
Ácido Úrico
Aproximadamente metade da capacidade antioxidante do plasma sanguíneo.
Aproximadamente
metade da capacidade antioxidante do plasma sanguíneo
Forte capacidade de doar electrões. Glutatião
Tripéptido sintetizado no fígado.
Presente na maioria das células (reservas próprias da mitocôndria e núcleo)
2 estados oxidação – defesa antioxidante importante para os organitos.
Cadeia mitocondrial de transporte electrónico (mecanismos de defesa inerentes)
(mecanismos de defesa inerentes)
Voltar Slide Comlexo II
Complexo II
p
Catalisa a oxidação do Succinato e a redução da coenzima Q a Ubquinol.
Componentes:
• Flavoproteina‐FAD ;
• Subunidades C e D são proteínas integradas com g p
grupos heme;
;
• Proteinas de Fe‐S
•
ç
g
Reacções Exergónicas:
•
Reacção total do complexo II
+ CoQ → Fumarato + CoQH
→ Fumarato + CoQH2
Succinato + CoQ
ROS – Reactive Oxigene Spieces (os grupos heme das
subunidades C/D impede que os electrões saiam para a célula)
ROS ?
ROS ?
ROS: acção benéfica
ç
ROS (pequenas quantidades)
• Sinalização celular
Sinalização celular
• Recrutamento de plaquetas – migração de plaquetas para o local da ruptura (sinalização l
l ld
( i li ã
oxidativa)
• Sistema imunitário
• Mobilização de sistemas de transporte iónico
M bili ã d i t
d t
t ió i
St ess o dat o
Stress oxidativo
Sumário geral
Respiração Celular
Respiração Celular
Constituintes e caracterização da cadeia mitocondrial de transporte cadeia mitocondrial
de transporte
de electrões Cadeia Respiratória
Mecanismos de transporte de electrões na Mitocôndria
Fosforilação oxidativa
Oxi‐reduções com e sem oxigénio
Formas activas de oxigénio
Formas activas de oxigénio Sistema de protecção celular anti‐oxidante
Bibliografia
(Bioenergética e reacções redoxmitocondriais) •
•
•
•
•
•
•
InteractiveAnimationaboutOxidativePhosp
Nelson DL; Cox MM (Apr 2005).
horylation
LehningerPrinciplesofBiochemistry, 4th
http://www.wiley.com/legacy/college/boyer/0470003790/animations/elec
ed W.
ed,
W H.
H Freeman
tron_transport/electron_transport.htm
Harper'sIllustratedBiochemistry
• Nicholls DG; Ferguson SJ (Jul 2002). (Murray, Mcgraw-Hill Medic, 26th ed
Bioenergetics 3. AcademicPress.
Luís S. Campos, Entender a
HA (1947) Antioxidants
• Matill HA (1947). Antioxidants. Bioquimica
AnnuRevBiochem 16: 177–192
Secção
• Voet D; Voet JG (Mar 2004). Biochemistry, “MetabolicPathwaysofBiochemistry” da
3rd ed, Wiley
George Washington University
• Lectures Antony Crofts, 1996, Lodish - Molecular CellBiology 5th
UniversityofIllinoisatUrbana‐Champaign
Oxford DictionaryofBiochemistryand • LecturesBioquimica e Biologia Molecular –
Molecular Biology
Instituto Superior Técnico
Instituto Superior Técnico
CellBiologyAnimations –
fromtheinstitute John Kyrk
http://www.johnkyrk.com/mitochondrion.html
•
InteractiveConceptsof Biochimestry –
Realizado no âmbito da unidade curricular de Metabolismo e Willy internet website –
Endocrinologia do Curso de MEBM (2Ano)por: Grupo 2
André Zamith, nº58556
Eduardo Bicacro, nº58615
Pedro teixeira , nº58482