Universidade de Brasília
Instituto de Ciências Biológicas
Departamento de Biologia Celular
Resistência a Sclerotinia sclerotiorum em plantas de soja
geneticamente modificadas para expressar o gene da oxalato
descarboxilase de Flammulina velutipes
Welcimar Gonçalves da Cunha
2010
Welcimar Gonçalves da Cunha
Resistência a Sclerotinia sclerotiorum em plantas de soja
geneticamente modificadas para expressar o gene da oxalato
descarboxilase de Flammulina velutipes
Tese apresentada à Universidade de Brasília,
como parte das exigências do Programa de PósGraduação em Biologia Molecular, para a
obtenção do título de “Doutor”.
Orientador
Dr. Francisco José Lima Aragão
Brasília
Distrito Federal – Brasil
2010
Aos meus pais Acimar Gonçalves da Cunha e Vera Lúcia Barbosa da Cunha, que
na simplicidade e no amor investiram todas as suas forças para o bem maior de
seus filhos.
DEDICO
AGRADECIMENTOS
Neste momento, externo os meus sinceros agradecimentos a todos os que
contribuíram para a realização deste trabalho.
Assim, sou grato ao nosso bom Deus, autor de toda vida e alimento do meu
viver.
Aos meus pais Acimar Gonçalves da Cunha e Vera Lúcia Barbosa da
Cunha, pelo amor, carinho, incentivo e confiança.
Aos meus irmãos Acimar Gonçalves da Cunha Junior e Gleicimar
Gonçalves da Cunha, espelho do meu viver.
Ao meu amigo e orientador Francisco José Lima Aragão externo
agradecimento especial pela sua dedicada orientação, disponibilidade e conselhos
dados ao longo deste curso. Serei eternamente grato pelo incentivo prestado no
momento em que eu fora chamado a assumir o desafio de ingressar na equipe de
melhoramento da Pioneer Sementes. Jamais esquecerei suas palavras de apoio.
A todos aqueles que se doaram a minha formação profissional em especial
aos professores Everaldo Anastácio Pereira, José Ricardo Peixoto, Magno Antonio
Patto Ramalho, César Augusto Brasil Pinto, João Bosco dos Santos e Ângela de
Fátima Barbosa Abreu. A Ana Cristina Miranda Brasileiro e a Érika Valeria Saliba
Albuquerque que me ajudaram a dar os primeiros passos na área de
transformação de plantas. Ao amigo, chefe e exemplo de dedicação e amor ao
melhoramento de plantas Luis Cláudio Prado.
Ao Hugo, Maria Laine pelo apoio concedido a conclusão deste trabalho. A
ajuda de vocês foi essencial.
A Renata Esteve Ribeiro, parceira ao longo dessa caminhada e que esteve
sempre presente, principalmente nos momentos de maiores dificuldades. O seu
amor tornou mais suave e especial essa conquista.
A UnB, Embrapa e CNPq.
A todos os professores e funcionários do Departamento de Biologia Celular.
A todos os pesquisadores e funcionários da Embrapa Recursos Genéticos e
Biotecnologia.
A todos os amigos do laboratório de Transferência e Expressão de Genes.
A todos os amigos da Pioneer que me ajudaram e incentivaram a continuar
a cursar o doutorado em Biologia Molecular.
Aos membros da banca, por dedicarem o seu tempo visando a melhoria
deste trabalho.
SUMÁRIO
RESUMO............................................................................................................................... 1
1 – INTRODUÇÃO .............................................................................................................. 2
1.1 – Sclerotinia sclerotiorum (Lib.) de Bary .............................................................. 2
1.2 – Mofo Branco da Soja .............................................................................................. 3
1.3 – O ácido oxálico e o seu papel durante o processo de infecção do fungo
S. sclerotiorum ............................................................................................................... 7
1.4 – Expressão de genes de oxalato oxidases e oxalato descarboxilases no
desenvolvimento de plantas transgênicas resistentes ao fungo S.
sclerotiorum .................................................................................................................. 11
2 – OBJETIVOS................................................................................................................. 15
3 – MATERIAIS E MÉTODOS ........................................................................................ 16
3.1 – Isolamento do gene oxdc do fungo Flammulina velutipes ........................ 16
3.2 – Clonagem do gene oxdc ...................................................................................... 17
3.3 – Transformação genética de soja com o vetor pBluKSPOXDCAHAS ...... 19
3.4 – PCR (Polymerase Chain Reaction) para a detecção do gene oxdc ......... 19
3.5 – Plantio da geração T0............................................................................................ 20
3.6 – Plantio da geração T1............................................................................................ 20
3.7 – Plantio da geração T2............................................................................................ 21
3.8 – Inoculação das folhas destacadas utilizando plugs de micélio do fungo
S. sclerotiorum ............................................................................................................. 22
3.8.1 – Produção do inóculo ......................................................................................... 22
3.8.2 – Teste das folhas destacadas........................................................................... 22
3.9 – Análise genético-estatística para avaliar a reação das plantas ao fungo
Sclerotinia sclerotiorum ............................................................................................ 24
3.10 – Southern blot ........................................................................................................ 25
3.11 – RT-PCR ................................................................................................................... 25
4 – RESULTADOS E DISCUSSÃO ............................................................................... 27
4.1 – Isolamento do gene oxdc do fungo Flammulina velutipes ........................ 27
4.2 – Clonagem do gene oxdc ...................................................................................... 28
4.3 – Transformação genética de soja com o vetor pBlukSPOXDCAHAS,
análise da PCR para a detecção do gene oxdc e obtenção da geração T2.. 29
4.4 – Inoculação de folhas destacadas das plantas T2 utilizando discos de
micélio do fungo S. sclerotiorum ............................................................................ 31
5 – CONCLUSÕES ........................................................................................................... 42
REFERÊNCIAS BIBLIOGRÁFICAS .............................................................................. 43
ANEXOS ............................................................................................................................. 53
ANEXO A ............................................................................................................................ 54
ANEXO B ............................................................................................................................ 76
RESUMO
O mofo branco, causado pelo fungo Sclerotinia sclerotiorum, é hoje um dos
principais problemas da cultura da soja e afeta diretamente a economia dos
principais países produtores. A incidência desse patógeno acarreta em danos
expressivos na produção e qualidade dos grãos, podendo atingir perdas em torno
de 80%. O ácido oxálico, produzido pelo fungo durante o processo de infecção, é
considerado o principal fator de patogenicidade do fungo S. sclerotiorum. A
expressão de enzimas que degradam o ácido oxálico em plantas transgênicas tem
sido utilizada em diversas culturas visando o desenvolvimento de cultivares
resistentes. No presente trabalho, o gene oxdc que codifica para a enzima oxalato
descarboxilase, isolado do fungo Flammulina velutipes, foi inserido via biobalística
no genoma da soja. Dezesseis eventos T 2 foram avaliados via inoculação de
discos de micélio do fungo S. sclerotiorum em folhas destacadas. A análise da
curva de progresso da doença revelou que todos os eventos transgênicos
apresentaram atraso no desenvolvimento dos sintomas quando comparados com
o controle não transgênico. A área abaixo da curva de progresso da doença foi
utilizada para sumarizar a severidade da doença em cada evento transgênico e no
controle. O teste de Kruskal-Wallis revelou que houve diferença significativa (P ≤
0,05) entre os tratamentos. Os eventos OXDC.9.21 e OXDC.8.18 tiveram os
menores índices de severidade. Tais eventos apresentaram respectivamente,
índices de severidade 96% e 93% menor que o apurado para o controle. Os
resultados impetrados a partir da curva de progresso da doença e da severidade
da doença utilizando o teste de inoculação da folha destacada com o fungo S.
sclerotiorum sugerem que a expressão do gene da oxdc em soja confere aumento
do nível de resistência das plantas ao patógeno.
1
1 – INTRODUÇÃO
1.1 – Sclerotinia sclerotiorum (Lib.) de Bary
De acordo com a atual classificação taxonômica, o fungo Sclerotinia
sclerotiorum (Lib.) de Bary pertence ao filo Ascomycota, classe Discomiceto,
ordem Helotiales e família Sclerotiniaceae. Patógeno necrotrófico e polífago, tem
como hospedeiros mais de 400 espécies incluindo culturas de importância
econômica e diversas plantas daninhas (Boland & Hall, 1994). Disperso por todo o
mundo, o fungo encontra condições ótimas de crescimento em temperaturas
amenas (15 a 25 oC) e em ambientes com alta umidade. Em temperaturas abaixo
de 0 oC e acima de 32 oC, o fungo apresenta baixa atividade (Purdy, 1979).
As perdas de produtividade causadas pelo fungo S. sclerotiorum variam de
acordo com a incidência do patógeno, região, clima, cultura e variedade plantada.
Segundo Purdy (1979), as perdas de produtividade podem chegar a 100%. O
custo anual das perdas oriundas do ataque de S. sclerotiorum nos EUA tem
excedido os US$ 200 milhões (Bolton et al., 2006).
Os sintomas variam de acordo com o hospedeiro, parte afetada do
hospedeiro e com as condições ambientais. Em geral, o desenvolvimento do
patógeno inicia em tecidos necróticos. O sintoma mais comum e característico da
doença é a formação de um aglomerado de micélios brancos com aspecto
cotonoso sob a área afetada e o posterior desenvolvimento dos escleródios. Os
escleródios desempenham papel de grande importância durante o ciclo
reprodutivo do fungo. Além de responsáveis pela produção de inóculo
2
(germinação micelogênica e/ou carpogênica), os escleródios são estruturas
primárias de sobrevivência do fungo. Na ausência do hospedeiro, a persistência
dos escleródios no solo pode atingir mais de oito anos (Adams & Ayers, 1979). Em
algumas culturas, como o girassol, soja e feijão, os escleródios atuam também
como estruturas de disseminação do patógeno. Durante a colheita em áreas
infestadas pelo patógeno, os escleródios são misturados às sementes e se o
beneficiamento não for adequado estas estruturas poderão infectar um novo
campo no plantio da próxima safra.
1.2 – Mofo Branco da Soja
O mofo branco, causado pelo fungo S. sclerotiorum, é hoje um dos
principais problemas da cultura da soja e afeta diretamente a economia dos
principais países produtores (EUA, Brasil e Argentina). A incidência desse
patógeno acarreta em danos expressivos na produção e qualidade dos grãos,
podendo atingir perdas em torno de 80%. Segundo trabalhos realizados, utilizando
diferentes genótipos, o aumento de 10% da incidência da doença acarreta em
perdas de produtividade que variam de 83 a 335 Kg/ha (Chun et al., 1987;
Hoffman et al., 1998; Yang et al., 1999; Danielson et al., 2004).
No Brasil, a doença ocorre predominantemente nas regiões produtoras do
Sul e de terras altas (acima de 700 m) do Brasil Central. O monocultivo e a
ausência de rotação com espécies não hospedeiras são as principais causas do
aumento da área infestada no Brasil. Segundo estimativas apresentadas pelo
pesquisador Luís Henrique Carregal P. da Silva no V Congresso Brasileiro de
3
Soja, realizado em maio de 2009, cerca de 45% da área plantada com soja no
estado de Goiás encontra-se infestada pelo fungo S. sclerotiorum. No sudoeste
goiano, principal pólo produtivo de soja do estado, cerca de 55% da área cultivada
está infestada e em algumas fazendas tem-se verificado perdas de produtividade
superiores a 60%.
Nos EUA, o principal foco da doença compreende os estados de Iowa,
Illinois, Minnesota, Nebraska, Pensilvânia, Dakota do Sul e Wisconsin (Wrather &
Koenning,
2009).
Historicamente,
esses
estados
são
responsáveis
por
aproximadamente 55% da produção de soja dos EUA. Em 2004, quando as
condições climáticas foram favoráveis ao desenvolvimento do patógeno, as perdas
de produtividade causadas pelo mofo branco nos EUA foram superiores a 27
milhões de sacos (Wrather & Koenning, 2009). Em preços atuais, o valor desse
prejuízo equivale a aproximadamente US$ 550 milhões.
A fase mais vulnerável da soja ao desenvolvimento do patógeno abrange os
estádios de floração plena (R2) e início de formação das vagens (R3/R4). Nesse
período, o dossel da planta cobre as entre linhas de plantio propiciando condições
favoráveis de umidade e temperatura para os escleródios, presentes no solo,
germinarem e produzirem os apotécios. Os apotécios, por sua vez, produzem os
ascósporos que são liberados no ar. Os ascósporos, ao encontrarem tecidos
senescentes, germinam e iniciam o processo de infecção da planta. Em geral, o
processo de infecção inicia a partir das inflorescências e das axilas das folhas e
ramos laterais. A Figura 1 resume de forma esquemática o ciclo de vida do mofo
branco da soja, incluindo os processos de infecção via germinação carpogênica e
micelogênica.
4
Figura 1. Esquema do ciclo de vida do fungo Sclerotinia sclerotiorum, agente
causador do mofo branco da soja. Adaptado de Wharton & Kirk (2007).
O controle da doença está concentrado principalmente em práticas
agronômicas como o plantio de cultivares resistentes ao acamamento, maior
espaçamento entre linhas, redução da população de plantas, plantio direto,
rotação com culturas não hospedeiras e aplicação de fungicidas. Contudo, em
condições ambientais favoráveis ao desenvolvimento do patógeno, tais práticas
têm se mostrado pouco eficientes. O uso de fungicidas é de baixa eficiência
porque o período inicial de infecção do patógeno ocorre quando a planta encontrase na fase reprodutiva. Nesse estágio, as entre linhas de plantio estão cobertas
5
pelo dossel da planta e as folhas dificultam a distribuição do produto na área de
ação do patógeno. Adicionalmente, o uso de fungicidas para o controle do mofo
branco aumenta demasiadamente os custos de produção, reduzindo assim o lucro
do agricultor. Desta forma, a alternativa economicamente viável para o controle é
o desenvolvimento de variedades resistentes ao patógeno.
Entretanto, a resistência genética ao hospedeiro é complexa e de baixa
herdabilidade e está restrita a genótipos que apresentam apenas resistência
parcial (Kim & Diers, 2000; Arahana et al., 2001; Guo et al., 2008; Vuong et al.,
2008). Por sua vez, a resistência parcial desses materiais pode ser devida tanto à
resistência fisiológica como a características da planta que propiciam condições
menos favoráveis ao desenvolvimento do patógeno (mecanismos de escape). Os
mecanismos de escape estão relacionados às características de acamamento,
arquitetura do dossel, altura da planta, período de floração e maturação relativa
(Kim & Diers, 2000). Trabalhos realizados visando a identificação de QTLs
(Quantitative Trait Loci) revelaram que alguns dos marcadores identificados
estavam associados com os mecanismos de escape da doença (Kim & Diers,
2000). A influência dos mecanismos de escape e do ambiente no desenvolvimento
do patógeno interfere diretamente no trabalho de avaliação a campo da resistência
fisiológica e dificulta o desenvolvimento de materiais resistentes ao mofo branco
(Arahana et al., 2001; Vuong et al., 2004).
Devido às dificuldades existentes no desenvolvimento de genótipos
resistentes ao mofo branco utilizando-se de avaliações a campo, a comunidade
científica tem buscado constantemente o uso de novos métodos ou técnicas
controladas que permitam a identificação de materiais resistentes (Chun et al.,
6
1987, Wegulo et al., 1998; Kim et al., 2000; Kull et al., 2003; Chen & Wang, 2005).
Os métodos mais comumente testados são: inoculação de cotilédones ou folhas
destacadas utilizando plugs de micélio, inoculação de pecíolos excisados e teste
de tolerância ao ácido oxálico. O conhecimento aprofundado desses novos
métodos de avaliação tem auxiliado no conhecimento do controle genético da
doença, no desenvolvimento de marcadores moleculares e na seleção de
materiais com maiores níveis de resistência ao fungo S. sclerotiorum. Contudo, até
o presente momento, não há registros de cultivares resistentes no mercado.
1.3 – O ácido oxálico e o seu papel durante o processo de infecção do fungo
S. sclerotiorum
Diversos trabalhos realizados ao longo do último século associaram a
produção do ácido oxálico (AO) com a patogenicidade de algumas das espécies
de Sclerotinia (Higgins, 1927; Bateman & Beer, 1965; Maxwell & Lumsden, 1970;
Kritzman et al., 1977; Noyes & Hancock, 1981; Marciano et al., 1983; Magro et al.,
1984; Stone & Armentrout, 1985; Godoy et al., 1990; Pierson & Rhodes, 1992;
Dutton & Evans, 1996). As principais evidências do envolvimento do AO no
processo de infecção do fungo Sclerotinia spp. são:
a) Presença de AO em tecidos infectados (Marciano et al., 1983; Godoy et al.,
1990; Ferrar & Walker, 1993).
b) Correlação positiva entre o nível de AO e a severidade da doença
(Bateman & Beer, 1965; Maxwell & Lumsden, 1970; Noyes & Hancock,
1981; Magro et al., 1984).
7
c) Desenvolvimento de sintomas semelhantes aos causados pelo patógeno
após a aplicação de AO ou filtrados de cultivo do fungo contendo AO
(Bateman & Beer, 1965; Noyes & Hancock, 1981; Marciano et al., 1983).
d) Plantas que apresentam tolerância ao AO são também mais tolerantes ao
fungo (Noyes & Hancock, 1981; Tu, 1985; Wegulo et al., 1998; Kolkman &
Kelly, 2000);
Além das evidências citadas acima, o envolvimento do AO no processo de
infecção do hospedeiro pode ser comprovado pelo trabalho de Godoy et al.
(1990). Eles verificaram que mutantes de S. sclerotiorum incapazes de sintetizar
AO foram não patogênicos ao feijoeiro (Phaseolus vulgaris), mesmo tendo
mantido todo o aparato de produção de enzimas que atuam na degradação da
parede celular.
O mecanismo de ação do AO durante o processo de infecção do
hospedeiro ainda não está completamente esclarecido. Contudo, diversas teorias
têm sido propostas e testadas com o intuito de elucidar o papel do AO na
interação patógeno hospedeiro e auxiliar no desenvolvimento de cultivares
resistentes ao fungo Sclerotinia spp. Adicionando as novas descobertas à revisão
apresentada por Bolton et al. (2006), o resumo dos principais mecanismos de
ação do AO pode ser descrito da seguinte maneira:
a) No início do processo de infecção, o AO acumula nos tecidos infectados e o
aumento da concentração ocorre com o avanço da colonização do
hospedeiro (Bateman & Beer, 1965). À medida que aumenta a
concentração de AO, o pH extracelular diminui para valores em torno de 48
5. A redução do pH extracelular a níveis abaixo de 5 aumenta a atividade
das enzimas que atuam na degradação da parede celular (CWDEs – CellWall Degrading Enzymes) (Bateman & Beer, 1965; Maxwell & Lumsden,
1970; Marciano et al., 1983; Magro et al., 1984). Durante a interação com o
hospedeiro, o fungo S. sclerotiorum secreta um conjunto de CWDEs
(pectinases,
β-1,3
glucanase,
glicosidases,
celulases,
xilanases
e
cutinases) com o intuito de facilitar a penetração e a colonização (Hancock,
1966; Lumsden, 1969; Riou et al., 1991).
b) O contínuo acumulo de AO conduz a redução do pH extracelular à valores
abaixo do nível ótimo de atividade das CWDEs. Contudo, a redução do pH
a níveis abaixo de 4 inibe a atividade das proteínas inibidoras de
poligalacturonases
(PGIPs
–
Polygalacturonase-Inhibiting
Protein)
produzidas pela planta (Favaron et al., 2004). As poligalacturonases (PG)
são importantes pectinases produzidas pelo fungo que atuam na
degradação da parede celular.
c) O AO pode afetar a regulação da transcrição de genes responsivos a
alteração do pH e necessários para a patogênese e desenvolvimento do
fungo S. sclerotiorum tais como pac1 (responsável pela ativação ou
repressão de genes em resposta ao pH extracelular) e smk1 (requerido
para o desenvolvimento dos escleródios) (Rollins & Dickman, 2001; Rollins,
2003; Chen et al., 2004).
d) O AO inibe a atividade da polifenoloxidase produzida pela planta, limitando
assim a produção dos compostos fenólicos que protegem a oxidação das
9
substâncias pécticas da parede celular (Marciano et al., 1983; Magro et al.,
1984).
e) O AO seqüestra os íons Ca2+ da parede celular, permitindo que as PG
hidrolisem os pectatos (composto oriundo da reação entre o ácido péctico
com Ca2+ e Mg2+ responsável pelo aumento da rigidez da lamela média e
das outras camadas da parede celular), alterando assim a integridade da
parede celular do hospedeiro (Bateman & Beer, 1965; Kurian & Stelzig,
1979). Além disso, as respostas de defesa da planta dependentes de íons
Ca2+ podem ser comprometidas (Bateman & Beer, 1965).
f) O AO promove a abertura dos estômatos induzindo a desidratação ou
murchamento foliar durante o processo de infecção do fungo S.
sclerotiorum. O AO manipula a função das células guarda induzindo a
abertura estomática por meio do acúmulo de solutos e pela inibição do
ácido abscísico (ABA) que promove o fechamento dos estômatos
(Guimarães & Stotz, 2004).
g) O AO atua como uma toxina móvel e a redução do pH decorrente do seu
acúmulo leva à perda de rigidez do tecido infectado (Noyes & Hancock,
1981).
h) Nas fases iniciais do processo de infecção, em pH relativamente elevado
(pH > 5), o AO induz a explosão oxidativa, resposta de defesa da planta
que dispara a morte celular programada (PCD – Programmed Cell Death)
que conduz à reação de hipersensibilidade (HR - Hypersensitive Response)
(Kim et al., 2008; Walz et al., 2008b). Esta resposta é fruto da produção de
espécies ativas de oxigênio (ROS – Reactive Oxygen Species), tais como
10
H2O2, O2-, e OH-. Apesar de ser um eficiente mecanismo de defesa da
planta
à
patógenos
biotróficos,
a
HR
favorece
o
processo
de
desenvolvimento de fungos necrotróficos, como S. sclerotiorum e Botrytis
cinerea, durante o processo de infecção e colonização do hospedeiro
(Govrin & Levine, 2000; Dickman et al. 2001; Thomma et al., 2001; Wang et
al., 2008). Com o acúmulo de AO, o pH é reduzido e a interação é
acompanhada pela supressão de ROS e da PCD, possibilitando maior
penetração do patógeno no tecido vegetal (Cessna et al., 2000; Kim et al.,
2008; Walz et al., 2008b).
1.4 – Expressão de genes de oxalato oxidases e oxalato descarboxilases no
desenvolvimento de plantas transgênicas resistentes ao fungo S.
sclerotiorum
As evidências do envolvimento do AO no processo de infecção e o maior
entendimento do seu papel na interação patógeno hospedeiro conduziu a
sociedade
científica
ao
estudo
de
novas
estratégias
que
auxiliem
no
desenvolvimento de cultivares resistentes ao fungo S. sclerotiorum. Dentre tais
estratégias, o uso da engenharia genética ganhou destaque e, na última década,
diversos trabalhos foram publicados apresentando resultados obtidos com plantas
transgênicas capazes de degradar o AO produzido pelo fungo (Kesarwani et
al.,2000; Donaldson et al., 2001; Cober et al., 2003; Hu et al., 2003; Livingstone et
al., 2005; Dias et al., 2006; Dong et al., 2008; Walz et al., 2008a; Walz et al.,
2008b). As duas principais alternativas utilizadas para o desenvolvimento de
11
plantas transgênicas capazes de degradar o AO consistem na introdução do gene
oxo, que codifica para a enzima oxalato oxidase (OXO) e do gene oxdc que
codifica para a enzima oxalato descarboxilase (OXDC).
A OXO converte o AO na presença de oxigênio (O2) em duas moléculas de
gás carbônico (CO2) e uma de peróxido de hidrogênio (H2O2). O H2O2 possui um
papel chave no sistema de defesa da planta, pois além de atuar como indutor de
genes de proteção celular e da reação de hipersensibilidade (Levine et al., 1994;
Tenhaken et al., 1995), participa do cruzamento oxidativo (cross-linking) de
proteínas da parede celular formando, com a matriz de polissacarídeos, um
grande polímero de várias glicoproteínas ricas em hidroxiprolina, reforçando
estruturalmente a parede celular (Resende et al., 2003). O H2O2 também atua
como importante substrato das peroxidases e, por conseguinte, dispara a química
de lignificação da parede celular tornando-a mais rígida e resistente à degradação
por enzimas secretadas pelos patógenos (Resende et al., 2003). Vale ressaltar
que a morte celular (HR) induzida pelo H2O2 atua como um mecanismo eficiente
de defesa da planta à patógenos biotróficos, mas favorece o processo de
desenvolvimento de fungos necrotróficos, como S. sclerotiorum (Govrin & Levine,
2000; Thomma et al., 2001; Wang et al., 2008).
Plantas transgênicas de tabaco e Arabidopsis thaliana incapazes de incitar
a HR mostraram maior resistência à S. sclerotiorum (Govrin & Levin, 2000;
Dickman et al. 2001). Além disso, o peróxido de hidrogênio presente em altas
concentrações na célula pode ser tóxico e causar a morte celular. Plantas
transgênicas de girassol que apresentaram altos níveis de expressão da enzima
12
OXO desenvolveram sintomas de clorose e necrose nas folhas e estes sintomas
foram associados à produção excessiva de H2O2 (Hu et al., 2003). Contudo, a
expressão de genes que codificam para a OXO tem sido utilizada com sucesso
em diferentes culturas (soja, girassol, canola, amendoim e tomate) visando o
desenvolvimento de materiais resistentes a Sclerotinia spp. (Donaldson et al.,
2001; Cober et al., 2003; Hu et al., 2003; Livingstone et al., 2005; Dong et al.,
2008; Walz et al., 2008a).
Em soja, plantas transgênicas expressando o gene de germe de trigo que
codifica para a OXO apresentaram redução do progresso da doença, quando
comparadas com o controle, em testes realizados utilizando os métodos de
inoculação de cotilédones e inoculação da haste com o fungo S. sclerotiorum
(Donaldson et al., 2001). Posteriormente, uma das linhagens obtidas por
Donaldson et al. (2001) foi avaliada em testes realizados a campo e os resultados
obtidos demonstraram que o material apresentava resistência parcial ao mofo
branco da soja, com índices de severidade inferior a testemunha irmã não
transgênica (Cober et al., 2003).
A OXDC cataboliza o AO produzindo ácido fórmico (ácido orgânico não
tóxico) e CO2. As vantagens atribuídas a OXDC referem-se à especificidade ao
AO, o não requerimento de cofatores e a alta atividade da enzima em pH ácido ou
neutro (3,0 a 7,0) (Mehta & Datta, 1991; Kesarwani et al., 2000). Como a OXDC é
ativa em pH baixo e a maioria dos oxalatos encontra-se em vacúolos de células
vegetais, é concebível que esta enzima possa ser direcionada a essa organela
para gerar plantas transgênicas livres de oxalato. Além disso, a ação da OXDC
13
não produz H2O2 adicional no sistema, podendo apresentar-se como alternativa à
OXO no desenvolvimento de plantas com maior nível de resistência a patógenos
necrotróficos.
Plantas transgênicas de tomate, fumo e alface transformadas com o gene
da OXDC apresentaram maior nível de resistência ao fungo S. sclerotiorum,
quando comparadas com o controle, em testes realizados utilizando folhas
destacadas (Kesarwani et al.,2000; Dias et al., 2006; Walz et al., 2008b). Dias et
al. (2006) e Walz et al. (2008b) mostraram que o nível de resistência ao fungo S.
sclerotiorum está correlacionado ao nível de transcritos e atividade da enzima
OXDC.
14
2 – OBJETIVOS
Considerando a importância do AO no processo de infecção, os resultados
obtidos com plantas transgênicas que expressam genes que degradam o AO e as
vantagens atribuídas a OXDC, o presente trabalho tem por objetivo principal a
introdução e expressão do gene oxdc em plantas de soja visando o
desenvolvimento de eventos transgênicos resistentes ao fungo S. sclerotiorum.
15
3 – MATERIAIS E MÉTODOS
3.1 – Isolamento do gene oxdc do fungo Flammulina velutipes
Os procedimentos realizados para o isolamento do gene oxdc do fungo
Flammulina velutipes foram previamente descritos por Dias et al. (2006) e serão
apresentados neste capítulo para melhor entendimento do trabalho.
Micélios do fungo F. velutipes (isolado: IJF 140502 – Embrapa Recursos
Genéticos e Biotecnologia) foram cultivados a 25 oC em meio de cultivo líquido
(Mehta & Datta, 1991) e, após 25 dias de cultivo, 12,5mM de ácido oxálico foram
acrescidos ao meio para indução da enzima oxalato descarboxilase (OXDC). A
extração do RNA total foi realizada depois de 12 horas de cultivo em meio
contendo ácido oxálico utilizando o kit Micro-to-Midi Total RNA Purification System
(Invitrogen) a partir de 250mg de tecido do fungo, segundo o protocolo sugerido
pelo fabricante.
A síntese do cDNA a partir do RNA total foi realizada utilizando a
®
transcriptase reversa SuperScript II
(Invitrogen), de acordo com o protocolo
descrito pelo fabricante.
A reação de RT–PCR foi processada em termociclador utilizando 50μL de
solução composta de 40ng de cDNA, 60mM de Tris–SO4 (pH 8.9), 18mM de
(NH4)2SO4, 2mM de MgSO4, 250nM de cada dNTP, 200nM de cada primer e 5U
da enzima taq DNA polymerase Platinum High Fidelity (Invitrogen). A mistura foi
submetida à reação de desnaturação inicial (94 oC por 2min) e a 35 ciclos de
16
amplificação (94 ºC por 30s, 55 ºC por 30s, 68 ºC por 2min) seguidos de um ciclo
de
elongação
final
de
10min
5´TCTAGATGTTCAACAACTTCCAACG3´
e
a
68
ºC.
Os
primers
5´GGATCCTCAGTTCACAGGACCAAC3´
foram utilizados para amplificar uma seqüência de 1.344pb que corresponde à
seqüência codificante do gene oxdc.
3.2 – Clonagem do gene oxdc
A região codificante do gene oxdc foi clonada no vetor pCR2.1 TOPO
(Invitrogen) gerando o vetor pTOPOOXDC e, logo em seguida, seqüenciada em
seqüenciador automático utilizando os primers universais M13 e T7.
Para a construção do vetor de expressão pOXDC, a seqüência codificante
do gene oxdc (1.344pb) foi clonada no vetor pUC19-35SdAMVNOS entre os sítios
de BamHI e XbaI sob o controle de duas cópias em tandem do promotor 35S RNA
do vírus do mosaico da couve-flor (CaMV35S) e uma seqüência enhancer do vírus
do mosaico da alfafa (AMV) (Figura 2).
O cassete de expressão (2.310pb) foi então removido do vetor pOXDC com
as enzimas EcoR1 e HindIII e clonado no vetor pBluKSP (Fermentas), dando
origem ao vetor pBluKSPOXDC (5.256pb) (Figura 2).
Por fim, o cassete de expressão contendo o gene mutante ahas, isolado de
Arabidopsis thaliana e que confere resistência ao herbicida imazapir (herbicida do
grupo das imidazolinonas) foi retirado do vetor pAC321 (Rech et al., 2008) com a
enzima XbaI e inserida no sítio de SpeI do vetor pBluKSPOXDC dando origem ao
vetor pBluKSPOXDCAHAS (10.968pb) (Figura 2).
17
ApaLI (178)
ApaLI (3282)
EcoRI (397)
NOS -T
BamHI (684)
AP r
XbaI (690)
AM V Tra ns la tiona l E nhance r
pUC19-35SdAMVNOS
1 - Clonagem do gene
oxdc no sítio de BamHI
e XbaI
Tras cript Sta rt S ite
3601 bp
Tande m 35 s Promote r
PstI (1355)
ApaLI (2036)
HindIII (1363)
A paLI ( 17 8)
A paLI ( 4626)
E coR I ( 3 97 )
AP r
NOS-T
B amH I ( 684)
2 - Clonagem do cassete
35SdAMV-OXDC-NOS no
sítio de EcoRI e HindIII
pO X D C
4945 bp
oxdc
A paLI ( 3 3 80)
PstI ( 1681)
X b aI ( 203 4)
AMV Translational Enhancer
H indI I I ( 27 07 )
Trascript Start Site
PstI ( 2699)
Tandem 35s Promoter
ApaLI (5012)
SpeI (684)
BamHI (690)
AP r
PstI (706)
EcoRI (708)
NOS-T
BamHI (995)
pBluKSPOXDC
5256 bp
ApaLI (3766)
3 - Clonagem do gene
ahas no sítio de SpeI
ox dc
HindIII (3018)
PstI (3010)
Tande m 35 s P romoter
PstI (1992)
AM V Tra ns lational Enha nce r
Tras cript S tart Site
ApaLI (10724)
FspI (10279)
FspI (483)
XbaI (678)
AP r
SpeI (775)
ApaLI (9478)
SpeI (1055)
BamHI (2147)
Tande m 35 s P romote r
Tras cript S tart Site
pBluKSPOXDCAHAS
AM V Tra ns lational Enhance r
10968 bp
XbaI (8057)
BamHI (2940)
EcoRI (2981)
ox dc
FspI (6983)
ahas
BamHI (6707)
NcoI (3915)
NOS-T
EcoRI (6420)
BamHI (6402)
EcoRI (5091)
Figura 2. Estratégia para a construção do vetor pBluKSPOXDCAHAS (10.968pb).
O gene oxdc foi isolado do fungo Flamulina velutipes e o gene mutante
ahas do vetor pAC321.
18
3.3 – Transformação genética de soja com o vetor pBluKSPOXDCAHAS
O vetor pBluKSPOXDCAHAS foi utilizado para transformar via biobalística
células meristemáticas de 1152 embriões zigóticos extraídos de sementes
esterilizadas da variedade BR-16.
A esterilização das sementes, a extração e posicionamento dos embriões
zigóticos, a preparação de partículas, o bombardeamento com o vetor
pBlukSPOXDCAHAS, a indução de multibrotação e a regeneração em meio
seletivo (MS + sacarose 3% + imazapir 500nM + agar 0,6%) dos brotos
transgênicos foi realizada conforme o protocolo descrito por Aragão et al. (2000) e
Rech et al. (2008).
3.4 – PCR (Polymerase Chain Reaction) para a detecção do gene oxdc
A análise molecular visando a detecção do gene oxdc foi realizada
utilizando o DNA extraído de discos foliares, segundo metodologia de Doyle &
Doyle (1987).
Para cada amostra analisada, 2μL de DNA (≈20ng) foram adicionados à
solução contendo 17,6μL de H2O; 2,5μL de tampão 10X; 0,8μL de dNTP (4μM);
0,6μL de MgCl2 (50μM); 0,5μL de cada primer (10μM); e 0,5μL de Taq polimerase
(10U/μL). Os primers OXDC371 (5´CTCGGCAGCAGAATGAGGTC3´) e OXDC873
(5´TCGGCTCGACAGAGGAGAAG3´) utilizados na reação amplificam
seqüência de 522pb contida na região codificante do gene oxdc.
19
uma
As condições de tempo e temperatura da PCR para a detecção do gene
oxdc encontram-se na Tabela 1.
Os produtos da PCR foram submetidos à eletroforese em gel de agarose
1% usando tampão TBE 0,5X e voltagem ajustada para 5 V/cm.
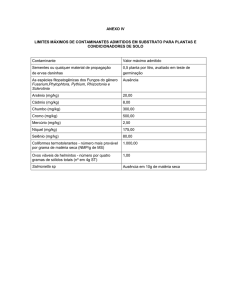
Tabela 1. Condições de tempo e temperatura da PCR utilizada para a detecção do
gene oxdc.
Etapas
1 - Desnaturação inicial
2 – Desnaturação
3 - Anelamento dos primers
4 - Alongamento das fitas de DNA
5 - Amplificação (Repetir 35 vezes as etapas 2, 3 e 4)
6 - Extensão final
Temperatura
95ºC
95ºC
57°C
72°C
Tempo
5min
1min
1min
2min
72°C
5min
3.5 – Plantio da geração T0
As plantas regenerantes em meio seletivo e positivas segundo as análises
moleculares (PCR) foram aclimatadas em vasos contendo solo fértil e alocadas
em casa de vegetação. As sementes de cada planta da geração T 0 foram
coletadas, identificadas e armazenadas em sacos de papel para o posterior plantio
da geração T1. Cada planta T0 foi considerada um evento distinto.
3.6 – Plantio da geração T1
As sementes obtidas de cada evento T 0 foram plantadas em copos
plásticos de 350ml contendo solo fértil. Discos foliares das plantas em estágio
vegetativo VC (Fehr et al., 1971) foram coletados para a extração de DNA e
20
posterior análise via PCR. A análise para a detecção do gene oxdc foi realizada
conforme descrito no item 3.4.
As plantas positivas segundo a análise molecular (PCR) foram transferidas
para vasos contendo solo fértil. Os vasos foram alocados em casa de vegetação.
As sementes de cada planta da geração T 1 foram coletadas separadamente
e identificadas para o plantio da geração T2. Cada planta foi considerada um
evento distinto.
3.7 – Plantio da geração T2
Vinte e quatro sementes de 16 eventos T1 (OXDC.1.01; OXDC.1.02;
OXDC.2.03; OXDC.2.04; OXDC.3.05; OXDC.3.06; OXDC.4.07 OXDC.4.08;;
OXDC.5.09; OXDC.5.10; OXDC.6.11; OXDC.6.12; OXDC.7.16; OXDC.7.17;
OXDC.8.18 e OXDC.9.21) foram plantadas em copos plásticos de 350ml contendo
solo fértil.
Discos foliares das plantas em estágio vegetativo VC (Fehr et al., 1971)
foram coletados para a extração de DNA e posterior análise via PCR. A análise
para a detecção do gene oxdc foi realizada conforme descrito no item 3.4.
Quinze plantas positivas, segundo a análise de PCR, de cada evento foram
transferidas para vasos contendo solo fértil. Os vasos foram alocados em casa de
vegetação com fotoperíodo de 14 horas, umidade relativa maior que 80% e
intensidade luminosa de 350μmol.m-2.s-1.
O teste para verificar a reação das plantas T2 ao fungo S. sclerotiorum foi
realizado conforme descrito no item 3.8.
21
3.8 – Inoculação das folhas destacadas utilizando plugs de micélio do fungo
S. sclerotiorum
3.8.1 – Produção do inóculo
Escleródio oriundo de um campo de soja infectado com mofo branco foi
cultivado em placa de Petry com meio BDA (Batata Dextrose Agar). Visando o
desenvolvimento de micélios, a placa contendo os escleródios foi mantida em
temperatura ambiente sob a bancada do laboratório.
Para a produção do inóculo utilizado no teste das folhas destacadas, um
disco de micélio de 5mm de diâmetro foi retirado da borda do halo formado pelo
crescimento do fungo e colocado no centro de uma nova placa contendo meio
BDA. Ao todo 20 placas foram produzidas para realizar o teste. As placas foram
transferidas para sala de cultivo com temperatura ambiente de 20 oC e retiradas
após 48 horas para a realização do teste das folhas destacadas.
3.8.2 – Teste das folhas destacadas
O experimento foi realizado utilizando trifólios retirados de plantas sadias T 2
e que apresentavam o mesmo estágio de desenvolvimento (V3). A Tabela 2
resume o número de plantas amostradas de cada evento. O terceiro trifólio de
cada planta foi retirado junto à haste principal e imediatamente depositado em
uma vasilha com água para o transporte até o laboratório.
22
Tabela 2. Número de plantas (trifólios) amostradas de cada evento oxdc na
geração T2 para o teste de inoculação da folha destacada com o fungo
S. sclerotiorum. Cada trifólio foi considerado uma repetição.
Evento
OXDC.1.01
OXDC.1.02
OXDC.2.03
OXDC.2.04
OXDC.3.05
OXDC.3.06
OXDC.4.07
OXDC.4.08
OXDC.5.09
OXDC.5.10
OXDC.6.11
OXDC.6.12
OXDC.7.16
OXDC.7.17
OXDC.8.18
OXDC.9.21
BR-16 (Controle)
Número de Plantas
10
9
10
6
10
10
10
10
10
4
10
10
8
6
9
10
10
No laboratório, as amostras foliares foram posicionadas em placa de Petri
sob 3 folhas umedecidas de papel de filtro. Discos de micélio de 5mm de diâmetro
foram retirados das margens do halo formado pelo crescimento do fungo S.
sclerotiorum em meio BDA e posicionados na superfície adaxial da folha ao lado
da nervura central. Somente a folha do meio de cada trifólio foi inoculada com o
plug de micélio. As placas contendo os trifólios inoculados foram transferidas para
sala de cultivo e mantidas no escuro com temperatura ambiente de 20 oC.
As folhas inoculadas foram fotografadas após 42, 66 e 90 horas de cultivo.
As imagens foram usadas para medir a área afetada em cada estágio com o
auxilio do programa v1.0.1 QUANT (Vale et al., 2003).
23
3.9 – Análise genético-estatística para avaliar a reação das plantas ao fungo
Sclerotinia sclerotiorum
Para a avaliação da reação das plantas ao fungo S. sclerotiorum, foi
utilizado o delineamento inteiramente casualizado conforme o seguinte modelo
estatístico:
Yij
m ti
eij
em que:
Yij :
valor observado na unidade experimental de repetição j que recebeu
o tratamento i, sendo j = 1, 2, ..., ji e i = 1, 2, ...,17;
m:
média geral do experimento;
ti :
efeito do tratamento i, sendo i = 1, 2, ...,17;
eij :
erro experimental associado à observação Yij, assumindo que os
erros são independentes e normalmente distribuídos, com média
zero e variância homogênea
2
e
.
A severidade da doença nos eventos oxdc e no controle (BR-16) foi
determinada por meio do cálculo da área abaixo da curva de progresso da doença
(AUDPC - Area Under the Disease Progress Curve), obtida a partir da estimativa
da média das AUDPC em cada repetição de acordo com a fórmula abaixo,
proposta por Shaner e Finney (1977):
n
AUDPC
[( xi
xi 1 ) / 2](t i
ti 1 )
i 1
em que:
n:
número de avaliações no tempo;
24
xi :
é a severidade da doença medida pelo programa QUANT V.1.0.1
(Vale et al., 2003) no tempo i, sendo i = 42, 66 e 90;
ti :
é o tempo em que foi realizada a avaliação i, sendo i = 42, 66 e 90.
Os dados obtidos a partir do cálculo da AUDPC de cada repetição foram
analisados utilizando o teste não paramétrico de Kruskal-Wallis (Kruskal & Wallis,
1952).
3.10 – Southern blot
O DNA genômico utilizado para a análise de Southern foi isolado de acordo
com Dellaporta et al. (1983). As análises de Southern foram realizadas como
descrito por Sambrook et al. (1989). O DNA genômico (15μg), digerido com EcoRI,
foi separado em gel de agarose 1%, transferido para uma membrana de nylon
(Hybond) e hibridizado com a sonda marcada com α[ 32P]-dCTP (3000 Ci mol-1)
usando o kit Random Primer DNA Labelling (Pharmacia Biotech), de acordo com
as instruções do fabricante. A sonda foi obtida a partir do isolamento e purificação
do fragmento de 1.350pb oriundo da digestão do vetor pBluKSPOXDCAHAS com
BamHI e XbaI. A sonda corresponde à seqüência codificante do gene oxdc. O
fragmento de 1.350pb foi isolado de um gel de agarose 1% e purificado utilizando
o kit Wizard SV Gel Clean-Up System (Promega).
3.11 – RT-PCR
25
A RT-PCR foi realizada utilizando o RNA total extraído de folhas do controle
BR-16 (repetição 1) e das plantas transgênicas OXDC.6.11.7 (repetição 7 do
evento OXDC.6.11) e OXDC.9.21.2 (repetição 2 do evento OXDC.9.21). O RNA
total foi extraído das folhas usando o kit Micro-to-Midi Total RNA Purification
System (Invitrogen). O DNA genômico remanescente nas amostras foi eliminado
com o uso de DNase. A síntese do cDNA a partir do RNA total foi realizada
®
utilizando a transcriptase reversa SuperScript II (Invitrogen), de acordo com o
protocolo descrito pelo fabricante. As reações de PCR foram realizadas como
descrito no item 3.4 com ≈25ng de cDNA. Os primers OXDC371 e OXDC873
foram utilizados para amplificar a seqüência de 522pb contida na região
codificante do gene oxdc. Como controle interno, os primers rRNA1 (5'AACGGCTACCACATCCAAGG-3') e rRNA2C (5'-TCATTACTCCGATCCCGAAG3') foram utilizados para amplificar uma seqüência do gene 18S rRNA. A
intensidade relativa das bandas foi determinada utilizando o escâner do gel de
PCR para análise da intensidade de banda com o programa Quantity One® v4.6.3.
A quantificação relativa foi feita comparando as intensidades das bandas do oxdc
e 18S rRNA.
26
4 – RESULTADOS E DISCUSSÃO
4.1 – Isolamento do gene oxdc do fungo Flammulina velutipes
O gene oxdc de 1.344pb que codifica para a enzima oxalato descarboxilase
apresentou 99,26% de identidade quando comparado com outra seqüência do
gene, previamente listada no GenBanK (acesso: AF2000683), também isolada do
fungo F. velutipes. As diferenças encontradas ocorreram em apenas 10 bases,
contudo a seqüência de aminoácidos não foi alterada. A seqüência de 1.344pb
(Figura 3) foi depositada no GenBank com o número de acesso AY238332.
1
61
121
181
241
301
361
421
481
541
601
661
721
781
841
901
961
1021
1081
1141
1201
1261
1321
atgttcaaca
gtgcctttgg
gagcccagcg
accagtgacc
ccggataatc
catggctttg
ggtggctggg
acaaatatgc
tgggcatatg
tatatttcca
ctccaagcga
gccttcaatg
gttatcctga
cagctataca
caggggacgg
tccggtggga
gtggccgagg
gacgagtgga
gtagcctcta
cattatgtag
cgttttgctg
gcgcacctga
actgttgttg
acttccaacg
cgtccaccac
cgactgtacc
cagcgcttgt
tgcctataga
tcggtaatgc
ctcggcagca
gtcttgaagc
ttctgaaggg
ccgtcggccc
cagctgatga
acgacggtac
agaacttcag
tcttccctag
ttccccttcc
cagcgaagat
ttacagttga
cattcttcat
cgtttgatta
agaacattgg
atgtcagtct
acttggacga
gtcctgtgaa
tctgctcact
gacgggaact
ctttgccagc
aaagccagag
ccttcagaat
gaagtggcca
gaatgaggtc
aggcgctatc
gtctacccaa
cggtgatttg
tccagaaggc
attcttgctc
agccaagaac
tgaacctcct
atattcattc
tgcagattcc
gcctggtgct
ctctggaaac
ccaaggtggt
aaacacgact
aagtcagtgg
cgagacactt
ctga
gtcatccttc
ggaactgcga
actgatccca
aggaaccagc
ccggacttgc
ttcagcttca
gttttgcctc
agggagttgc
atctcagctg
tggtatttcc
tcagagttca
actgactggc
cccgccgcat
gcggacaacc
aacttctcct
acgacgttca
ttgagagagc
gcgagggtga
gatatcgctt
ttgacttatc
ctggcgttaa
gcggagctca
tctccggttt
ccggtacctc
accccgtgct
ttggtgcgac
tcgccccacc
gcaagcagcg
tcgcgactaa
attggcacaa
tcgataacga
caccaggcat
tcttggtgtt
tttcgcatgt
ggtctcacat
agccggaccc
ctgtcgagcc
acatttccgt
tgcactggca
caattttcgc
atgttcctgc
tggaggtctt
cacctccgag
agcagtttgc
taccgctgga
aaccgccgca
ctggaatgag
aatccaagga
gactactgat
actgcagacg
tctcgcttgc
gaacgctgag
agggcgcaat
tcctcactcg
tgattcaggc
tccaatggaa
acctgctcaa
cgttagccca
gacgcagtat
cgctatcgcc
tccgactgag
tgcgcagagt
atctatgggc
caataccgac
tgtcgtgcag
gaccaaggcg
Figura 3. Seqüência do gene oxdc de 1.344pb isolado do fungo Flammulina
velutipes (isolado: IJF 140502, Embrapa Recursos Genéticos e
Biotecnologia)
27
4.2 – Clonagem do gene oxdc
O
processo
de
clonagem
do
gene
oxdc
deu
origem
ao
vetor
pBluKSPOXDCAHAS (10.968pb). A Figura 4 apresenta a digestão do vetor
pBluKSPOXDCAHAS com a enzima FspI realizada para confirmar a inserção do
cassete de expressão do gene ahas.
Figura 4. Digestão do vetor pBluKSPOXDCAHAS com a enzima FspI (2).
Marcador 1-kb ladder-Invitrogen (1).
Como o fungo S. sclerotiorum é capaz de afetar todas as partes da planta
de soja, o gene oxdc foi clonado sob o controle de duas seqüências em tandem do
promotor constitutivo CaMV35S. Este promotor tem sido utilizado com sucesso no
controle da expressão de transgenes em diferentes órgãos de várias espécies de
plantas, incluindo a soja. Kay et al. (1987) demonstraram que a duplicação em
28
tandem das seqüências do CaMV35S aumenta a atividade transcricional em
aproximadamente 10 vezes quando comparada com o promotor natural.
O
cassete
de
expressão
do
gene
oxdc
presente
no
vetor
pBluKSPOXDCAHAS foi destinado previamente para a construção do vetor
pCambOxDc e utilizado para transformar, via Agrobacterium, a alface visando o
desenvolvimento de plantas transgênicas resistentes ao mofo branco (Dias et al.,
2006). Os resultados obtidos revelaram que o gene oxdc sob o controle da
seqüência em tandem do CaMV35S e do enhancer AMV é capaz de prover
aumento da resistência ao fungo S. sclerotiorum. Adicionalmente, o promotor
CaMV35S foi utilizado com sucesso no controle da expressão do gene oxdc em
plantas transgênicas de fumo e tomate resistentes a S. sclerotiorum (Kesarwani et
al.,2000; Walz et al., 2008b).
4.3 – Transformação genética de soja com o vetor pBlukSPOXDCAHAS,
análise da PCR para a detecção do gene oxdc e obtenção da geração T2
O vetor pBluKSPOXDCAHAS foi utilizado para transformar via biobalística
células meristemáticas de 1.152 embriões zigóticos. Após o período de indução de
multibrotação, os embriões bombardeados foram transferidos para o meio seletivo
contendo imazapir (500nM). Quarenta e oito (48) plantas regenerantes em meio
seletivo foram analisadas via PCR. A análise da PCR detectou a presença do
gene oxdc em 10 plantas (Figura 5). Cada planta oxdc positiva, segundo a análise
molecular (PCR), foi considera um evento T 0 distinto (OXDC.1; OXDC.2; OXDC.3;
OXDC.4; OXDC.5; OXDC.6; OXDC.7; OXDC.8; OXDC.9 e OXDC.10). A eficiência
29
de transformação, considerando o número final de plantas transgênicas e o
número total de embriões bombardeados foi de 0,87%.
Figura
5.
PCR das plantas de soja transformadas com o vetor
pBlukSPOXDCAHAS. Os números de 1 a 10 indicam
respectivamente os eventos OXDC.1; OXDC.2; OXDC.3; OXDC.4;
OXDC.5; OXDC.6; OXDC.7; OXDC.8; OXDC.9 e OXDC.10). Os
números
11
e
12
indicam
respectivamente
o
vetor
pBluKSPOXDCAHAS e a cultivar BR-16 não transgênica. O
marcador utilizado foi o 1-kb ladder-Sigma. As bandas possuem
522pb.
As 10 plantas positivas, segundo a análise da PCR, foram aclimatadas na
casa de vegetação visando à obtenção da geração T 1. O estresse causado pela
cultura de tecidos associado às baixas temperaturas durante o período de
aclimatação acarretou no florescimento precoce das plantas T 0 e impediu o
desenvolvimento normal das plantas. Decorrente do desenvolvimento anormal das
plantas, o número de sementes obtidas de cada evento na geração T0 foi
extremamente baixo (Tabela 3). Este fato impediu que fosse realizada a análise de
segregação do transgene na geração T1.
As sementes obtidas de cada evento T 0 foram plantadas em casa de
vegetação e as plantas T1 foram analisadas via PCR para detectar a presença do
gene oxdc. Os transgênicos apresentaram fenologia (altura da planta, local de
inserção da primeira vagem, número de ramos, comprimento de internós, área
30
foliar e número total de flores e vagens) semelhante às plantas nãotransformadas. Cada planta T1 foi considerada um evento distinto.
Tabela 3. Número total de sementes obtidas de cada evento na geração T 0.
Evento T0
OXDC.1
OXDC.2
OXDC.3
OXDC.4
OXDC.5
OXDC.6
OXDC.7
OXDC.8
OXDC.9
OXDC.10
Número de sementes obtidas na geração T0
6
8
5
8
2
23
5
1
1
6
4.4 – Inoculação de folhas destacadas das plantas T2 utilizando discos de
micélio do fungo S. sclerotiorum
Vinte e quatro sementes de 16 eventos T 1 (OXDC.1.01; OXDC.1.02;
OXDC.2.03; OXDC.2.04; OXDC.3.05; OXDC.3.06; OXDC.4.07 OXDC.4.08;;
OXDC.5.09; OXDC.5.10; OXDC.6.11; OXDC.6.12; OXDC.7.16; OXDC.7.17;
OXDC.8.18 e OXDC.9.21) foram plantadas na casa de vegetação e as plantas T2
foram analisadas via PCR para a detecção do gene oxdc. Cerca de 10 plantas
PCR positivas de cada evento T2 e 10 plantas não transgênicas da variedade BR16, que apresentaram desenvolvimento similar, foram selecionadas para realizar o
teste da folha destacada inoculada com o fungo S. sclerotiorum (Tabela 2).
A análise da curva de progresso da doença revela que todos os eventos
transgênicos apresentaram atraso no desenvolvimento dos sintomas quando
comparados com o controle não transgênico (Figura 6). Após 42 horas da
31
inoculação, os primeiros sintomas eram facilmente observados no controle (áreas
lesionadas variando de 0.84 a 2.69 cm 2). No mesmo estágio, os eventos
transgênicos, em sua grande maioria, apresentavam pequenos sintomas
localizados apenas ao redor do disco de micélio. A área lesionada do controle,
após 42 horas, foi, aproximadamente, 2 vezes maior que o pior evento transgênico
(OXDC.1.02) e 7 vezes maior que o melhor evento (OXDC.9.21) nesse mesmo
estágio. A média da área lesionada de todos os eventos transgênicos foi de 0,41
cm2, enquanto que o valor obtido para o controle foi de 1,49 cm 2. Considerando
que, para o cálculo da área lesionada, a área do disco de micélio (≈0.2 cm 2) fora
apreciada, mesmo que o fungo não tenha penetrado no tecido, a média obtida
para os eventos transgênicos está superestimada, pois parte dos eventos não
apresentavam sintomas visíveis ao redor do halo formado pelo plug. Desta forma,
a diferença real entre os transgênicos e o controle neste primeiro estágio de
avaliação é ainda maior.
Após 66 horas, com a evolução dos sintomas em alguns eventos
transgênicos, observou-se que o crescimento do patógeno ocorre, principalmente,
através das nervuras das folhas. Nesse estágio, a área infectada do controle foi
2,8 vezes maior que o pior evento transgênico (OXDC.1.02) e 23,4 vezes maior
que o melhor evento (OXDC.9.21). A média da área lesionada de todos os
eventos transgênicos foi de 1,41 cm2, enquanto que o valor obtido para o controle
foi de 6,48 cm2. Vale ressaltar que a média da área lesionada de todos os eventos
transgênicos após 66 horas do início do teste foi menor que a obtida no controle
após 42 horas.
32
Figura 6. Curva de progresso da doença obtida a partir da inoculação de folhas
destacadas com discos de micélio do fungo S. sclerotiorum. A área
infectada medida em cada tempo (42, 66 e 90 horas) é a média de 10
repetições, exceto para os eventos OXDC.1.02, OXDC.2.04,
OXDC.5.10, OXDC.7.16, OXDC.7.17 e OXDC.8.18 que tiveram 9, 6, 4,
8, 6 e 9 repetições, respectivamente. As barras indicam o desvio padrão
das médias.
No último estágio, considerado para a avaliação da curva de progresso da
doença, as lesões observadas nas folhas das plantas controles atingiram as
bordas e estenderam-se por quase a totalidade da folha (Figura 1A). Nesse
estágio, a magnitude do valor obtido para a média da área lesionada do controle
(17,60 cm2) foi 5 vezes maior que a média da área lesionada de todos os eventos
transgênicos (3,5 cm2). A média da área infectada obtida 90 horas após a
inoculação, variou de 0,45 cm2 (OXDC.9.21) a 7,19 cm2 (OXDC.2.03) nos eventos
transgênicos. Detalhes das lesões observadas em cada evento transgênico após
90 horas do início do teste podem ser observados nas Figuras 2A a 17A. Nesse
estágio, as áreas anotadas para o evento OXDC.9.21 variaram de 0,2 a 0,84 cm2.
33
Vale ressaltar que toda a área anotada inclui o valor da área do disco de micélio
(≈0.2 cm2), mesmo que não tenha sido observado sintoma oriundo da penetração
do fungo na folha. Após 90 horas, nas repetições 2 e 7 do evento OXDC.9.21 o
crescimento do fungo S. sclerotiorum ocorreu apenas sob a superfície das folhas
não sendo visualizada penetração dos micélios, mesmo quando analisadas com o
auxílio da lupa (Figuras 8 e 17A).
A análise para determinar a curva de progresso da doença foi encerrada
após 90 horas da inoculação das folhas destacadas, pois nesse estágio as lesões
observadas no controle haviam atingido as extremidades do tecido. Contudo,
como o fato verificado no controle não fora observado nos eventos transgênicos,
uma nova avaliação foi realizada após 24 horas da última avaliação, ou seja, 114
horas após o início do teste. Nesse momento, observou-se que a média da área
lesionada do evento OXDC.9.21 foi de 0,54 cm 2, valor 2,75 vezes menor que o
observado no controle no primeiro estágio de avaliação (42 horas). As Figuras 18A
e 19A mostram respectivamente as fotos do controle e do evento OXDC.9.21 após
114 horas do início do teste.
A área abaixo da curva de progresso da doença (AUDPC) foi utilizada para
sumarizar a severidade da doença em cada evento transgênico e no controle. O
teste de Kruskal-Wallis revelou que houve diferença significativa (P ≤ 0,05) entre
os tratamentos (Figura 7). O único evento que não diferiu significativamente ao
nível de 5% de probabilidade da cultivar BR-16 foi o OXDC.2.03. Contudo, vale
ressaltar que este difere do controle se considerar o valor de P ≤ 0,10. Outro ponto
importante a ser considerado na comparação entre o evento OXDC.2.03 e o
controle refere-se ao fato de que a diferença estatística obtida a partir do teste de
34
Kruskal-Wallis é uma função dos postos das observações na amostra combinada
e não das médias propriamente ditas. Adicionalmente, a severidade do evento
OXDC.2.03 foi 61% menor que a severidade obtida no controle. A severidade
média de todos os eventos transgênicos foi 79% inferior a determinada para o
controle. Os eventos OXDC.9.21 e OXDC.8.18 tiveram os menores índices de
severidade. Tais eventos apresentaram, respectivamente, índices de severidade
96% e 93% menor que o apurado para o controle.
Figura 7. Severidade da doença dos eventos oxdc e do controle não transgênico
(BR-16) medida pelo cálculo da área abaixo da curva de progresso da
doença (AUDPC). Letras iguais presentes acima das barras de média
indicam que os eventos não diferem significativamente ao nível de 5%
de probabilidade de acordo com o teste de Kruskal-Wallis.
Os resultados impetrados a partir da curva de progresso da doença e da
severidade da doença utilizando o teste de inoculação da folha destacada com o
fungo S. sclerotiorum sugerem que a expressão do gene da oxdc em soja confere
35
aumento do nível de resistência das plantas ao patógeno. Resultados similares
foram previamente relatados em plantas de tabaco, tomate e alface transformadas
para expressar o gene que codifica para a OXDC (Kesarwani et al., 2000; Dias et
al., 2006; Walz et al., 2008b). Paralelamente, e seguindo estratégia similar, a
expressão da enzima OXO em plantas transgênicas de soja, girassol, canola,
amendoim e tomate também culminou no aumento do nível de resistência a
Sclerotinia (Donaldson et al., 2001; Cober et al., 2003; Hu et al., 2003; Livingstone
et al., 2005; Dong et al., 2008; Walz et al., 2008a).
Com o objetivo de verificar a correlação entre a resistência da planta ao
fungo S. sclerotiorum e o nível de transcritos do gene oxdc, foi realizada a análise
de RT-PCR utilizando folhas extraídas do controle (repetição 1) e das plantas
transgênicas OXDC.6.11.7 (repetição 7 do evento OXDC.6.11) e OXDC.9.21.2
(repetição 2 do evento OXDC.9.21). A planta OXDC.6.11.7 apresentou resistência
parcial a S. sclerotiorum enquanto que a OXDC.9.21.2 exibiu o maior nível de
resistência a S. sclerotiorum (Figura 8). A análise de RT-PCR revelou a presença
de transcritos do gene oxdc apenas nas plantas transgênicas OXDC.9.21.2 e
OXDC.6.11.7 (Figura 9). Por sua vez, a planta OXDC.9.21.2, que apresentou alto
nível de resistência a S. sclerotiorum, obteve nível de transcritos 2,75 vezes maior
que a planta OXDC.6.11.7, que acusou moderada resistência ao fungo (Figura
9). Estes resultados sugerem que a expressão do gene oxdc está associada à
resistência ao fungo, e que o nível de resistência é dependente do nível de
expressão do transgene. A associação entre a presença do gene e a resistência é
também apoiada pelo fato de que todos os eventos transgênicos apresentaram
algum nível de resistência ao patógeno quando comparados com o controle.
36
Figura 8. Resposta a S. sclerotiorum obtida pela inoculação de folhas destacadas
com discos de micélio. Detalhe do trifólio da planta OXDC.9.21.2 após
42 (a), 66 (b) e 90 (c) horas. Detalhe do trifólio da planta OXDC.6.11.7
após 42 (d), 66 (e) e 90 (f) horas. Detalhe do trifólio da repetição 1 do
controle BR-16 após 42 (g), 66 (h) e 90 (i) horas. Detalhe do
crescimento do micélio na folha da planta OXDC.9.21.2 após 90 (j) e
114 (k) horas e no controle BR-16 após 90 (l) horas.
Os resultados obtidos pela análise de RT-PCR corroboram com estudos
realizados previamente que correlacionaram o nível de resistência ao fungo S.
37
sclerotiorum ao nível de transcritos do gene oxdc e da atividade da enzima OXDC
(Dias et al., 2006; Walz et al., 2008b). Kesarwani et al. (2000) observaram que o
nível de expressão da enzima OXDC, em plantas transgênicas de fumo, foi cinco
vezes maior quando direcionada para o vacúolo em comparação com o citosol.
Sendo assim, o uso de construções utilizando peptídeos sinais que direcionam a
expressão do gene oxdc para o vacúolo da planta apresenta-se como estratégia
potencial para o desenvolvimento de cultivares resistentes ao mofo branco.
Figura 9. (A) RT-PCR para a detecção da expressão do trasngene oxdc e do gene
endógeno 18S rRNA nas plantas transgênicas OXDC.6.11.7 e
OXDC.9.21.2 e no controle (BR-16). (B) Quantificação da expressão do
gene oxdc relativa à do 18S rRNA.
O evento OXDC.9.21, que apresentou a menor severidade nos testes
realizados utilizando o método da folha destacada, foi selecionado para a
38
caracterização adicional por Southern blot. Os resultados revelaram que todas as
plantas analisadas do evento OXDC.9.21 possuem duas cópias do gene oxdc e o
mesmo padrão de integração (Figura 10). Este fato suplanta, pelo menos para
este evento, a decisão de considerarmos cada planta testada como uma
repetição.
Figura 10 Análise da presença do transgene oxdc nas plantas transgênicas do
evento OXDC.9.21 (1 a 8). Planta controle BR-16 (9).
Os resultados obtidos no presente estudo suportam a hipótese que o AO
produzido pelo fungo exerce função estratégica durante o processo de infecção do
hospedeiro e que a introdução de genes capazes de produzir enzimas que
degradam este ácido é aplicável ao desenvolvimento de linhagens de soja
resistentes a S. sclerotiorum. Previamente, Donaldson et al. (2001) verificaram
que plantas de soja transformadas com o gene oxo apresentaram redução do
progresso da doença, quando comparadas com o controle, em testes realizados
utilizando os métodos de inoculação de cotilédones e inoculação da haste com o
fungo S. sclerotiorum (Donaldson et al., 2001). Uma das linhagens obtidas por
39
Donaldson et al. (2001) avaliada em testes a campo apresentou resistência parcial
ao mofo branco da soja com índices de severidade inferior a testemunha irmã não
transgênica (Cober et al., 2003).
Em contraste com o trabalho realizado por Donaldson et al. (2001), os
eventos transgênicos obtidos neste estudo expressam a OXDC e, por
conseqüência, não produzem H2O2 adicional no sistema. Embora, comumente
apresentado como importante componente do sistema de defesa das plantas a
patógenos, o papel do H2O2 na interação Sclerotinia x planta, mesmo que não
totalmente esclarecido, parece atuar como facilitador do desenvolvimento do
fungo. Recentes estudos (Kim et al., 2008; Walz et al., 2008b) concluíram que, no
início do processo de infecção (pH > 5), o AO secretado pelo fungo S. sclerotiorum
induz o aumento dos níveis de espécies ativas de oxigênio (ROS), tais como H2O2,
que dispara a morte celular programada (PCD) e conduz a reação de
hipersensibilidade (HR). Por ser um fungo necrotrófico, a morte celular produzirá o
ambiente favorável ao seu desenvolvimento e fornecerá o suprimento necessário
para a infecção e colonização do hospedeiro. Em concordância, plantas
transgênicas de tabaco e A. thaliana incapazes de incitar a HR apresentaram
maior nível de resistência à S. sclerotiorum (Govrin & Levin, 2000; Dickman et al.
2001). Todavia, em termos práticos, estudos adicionais são necessários para
determinar a melhor estratégia visando o desenvolvimento de plantas resistentes a
S. sclerotiorum via introdução de genes capazes de gerar enzimas que degradam
o AO.
40
Por fim, visando o desenvolvimento de variedades de soja resistentes a S.
sclerotiorum faz-se necessário a introdução dos materiais obtidos nesse trabalho
em programas de seleção recorrente, utilizando no cruzamento outras fontes de
tolerância ao mofo branco. Bidney et al (2000) indica que o cruzamento entre
linhagens que expressam enzimas capazes de degradar o AO com linhagens
tolerantes ao mofo branco determina aumento significativo da resistência ao
patógeno. Nesse estudo, o autor demonstra que o efeito sinérgico da expressão
de enzimas como a OXO e OXDC em materiais tolerante a S. sclerotiorum provê
imunidade ou significativo aumento da resistência em plantas de girassol e canola.
41
5 – CONCLUSÕES
A expressão do gene oxdc em soja confere aumento do nível de resistência
das plantas ao fungo S. sclerotiorum.
Os resultados obtidos no presente estudo suportam a hipótese que o AO
produzido pelo fungo possui importante papel na interação Sclerotinia x Soja e que
a introdução de genes capazes de produzir enzimas que degradam este ácido é
aplicável ao desenvolvimento de linhagens de soja resistentes a S. sclerotiorum.
42
REFERÊNCIAS BIBLIOGRÁFICAS
1.
Adams PB, Ayers WA: Ecology of Sclerotinia species. Phytopathology 69:
896-899 (1979).
2.
Aragão FJL, Sarokin L, Vianna GR, Rech EL: Selection of transgenic
meristematic cells utilizing a herbicidal molecule results in the recovery of
fertile transgenic soybean (Glycine max (L.) Merrill) plants at a high
frequency. Theoretical and Applied Genetics 101: 1-6 (2000).
3.
Arahana VS, Graef GL, Specht JE, Steadman JR, Eskridge KM:
Identification of QTLs for resistance to Sclerotinia sclerotiorum in soybean.
Crop Science 41: 180-188 (2001).
4.
Bateman DF, Beer SV: Simultaneous production and synergistic action of
oxalic acid and polygalacturonase during pathogenesis by Sclerotinia rolfsii.
Phytopathology 55: 204-11 (1965).
5.
Bidney DL, Scelonge CJ, Charne DG, Mancl MK, Falak I, Nazarian KAP,
Cole GS: Production of pathogen resistant plants. United States Patent
6166291 (2000).
6.
Boland GJ, Hall R: Index of plant hosts of Sclerotinia sclerotiorum. Canadian
Journal of Plant Pathology 16: 93-108 (1994).
7.
Bolton MD, Thomma BPHJ, Nelson BD: Sclerotinia sclerotiorum (Lib.) de
Bary: Biology and molecular traits of a cosmopolitan pathogen. Molecular
Plant Pathology 7: 1-16 (2006).
43
8.
Cessna SG, Sears VE, Dickman MB, Low PS: Oxalic acid, a pathogenicity
factor for Sclerotinia sclerotiorum, suppresses the oxidative burst of the host
plant. Plant Cell 12: 2191-2199 (2000).
9.
Chen C, Harel A, Gorovoits R, Yarden O, Dickman MB: MAPK regulation of
sclerotial development in Sclerotinia sclerotiorum is linked with pH and
cAMP sensing. Molecular Plant-Microbe Interactions 17: 404-413 (2004).
10.
Chen Y, Wang D: Two convenient methods to evaluate soybean for
resistance to Sclerotinia sclerotiorum. Plant Disease 89: 1268-1272 (2005).
11.
Chun D, Kao LB, Lockwood JL, Isleib TG: Laboratory and field assessment
of resistance in soybean to stem rot caused by Sclerotinia sclerotiorum.
Plant Disease 71: 811-815 (1987).
12.
Cober ER, Rioux S, Rajcan I, Donaldson PA, Simmonds DH: Partial
resistance to white mold in a transgenic soybean line. Crop Science 43: 9295 (2003).
13.
Danielson GA, Nelson BD, Helms TC: Effect of Sclerotinia stem rot on yield
of soybean inoculated at different growth stages. Plant Disease 88: 297-300
(2004).
14.
Dellaporta SL, Wood J, Hicks JB: A plant DNA minipreparation: Version II.
Plant Molecular Biology Reporter 1: 19-21 (1983).
15.
Dias BBA, Cunha WG, Morais LS, Vianna GR, Rech EL, Capdeville Gd,
Aragão FJL: Expression of an oxalate decarboxylase gene from Flammulina
sp. in transgenic lettuce (Lactuca sativa) plants and resistance to Sclerotinia
sclerotiorum. Plant Pathology 55: 187-193 (2006).
44
16.
Dickman MB, Park YK, Oltersdorf T, Li W, Clemente T, French R:
Abrogation
of
disease
development
in
plants
expressing
animal
antiapoptotic genes. Proceedings of the National Academy of Sciences 98:
6957-6962 (2001).
17.
Donaldson PA, Anderson T, Lane BG, Davidson AL, Simmonds DH:
Soybean plants expressing an active oligomeric oxalate oxidase from the
wheat gf-2.8 (germin) gene are resistant to the oxalate-secreting pathogen
Sclerotina sclerotiorum. Physiological and Molecular Plant Pathology 59:
297-307 (2001).
18.
Dong X, Ji R, Guo X, Foster SJ, Chen H, Dong C, Liu Y, Hu Q, Liu S:
Expressing a gene encoding wheat oxalate oxidase enhances resistance to
Sclerotinia sclerotiorum in oilseed rape (Brassica napus). Planta 228: 331340 (2008).
19.
Doyle JJ, Doyle JL: Genomic Plant DNA preparation from fresh tissue:
CTAB method. Phytochemical Bulletin 19: 11-14 (1987).
20.
Dutton MV, Evans CS: Oxalate production by fungi: its role in pathogenicity
and ecology in the soil environment. Canadian Journal of Microbiology 42:
881–895 (1996).
21.
Favaron
F,
Sella
L,
D'Ovidio
R:
Relationships
among
endo-
polygalacturonase, oxalate, pH, and plant polygalacturonase-inhibiting
protein (PGIP) in the interaction between Sclerotinia sclerotiorum and
soybean. Molecular Plant-Microbe Interactions 17: 1402-1409 (2004).
22.
Fehr WR, Caviness CE, Burmood DT, Pennington JS: Stage of
development descriptions for soybeans, Glycine max (L.) Merrill. Crop
Science 11: 929-931 (1971).
45
23.
Ferrar PH, Walker JRL: o-Diphenol oxidase inhibition-an additional role for
oxalic acid in the phytopathogenic arsenal of Sclerotinia sclerotiorum and
Sclerotium rolfsii. Physiological and Molecular Plant Pathology 43: 415-422
(1993).
24.
Godoy G, Steadman JR, Dickman MB, Dam R: Use of mutants to
demonstrate the role of oxalic acid in pathogenicity of Sclerotinia
sclerotiorum on Phaseolus vulgaris. Physiological and Molecular Plant
Pathology 37: 179-191 (1990).
25.
Govrin EM, Levine A: The hypersensitive response facilitates plant infection
by the necrotrophic pathogen Botrytis cinerea. Current Biology 10: 751-757
(2000).
26.
Guimarães RL, Stotz HU: Oxalate production by Sclerotinia sclerotiorum
deregulates guard cells during infection. Plant Physiology 136: 3703-3711
(2004).
27.
Guo X, Wang D, Gordon SG, Helliwell E, Smith T, Berry SA, St Martin SK,
Dorrance AE: Genetic mapping of QTLs underlying partial resistance to
Sclerotinia sclerotiorum in soybean PI 391589A and PI 391589B. Crop
Science 48: 1129-1139 (2008).
28.
Hancock
JC:
Degradation
of
pectic
substances
associated
with
pathogenesis by Sclerotinia sclerotiorum in sunflower and tomato stems.
Phytopathology 56: 975–979 (1966).
29.
Higgins BB: Physiology and parasitism of Sclerotium rolfsii Sacc.
Phytopathology 17: 417-448 (1927).
46
30.
Hoffman DD, Hartman GL, Mueller DS, Leits RA, Nickell CD, Pedersen WL:
Yield and seed quality of soybean cultivars infected with Sclerotinia
sclerotiorum. Plant Disease 82: 826-829 (1998).
31.
Hu X, Bidney DL, Yalpani N, Duvick JP, Crasta O, Folkerts O, Lu GH:
Overexpression of a gene encoding hydrogen peroxide-generating oxalate
oxidase evokes defense responses in sunflower. Plant Physiology 133: 170181 (2003).
32.
Kay R, Chan A, Daly M, McPherson J: Duplication of CaMV 35S promoter
sequences creates a strong enhancer for plant genes. Science 236: 12991302 (1987).
33.
Kesarwani M, Azam M, Natarajan K, Mehta A, Datta A: Oxalate
decarboxylase
from
Collybia
velutipes.
Molecular
cloning
and
its
overexpression to confer resistance to fungal infection in transgenic tobacco
and tomato. Journal of Biological Chemistry 275: 7230-7238 (2000).
34.
Kim HS, Diers BW: Inheritance of partial resistance to Sclerotinia stem rot in
soybean. Crop Science 40: 55-61 (2000).
35.
Kim HS, Hartman GL, Manandhar JB, Graef GL, Steadman JR, Diers BW:
Reaction of soybean cultivars to Sclerotinia stem rot in field, greenhouse,
and laboratory evaluations. Crop Science 40: 665-669 (2000).
36.
Kim KS, Dickman MB, Min JY: Oxalic acid is an elicitor of plant programmed
cell death during Sclerotinia sclerotiorum disease development. Molecular
Plant-Microbe Interactions 21: 605-612 (2008).
47
37.
Kolkman JM, Kelly JD: An indirect test using oxalate to determine
physiological resistance to white mold in common bean. Crop Science 40:
281-285 (2000).
38.
Kritzman G, Chet I, Henis Y: The role of oxalic acid in the pathogenic
behavior of Sclerotium rolfsii Sacc. Experimental Mycology 1: 280-285
(1977).
39.
Kruskal WH, Wallis WA: Use of ranks in one-criterion variance analysis.
Journal of the American Statistical Association 47: 583–621 (1952).
40.
Kull LS, Vuong TD, Powers KS, Eskridge KM, Steadman JR, Hartman GL:
Evaluation of resistance screening methods for Sclerotinia stem rot of
soybean and dry bean. Plant Disease 87: 1471-1476 (2003).
41.
Kurian
P,
Stelzig
DA:
The
synergistic
role
of
andendopolygalacturonase in bean leaves infected by
oxalic
acid
Cristulariella
pyramidalis. Phytopathology 69: 1301–1304 (1979).
42.
Levine A, Tenhaken R, Dixon R, Lamb C: H2O2 from the oxidative burst
orchestrates the plant hypersensitive disease resistance response. Cell 79:
583–593. (1994).
43.
Livingstone DM, Hampton JL, Phipps PM, Grabau EA: Enhancing
resistance to Sclerotinia minor in peanut by expressing a barley oxalate
oxidase gene. Plant Physiology 137: 1354-1362 (2005).
44.
Lumsden RD: Sclerotinia sclerotiorum infection of bean and the production
of cellulase. Phytopathology 59: 653–657 (1969).
48
45.
Magro P, Marciano P, Di Lenna P: Oxalic acid production and its role in
pathogenesis of Sclerotinia sclerotiorum. FEMS Microbiology Letters 24: 912 (1984).
46.
Marciano P, Di Lenna P, Magro P: Oxalic acid, cell wall-degrading enzymes
and pH in pathogenesis and their significance in the virulence of two
Sclerotinia sclerotiorum isolates on sunflower. Physiological Plant Pathology
22: 339-345 (1983).
47.
Maxwell DP, Lumsden RD: Oxalic acid production by Sclerotinia
sclerotiorum in infected bean and in culture. Phytopathology 60: 1395–1398
(1970).
48.
Mehta A, Datta A: Oxalate decarboxylase from Collybia velutipes.
Purification, characterization, and cDNA cloning. The Journal of Biological
Chemistry 266: 23548-23553 (1991).
49.
Noyes RD, Hancock JG: Role of oxalic acid in the Sclerotinia wilt of
sunflower. Physiological Plant Pathology 18: 123-132 (1981).
50.
Pierson PE, Rhodes LH: Effect of culture medium on the production of
oxalic acid by Sclerotinia trifoliorum. Mycologia 84: 467-469 (1992).
51.
Purdy LH: Sclerotinia sclerotiorum: history, diseases and symptomatology,
host range, geographic distribution, and impact. Phytopathology 69: 875880 (1979).
52.
Rech EL, Vianna GR, Aragão FJL: High-efficiency transformation by
biolistics of soybean, common bean and cotton transgenic plants. Nature
Protocols 3: 410-418 (2008).
49
53.
Resende MLV, Salgado SML, Chaves ZM: Espécies ativas de oxigênio na
resposta de defesa de plantas a patógenos. Fitopatologia Brasileira 28:
123-130 (2003).
54.
Riou C, Freyssinet G, Fevre M: Production of cell wall-degrading enzymes
by the phytopathogenic fungus Sclerotinia sclerotiorum. Applied and
Environmental Microbiology 57: 1478-1484 (1991).
55.
Rollins JA: The Sclerotinia sclerotiorum pac1 gene is required for sclerotial
development and virulence. Molecular Plant-Microbe Interactions 16: 785795 (2003).
56.
Rollins JA, Dickman MB: pH signaling in Sclerotinia sclerotiorum:
Identification of a pacC/RIM1 homolog. Applied and Environmental
Microbiology 67: 75-81 (2001).
57.
Sambrook J, Fritsch EF, Maniatis T: Molecular cloning : a laboratory manual
/ J. Sambrook, E.F. Fritsch, T. Maniatis. Cold Spring Harbor, N.Y. : Cold
Spring Harbor Laboratory, 1989. (1989).
58.
Shaner G, Finney RE: The effect of nitrogen fertilization on the expression
of slow-mildewing resistance in Knox wheat. Phytopathology 67: 1051-1056
(1977).
59.
Stone HE, Armentrout VN: Production of oxalic acid by Sclerotinia
cepivorum during infection of onion. Mycologia 77: 526–530 (1985).
60.
Tenhaken R, Levine A, Brisson LF, Dixon RA, Lamb C: Function of the
oxidative burst in hypersensitive disease resistance. Proceedings of the
National Academy of Sciences 92: 4158-4163 (1995).
50
61.
Thomma BPHJ, Penninckx IAMA, Broekaert WF, Cammue BPA: The
complexity of disease signaling in Arabidopsis. Current Opinion in
Immunology 13: 63–68 (2001).
62.
Tu JC: Tolerance of white bean (Phaseolus vulgaris) to white mold
(Sclerotinia sclerotiorum) associated with tolerance to oxalic acid.
Physiological Plant Pathology 26: 111-117 (1985).
63.
Vale FXR, Fernandes Filho EI, Liberato JR: Quant. A software for plant
disease severity assessment. In: 8th International Congress of Plant
Pathology, Christchurch, New Zealand: 105 (2003).
64.
Vuong TD, Diers BW, Hartman GL: Identification of QTL for resistance to
Sclerotinia stem rot in soybean plant introduction 194639. Crop Science 48:
2209-2214 (2008).
65.
Vuong TD, Hoffman DD, Diers BW, Miller JF, Steadman JR, Hartman GL:
Evaluation of soybean, dry bean, and sunflower for resistance to Sclerotinia
sclerotiorum. Crop Science 44: 777-783 (2004).
66.
Walz A, Zingen-Sell I, Loeffler M, Sauer M: Expression of an oxalate
oxidase gene in tomato and severity of disease caused by Botrytis cinerea
and Sclerotinia sclerotiorum. Plant Pathology 57: 453-458 (2008a).
67.
Walz A, Zingen-Sell I, Theisen S, Kortekamp A: Reactive oxygen
intermediates and oxalic acid in the pathogenesis of the necrotrophic fungus
Sclerotinia sclerotiorum. European Journal of Plant Pathology 120: 317-330
(2008b).
68.
Wang Z, Song J, Zhang Y, Yang B, Wang Y, Chen S: Mechanism analysis
of broad-spectrum disease resistance induced by expression of anti51
apoptotic p35 gene in tobacco. Chinese Journal of Biotechnology 24: 17071713 (2008).
69.
Wegulo SN, Yang XB, Martinson CA: Soybean cultivar responses to
Sclerotinia sclerotiorum in field and controlled environment studies. Plant
Disease 82: 1264-1270 (1998).
70.
Wharton P, Kirk W: White Mold Michigan Potato Diseases Series; MSU
Extension bulletin E-2989 (2007).
71.
Wrather JA, Koenning SR: Effects of diseases on soybean yields in the
United States 1996 to 2007. Plant Health Progress: doi:10.1094/PHP-20090401-01-RS (2009).
72.
Yang XB, Lundeen P, Uphoff MD: Soybean varietal response and yield loss
caused by Sclerotinia sclerotiorum. Plant Disease 83: 456-461 (1999).
52
ANEXOS
53
ANEXO A
Figura 1A. Folhas de plantas não transgênicas da variedade BR-16 após 90 horas
do posicionamento dos discos de micélio do fungo S. sclerotiorum. O
diâmetro do círculo no qual as folhas estão contidas possui 15 cm. ... 57
Figura 2A. Folhas do evento OXDC.1.01 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 58
Figura 3A. Folhas do evento OXDC.1.02 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 59
Figura 4A. Folhas do evento OXDC.2.03 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 60
Figura 5A. Folhas do evento OXDC.2.04 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 61
Figura 6A. Folhas do evento OXDC.3.05 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 62
Figura 7A. Folhas do evento OXDC.3.06 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 63
Figura 8A. Folhas do evento OXDC.4.07 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 64
54
Figura 9A. Folhas do evento OXDC.4.08 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 65
Figura 10A. Folhas do evento OXDC.5.09 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 66
Figura 11A. Folhas do evento OXDC.5.10 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 67
Figura 12A. Folhas do evento OXDC.6.11 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 68
Figura 13A. Folhas do evento OXDC.6.12 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 69
Figura 14A. Folhas do evento OXDC.7.16 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 70
Figura 15A. Folhas do evento OXDC.7.17 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 71
Figura 16A. Folhas do evento OXDC.8.18 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 72
55
Figura 17A. Folhas do evento OXDC.9.21 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 73
Figura 18A. Folhas de plantas não transgênicas da variedade BR-16 após 114
horas do posicionamento dos discos de micélio do fungo S.
sclerotiorum. O diâmetro do círculo no qual as folhas estão contidas
possui 15 cm. ....................................................................................... 74
Figura 19A. Folhas do evento OXDC.9.21 após 114 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm. ........................................ 75
56
Figura 1A. Folhas de plantas não transgênicas da variedade BR-16 após 90 horas
do posicionamento dos discos de micélio do fungo S. sclerotiorum. O
diâmetro do círculo no qual as folhas estão contidas possui 15 cm.
57
Figura 2A. Folhas do evento OXDC.1.01 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
58
Figura 3A. Folhas do evento OXDC.1.02 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
59
Figura 4A. Folhas do evento OXDC.2.03 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
60
Figura 5A. Folhas do evento OXDC.2.04 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
61
Figura 6A. Folhas do evento OXDC.3.05 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
62
Figura 7A. Folhas do evento OXDC.3.06 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
63
Figura 8A. Folhas do evento OXDC.4.07 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
64
Figura 9A. Folhas do evento OXDC.4.08 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
65
Figura 10A. Folhas do evento OXDC.5.09 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
66
Figura 11A. Folhas do evento OXDC.5.10 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
67
Figura 12A. Folhas do evento OXDC.6.11 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
68
Figura 13A. Folhas do evento OXDC.6.12 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
69
Figura 14A. Folhas do evento OXDC.7.16 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
70
Figura 15A. Folhas do evento OXDC.7.17 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
71
Figura 16A. Folhas do evento OXDC.8.18 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
72
Figura 17A. Folhas do evento OXDC.9.21 após 90 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
73
Figura 18A. Folhas de plantas não transgênicas da variedade BR-16 após 114
horas do posicionamento dos discos de micélio do fungo S.
sclerotiorum. O diâmetro do círculo no qual as folhas estão contidas
possui 15 cm.
74
Figura 19A. Folhas do evento OXDC.9.21 após 114 horas do posicionamento dos
discos de micélio do fungo S. sclerotiorum. O diâmetro do círculo no
qual as folhas estão contidas possui 15 cm.
75
ANEXO B
Artigo 1B. Cunha WG, Tinoco MLP, Pancoti HL, Ribeiro RE, Aragão FJL: High
resistance to Sclerotinia sclerotiorum in transgenic soybean plants
transformed to express an oxalate decarboxylase gene. Plant Pathology
Doi: 10.1111/j.1365-3059.2010.02279.x (2010)…………………………77
Artigo 2B. Dias BBA, Cunha WG, Morais LS, Vianna GR, Rech EL, Capdeville Gd,
Aragão FJL: Expression of an oxalate decarboxylase gene from
Flammulina sp. in transgenic lettuce (Lactuca sativa) plants and
resistance to Sclerotinia sclerotiorum. Plant Pathology 55: 187-193
(2006)………………………………………………………………………...84
76
77
2
W. G. Cunha et al.
Previous studies showed that some of the identified
quantitative trait loci (QTL) for resistance to SSR
were associated with escape mechanisms (Kim & Diers,
2000). For these reasons, soybean breeding has not made
available a SSR-resistant variety on the market.
Previous studies provided evidence for the involvement
of oxalic acid (OA) in S. sclerotiorum pathogenesis and
OA tolerance has been correlated to disease tolerance
(Bateman & Beer, 1965; Maxwell & Lumsden, 1970;
Noyes & Hancock, 1981; Marciano et al., 1983; Magro
et al., 1984; Tu, 1985; Godoy et al., 1990; Wegulo et al.,
1998; Cessna et al., 2000; Kolkman & Kelly, 2000; Favaron et al., 2004; Guimarã es & Stotz, 2004; Kim et al.,
2008; Walz et al., 2008b). Treatment of healthy plants
with OA or fungal culture filtrates resulted in foliar symptoms identical to those found in diseased plants (Bateman
& Beer, 1965; Noyes & Hancock, 1981; Marciano et al.,
1983). In addition, plants that showed in vitro and field
tolerance to OA were more tolerant to S. sclerotiorum
(Noyes & Hancock, 1981; Tu, 1985; Wegulo et al.,
1998; Kolkman & Kelly, 2000) and mutants of S. sclerotiorum unable to synthesize OA were less pathogenic
when compared with a wild type (Godoy et al., 1990).
A potential alternative to developing an SSR-resistant
soybean variety is the introduction of genes that generate
enzymes capable of degrading the OA. Several transgenic
plants expressing genes encoding enzymes that can
metabolize OA, such as oxalate oxidases (OXO) and
oxalate decarboxylases (OXDC), have shown an
enhanced resistance to S. sclerotiorum (Kesarwani et al.,
2000; Donaldson et al., 2001; Cober et al., 2003; Hu
et al., 2003; Livingstone et al., 2005; Dias et al., 2006;
Dong et al., 2008; Walz et al., 2008a). OXO catalyses the
oxygen-dependent oxidation of oxalate to carbon dioxide and hydrogen peroxide. OXDC breaks down oxalate
to generate carbon dioxide and formate in the absence of
any cofactor requirement. In addition, OXDC is specific
to OA and has high activity at acidic or neutral pH
(Kesarwani et al., 2000).
The main goal of this research was to introduce an oxalate decarboxylase gene (oxdc) from a Flammulina sp.
into the soybean genome in order to generate transgenic
lines resistant to S. sclerotiorum.
Materials and methods
Plasmid vector and soybean transformation
The oxdc coding sequence was removed from pTOPOOxDc and cloned into the vector pUC19-35SdAMVNOS, between the XbaI and BamHI sites, under the
control of the doubled 35S promoter from Cauliflower
mosaic virus and a sequence enhancer from Alfalfa
mosaic virus (Dias et al., 2006). The oxdc expression cassette was excised with EcoRI and HindIII from the vector
pOXDC (Dias et al., 2006) and inserted into the pBluKSP
(Fermentas) to generate the pBluKSPOXDC vector. The
oxdc cassette is composed of the oxdc coding sequence
under control of the doubled 35S promoter from Cauli-
Figure 1 Diagram representing the pBluKSPOXDCAHAS
transformation vector containing the ahas gene (ahas5¢: ahas gene
promoter; ahasCDS: Arabidopsis thaliana AHAS coding sequence;
ahas3¢: ahas gene terminator) and oxdc expression cassettes (d35S:
doubled 35S promoter from Cauliflower mosaic virus; AMV: nontranslated sequence enhancer from Alfalfa mosaic virus; nos3¢:
nopaline synthase terminator). Black bar represents the probe used
in the Southern analysis.
flower mosaic virus and a sequence enhancer from Alfalfa
mosaic virus, and nos gene terminator. The 5718-bp fragment containing the mutated Arabidopsis ahas gene
(selectable marker that confers imidazolinone-specific
resistance) was removed with XbaI from the vector
pAC321 (Rech et al., 2008) and cloned into the SpeI site
of the vector pBluKSPOXDC, resulting in the transformation vector pBluKSPOXDCAHAS (Fig. 1).
Soybean transformation was carried out according to
Rech et al. (2008) and Aragã o et al. (2000). Mature seeds
of a commercial variety (BR-16) were surface-sterilized
and soaked in distilled water for 18–20 h. The embryonic
axes were excised from seeds, and the apical meristems
were exposed by removing the primary leaves and bombarded as previously described by Aragã o et al. (2000).
Multiple shooting was induced by cultivating the embryonic axes in BAP-supplemented medium immediately
after bombardment. As soon as the embryonic axesderived shoots were 2–3 cm in length, they were individually transferred to a plastic pot containing a mixture of
fertilized soil and vermiculite and acclimatized in a greenhouse to produce seeds. A total of 1152 explants were
bombarded with the vector pBluKSPOXDCAHAS.
PCR screening of transformed plants
The recovered plants and progenies were screened by
PCR to detect the presence of the oxdc gene. Genomic
DNA from young leaves was extracted by the CTAB
method (Doyle & Doyle, 1987). The PCR analyses were
carried out according to Aragã o et al. (2002). The primers
OXDC 371 (5¢-CTCGGCAGCAGAATGAGGTC-3¢)
and OXDC 873 (5¢-TCGGCTCGACAGAGGAGAAG-3¢)
were used to amplify a 522-bp sequence within the oxdc
coding sequence.
Detached leaf assays
The detached leaf assay was carried out using plants from
the T2 generation. Sclerotia were collected from a soybean infected field located in Distrito Federal (Brazil) and
Plant Pathology (2010)
78
79
4
W. G. Cunha et al.
Figure 3 Disease progress curve of T2 oxdc
soybean transgenic events and the
nontransgenic control (BR-16) obtained by
the detached leaf assay using Sclerotinia
sclerotiorum mycelial agar plug. The infected
area measured in each time was an average
of 10 different plant repetitions except for the
OXDC.1.02, OXDC.2.04, OXDC.5.10,
OXDC.7.16, OXDC.7.17 and OXDC.8.18 that
were 9, 6, 4, 8, 6 and 9 repetitions,
respectively. Bars = standard deviation.
(a)
(b)
(c)
(d)
(e)
(f)
(g)
(h)
(i)
(j)
(k)
(l)
Figure 4 Resistance response of transgenic
plants to Sclerotinia sclerotiorum inoculation.
Symptoms were observed on detached
leaves 42 h (a, d and g), 66 h (b, e and h)
and 90 h (c, f and i) after inoculation of
transgenic plants OXDC.9.21.2 (a–c),
OXDC.6.11.7, (d–f) and nontransgenic control
(g–i) with 5-mm mycelial agar plugs.
Detail of soybean line OXDC.9.21.2 response
to the mycelium of S. sclerotiorum growth
90 h (j) and 114 h (k) after inoculation
compared to a nontransgenic plant 90 h
after inoculation (l).
Plant Pathology (2010)
80
S. sclerotiorum resistance in transgenic soybean plants
(a)
(b)
Figure 5 (a) RT-PCR for detection of expression of the foreign oxdc
and endogenous 18S rRNA genes in transgenic soybean lines. (b)
Quantification of the oxdc gene expression relative to that of 18S
rRNA housekeeping gene. Lane 1: line OXDC.6.11.7; lane 2: line
OXDC.9.21.2; lane 3: nontransgenic plant.
Figure 6 Southern blot analysis of genomic DNA to detect the
foreign oxdc gene expression cassette in the soybean plants (T2
generation) from transgenic event OXDC.9.21. Lanes 1–8:
transgenic plants; lane 9: nontransgenic plant.
Discussion
The progenies (T2 generation) of self-pollinated transgenic lines were tested for resistance to S. sclerotiorum.
Results from the detached leaf assays showed that plants
transformed with the oxdc gene presented different levels
of resistance to S. sclerotiorum. Compared to the nontransformed control, all transgenic events demonstrated a
significant delay in lesion development. Similar results
were previously reported in tobacco, tomato and lettuce
transgenic plants transformed to express an oxdc coding
gene (Kesarwani et al., 2000; Dias et al., 2006; Walz
et al., 2008a).
RT-PCR analysis revealed the expression of the oxdc
gene in the resistant lines tested (OXDC.9.21.2,
OXDC.6.11.7), while no transcripts corresponding to
the oxdc gene were observed in the susceptible nontransgenic lines analyzed. Results suggested that line
OXDC.6.11.7, exhibiting only moderate resistance to S.
sclerotiorum, revealed a presence of oxdc gene transcripts
at a much lower level (Fig. 5b) than observed in the line
OXDC.9.21.2, which exhibited a high resistance level to
the pathogen. These results suggest that expression of the
oxdc gene is associated with resistance to the fungus and
5
that the resistance level is dependent on the transgene
expression level. The association of the presence of the
gene and resistance is also supported by the fact that all
transgenic lines presented a level of resistance to the pathogen while all nontransgenic genotypes tested were susceptible to infection. The results have shown that the
generation of highly S. sclerotiorum-resistant soybean
lines is feasible by the expression of the oxalate decarboxylase gene. The interaction of Sclerotinia with epidermal
cells of transgenic and nontransgenic soybean plants is
currently being studied at the ultra-structural level. This
may help to elucidate the cellular basis of this plant-pathogen interaction. In addition, studies will be carried out
to evaluate the resistance of soybean lines under field conditions. To confirm the enhanced resistance shown by the
detached leaf assay, transgenic event OXDC.9.21 will be
further tested under field conditions. Although the values
were inconsistent in some situations, a significant correlation of SSR disease ratings between the detached leaf
assay and field evaluations has been reported (Wegulo
et al., 1998; Kim et al., 2000; Hoffman et al., 2002). To
ensure the consistency of the detached leaf assay, this
study used uniform leaf size, fixed the inoculum placement and provided adequate moisture during the test, as
discussed by Wegulo et al. (1998).
Expression of oxalate-detoxifying enzymes in transgenic plants has been successful in generating resistant
lines. Wheat oxalate oxidase has been constitutively
expressed in canola, tobacco, soybean, poplar, sunflower, peanut and tomato (Thompson et al., 1995; Berna
& Bernier, 1997; Donaldson et al., 2001; Cober et al.,
2003; Hu et al., 2003; Livingstone et al., 2005; Dong
et al., 2008) and the oxalate decarboxylase gene has been
incorporated into tobacco, tomato and lettuce (Kesarwani et al., 2000; Dias et al., 2006; Walz et al., 2008a). In
contrast to oxalate oxidase enzyme activity, which converts OA into carbon dioxide and hydrogen peroxide,
oxalate decarboxylase promotes OA conversion into carbon dioxide and formate and does not lead to a development of additional hydrogen peroxide (Kesarwani et al.,
2000; Walz et al., 2008a). The production of oxygen radical synthesis interactions seems to be important, as they
weaken the host tissue at early stages of infection and consequently enhance the growth and development of the
pathogen (Govrin & Levine, 2000). Kim et al. (2008)
concluded that S. sclerotiorum-secreted oxalate induces
increased levels of reactive oxygen species (ROS) such as
hydrogen peroxide and superoxide in the plant in the
early stages of the infection, which appears to trigger a
programmed cell death (PCD) pathway, resulting in plant
cell death and the generation of a suitable environmental
niche for fungal pathogenic development, nutrient acquisition, and the establishment of a necrotrophic relationship. Walz et al. (2008b) observed moderate hydrogen
peroxide accumulation in inoculated tobacco plants in
the first 24 h after infection and a subsequent decrease.
These studies suggested that in the early stages of pathogenesis at relatively high pH (>5) the oxalate produced by
the fungus induces increased reactive oxygen species
Plant Pathology (2010)
81
6
W. G. Cunha et al.
(hydrogen peroxide and superoxide) levels and a programmed cell death response in plant tissue that is
required for disease development (Kim et al., 2008). As
OA accumulates, the pH decreases and it suppresses the
reactive oxygen species and programmed cell death,
enabling the pathogen’s further ingress into plant tissue
(Kim et al., 2008). OXDC transgenic plants would be a
better model in which to study the plant pathogen interaction, considering that there is no additional hydrogen
peroxide production, unlike in OXO plants. In practical
terms, more studies are needed to determine which oxalate-detoxifying strategy would be more appropriate.
Acknowledgements
We gratefully acknowledge the financial support of
FINEP and CNPq (Conselho Nacional de Desenvolvimento Cientı́fico e Tecnoló gico, grant number 500028 ⁄
2006-0). W. Cunha was supported by a fellowship from
CNPq.
References
Aragã o FJL, Sarokin L, Vianna GR, Rech EL, 2000. Selection of
transgenic meristematic cells utilizing a herbicidal molecule
results in the recovery of fertile transgenic soybean (Glycine max
(L.) Merrill) plants at a high frequency. Theoretical and
Applied Genetics 101, 1–6.
Aragã o FJL, Vianna GR, Albino MMC, Rech EL, 2002.
Transgenic dry bean tolerant to the herbicide glufosinate
ammonium. Crop Science 42, 1298–302.
Bateman DF, Beer SV, 1965. Simultaneous production and
synergistic action of oxalic acid and polygalacturonase during
pathogenesis by Sclerotium rolfsii. Phytopathology 55,
204–11.
Berna A, Bernier F, 1997. Regulated expression of a wheat germin
gene in tobacco: oxalate oxidase activity and apoplastic
localization of the heterologous protein. Plant Molecular
Biology 33, 417–29.
Boland GJ, Hall R, 1994. Index of plant hosts of Sclerotinia
sclerotiorum. Canadian Journal of Plant Pathology 16,
93–100.
Cessna SG, Sears VE, Dickman MB, Low PS, 2000. Oxalic acid, a
pathogenicity factor for Sclerotinia sclerotiorum, suppresses the
oxidative burst of the host plant. The Plant Cell 12, 2191–9.
Cober ER, Rioux S, Rajcan I, Donaldson PA, Simmonds DH,
2003. Partial resistance to white mold in a transgenic soybean
line. Crop Science 43, 92–5.
Danielson GA, Nelson BD, Helms TC, 2004. Effect of Sclerotinia
stem rot on yield of soybean inoculated at different growth
stages. Plant Disease 88, 297–300.
Dellaporta SL, Wood J, Hicks JB, 1983. A plant DNA
minipreparation: Version II. Plant Molecular Biology Reporter
1, 19–21.
Dias BBA, Cunha WG, Morais LS et al., 2006. Expression of an
oxalate decarboxylase gene from Flammulina sp. in transgenic
lettuce (Lactuca sativa) plants and resistance to Sclerotinia
sclerotiorum. Plant Pathology 55, 187–93.
Donaldson PA, Anderson T, Lane BG, Davidson AL, Simmonds
DH, 2001. Soybean plants expressing an active oligomeric
oxalate oxidase from the wheat gf-2.8 (germin) gene are resistant
to the oxalate-secreting pathogen Sclerotina sclerotiorum.
Physiological and Molecular Plant Pathology 59, 297–307.
Dong X, Ji R, Guo X et al., 2008. Expressing a gene encoding
wheat oxalate oxidase enhances resistance to Sclerotinia
sclerotiorum in oilseed rape (Brassica napus). Planta 228, 331–
40.
Doyle JJ, Doyle JL, 1987. Genomic plant DNA preparation from
fresh tissue: CTAB method. Phytochemical Bulletin 19, 11–4.
Favaron F, Sella L, D’Ovidio R, 2004. Relationships among endopolygalacturonase, oxalate, pH, and plant polygalacturonaseinhibiting protein (PGIP) in the interaction between Sclerotinia
sclerotiorum and soybean. Molecular Plant-Microbe
Interactions 17, 1402–9.
Fehr WR, Caviness CE, Burmood DT, Pennington JS, 1971. Stage
of development descriptions for soybeans, Glycine max (L.)
Merrill. Crop Science 11, 929–31.
Godoy G, Steadman JR, Dickman MB, Dam R, 1990. Use of
mutants to demonstrate the role of oxalic acid in pathogenicity
of Sclerotinia sclerotiorum on Phaseolus vulgaris. Physiological
and Molecular Plant Pathology 37, 179–91.
Govrin EM, Levine A, 2000. The hypersensitive response facilitates
plant infection by the necrotrophic pathogen Botrytis cinerea.
Current Biology 10, 751–7.
Guimarã es RL, Stotz HU, 2004. Oxalate production by Sclerotinia
sclerotiorum deregulates guard cells during infection. Plant
Physiology 136, 3703–11.
Hoffman DD, Diers BW, Hartman GL et al., 2002. Selected
soybean plant introductions with partial resistance to Sclerotinia
sclerotiorum. Plant Disease 86, 971–80.
Hu X, Bidney DL, Yalpani N et al., 2003. Overexpression of a
gene encoding hydrogen peroxide-generating oxalate oxidase
evokes defense responses in sunflower. Plant Physiology 133,
170–81.
Kesarwani M, Azam M, Natarajan K, Mehta A, Datta A, 2000.
Oxalate decarboxylase from Collybia velutipes. Molecular
cloning and its overexpression to confer resistance to fungal
infection in transgenic tobacco and tomato. Journal of
Biological Chemistry 275, 7230–8.
Kim HS, Diers BW, 2000. Inheritance of partial resistance to
sclerotinia stem rot in soybean. Crop Science 40, 55–61.
Kim KS, Dickman MB, Min JY, 2008. Oxalic acid is an elicitor of
plant programmed cell death during Sclerotinia sclerotiorum
disease development. Molecular Plant-Microbe Interactions
21, 605–12.
Kim HS, Hartman GL, Manandhar JB, Graef GL, Steadman JR,
Diers BW, 2000. Reaction of soybean cultivars to Sclerotinia
stem rot in field, greenhouse, and laboratory evaluations. Crop
Science 40, 665–9.
Kolkman JM, Kelly JD, 2000. An indirect test using oxalate to
determine physiological resistance to white mold in common
bean. Crop Science 40, 281–5.
Livingstone DM, Hampton JL, Phipps PM, Grabau EA, 2005.
Enhancing resistance to Sclerotinia minor in peanut by
expressing a barley oxalate oxidase gene. Plant Physiology 137,
1354–62.
Magro P, Marciano P, Di Lenna P, 1984. Oxalic acid production
and its role in pathogenesis of Sclerotinia sclerotiorum. FEMS
Microbiology Letters 24, 9–12.
Marciano P, Di Lenna P, Magro P, 1983. Oxalic acid, cell walldegrading enzymes and pH in pathogenesis and their significance
Plant Pathology (2010)
82
S. sclerotiorum resistance in transgenic soybean plants
in the virulence of two Sclerotinia sclerotiorum isolates on
sunflower. Physiological Plant Pathology 22, 339–45.
Maxwell DP, Lumsden RD, 1970. Oxalic acid production by
Sclerotinia sclerotiorum in infected bean and in culture.
Phytopathology 60, 1395–8.
Noyes RD, Hancock JG, 1981. Role of oxalic acid in the
Sclerotinia wilt of sunflower. Physiological Plant Pathology
18, 123–32.
Rech EL, Vianna GR, Aragã o FJL, 2008. High-efficiency
transformation by biolistics of soybean, common bean and
cotton transgenic plants. Nature Protocols 3, 410–8.
Sambrook J, Fritsch EF, Maniatis T, 1989. Molecular Cloning:
A Laboratory Manual. Cold Spring Harbor, NY, USA:
Cold Spring Harbor Laboratory Press.
Shaner G, Finney RE, 1977. The effect of nitrogen fertilization on
the expression of slow-mildewing resistance in Knox wheat.
Phytopathology 67, 1051–6.
Thompson C, Dunwell JM, Johnstone CE et al., 1995.
Degradation of oxalic acid by transgenic oilseed rape plants
expressing oxalate oxidase. Euphytica 85, 169–72.
Tu JC, 1985. Tolerance of white bean (Phaseolus vulgaris) to white
mold (Sclerotinia sclerotiorum) associated with tolerance to oxalic
acid. Physiological Plant Pathology 26, 111–7.
7
Vale FXR, Fernandes Filho EI, Liberato JR, 2003. QUANT. A
software for plant disease severity assessment. In: 8th
International Congress of Plant Pathology. Christchurch, New
Zealand: 105.
Vuong TD, Diers BW, Hartman GL, 2008. Identification of QTL
for resistance to sclerotinia stem rot in soybean plant
introduction 194639. Crop Science 48, 2209–14.
Walz A, Zingen-Sell I, Loeffler M, Sauer M, 2008a. Expression of
an oxalate oxidase gene in tomato and severity of disease caused
by Botrytis cinerea and Sclerotinia sclerotiorum. Plant
Pathology 57, 453–8.
Walz A, Zingen-Sell I, Theisen S, Kortekamp A, 2008b.
Reactive oxygen intermediates and oxalic acid in the
pathogenesis of the necrotrophic fungus Sclerotinia
sclerotiorum. European Journal of Plant Pathology 120,
317–30.
Wegulo SN, Yang XB, Martinson CA, 1998. Soybean cultivar
responses to Sclerotinia sclerotiorum in field and controlled
environment studies. Plant Disease 82, 1264–70.
Wrather JA, Koenning SR, 2009. Effects of diseases on soybean
yields in the United States 1996 to 2007. Plant Health Progress.
doi:10.1094/PHP-2009-0401-01-RS.
Plant Pathology (2010)
83
Plant Pathology (2006) 55, 187–193
Doi: 10.1111/j.1365-3059.2005.01342.x
Expression of an oxalate decarboxylase gene from
Flammulina sp. in transgenic lettuce (Lactuca sativa)
plants and resistance to Sclerotinia sclerotiorum
B. B. A. Diasab, W. G. Cunhaac, L. S. Moraisa, G. R. Viannaa, E. L. Recha,
G. de Capdevillea and F. J. L. Aragãoa*
a
Embrapa Recursos Genéticos e Biotecnologia, Laboratório de Introdução e Expressão de Genes, PqEB W5 Norte, 70770-900, Brasília,
DF; bUniversidade de Brasília, Departamento de Botânica, Instituto de Ciências Biológicas, CP 04457, 70919-970, Brasília, DF; and
c
Universidade de Brasília, Departamento de Biologia Celular, Instituto de Ciências Biológicas, 70919-970, Brasília, DF, Brazil
Sclerotinia sclerotiorum causes rot in a broad range of crops including lettuce, soybean, dry bean and tomato. Pathogenesis
of Sclerotinia has been associated with the copious production of oxalic acid. Enzymes capable of degrading oxalic acid
have been utilized to produce transgenic resistant plants. Transgenic lettuce lines containing the decarboxylase gene (oxdc)
isolated from a Flammulina sp. were produced by Agrobacterium-mediated transformation. Out of 80 regenerated
plants, PCR analysis revealed the presence of the oxdc gene in 34 lines. Except for eight lines, the primary transformants
transferred the foreign gene to the first generation in a Mendelian fashion. In a detached-leaf assay inoculated with agar
plugs of a 2-day-old S. sclerotiorum culture, two lines (P100 and P43) were symptomless, while line P57 showed a delay in
symptom development when compared with a nontransgenic control line. RT-PCR analysis carried out with the resistant
lines showed the expression of oxdc gene transcripts.
Keywords: Flammulina sp., oxalate decarboxylase, oxalic acid, Sclerotinia sclerotiorum, transgenic lettuce
Introduction
Sclerotinia sclerotiorum is a broad host-range pathogenic
ascomycete, which can cause diseases in more than 400
plant species including many agronomically important crops
such as tomato, soybean, dry bean and lettuce (Boland &
Hall, 1994). In lettuce (Lactuca sativa), diseased plants
are unmarketable as they rot once infected with the fungus. The disease is difficult to control when the fungus is
established in the soil because the sclerotia of S. sclerotiorum are long-lived (Tu, 1997). Although some breeding lines of L. sativa and L. serriola have shown some
degree of resistance against S. sclerotiorum, there are no
resistant commercial cultivars of lettuce, and disease control is based on the use of fungicides, with ascospores as
the target (Whipps et al., 2002; Young et al., 2004).
Pathogenesis of S. sclerotiorum, Sclerotium cepivorum
and Sclerotium rolfsii has been associated with the production of oxalic acid by these fungi (Bateman & Beer, 1965;
Magro et al., 1984; Godoy et al., 1990). Previous studies
*E-mail: [email protected]
Accepted 1 September 2005
provided evidence for the involvement of oxalic acid in
fungal pathogenesis. Treatment of healthy sunflower and
common bean plants with oxalic acid or fungal culture
filtrates resulted in foliar symptoms identical to those found
in diseased plants (Noyes & Hancock, 1981; Marciano
et al., 1983; Godoy et al., 1990). In addition, plants that
showed in vitro resistance to oxalic acid were more tolerant
to S. sclerotiorum (Noyes & Hancock, 1981; Rowe, 1993;
Kolkman & Kelly, 2000). Marciano et al. (1983) detected
high concentrations of oxalic acid in sunflower tissues
infected by S. sclerotiorum. Moreover, prototrophic
mutants of S. sclerotiorum deficient in oxalic acid production were nonpathogenic to common bean plants. In contrast, the oxalic acid-producing wild type was pathogenic
(Godoy et al., 1990). The exact role of oxalic acid during
infection is not well understood. However, several cellulolytic and pectolytic enzymes secreted by the fungi during
invasion of plant tissues have maximal activities at low pH,
and oxalate might increase enzymatic activity by shifting
the apoplastic pH (Bateman & Beer, 1965; Lumsden, 1976;
Magro et al., 1984). Oxalic acid may chelate calcium,
compromising the function of calcium-dependent defence
responses and weakening the cell wall (Bateman & Beer,
1965; Marciano et al., 1983; Ferrar & Walker, 1993).
In addition, oxalate suppresses oxidant biosynthesis,
187
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
84
188
B. B. A. Dias et al.
disabling the earliest resistance response in plant cells
(Cessna et al., 2000).
With a view to the degradation of oxalic acid, genes for
enzymes such as oxalate oxidase and oxalate decarboxylase
have been isolated and characterized. Oxalate oxidase
catalyses the oxygen-dependent oxidation of oxalate to
CO2 and hydrogen peroxide (Kotsira & Clonis, 1997).
Oxalate decarboxylases break down oxalate to generate
formate and carbon dioxide (Reinhardt et al., 2003). The
introduction of these genes in transgenic plants has been
proposed in order to produce Sclerotinia-resistant lines.
The barley oxalate oxidase gene was introduced into
canola (Thompson et al., 1995) and peanut (Livingstone
et al., 2005). The wheat oxalate oxidase gene was introduced into poplar (Liang et al., 2001), tobacco (Berna
& Bernier, 1997), soybean (Donaldson et al., 2001)
and sunflower (Burke & Rieseberg, 2003). The oxalate
decarboxylase gene from Collybia velutipes (syn.
Flammulina velutipes) was introduced into tomato and
tobacco (Kesarwani et al., 2000).
As S. sclerotiorum is one of the most important pathogens
of lettuce, the main goal of this research was to isolate and
to introduce an oxalate decarboxylase gene (oxdc) from a
Flammulina sp. into lettuce plants.
Materials and methods
Isolation of the oxalate decarboxylase gene
An oxalate decarboxylase gene from the edible mushroom
Flammulina sp. was isolated using RT-PCR. The mycelium
of the fungus (isolate IJF 140502, Embrapa Germplasm
Bank) was cultivated on static liquid medium (5% dextrose,
1% peptone, 0·1% KH2PO4, 0·05% MgSO4·7H2O and
1% Difco malt extract, pH 5·2) (Mehta & Datta, 1991)
for 25 days at 25°C. Oxalic acid was added to the culture
at 12·5 mm. After 12 h, total RNA was isolated from 250
mg of mycelium of Flammulina sp. using the Micro-toMidi Total RNA kit (Invitrogen). Total RNA was used to
produce cDNA using the reverse transcriptase Superscript
II (Invitrogen), according to the protocol suggested by the
manufacturer. PCR reaction was carried out in a PTC-100
thermocycler (MJ Research) in 50 µL solution containing
40 ng cDNA, 60 mm Tris–SO4 pH 8·9, 18 mm (NH4)2SO4,
2 mm MgSO4, 250 nm of each dNTP, 200 nm of each
primer and 5 U Platinum Taq DNA Polymerase High
Fidelity (Invitrogen). The mixture was overlaid with
mineral oil, denatured at 94°C (2 min), and subjected to
35 cycles of amplification (94°C for 30 s, 55°C for 30 s,
68°C for 2 min) with a final elongation step of 10 min at
68°C. The primers 5′-TCTAGATGTTCAACAACTTCCAACG-3′ and 5′-GGATCCTCAGTTCACAGGACCAAC-3′ were used to amplify a sequence of 1344 bp,
corresponding to the coding sequence from the oxalate
decarboxylase (oxdc) gene. The sequence was cloned
into pCR2·1TOPO (Invitrogen) to generate the vector
pTOPOOxDc, sequenced by using universal M13 and T7
primers on an automatic sequencer (Applied Biosystems)
and deposited in GenBank (accession no. AY238332).
Plasmid vector
The oxdc coding sequence was removed from pTOPOOxDc
and cloned into the vector pUC19-35SAMVNOS, between
the XbaI and BamHI sites, under the control of the doubled
35S promoter from Cauliflower mosaic virus and a
sequence enhancer from Alfalfa mosaic virus. The pUC1935SAMVNOS vector was derived from the pBI426 (Datla
et al., 1991) in which the gus–nptII gene fusion was
removed with NcoI and SacI, and the NcoI site was deleted
by partial digestion of nuclease S1. The oxdc expression
cassette was removed from the pUC19-35SAMVNOS
vector with PvuII and cloned into the binary vector
pCAMBIA1390 (CAMBIA) in the SmaI site, resulting in
the transformation vector pCambOxDc. The vector
pCambOxDc carries the selectable marker gene htp to
confer hygromycin resistance.
Agrobacterium strain EHA 105, containing the vector
pCambiaOxDc, was used to transform lettuce plants.
Lettuce transformation
The transformation of lettuce cv. Verônica was performed
according to Curtis et al. (1994). Cotyledons from 48-hgerminated seeds were excised, then cocultured with
bacterial suspension for 15 min. Explants were transferred
to MS medium (Murashige & Skoog, 1962) supplemented
with 0·1 mg L −1 6-benzylaminopurine (BAP), 0·1 mg
indolylbutyric acid (IBA), 10 mg hygromycin and 250 mg
cefotaxime L−1. Calluses were transferred to MS medium
containing 0·1 mg BAP L−1 for shoot regeneration.
PCR screening of transformed plants
Plantlets were screened by PCR for the presence of the
oxdc gene. Genomic DNA was isolated from young leaf
discs according to Doyle & Doyle (1987). PCR reactions
were carried out according Aragão et al. (2002). The
primers OXDC 873 (5′-TGGGCTCGACAGAGGAGAAG-3′) and OXDC 371 (5′-CTCGGCAGCAGAATGAGGTC-3′) within the gene oxdc coding sequence were
used to amplify a 502-bp sequence.
Progeny analysis
Seeds of the first generation (R1) of self-pollinated plants
were germinated on half-strength MS medium containing
10 mg hygromycin and 250 mg cefotaxime L−1. χ2 analyses, using the correction factor of Yates (Steel & Torrie,
1980), were performed to determine whether or not the
observed segregation ratio was consistent with a Mendelian ratio (3 : 1 or 15 : 1), with a 95% level of confidence.
Inoculation of transgenic plants with S. sclerotiorum
An isolate of S. sclerotiorum obtained from tomato plants
grown in Guaíra, SP, Brazil and kept at Embrapa Hortaliças (Brasília, DF, Brazil) was used in the experiments.
The fungus was grown on PDA medium (20% potato,
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
85
Resistance to Sclerotinia in transgenic lettuce
2% dextrose, 1·5% agar). Inoculation was carried out
according to Dickson & Hunter (1983). A mycelial agar
plug 2 mm in diameter was cut from the growing margins
of a 2-day-old S. sclerotiorum culture and applied to the
adaxial surface of a leaf detached from a 9-week-old plant
(10 leaves from each transgenic and nontransgenic line).
Symptoms were observed every 12 h and lesion length
recorded. Leaves were kept in a plant growth chamber
(Conviron) at 20°C, 90–100% relative humidity and a
photoperiod (50 µmol m−2 s−1) of 12 h.
RT-PCR expression analysis
Lines P20, P43, P57 and P100 were analysed for the presence of oxdc gene transcripts. Total RNA was extracted
from leaves using the Micro-to-Midi Total RNA kit. The
remaining genomic DNA was eliminated by DNase digestion of the RNA samples. Total RNA was used to produce
cDNA using the reverse transcriptase Superscript II,
according to the protocol suggested by the manufacturer.
PCR reactions were carried out as described above, except
for the following changes: 25 ng cDNA, 1·5 U Taq DNA
polymerase, and amplification cycles of 95°C for 1 min,
57°C for 1 min and 72°C for 1 min, with a final elongation step of 5 min at 72°C. Primers OXDC 873 and
OXDC 371 were used to amplify a sequence within
the oxdc gene. As an internal control, primers rRNA1
(5′-AACGGCTACCACATCCAAGG-3′) and rRNA2C
(5′-TCATTACTCCGATCCCGAAG-3′) were used to
amplify a sequence from the 18S rRNA gene.
Results
The oxalate decarboxylase gene (oxdc) from Flammulina
sp. isolate IJF 140502 showed 99·26% identity when
compared with the GenBank sequence from F. velutipes
(accession AF2000683), revealing differences in only
10 bp. No differences were found in the protein amino
acid sequence.
Out of 80 regenerated plants, 34 lines (42·5%) revealed
the presence of the oxdc gene in the PCR analysis. All
transgenic lines were rooted and acclimatized. Seven lines
showed an abnormal phenotype with smaller leaves and
thinner stems.
All acclimatized transgenic lines (R0 generation) were
allowed to produce seeds. The progeny (R1 generation) of
34 self-fertilized transgenic lines were screened by PCR
analysis for the presence of the oxdc gene (Fig. 1). With
the exception of eight lines (P11, P37, P39, P41, P61, P81,
P82, P88), the R0 plants transferred the foreign gene to the
R1 generation in a Mendelian fashion (Table 1). Twentythree lines presented a segregation ratio of 3 : 1 and three
lines a segregation ratio of 15 : 1.
Detached leaves were inoculated with 2-mm-diameter
agar plugs from growing margins of 2-day-old S. sclerotiorum cultures and lesion length was recorded. Lines P100
and P43 did not show any symptoms (Fig. 2). Although
the mycelium of S. sclerotiorum was able to initiate
growth from the plug and attach to the leaf surface at
189
Figure 1 PCR analysis of putative transformed lettuce lines for
detection of the oxdc gene. Lane 1, positive control (plasmid
pCambiaOxDc); lane 2, nontransgenic plant; lanes 3 –15, transgenic
lines.
Table 1 Segregation analysis in 34 lines of transgenic lettuce
R1 generationa
Line R 0
Positive
Negative
Segregation
ratio tested
χ2
Pb
P1
P2
P3
P5
P6
P11
P14
P17
P19
P20
P21
P22
P23
P37
P39
P40
P41
P42
P43
P48
P54
P57
P58
P59
P61
P63
P81
P82
P88
P99
P100
P101
P102
P103
42
35
42
40
45
20
39
41
35
39
39
41
36
24
44
40
27
41
37
40
37
39
37
37
29
33
5
29
7
33
36
41
32
36
8
15
8
10
4
25
11
6
15
6
11
4
13
25
6
10
22
9
11
8
12
11
12
13
19
17
43
18
41
17
12
9
18
12
3:1
3:1
3:1
3:1
15 : 1
3:1
3:1
15 : 1
3:1
3:1
3:1
15 : 1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
3:1
2·16
0·66
2·16
0·66
0·30
22·41
0·24
3·40
0·66
3·26
0·24
0·56
0·06
17·69
4·51
0·67
10·35
1·31
0·11
1·77
0·01
0·24
0·01
0·03
5·44
2·16
106·77
4·43
93·44
2·16
0·00
1·31
3·22
0·00
0·14
0·41
0·14
0·41
0·58
0·00
0·62
0·07
0·41
0·07
0·62
0·46
0·80
0·00
0·03
0·41
0·01
0·25
0·73
0·18
0·93
0·62
0·93
0·87
0·02
0·14
0·00
0·03
0·00
0·14
1·00
0·25
0·07
1·00
a
Data are based on in vitro tolerance to hygromycin.
3 : 1 or 15 : 1.
inoculation sites of resistant transgenic plants, no colonization of the foliar tissue was observed (Fig. 2c). In contrast, tissue colonization was extensive on nontransgenic
plants (Fig. 2d). Line P57 showed a delay in symptom
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
86
190
B. B. A. Dias et al.
Figure 2 Pathogenesis assay of transgenic
lines P100, P43 and P57 for resistance to
Sclerotinia sclerotiorum. Symptoms were
observed on detached leaves (a) 12; (b) 24 h
after inoculation with 2-mm mycelial agar
plugs. (c) Detail of the mycelium of S.
sclerotiorum initiating growth from the plug and
attaching to the leaf surface at the inoculation
site of a resistant transgenic plant (arrows);
(d) line P43 and damaged susceptible
nontransgenic plants. NT, nontransgenic line.
development compared with the nontransgenic line
(Fig. 2a,b). The progression of disease development in
33 transgenic lettuce lines over a 36-h period is illustrated
(Fig. 3). Except for transgenic lines P57, P43 and P100
(Fig. 3a,d,h, respectively), there were no significant differences in lesion length compared with the controls (nontransgenic plants). Symptoms were more severe for line
P2 at 36 h than for the other lines from its group (Fig. 3c).
As observed in the control plants, in all transgenic susceptible lines the lesions extended across the whole leaf within
48 h (data not shown).
RT-PCR analysis for detection of oxdc gene transcripts
was carried out with three resistant lines (P43, P57, P100)
and one susceptible transgenic line (P20). The resistant
lines showed oxdc gene expression, while line P20 and the
nontransgenic plant did not produce oxdc gene transcripts (Fig. 4). All plants tested displayed similar levels of
expression of the 18S rRNA gene.
Discussion
The expression of the oxalate decarboxylase gene (oxdc)
from Flammulina sp. in lettuce has allowed the produc-
tion of transgenic lines resistant to the necrotrophic
fungus S. sclerotiorum.
With the exception of seven lines, the transgenic plants
produced presented a normal phenotype. Seven transgenic lines showed an abnormal phenotype, with smaller
leaves and narrow stems. Similar results were observed by
Pileggi et al. (2001). These phenotypes may be attributable to somaclonal variation caused by exposure to growth
regulators during callus growth and plant regeneration.
Insertional gene mutation could also be involved. Further
experiments with plasmid rescue should be considered in
order to evaluate this possibility.
The progenies (R1 generation) of self-pollinated transgenic lines were tested for the presence of the oxdc gene.
The analyses indicated that most of the transgenic plants
contained the transgene(s) integrated in a single locus, as
indicated by the 3 : 1 segregation ratio. This is a desirable
property for introducing transgenic plants into a breeding
programme aimed at the development of new cultivars.
Several studies support the concept that most of the
foreign genes introduced by Agrobacterium are normally
transmitted to the progeny (Gelvin, 1998). In this study,
eight lines did not transfer the introduced foreign gene to
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
87
Resistance to Sclerotinia in transgenic lettuce
191
Figure 3 Lesion-length progression following inoculation of detached leaves of 33 transgenic lettuce lines and control with mycelial agar plugs
containing Sclerotinia sclerotiorum. Transgenic lines and control indicated on right border of each block. Bars, SD (n = 10).
Figure 4 RT-PCR for detection of expression of oxdc and 18S rRNA
genes in transgenic lettuce lines. Upper lanes: (1) nontransgenic plant;
(2) P20; (3) P43; (4) P57; (5) P100; (6) plasmid vector used in the PCR
reaction. Lower lanes: lettuce 18S rRNA gene as internal control.
the R1 generation in the Mendelian segregation ratio
expected for self-pollinated plants. An insertional mutation of an essential gene required for ovule fecundation or
development might account for this aberrant inheritance.
In addition, physical transgene elimination has been reported
in several plants and has been attributed to intrachromosomal recombination (Fladung, 1999); genetic instability
resulting from the conditions of tissue culture (Risseeuw
et al., 1997; Joersbo et al., 1999); or a genomic defence
process (Srivastava et al., 1996; Romano et al., 2005).
From the total of 34 putative transgenic lines produced,
only three lines presented resistance to S. sclerotiorum.
The expression of a transgene located in active chromatin
or heterochromatin is highly variable, even among lines
independently transformed with the same construct.
Many factors may be responsible for variable transgene
expression, including the tendency for exogenous DNA
to undergo rearrangement prior to integration, effects
related to the transgene copy number and integration
position, and effects of DNA hypermethylation (Meyer,
1998; Abranches et al., 2000).
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
88
192
B. B. A. Dias et al.
The introduction of genes coding for enzymes able to
degrade oxalic acid in transgenic plants has been successful in generating Sclerotinia-resistant canola (Thompson
et al., 1995); poplar (Liang et al., 2001); tobacco (Berna
& Bernier, 1997; Kesarwani et al., 2000); soybean (Donaldson et al., 2001); sunflower (Burke & Riesenberg,
2003); tomato (Kesarwani et al., 2000); and peanut
(Livingstone et al., 2005). Apparently, only transgenic
soybean and sunflower plants with partial resistance have
so far been tested under field conditions (Burke &
Rieseberg, 2003; Cober et al., 2003). Correlation of
Sclerotinia disease ratings between glasshouse, laboratory
and field evaluations has been reported (Kim et al., 2000).
Although this correlation was inconsistent in some cases
(Vuong et al., 2004), in vivo resistance assays with both
oxalic acid and Sclerotinia mycelium plug inoculation
have consistently been correlated with resistance in the
field (Kesarwani et al., 2000; Kolkman & Kelly, 2000;
Chipps et al., 2005). In soybean, Wegulo et al. (1998)
demonstrated that both mycelial inoculation of detached
leaves and the response of detached stems to oxalic acid
correlated with disease resistance in the field.
RT-PCR analyses revealed the expression of the oxdc
gene in the three resistant lines (P43, P57, P100), while no
oxdc gene transcripts were observed in the susceptible
transgenic and nontransgenic lines analysed. These results
suggest that expression of the oxdc gene is associated with
resistance to Sclerotinia.
The results show that expression of the oxalate decarboxylase gene in a highly susceptible species is efficient in
generating resistance to S. sclerotiorum. The interaction
of Sclerotinia with epidermal cells of transgenic and
nontransgenic lettuce is currently being studied at the
ultrastructural level. This may help to elucidate the
cellular basis of this plant–pathogen interaction. In
addition, studies are being carried out to evaluate the
resistance of lettuce lines under field conditions.
Acknowledgements
We would like to thank Dr Arailde Fontes Urben (Embrapa
Recursos Genéticos e Biotecnologia) and Dr Gilmar Paulo
Henz (Embrapa Hortaliças) for providing the Flammulina
sp. and Sclerotinia isolates, respectively, and Warley
Almeida for his technical assistance. This work was
supported by CNPq (grant number 305441/2004-3).
References
Abranches R, Santos AP, Wegel E, Williams S, Castilho A,
Christou P, Shaw P, Stoger E, 2000. Widely separated
multiple transgene integration sites in wheat chromosomes
are brought together at interphase. The Plant Journal 24,
713–23.
Aragão FJL, Vianna GR, Albino MMC, Rech EL, 2002.
Transgenic dry bean (Phaseolus vulgaris L.) tolerant to the
herbicide glufosinate ammonium. Crop Science 42, 1298–302.
Bateman DF, Beer SV, 1965. Simultaneous production and
synergistic action of oxalic acid and polygalacturonase during
pathogenesis by Sclerotium rolfsii. Phytopathology 55,
204–11.
Berna A, Bernier F, 1997. Regulated expression of wheat germin
gene in tobacco: oxalate oxidase activity and apoplastic
localization of the heterologous protein. Plant Molecular
Biology 33, 417–29.
Boland GJ, Hall R, 1994. Index of plant hosts of Sclerotinia
sclerotiorum. Canadian Journal of Plant Pathology 16,
93–108.
Burke JM, Riesenberg LH, 2003. Fitness effect of transgenic
disease resistance in sunflowers. Science 300, 1250.
Cessna SG, Sears VE, Dickman MB, Low PS, 2000. Oxalic acid,
a pathogenicity factor for Sclerotinia sclerotiorum, suppresses
the oxidative burst of the host plant. The Plant Cell 12, 2191–9.
Chipps TJ, Gilmore B, Myers JR, Stotz HU, 2005. Relationship
between oxalate, oxalate oxidase activity, oxalate sensitivity,
and white mold susceptibility in Phaseolus coccineus.
Phytopathology 95, 292–9.
Cober ER, Rioux S, Rajcan I, Donaldson PA, Simmonds DH,
2003. Partial resistance to white mold in a transgenic soybean
line. Crop Science 43, 92–5.
Curtis IS, Power JB, Blackhall NM, de Laat AMM, Davey MR,
1994. Genotype-independent transformation of lettuce using
Agrobacterium tumefaciens. Journal of Experimental Botany
45, 1441–9.
Datla RS, Hammerlindl JK, Pelcher LE, Crosby WL, Selvaraj G,
1991. A bifunctional fusion between β-glucuronidase and
neomycin phosphotransferase: a broad-spectrum marker
enzyme for plants. Gene 101, 239–46.
Dickson MH, Hunter JE, 1983. Modification of methods for
screening for white mold resistance in greenhouse. Annual
Report of the Bean Improvement Cooperative 26, 85–6.
Donaldson PA, Anderson T, Lane BG, Davidson AL, Simmonds
DH, 2001. Soybean plants expressing an active oligomeric
oxalate oxidase from the wheat gf-2·8 (germin) gene are
resistant to the oxalate-secreting pathogen Sclerotinia
sclerotiorum. Physiological and Molecular Plant Pathology
59, 297–307.
Doyle JJ, Doyle JL, 1987. A rapid DNA isolation procedure for
small quantities of fresh leaf tissue. Phytochemical Bulletin
19, 11–5.
Ferrar PH, Walker JRL, 1993. σ-Diphenol oxidase inhibition –
an additional role for oxalic acid in the phytopathogenic
arsenal of Sclerotinia sclerotiorum and Sclerotium rolfsii.
Physiological and Molecular Plant Pathology 43, 415–22.
Fladung M, 1999. Gene stability in transgenic aspen (Populus).
I. Flanking DNA sequences and T-DNA structure. Molecular
and General Genetics 260, 574 – 81.
Gelvin SB, 1998. The introduction and expression of transgenes
in plants. Current Opinion in Biotechnology 9, 227–32.
Godoy G, Steadman JR, Dickman MB, Dam R, 1990. Use of
mutants to demonstrate the role of oxalic acid in
pathogenicity of Sclerotinia sclerotiorum on Phaseolus
vulgaris. Physiological and Molecular Plant Pathology 37,
179–91.
Joersbo M, Brunstedt J, Marcussen J, Okkels FT, 1999.
Transformation of the endospermous legume guar
(Cyamopsis tetragonoloba L.) and analysis of transgene
transmission. Molecular Breeding 5, 521–9.
Kesarwani M, Azam M, Natarajan K, Mehta A, Datta A, 2000.
Oxalate decarboxylase from Collybia velutipes. Molecular
cloning and its overexpression to confer resistance to fungal
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
89
Resistance to Sclerotinia in transgenic lettuce
infection in transgenic tobacco and tomato. Journal of
Biological Chemistry 275, 7230 – 8.
Kim HS, Hartman GL, Manandhar JB, Graef GL, Steadman JR,
Diers BW, 2000. Reaction of soybean cultivars to sclerotinia
stem rot in field, greenhouse, and laboratory evaluations.
Crop Science 40, 665–9.
Kolkman JM, Kelly JD, 2000. An indirect test using oxalate to
determine physiological resistance to white mold in common
bean. Crop Science 40, 281–5.
Kotsira VP, Clonis YD, 1997. Oxalate oxidase from barley
roots: purification to homogeneity and study of some
molecular, catalytic, and binding properties. Archives of
Biochemistry and Biophysics 340, 239 – 49.
Liang H, Maynard CA, Allen RD, Powell WA, 2001. Increased
Septoria musiva resistance in transgenic hybrid poplar leaves
expressing wheat oxalate oxidase gene. Plant Molecular
Biology 45, 619 –29.
Livingstone DM, Hampton JL, Phipps PM, Grabau EA, 2005.
Enhancing resistance to Sclerotinia minor in peanut by
expressing a barley oxalate oxidase gene. Plant Physiology
137, 1354 – 62.
Lumsden RD, 1976. Pectolytic enzymes of Sclerotinia
sclerotiorum and their localization in infected bean. Canadian
Journal of Botany 54, 2630 – 41.
Magro P, Marciano P, Di Lenna P, 1984. Oxalic acid
production and its role in pathogenesis of Sclerotinia
sclerotiorum. FEMS Microbiology Letters 49, 9–12.
Marciano P, Di Lenna P, Magro P, 1983. Oxalic acid, cell
wall-degrading enzymes and pH in pathogenesis and their
significance in virulence of two Sclerotinia sclerotiorum
isolates on sunflower. Physiological Plant Pathology 22,
339–45.
Mehta A, Datta A, 1991. Oxalate decarboxylase from Collybia
velutipes. Purification, characterization, and cDNA cloning.
Journal of Biological Chemistry 266, 23548–53.
Meyer P, 1998. Stabilities and instabilities in transgene
expression. In: Lindsey K, ed. Transgenic Plant Research.
Chur, Switzerland: Harwood Academic, 263–75.
Murashige T, Skoog F, 1962. A revised medium for rapid
growth and bioassays with tobacco tissue cultures.
Physiologia Plantarum 15, 473–97.
Noyes RD, Hancock JG, 1981. Role of oxalic acid in the
Sclerotinia wilt of sunflower. Physiological Plant Pathology
18, 123–32.
Pileggi M, Pereira AAM, Silva JS, Pileggi SAV, Verma DPS,
2001. An improved method for transformation of lettuce by
193
Agrobacterium tumefaciens with a gene that confers freezing
resistance. Brazilian Archives of Biology and Technology 44,
191– 6.
Reinhardt LA, Svedruzic D, Chang CH, Cleland WW, Richards
NGJ, 2003. Heavy atom isotope effects on the reaction
catalyzed by the oxalate decarboxylase from Bacillus subtilis.
Journal of the American Chemical Society 125, 1244 –52.
Risseeuw E, Franke-van Dijk ME, Hooykaas PJ, 1997. Gene
targeting and instability of Agrobacterium T-DNA loci in the
plant genome. The Plant Journal 11, 717–28.
Romano E, Soares A, Proite K, Neiva S, Grossi M, Faria JC,
Rech EL, Aragão FJL, 2005. Transgene elimination in
genetically modified dry bean and soybean lines. Genetics and
Molecular Research 4, 177–84.
Rowe DE, 1993. Oxalic acid effects in exudates of Sclerotinia
trifoliorum and S. sclerotiorum and potential use in selection.
Crop Science 33, 1146 – 9.
Srivastava V, Vasil V, Vasil IK, 1996. Molecular
characterization of the fate of transgenes in transformed
wheat (Triticum aestivum L.). Theoretical and Applied of
Genetics 92, 1031–7.
Steel RGD, Torrie JH, 1980. Principles and Procedures of
Statistics. New York, USA: McGraw-Hill.
Thompson C, Dunwell JM, Johnstone CE, Lay V, Ray J, Schmitt
M, Watson H, Nisbet G, 1995. Degradation of oxalic acid by
transgenic oilseed rape plants expressing oxalate oxidase.
Euphytica 85, 169–72.
Tu JC, 1997. An integrated control of white mold (Sclerotinia
sclerotiorum) of beans, with emphasis on recent advances in
biological control. Botanical Bulletin of Academia Sinica 38,
73– 6.
Vuong TD, Hoffman DD, Diers BW, Miller JF, Steadman JR,
Hartman GL, 2004. Evaluation of soybean, dry bean, and
sunflower for resistance to Sclerotinia sclerotiorum. Crop
Science 44, 777– 83.
Wegulo SN, Yang XB, Martinson CA, 1998. Soybean cultivar
responses to Sclerotinia sclerotiorum in field and controlled
environment studies. Plant Disease 82, 1264 –70.
Whipps JM, Budge SP, McClement S, Pink DAC, 2002. A
glasshouse cropping method for screening lettuce lines for
resistance to Sclerotinia sclerotiorum. European Journal of
Plant Pathology 108, 373–8.
Young CS, Clarkson JP, Smith JA, Watling M, Phelps K, Whipps
JM, 2004. Environmental conditions influencing Sclerotinia
sclerotiorum infection and disease development in lettuce.
Plant Pathology 53, 387–97.
Plant Pathology (2006). © 2006 The Authors
Journal compilation © 2006 BSPP
90