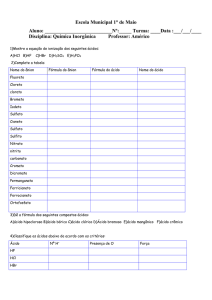
01) (Mackenzie-SP) Um ácido, quanto à força, classificase como forte, moderado e fraco, conforme a escala
de grau de ionização dada abaixo.
Assim, comparando-se o ácido A, cujo grau de
ionização é de 40%, com outro B, no qual, na
ionização de 1 mol de moléculas, somente 2,4 · 1023
moléculas não ionizam, podemos dizer que:
a)
b)
c)
d)
e)
Em qual das soluções, todas com mesma
concentração e temperatura, a lâmpada apresenta
maior brilho?
A é mais forte que B.
A e B são igualmente moderados.
A é tão fraco quanto B.
B é mais forte que A.
B é tão forte quanto A.
a)
b)
c)
d)
e)
02) (PUC-Campinas-SP) A respeito das substâncias
denominadas ácidos, um estudante anotou as
seguintes características:
I.
II.
III.
IV.
05) (FMU-SP) Os nomes dos ácidos abaixo são
respectivamente: HNO3; HClO; H2SO3, H3PO3
têm poder corrosivo;
são capazes de neutralizar bases;
são compostos por dois elementos químicos;
formam soluções aquosas condutoras de
corrente elétrica.
a)
b)
c)
d)
e)
Ele cometeu erros somente em:
a) I e II
b) I e III
c) I e IV
d) II e III
e) III e IV
a)
b)
c)
d)
e)
H2SO4
HI
HNO2
HClO4
H2S
nitroso, clórico, sulfuroso, metafosfórico.
nítrico, clorídrico, sulfúrico, fosfórico.
nítrico, hipocloroso, sulfuroso, fosforoso.
nitroso, perclórico, sulfúrico, fosfórico.
nítrico, cloroso, sulfúrico, hipofosforoso
06) (ACAFE-SC) Os nomes dos ácidos oxigenados
abaixo são respectivamente:
HNO2, HClO3, H2SO3 e H3PO4
a)
b)
c)
d)
e)
03) (Mackenzie-SP) Associe corretamente as duas
colunas e assinale a alternativa correta.
I.
II.
III.
IV.
V.
HF
H2S
H3PO4
H4SiO4
HNO3
(A) hidrácido, monoácido, forte, volátil
(B) hidrácido, diácido, fraco, volátil
(C) oxiácido, monoácido, forte, volátil
(D) oxiácido, diácido, forte, fixo
(E) oxiácido, monoácido, semiforte, volátil
nitroso, clórico, sulfuroso, fosfórico.
nítrico, clorídrico, sulfúrico, fosfórico.
nítrico, hipocloroso, sulfuroso, fosforoso.
nitroso, perclórico, sulfúrico, fosfórico.
nítrico, cloroso, sulfúrico, hipofosforoso.
07) (UFMT-MT) Alguns ácidos oxigenados podem formar
três ácidos com diferentes graus de hidratação. Estes
ácidos recebem prefixos: ORTO, META e PIRO.
O prefixo
apresenta:
I - A; II - B; III - C; IV - D; V - E
I - D; II - B; III - E; IV - C; V - A
I - D; II - A; III - E; IV - C; V - B
I - E; II - D; III - C; IV - B; V - A
I - C; II - A; III - D; IV - E; V - B
a)
b)
c)
d)
e)
04) (UFCE-CE) O esquema a seguir mostra aparelhagem
que pode ser utilizada para testar a força dos ácidos.
ORTO
corresponde
ao
ácido
que
menor teor de água na molécula.
teor de água intermediário entre o META e o PIRO.
maior teor de água na molécula.
teor de água menor que o META.
teor de água menor que o PIRO.
Valério – Material Complementar de Química – 04.05.2015
1
08) (PUC-MG) A tabela apresenta algumas características e
aplicações de alguns ácidos:
Nome do ácido
Ácido muriático
Ácido fosfórico
Ácido sulfúrico
Ácido nítrico
11) (Fuvest-SP)
a) Qual o produto de uso doméstico que contém
ácido acético?
b) Indique quatro espécies químicas (íons,
moléculas) que existem em uma solução aquosa
de ácido acético.
Aplicações e
características
Limpeza doméstica
Usado como acidulante
Desidratante, solução
de bateria
Explosivos
12) (UFPE-PE) Ácido perclórico (HClO4) é um ácido
muito forte. Quais as espécies químicas presentes,
em maior concentração, em uma solução aquosa
deste ácido?
As fórmulas dos ácidos da tabela são, respectivamente:
a)
b)
c)
d)
e)
HCl, H3PO4, H2SO4, HNO3.
HClO, H3PO3, H2SO4, HNO2.
HCl, H3PO3, H2SO4, HNO2.
HClO2, H4P2O7, H2SO3, HNO2.
HClO, H3PO4, H2SO3, HNO3.
a)
b)
c)
d)
e)
09) (ENEM) O processo de industrialização tem gerado
sérios problemas de ordem ambiental, econômica e
social, entre os quais se pode citar a chuva ácida. Os
ácidos usualmente presentes em maiores proporções
na água da chuva são o H2CO3, formado pela reação do
CO2 atmosférico com a água, o
HNO3, o HNO2, o
H2SO4 e o H2SO3. Esses quatro últimos são formados
principalmente a partir da reação da água com os
óxidos de nitrogênio e de enxofre gerados pela queima
de combustíveis fósseis.
A formação de chuva mais ou menos ácida depende
não só da concentração do ácido formado, como
também do tipo de ácido. Essa pode ser uma
informação útil na elaboração de estratégias para
minimizar esse problema ambiental. Se consideradas
concentrações idênticas, quais dos ácidos citados no
texto conferem maior acidez às águas das chuvas?
a)
b)
c)
d)
e)
13) (UEFS-BA)
I. A ionização dos ácidos ocorre em meio aquoso.
II. Os ácidos fortes possuem alto grau de
ionização ( > 50%).
III. O produto da ionização do ácido sulfúrico é: 2 H+ e
SO42Das afirmações estão corretas, somente:
a) I
b) II
c) III
d) I, II
e) I, II, III
14) (UFPE-PE) O ácido hipocloroso é um ácido fraco.
Quais as espécies químicas presentes em maior
concentração em uma solução aquosa (0,1 M) deste
ácido.
HNO3 e HNO2.
H2SO4 e H2SO3.
H2SO3 e HNO2.
H2SO4 e HNO3.
H2CO3 e H2SO3.
a)
b)
c)
d)
e)
10) (Fepcs-DF) Considere as informações abaixo, que
tratam de maneira pela qual se atribuem nomes aos
ácidos inorgânicos.
H+ e ClOH+ e H2O
HClO e H2O
HClO3 e H2O
ClO3- e H+
15) (UFES-ES) Os ânions CℓO3, HPO32-, MnO4 e S2O32- são
respectivamente, denominados:
I. A nomenclatura dos hidrácidos apresenta sufixo
“ídrico”.
II. Na hipótese de um elemento estar presente
exclusivamente em dois oxiácidos, como os do
grupo 5A, aquele cujo elemento central tem maior
número de oxidação, terá sufixo “ico” e o que tem
menor número de oxidação, sufixo “oso”.
III. Na hipótese de um elemento estar presente
exclusivamente em quatro oxiácidos, como os do
grupo 7A, acrescentam-se, ainda, os prefixos “hipo”
e “per” para o menor e maior número de oxidação,
respectivamente.
a) clorato, fosfito, permanganato e tiossulfato.
b) perclorato, fosfito, manganato e tiossulfato.
c) perclorato,
pirofosfato,
permanganato
e
persulfato.
d) hipoclorito, fosfito, manganato, tiossulfato.
e) clorato, pirofosfato, permanganato e persulfato.
16) (FGV-SP) Uma solução obtida pela adição de sulfato
de alumínio e nitrato de amônio sólidos em água
contém os íons NH4+(aq), Aℓ3+(aq), SO42-(aq) e NO3(aq).
Assim sendo, assinale a opção na qual a
nomenclatura corresponde corretamente à fórmula
do ácido.
a)
b)
c)
d)
e)
H+ e ClO4HClO4 e H+
HClO4 e OHH+, Cl- e O2
OH-, Cl- e O2
As citadas substâncias podem ser representadas
pelas fórmulas
HCN – ácido ciânico
HBrO – ácido hipobromídrico
H3PO4 – ácido fosforoso
HClO4 – ácido percloroso
HNO3 – ácido nítrico
a)
b)
c)
d)
e)
AℓSO4 e (NH4)3NO3
Aℓ2SO4 e (NH4)3NO
Aℓ2(SO4)3 e NH4NO3
Aℓ3SO4 e NH4NO3
Aℓ3(SO4)2 e NH4(NO3)2
Valério – Material Complementar de Química – 04.05.2015
2
17) (UNESP-SP) Sobre o ácido fosfórico, são feitas as
cinco afirmações seguintes.
20) (Cesgranrio-RJ) Um elemento de grande importância
do subgrupo VA é o fósforo, que ocorre na natureza,
principalmente nos minérios da apatita. Como não é
encontrado
isolado,
costuma
ser
obtido
industrialmente através da redução da rocha
fosfática, mediante carvão e areia num forno elétrico.
I. Tem fórmula molecular H3PO4 e fórmula estrutural.
2 Ca3(PO4)2 + 6 SiO2 + 10C → P4 + 6 CaSiO3 + 10 CO
A partir da variedade alotrópica obtida do fósforo,
um grande número de compostos podem ser
produzidos, como no caso do anidrido fosfórico,
segundo a reação a seguir:
II. É um ácido triprótico cuja molécula libera três íons
H+ em água.
III. Os três hidrogênios podem ser substituídos por
grupos orgânicos formando ésteres.
IV. É um ácido tóxico que libera, quando aquecido,
PH3 gasoso de odor irritante.
V. Reage com bases para formar sais chamados
fosfatos.
P4 + 5 O2 → 2 P2O5
O P2O5 pode reagir com uma, duas e três moléculas
de água, de acordo com as seguintes reações:
Dessas afirmações, estão corretas:
a) I e II, somente.
b) II, III e IV, somente.
c) I e V, somente.
d) III e V, somente.
e) I, II, III e V, somente.
P2O5 + H2O → 2 HPO3
P2O5 + 2 H2O → H4P2O7
P2O5 + 3 H2O → 2 H3PO4
Com base nos ácidos obtidos, é correto afirmar que
a molécula de:
18) (UFSM-RS) Analise as seguintes afirmativas:
I. HClO3 possui duas ligações covalentes normais e
duas ligações dativas.
II. H3PO3 apresenta apenas ligações covalentes
simples.
III. H2SO4 possui seis ligações covalentes normais e
uma ligação dativa.
a) HPO3 apresenta 4 ligações covalentes simples e
1 ligação covalente dativa.
b) HPO3 apresenta 3 ligações covalentes simples e
1 ligação covalente dativa.
c) H3PO4 apresenta 3 ligações covalentes simples e
1 ligação covalente dativa.
d) H4P2O7 apresenta 6 ligações covalentes simples
e 2 ligações covalentes dativas.
e) H4P2O7 apresenta 10 ligações covalentes simples
e 4 ligações covalentes dativas.
Está(ão) correta(s)
a) I apenas.
b) II apenas.
c) III apenas.
d) I e II apenas.
e) I e III apenas.
21) Na experiência abaixo, compare o brilho das
lâmpadas quando os eletrodos estiverem
mergulhados em soluções aquosas de:
19) (EXERCICIO REPETIDO N° 17)(UNESP-SP) Sobre o
ácido fosfórico, são feitas as cinco afirmações
seguintes.
a)
b)
c)
d)
I. Tem fórmula molecular H3PO4 e fórmula estrutural.
NaOH
NH4OH
C6H12O6
H3C-CH2-OH
22) (UMC-SP) A equação que representa corretamente a
dissociação iônica de uma substância de fórmula
M(OH)x é:
II. É um ácido triprótico cuja molécula libera três íons
H+ em água.
III. Os três hidrogênios podem ser substituídos por
grupos orgânicos formando ésteres.
IV. É um ácido tóxico que libera, quando aquecido,
PH3 gasoso de odor irritante.
V. Reage com bases para formar sais chamados
fosfatos.
a)
b)
c)
d)
M(OH)x M1+ + x OH1M(OH)x x M1+ + x OH1M(OH)x Mx+ + x OH1M(OH)x MX+ + x OHX1-
23) Classifique as bases, quanto à força, nº de OH1- e a
solubilidade em água.
Dessas afirmações, estão corretas:
a) I e II, somente.
b) II, III e IV, somente.
c) I e V, somente.
d) III e V, somente.
e) I, II, III e V, somente.
a)
b)
c)
d)
Valério – Material Complementar de Química – 04.05.2015
3
CsOH
Sr(OH)2
Sn(OH)4
NH4OH
28) (UFG-GO)
24) (Osec-SP) Uma base forte deve ter o grupo OH–
ligado a um:
a)
b)
c)
d)
e)
SANGUE DE MENTIRINHA!
De tanto assistir a filmes de terror, ou mesmo a filmes
de ação, nos quais o mocinho tem sempre que apanhar
primeiro, cabe sempre uma constatação e ao mesmo
tempo uma pergunta: "Nossa, quanto sangue!". É claro,
tudo é de mentirinha mas, na maioria das vezes (quando
não há efeitos especiais), os diretores de filmes recorrem
ao velho truque do sangue-de-mentirinha.
Uma forma de fazê-lo, sem manchar roupas, é medir
6 mL de água e 1 mL de detergente com amoníaco
(amônia) e adicionar, com um conta-gotas, de 2 a 3 gotas
de fenolftaleína, e colocar a solução num frasco de spray
(do tipo desodorante). Ao borrifar a mistura num tecido
branco, ele fica imediatamente manchado de vermelho.
Aos poucos a mancha desaparece.
elemento muito eletropositivo.
elemento muito eletronegativo.
semimetal.
metal que forneça 3 elétrons.
ametal.
25) Qual das afirmativas abaixo se aplica ao hidróxido de
amônio?
a) É uma base forte, solúvel em água destilada e
bem estável em temperaturas altas.
b) É uma base fraca, pouco solúvel em água
destilada, mas muito estável em função da atração
elétrica entre os íons NH41+ e OH1-.
c) A molécula do hidróxido de amônio é fortemente
polar, tem geometria tetraédrica, com a oxidrila
ocupando o centro do tetraedro.
d) Na prática, quando se fala do grau de ionização
do hidróxido de amônio, refere-se, portanto, ao
grau de ionização do NH3.
e) É a única base da química inorgânica que,
dissolvida em água, origina um meio neutro em
função da volatilidade da amônia.
Disponível em: <http://www.geocities.com/CollegePark/Bookstore/2334/sangue.htmladaptado>
a) Escreva a equação química que descreve o
processo, explicando o fenômeno relatado.
b) Explique o que ocorreria se a peça de roupa em
questão fosse lavada com sabão sem antes ser
lavada somente com água.
29) Considere a ionização total do ácido fosfórico
(H3PO4):
H3PO4 3 H1++ PO43Identifique a alternativa que apresenta uma base que,
na sua dissociação total, produz o mesmo número de
íons, por fórmula, que o ácido fosfórico:
26) Escreva as fórmulas de:
a)
b)
c)
d)
e)
f)
g)
h)
i)
j)
a)
b)
c)
d)
e)
hidróxido de sódio.
hidróxido de cálcio.
hidróxido de níquel II.
hidróxido áurico.
hidróxido cuproso.
hidróxido cúprico.
hidróxido de estanho II.
hidróxido de estanho IV.
hidróxido de amônio.
hidróxido de alumínio.
30) (UFPB) A reação do sódio com a água ocorre
segundo a equação:
Na(s) + H2O(ℓ) NaOH(aq) + H2(g)
A partir da informação apresentada, é correto afirmar:
a) A equação esta devidamente balanceada.
b) A reação do sódio com a água é de síntese.
c) A reação do sódio com a água é de redução.
d) Os produtos da reação são hidróxido de sódio e
hidrogênio.
e) Os produtos da reação são, respectivamente, uma
substancia metálica e uma covalente.
27) (FEI-SP) Num recipiente contendo uma solução
aquosa de uma substância A, foram adicionadas
gotas de fenolftaleína dando uma coloração rósea.
Adicionando-se uma substância B em A, a solução
apresenta-se incolor. Com base nessas informações,
podemos afirmar que:
a)
b)
c)
d)
e)
hidróxido de sódio.
hidróxido de cálcio.
hidróxido de prata.
hidróxido de alumínio.
hidróxido de bário.
GABARITO:
01) B
16) C
30) C
02) B
17) E
03) C
18) A
04) E
19) E
05) C
20) A
06) A
21) B
07) C
22) D
08) A
23) H2SO4 + 2H2O ⇌ 2H+ SO42-, ou H2SO4 ⇌ 2H+ + SO4209) D
24) A
10) E
25) 15
11) a) Vinagre
b) CH3COOH + H2O
H3O+ + CH3COO12) A
26) 15
13) E
27) D
14) C
28) B
15) A
29) D
A e B são bases.
A é um ácido e B é uma base.
A é uma base e B é um ácido.
A e B são ácidos.
A e B são sais neutros.
Valério – Material Complementar de Química – 04.05.2015
4