número 26- setembro/2016
DECISÃO FINAL
RELATÓRIO PARA A
SOCIEDADE
informações sobre recomendações de incorporação de medicamentos e outras tecnologias no SUS
VERUPREVIR, OMBITASVIR, DASABUVIR
E RITONAVIR PARA HEPATITE CRÔNICA
TIPO C - GENÓTIPO 1
RELATÓRIO PARA A SOCIEDADE
Este relatório é uma versão resumida do relatório técnico da Comissão Nacional de
Incorporação de Tecnologias no SUS – CONITEC e foi elaborado numa linguagem simples, de
fácil compreensão, para estimular a participação da sociedade no processo de avaliação de
tecnologias em saúde que antecede a incorporação, exclusão ou alteração de medicamentos,
produtos e procedimentos utilizados no SUS.
Todas as recomendações da CONITEC são submetidas à consulta pública pelo prazo de
20 dias. Após analisar as contribuições recebidas na consulta pública, a CONITEC emite a
recomendação final, que pode ser a favor ou contra a incorporação/exclusão/alteração da
tecnologia analisada.
A recomendação da CONITEC é, então, encaminhada ao Secretário de Ciência, Tecnologia
e Insumos Estratégicos do Ministério da Saúde, que decide sobre quais medicamentos,
produtos e procedimentos serão disponibilizados no SUS.
Para saber mais sobre a CONITEC, acesse<conitec.gov.br>
HEPATITE C
As hepatites virais estão entre as principais causas de transplantes de fígado no mundo – com destaque
para a hepatite C (HCV), que hoje supõe-se que afete mais de 185 milhões de pessoas em todos os continentes.
A agressão às células do fígado causada pelo vírus da hepatite C pode levar a alterações importantes na
estrutura e função do fígado (o que é chamado de fibrose e cirrose, respectivamente) e até câncer de fígado.
Nas fases avançadas, pode até levar à morte. Pessoas que receberam transfusão de sangue total ou frações
antes de 1993, pessoas que compartilham seringas e agulhas (como usuários de drogas injetáveis), usuários
de cocaína inalada, pessoas com tatuagem e piercing têm maior risco de infecção pelo HCV. Na fase aguda
(até seis meses após a infecção), cerca de 80% dos casos não apresentam sintomas, o que dificulta o
diagnóstico. Após isso, podem aparecer sintomas como dor abdominal, cor amarelada da pele e olhos, coceira,
urina escura, fezes claras e dores nas articulações. Normalmente a hepatite C é diagnosticada em sua fase
crônica (a partir de seis meses após a infecção), por meio de exames de sangue.
olhos
amarelados
pele
amarelada
s
i
n
e
t
o
s
m
i
a
a
n
s
i
s
s
n
u
g
al
dor
abdominal
urina escura/
fezes claras
dores nas
articulações
coceira
COMO O SUS TRATA OS PACIENTES
COM HEPATITE CRÔNICA TIPO C- GENÓTIPO 1
O Ministério da Saúde atualiza frequentemente seu protocolo de tratamento conforme novos medicamentos vão sendo
incorporados às listas do SUS. A última atualização do PCDT de Hepatite viral C e co-infecções, em julho de 2015,
incluiu os medicamentos sofosbuvir, simeprevir e sofosbuvir e daclatasvir priorizando-se os indivíduos com fibrose
hepática avançada (METAVIR F3 ou F4). Com essa atualização, foi possível substituir novos tratamentos por outros
que não estavam apresentando as taxas de sucesso desejadas, além de encurtar o tempo de tratamento, trazer maior
comodidade no uso pelo paciente e reduzir os efeitos indesejáveis.
MEDICAMENTOS ANALISADOS
VERUPREVIR, OMBITASVIR, DASABUVIR E RITONAVIR
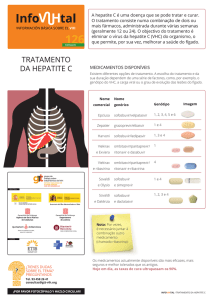
Os medicamentos analisados são utilizados no tratamento da hepatite C de forma associada, o que garante uma
melhor resposta do tratamento, do que se usados isoladamente, pois cada um age de uma forma diferente, o que
aumenta o sucesso do tratamento. O ombitasvir, veruprevir e ritonavir estão disponíveis em um mesmo comprimido,
ao passo que o dasabuvir encontra-se em outro, que deve ser tomado logo em seguida ao primeiro. Eles são utilizados
apenas em pacientes que apresentam o genótipo 1 da doença. Este é o genótipo mais prevalente nas pessoas com
Hepatite C no Brasil.
A Conitec já havia feito uma avaliação deste esquema de tratamento no final de 2015, onde recomendou
desfavoravelmente pela incorporação, por não haver dados suficientes fora do ambiente da pesquisa clínica, ou
seja, na vida real. Contudo, entre a última avaliação até agora, foram publicados diversos estudos de vida real que
comprovaram os benefícios já identificados na fase de pesquisa clínica, assim como informações sobre a segurança
destes medicamentos.
Os estudos avaliaram a resposta virológica sustentada (RVS), ou seja, a negativação do vírus causador da Hepatite C
três meses após o término do tratamento, e a análise destes estudos pela Conitec considerou os diversos grupos de
pacientes, de acordo com suas características: indivíduos não tratados previamente; indivíduos falhos de tratamento
prévio com peginterferon e ribavirina; falhos de tratamento prévio com telaprevir, boceprevir, simeprevir; falhos de
tratamento prévio com sofosbuvir e associações; indivíduos co-infectados pelo HIV/HCV; indivíduos com doença
hepática avançada (cirrose descompensada) e indivíduos que se submeteram a transplante hepático e indivíduos
com doença renal crônica avançada.
A análise concluiu que estes medicamentos têm eficácia semelhante aos medicamentos já incorporados ao SUS no
tratamento da Hepatite C. Considerando também a segurança do seu uso, foi concluído que podem se apresentar como
uma alternativa eficaz aos pacientes do genótipo 1(cerca de 65% dos casos de Hepatite C), principalmente aqueles
com grau F3 e F4, ou seja, aqueles que com fibrose hepática avançada e cirrose compensada.
Além disso, nesta segunda proposta, o custo do tratamento tornou-se mais adequado, pois leva a uma redução de
custos de 6 a 29% em relação ao tratamento vigente, a depender da gravidade da fibrose ou cirrose hepática. Assim,
além de ser mais uma opção terapêutica no tratamento, poderá trazer economia de recursos ao SUS, nos casos em
que esta opção for indicada.
QUAL A RECOMENDAÇÃO INICIAL DA CONITEC
Neste novo pedido, considerando o balanço favorável de riscos e benefícios e os custos associados aos tratamentos
propostos, a CONITEC recomendou inicialmente a incorporação no SUS dos medicamentos veruprevir, ombitasvir e
dasabuvir e ritonavir para o tratamento da hepatite viral C, conforme revisão do protocolo clínico e diretrizes terapêuticas.
A recomendação foi disponibilizada em consulta pública por 20 dias.
RESULTADO DA CONSULTA PÚBLICA
Foram recebidas 127 contribuições. A maioria das contribuições foram de apoio à recomendação da Conitec. Algumas
contribuições solicitavam a ampliação do tratamento a outros grupos de pacientes, em estágios menos grave
da doença, e algumas delas traziam experiências positivas de pessoas que já utilizaram o tratamento que está
sendo avaliado.
RECOMENDAÇÃO FINAL DA CONITEC
Os membros da CONITEC presentes na 49º reunião do plenário da Conitec no dia 06/10/2016 recomendaram a inclusão
do ombitasvir, veruprevir, ritonavir, e dasabuvir para o tratamento de Hepatite C crônica causada pelo genótipo 1
em indivíduos com fibrose avançada e cirrose no SUS, conforme Protocolo Clínico e Diretrizes Terapêuticas do
Ministério da Saúde.
DECISÃO FINAL
Com base na recomendação da CONITEC, o Secretário de Ciência, Tecnologia e Insumos Estratégicos do Ministério
da Saúde, no uso de suas atribuições legais, decidiu incorporar o ombitasvir, veruprevir, ritonavir e dasabuvir para o
tratamento da Hepatite C crônica causada pelo genótipo 1 em indivíduos com fibrose avançada e cirrose, conforme
Protocolo Clínico e Diretrizes Terapêuticas do Ministério da Saúde, no âmbito do Sistema Único de Saúde - SUS.
O relatório técnico completo de recomendação da CONITEC está disponível em:
http://conitec.gov.br/images/Relatorios/2016/Relatorio_ViekiraPak_HepatiteC_final.pdf
http://conitec.gov.br/