Ensino Secundário – 10º ano de escolaridade
Componente de Química
Banco de Questões nº 1
Módulo Inicial – Materiais: diversidade e constituição
Grupo I
1. No laboratório, encontras vários frascos com substâncias químicas. O que significam os seguintes
símbolos de segurança:
(A)
(B)
(C)
A Substâncias corrosivas, inflamáveis, explosivas e
irritantes.
B
(D)
Substâncias corrosivas, nocivas, explosivas e
irritantes.
C Substâncias corrosivas, inflamáveis, nocivas e
explosivas.
D
Substâncias corrosivas, perigosas, nocivas e
explosivas.
2. Vais utilizar um frasco no laboratório como o da figura a seguir. Os cuidados que deves ter são:
A Movimentar com cuidado. Não é necessário o uso
de luvas.
B Manusear com luvas e não permitir o contacto com
a roupa. Nunca respirar os vapores.
C Não é necessário ter cuidados relativamente a D Evitar choques ou colisões com o frasco. Manusear
ventilação. Manusear com luvas.
3. Faz as respectivas associações:
(A) Comportamento no laboratório.
(B)
Utilização de material.
(C)
Utilização
de
com luvas.
(1)
Nunca verificar se um material está “quente” com as
mãos.
(2)
Usar bata.
substâncias (3)
Não correr.
químicas.
(D)
Vestuário no laboratório.
QuÝmica 10 ano BQ1.doc
(4)
Segurar com firmeza os frascos de substâncias químicas.
Utilizar sempre as duas mãos.
(5)
Utilizar óculos de protecção quando manusear substâncias
explosivas, nocivas ou inflamáveis.
(6)
Manter os espaços da área de trabalho livres.
(7)
Ler com atenção o rótulo dos frascos das substâncias
químicas.
NetProf
-1-
Ensino Secundário – 10º ano de escolaridade
Componente de Química
4. Identifica os materiais de laboratório que se seguem:
(A)
(B)
(C)
(D)
(E)
(F)
(G)
(H)
(I)
(J)
(K)
(L)
5. A fotólise é:
(A)
Uma transformação química por acção do calor.
(B)
Uma transformação química por acção da corrente eléctrica.
(C)
Uma transformação química por acção da luz.
(D)
Uma transformação física por acção da luz.
(E)
Uma transformação física por acção do calor.
6. Quanto aos gases, podemos afirmar que:
(A)
Possuem forma definida e os seus corpúsculos estão muito próximos uns dos outros.
(B)
Não têm forma definida e os seus corpúsculos estão muito próximos uns dos outros.
(C)
Não têm forma definida e os seus corpúsculos estão muito afastados uns dos outros.
(D)
Apresentam volume constante e os seus corpúsculos estão muito afastados uns dos outros.
(E)
Apresentam volume constante e os seus corpúsculos estão muito próximos uns dos outros.
7. Duas técnicas experimentais que permitem confirmar a constituição atómica da matéria, são:
QuÝmica 10 ano BQ1.doc
NetProf
-2-
Ensino Secundário – 10º ano de escolaridade
Componente de Química
(A)
A cromatografia e a destilação simples.
(B)
A difracção de raios X e a microscopia electrónica de alta resolução.
(C)
A refracção atmosférica e a determinação do ponto de fusão.
(D)
A destilação fraccionada e a cromatografia em fase gasosa.
(E)
A magnetização e extracção por solvente.
8. Os protões e os electrões, além da massa, possuem uma outra propriedade da matéria denominada:
(A)
Velocidade.
(B)
Carga eléctrica.
(C)
Aceleração.
(D)
Energia.
(E)
Força.
9. Substâncias elementares:
(A)
São substâncias formadas apenas por um “tipo” de átomo.
(B)
São substâncias formadas por vários “tipos” de átomos.
(C)
São substâncias sem electrões.
(D)
São substâncias sem protões.
(E)
São substâncias que perderam electrões.
10. A electroforese é um processo que permite comprovar a existência de:
(A)
Moléculas.
(B)
Gases.
(C)
Sólidos.
(D)
Substâncias que perderam os seus protões.
(E)
Iões.
11 – Das afirmações que se seguem, assinale a correcta.
A Os átomos são partículas de grandes dimensões que
formam todas as substâncias da natureza.
B Os núcleos dos átomos são neutros, e à volta do
átomo há partículas de cargas eléctricas positivas.
C Os átomos são constituídos por uma região, uma
D O átomo é formado de partículas neutras.
espécie de nuvem, onde encontramos os electrões, de
carga negativa, à volta de um núcleo com carga positiva.
E A massa do electrão é maior que a massa do protão.
QuÝmica 10 ano BQ1.doc
NetProf
-3-
Ensino Secundário – 10º ano de escolaridade
Componente de Química
12 – O que caracteriza um elemento químico é:
A O seu número de massa.
B O seu número de neutrões.
C O seu número de electrões.
D O seu número de protões.
E O seu número de variedades.
13 – O electrão, o núcleo e o neutrão foram descobertos, respectivamente, por:
A Planck, Rutherford e Bohr.
B Ruhterford, Thomson e Einstein.
C Einstein, Bohr e Rutherford.
D Thomson, Rutherford e Chadwick
E Thomson, Bohr e Chadwick.
14 – Isótopos são:
A Átomos de um mesmo elemento químico, só que
com diferente número de electrões.
B Átomos de um mesmo elemento químico, só que
com diferente número de massa.
C Átomos de um mesmo elemento químico, só que
com diferente número de protões
D Átomos que possuem o mesmo número de
neutrões.
E Átomos que possuem o mesmo número de massa.
15 – A massa atómica relativa de um átomo indica:
A A massa que esse átomo possui quando comparado
com o quilograma padrão.
B A massa que esse átomo possui relativamente ao
electrão.
C A massa desse átomo relativa à massa da água.
D A massa desse átomo relativa ao hidrogénio.
E O número de vezes que a massa desse átomo é
superior à massa do átomo que se toma por comparação.
16 – Seleccione a afirmação correcta:
A As moléculas de substâncias elementares são B A fórmula química da molécula de água é H2O2.
formadas por átomos de mais do que um elemento
químico.
C As
moléculas
de substâncias compostas
formadas por átomos de um único elemento químico.
são D A fórmula química duma substância nos indica
os elementos químicos que constituem a substância e
o número de átomos de cada elemento presente na
molécula.
E A fórmula química da molécula de Bromo é Br.
17 – Considere as moléculas de F2, H2O e NH3. Quanto a geometria molecular dessas moléculas, podemos
afirmar que:
QuÝmica 10 ano BQ1.doc
NetProf
-4-
Ensino Secundário – 10º ano de escolaridade
Componente de Química
A F2 é angular, H2O é triangular plana e NH3 é
B F2 é linear, H2O é angular e NH3 é piramidal.
piramidal.
C F2 é angular H2O é angular e NH3 é tetraédrica.
D F2 é linear, H2O é piramidal e NH3 é tetraédrica.
E F2 é linear, H2O é linear e NH3 é piramidal.
18 – Considere a tabela periódica:
1
18
2
13 14 15 16 17 He
1º H
2º Li Be
B
C
N
O
F
Ne
3º Na Mg 3
4
5
6
7
8
9
10
11
12 Aℓ Si
P
S
Cℓ Ar
4º K Ca Sc Ti V Cr Mn Fe Co Ni
Cu
Zn Ga Ge As Se Br Kr
5º Rb Sr Y Zr Nb Mo Tc Ru Rh Pd
Ag
Cd In
Sn Sb Te
I
Xe
6º Cs Ba La Hf Ta W Re Os Ir
Pt
Au Hg Tℓ Pb Bi Po At Rn
7º Fr Ra Ac Rf Db Sg Bh Hs Mt Uun Uuu Uub
Uuq
Uuh
Uuo
18.1 O primeiro e segundo grupos da tabela periódica são os grupos dos:
A Metais alcalinos e halogéneos.
B Gases Nobres e metais alcalino-terrosos.
C Matais alcalinos e metais alcalinos terrosos.
D Halogéneos e gases nobres.
E Calcogéneos e halogéneos.
18.2 O primeiro período da tabela periódica contém apenas os elementos:
A Li e Be.
B H e He.
C He e Ne.
D Aℓ e Cℓ
E Na e Mg.
18.3 Dos elementos do grupo 1 uma das suas características é:
A Possuírem a mesma massa.
B Possuírem apenas um electrão de valência.
C Possuírem o mesmo número de neutrões.
D Não reagirem com nenhum outro elemento
químico.
E Não formarem iões.
Grupo II
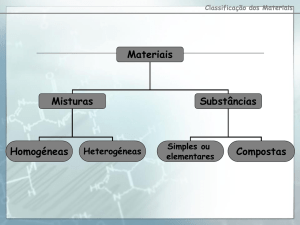
I. Há vários critérios para a classificação dos materiais. Completa os espaços abaixo com a chave:
Natural – manufacturado – sólido – líquida – gasosa – orgânica – inorgânica – combustível – incombustível
– solúvel – insolúvel.
(A) O açúcar é ____________ em água. Para além deste facto, o açúcar é um material ____________, ao
contrário do sal de cozinha que é ____________.
(B) O ar que respiramos é ___________, o solo que pisamos é __________ e a água que bebemos é
_____________.
QuÝmica 10 ano BQ1.doc
NetProf
-5-
Ensino Secundário – 10º ano de escolaridade
Componente de Química
(C) A terra é ______________ em água. As árvores que plantamos na terra fornecem madeira, que é um
material _______________, ao contrário da própria terra que é __________________.
(D) O minério a parir do qual extraímos o ferro, é um material ______________. O aço que utiliza ferro na
sua composição é um material ________________.
II. Considera os elementos químicos:
3
1
H
2
1
H 11 H
40
20
Ca
235
92
U
238
92
U
II.1 Indica os nomes desses elementos químicos.
II.2 Indica justificando quais são isótopos.
II.3 Determina o número de neutrões do cálcio.
II.4 Quantos electrões possui o átomo de cálcio neutro?
II.5 Tendo em conta a tabela periódica da questão 8 do grupo I, o cálcio possui quantos electrões de
valência?
2+
II.6 Quantos electrões possui o ião 40
?
20 Ca
II.7
III. Dadas as massas atómicas relativas dos seguintes elementos:
Ar(H) = 1,0; Ar(S) = 32,1; Ar(O) = 16,0; Ar(Aℓ) = 27,0; Ar(Cℓ) = 35,5; Ar(K) = 39,1; Ar(C) = 12,0.
Determina a massa molecular relativa das seguintes moléculas:
III.1 Mr(H2SO4);
III.2 Mr(CCℓ4);
III.3 Mr(Aℓ2O3);
III.4 Mr(KOH);
III.5 Mr(H2O2);
IV. Considera o esquema a seguir representativo da tabela periódica. As letras representadas nas “casas” não
são símbolos de elementos químicos.
1
18
13 14 15 16 17
2
k q
x
3 4 5 6 7 8 9 10 11 12
b
y
w
a d
f
Utiliza a tabela da questão 8 do grupo I e responde:
IV.1 Indica as letras que representam metais alcalinos e alcalino-terrosos.
IV.2 Indica a letra que está na casa do zinco.
IV.3 Indica a letra que está na “casa” do grupo dos gases nobres.
IV.4 Indica a letra que está na casa do grupo dos halogéneos.
IV.5 Qual é a letra que representa o elemento com menor número atómico?
IV.6 Qual é a letra que representa o elemento com maior número atómico?
QuÝmica 10 ano BQ1.doc
NetProf
-6-