54
CAPÍTULO 3
HEMOGLOBINAS NORMAIS
A ORIGEM E EVOLUÇÃO DAS HEMOGLOBINAS
A origem da hemoglobina e seu processo evolutivo está relacionado
com o desenvolvimento de vida em nosso planeta. A primeira evidência científica de
vida na Terra foi obtida por meio de análises de sedimentos da Groelândia que
indicaram por métodos indiretos de isótopo de carbono
(C12) que as rochas
continham componentes orgânicos datados de aproximadamente 3,8 bilhões de
anos. Fósseis de colônias bacterianas datados de 3 bilhões de anos foram
encontrados nos mares do Caribe e do oeste da Austrália, indicando efetiva
organização de microorganismos ao longo desse tempo.
Animais e plantas não microscópicos emergiram do mar há 800
milhões de anos e se desenvolveram no solo há 400 milhões de anos. Estudos
efetuados em plantas leguminosas, leveduras e paramécio, revelaram que os genes
codificadores para hemoglobinas devem ter se manifestado há cerca de 800
milhões de anos. É provável que neste período as moléculas de hemoglobinas
primitivas surgiram como subprodutos resultantes da formação de citocromo c- uma
proteína pigmentada essencial para a respiração celular. Pesquisas realizadas com
o objetivo de avaliar a evolução de genes codificadores de proteínas (ou exons)
mostraram que em plantas leguminosas, essas proteínas conhecidas por
leghemoglobinas, tinham quatro exons (ou genes codificadores) entremeados por
três introns (estrutura do DNA sem capacidade de codificar), em um mesmo
cromossomo, conforme mostra a etapa 1 da figura 29. Os estudos feitos em
algumas espécies de peixes primitivos mostraram que houve a redução para três
genes codificadores de hemoglobina num mesmo cromossomo, caracterizado por
três exons entremeados por dois introns (etapa 2 da figura 29), fato sugestivo de
que esses peixes primitivos divergiram durante o processo evolutivo dos
vertebrados que tiveram a duplicação de cromossomos (etapa 3 da figura 29).
Acredita-se que essa duplicação se manteve por muito tempo, pois há 500 milhões
55
de anos duas cópias se diferenciaram por mutações adaptativas para formar dois
grupos de exons denominados por alfa e beta, e agrupados em um único
cromossomo (etapa 4 da figura 29). Outros milhões de anos seguintes fizeram com
que o processo evolutivo desenvolvido por meio de transposição ou translocação,
duplicasse o cromossomo em dois cromossomos com características específicas:
um com genes alfa e outro com genes beta (etapa 5 da figura 29). Por volta de 100
milhões de anos os genes codificadores de globinas alfa e beta se diferenciaram
individualmente para se processarem durante as fases de desenvolvimento de um
ser mais complexo, caracterizadas pelas diferenças morfo-funcionais que ocorreram
nos períodos embrionário, fetal e pós-nascimento (etapa 6 da figura 29). Assim, por
volta de 70 milhões de anos quando surgiram os primeiros primatas, identificados
pelo Ancestral Hominídeo Comum, os genes para a síntese de globinas alfa e beta
já estavam bem definidos (etapa 7 da figura 29).
Esses primatas primitivos demoraram quase 60 milhões de anos para
se desenvolverem e se diferenciarem em dois sub-grupos: o Ancestral HumanoChimpanzé e os gorilas. Pesquisas realizadas nos diferentes continentes mostraram
que a África certamente foi o local em que os primatas evoluíram para o bipedismo,
entre 5 e 10 milhões de anos. Por volta de 4 milhões de anos surge o
Australopithecus africanus com características morfológicas de chimpanzé e
humana.
Entre 2,5 e 1,6 milhões de anos surgiu o Homo habilis que conviveu
com
o
Australopithecus.
Nessa
fase
ocorreram
expressivas
mudanças
morfológicas especialmente na estrutura da cabeça e face. Por volta de 1,5 milhões
de anos destaca-se o aparecimento do Homo ergaster, também na África, e desse
ancestral partem duas linhagens bem definidas, a do Homo erectus que viveu
exclusivamente na África e o Homo heidelbergensis cujos fósseis foram
encontrados na África, Ásia e Europa. Ambos apresentam diferenças morfológicas
em relação ao ancestral comum (H. ergaster) evidenciadas pelos alongamentos da
cabeça e das pernas.
Proveniente do H. heidelbergensis, surgiram há 100 mil anos o
Homo sapiens neanderthalis, e há 40 mil anos o Homo sapiens sapiens. A figura
30 mostra o resumo da árvore genealógica da espécie humana. É fundamental que
seja destacado que durante todo o processo da evolução da espécie humana,
desde o Ancestral Hominídeo Comum (há 70 milhões de anos) até o Ancestral
56
Humano-Chimpanzé (há 4 milhões de anos) a molécula de hemoglobina se
diferenciou em apenas um aminoácido na posição 23 da globina alfa, onde o ácido
aspártico foi substituído pelo ácido glutâmico (figura 31). E há 4 milhões de anos a
seqüência de aminoácidos da hemoglobina humana, em relação aos seus
ancestrais, permanece estável.
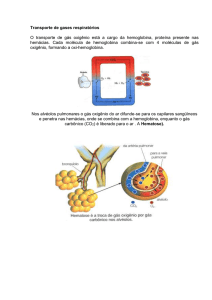
Como foi possível observar na leitura desse breve resumo sobre o
desenvolvimento da hemoglobina em relação aos seres vivos desde os primórdios
do nosso planeta, a hemoglobina teve realmente sua origem há milhões de anos em
vertebrados marinhos. Embora proteínas com características de transportadoras de
oxigênio tenham sido relatadas entre leguminosas e em invertebrados, foi somente
com os vertebrados que a hemoglobina se desenvolveu como molécula
especializada no transporte de oxigênio devido ao fato de ter uma célula específica
para este fim, qual seja, o eritrócito. O desenvolvimento do eritrócito e da
hemoglobina como um conjunto harmonioso na fisiologia do transporte de oxigênio,
teve importância fundamental na evolução das diversas espécies de vertebrados.
Estudos realizados em sangue de lampréias mostraram que o transporte de
oxigênio é realizado por moléculas de hemoglobinas formadas por um único tipo de
globina (ver etapas 1 e 2 da figura 29). Admite-se, portanto, que no período de
divergência da lampréia para outras formas de vertebrados ocorreu a duplicação
dos genes codificadores em genes específicos: alfa e beta. A especialização
fisiológica de captação, transporte e liberação de oxigênio tornou-se maior e mais
efetiva com a formação de tetrâmeros de moléculas de hemoglobinas compostas
por duas globinas alfa e duas beta (ou α2 β2). Esse tipo de estrutura tetramérica é
encontrada em peixes, répteis, anfíbios, aves e mamíferos. Para quase todas as
espécies de animais vertebrados ocorre a síntese de diferentes formas tetraméricas
de moléculas de hemoglobinas que são específicas para as diversas fases de
transformações que acontecem desde a fecundação do ovo até a fase adulta. Por
exemplo, em anfíbios as moléculas das hemoglobinas do girino diferem daquelas
encontradas em rãs adultas. Na espécie humana ocorre o mesmo fenômeno de
diferenciação de hemoglobinas nas três fases de desenvolvimento: embrionário,
fetal e pós-nascimento, caracterizando respectivamente as Hb embrionárias, a
Hb Fetal, e as Hb adultas (ou Hb A/A2). Cada um desses três tipos básicos de
hemoglobinas humanas apresentam processos fisiológicos de captação, transporte
e liberação de oxigênio que estão relacionados com as diferentes fases do
57
desenvolvimento embrionário e fetal, bem como após o nascimento. Todos esses
fenômenos relativos à síntese de hemoglobinas é bem conhecido geneticamente,
como se verá adiante.
58
Etapa 1
(800 m.a.)
Etapa 2
(700 m.a.)
Etapa 3
(600 m.a.)
Etapa 4
(500 m.a.)
α
β
Etapa 5
(300 m.a.)
Etapa 6
(100 m.a.)
α
ζ
ε
γ
Etapa 7
(70 m.a.)
ζ
ψζ
ψ α1 α2
α1
ε
γG
β
γA ψ β
δ
Feto
PN PN
Pseudogene
β
Pseudogene
Embrião
Feto Feto
PN PN
Embrião
Feto
Figura 29 – Proposta sobre evolução do gene da globina durante 800 milhões
de anos
m.a.: milhões de anos; PN: pós-nascimento
Pseudogenes: são genes que tem seqüência de DNA, porém estão
inativos por processo de mutação ou deleção.
59
70 milhões de anos
ANCESTRAL HOMINÍDEO COMUM
4 milhões de anos
ANCESTRAL HUMANO - CHIMPANZÉ
Australopithecus africanus
2,5 – 1,6 milhões de anos
1,5 milhões de anos
1 milhão de anos
100 mil anos
Homo habilis
CHIMPANZÉ
Homo ergaster
Homo erectus
Homo heidelbergensis
Homo sapiens neanderthalis
40 mil anos
Figura 30 – Resumo da árvore genealógica humana.
Homo sapiens sapiens
60
ANCESTRAL HOMINÍDEO COMUM
70 milhões de anos
globina α 23: Ácido aspártico (Asp)
globina β 104: Arginina (Arg)
4 milhões de anos
ANCESTRAL HUMANO - CHIMPANZÉ
Globina α 23: Asp → Ácido Glutâmico
HUMANO
CHIMPANZÉ
GORILA
Figura 31 – Divergência da linhagem humano - chimpanzé e da linhagem
gorila
do ancestral hominídeo comum, e a diferença entre
aminoácidos ao longo de 70 milhões de anos até o presente.
61
A SÍNTESE DAS GLOBINAS
A síntese das globinas na espécie humana requer um rígido controle
genético do DNA inserido nos genes de globinas do tipo alfa no cromossomo 16 e
nos genes de globinas do tipo beta no cromossomo 11. Esses genes se tornam
ativos à medida que os precursores eritrocitários amadurecem conforme foi
apresentado no capítulo 2. Entretanto a síntese da globina tem dinamismos
diferentes para cada fase do desenvolvimento humano, morfologicamente
caracterizada por embrionária, fetal e pós-nascimento. Esse processo que
diferencia os tipos de globinas e, consequentemente, das hemoglobinas, se deve
não somente ao estímulo de cada gene para respectiva fase de desenvolvimento,
mas decorre notadamente de enzimas estimuladoras do DNA (DNA polimerase)
que reproduz um molde que configura o seu RNA complementar. Este RNA, por
sua vez, precisa de uma enzima complexa conhecida por RNA polimerase para
induzir o seu crescimento em forma de fita que gradualmente se desprende do DNA
que foi copiado. Por essa razão a RNA polimerase tem fundamental importância na
síntese de proteínas, quer no sentido da sua composição estrutural, bem como da
sua concentração. Para que seja possível entender a síntese dos diferentes tipos
de globinas podemos admitir que cada um dos genes de globinas tipo alfa (ζ, α2,
α1), e os de globinas tipo beta (ε, γG, γA, δ, β) são estimulados por RNA polimerases
específicos. Na região do cromossomo 16 onde se localizam o grupo de genes de
globinas tipo alfa há uma pequena extensão de bases nitrogenadas cujo conjunto é
conhecido por região controladora dos genes (RCG) de globinas alfa, e o mesmo
ocorre com relação ao cromossomo 11 (figura 32). É justamente na RCG que as
RNA polimerases específicas para cada genes de globinas tipo alfa e tipo beta são
formadas e estimuladas a induzirem as sínteses de globinas em cada um desses
genes.
A análise da figura 32 mostra que o agrupamento de genes de
globinas do tipo alfa (RCG – ζ – ψζ – ψα1 – α2 – α1) tem seqüência aproximada de
40 mil de bases nitrogenadas, sendo portanto menor que os genes de globinas do
tipo beta (RCG – ε – γG – γA – δ – β) com cerca de 60 mil bases nitrogenadas. Em
biologia molecular considera-se que a leitura das bases se faz no sentido 5' → 3' e
assim
é
possível
observar
que
há
um
sentido
lógico
relacionando
o
62
desenvolvimento morfológico do ser humano com as sínteses específicas de
globinas para as respectivas fases embrionária, fetal e pós-nascimento. É preciso
também considerar que a estimulação de cada um desses genes de globinas
depende da quantidade de RNA polimerase específica para esse fim. Certamente
há mecanismos que ainda não estão bem definidos para determinar o início e o fim
de cada tipo de RNA polimerase para cada fase do desenvolvimento humano, até o
momento em que esse processo se estabiliza, fato que ocorre por volta do sexto
mês de vida (tabela 8). A figura 33 mostra a eletroforese de globinas normais
extraídas de pessoa adulta e de recém-nascido. Enquanto no adulto a síntese de
globinas alfa e beta está bem estabilizada e equilibrada, no recém-nascido ainda
há, além da globina alfa, outras duas globinas gama: γA e γG, que compõe a Hb
Fetal.
É importante destacar que os genes duplicados de globinas gama são
diferenciados pela inserção de um único aminoácido na posição 136 de cada
polipeptídeo gama sintetizado e, por isso, se diferenciam em γG quando o
aminoácido glicina ocupa esta posição, ou γA no caso de ser a alanina. A proporção
de síntese dessas duas globinas que compõe a Hb Fetal é constante durante a fase
fetal, ou seja 70% de γG e 30% de γA. Por outro lado, após o nascimento, em
situações em que a Hb Fetal permanece elevada – como são os casos de
persistência hereditária da Hb Fetal, ou em condições patológicas por
descoordenação de sua síntese – como são os casos de talassemias beta, a
relação γG : γA apresenta ampla variação sem que seja possível estabelecer relação
consistente entre a proporção desses dois tipos de globinas gama com causas que
determinam a elevação de Hb Fetal.
63
A SÍNTESE DO GRUPO HEME
Síntese da Porfirina
A síntese do grupo heme ocorre nas mitocôndrias dos eritroblastos
após várias reações químicas que resultam em expressivas transformações
estruturais envolvendo a biossíntese das porfirinas e a introdução do ferro neste
complexo molecular. A síntese de porfirina tem início durante o metabolismo do
ácido cítrico (ciclo do ácido cítrico ou ciclo de Krebs), onde compostos químicos
intermediários são formados e participam como precursores ou substratos para
muitas vias biosintéticas, entre as quais se destaca a síntese da porfirina (figura
34). Os produtos intermediários do ciclo do ácido cítrico como a succinil coenzima A
(succinil Co-A) e o aminoácido glicina se combinam por reação catalítica
intermediada por uma enzima mitocondrial, a delta-amino levulinato sintetase, ou
ALA-sintetase, com a participação da vitamina B6. Nesse processo forma-se um
composto
instável de
ácido
alfa-amino-beta-adípico,
que
se
descarboxila
espontaneamente em ácido-delta-aminolevulínico (ALA).
A
partir
dessa
fase,
ocorrem
várias
reações
químicas
de
transformações, com participações de enzimas que atuam na desaminação,
descarboxilação e na oxidação de produtos intermediários, até formarem a
molécula de porfirina (figura 35). Após a configuração do anel da porfirina, o ferro é
introduzido no seu interior para se ligar com quatro átomos de nitrogênio (figura 36).
Esse conjunto caracterizado como grupo heme se prende à globina por meio de
ligações com dois aminoácidos histidina, molecularmente distinguidas por histidina
proximal e histidina distal (figura 37).
64
Metabolismo do ferro
A maioria do ferro orgânico presente na hemoglobina é encontrada
nos eritrócitos circulantes. Os macrófagos do sistema retículo endotelial armazenam
o ferro liberado pela hemoglobina de eritrócitos velhos fagocitados sob forma de
ferritina e hemossiderina. Os macrófagos também liberam átomos de ferro no
plasma que se ligam à transferrina e são transportados para os tecidos
hematopoiéticos, incorporando-se nos precursores dos eritrócitos – os eritroblastos.
O balanço de ferro é rigidamente controlado entre perda e ganho. Há uma perda de
ferro diária que ocorre através da urina, fezes, pele, unhas e menstruação. Esta
perda, variável entre 1 e 2 miligramas diárias, é restabelecida pelo ferro absorvido
na dieta, que oscila também entre 1 e 2 miligramas/dia. O ferro circulante na
hemoglobina tem concentrações variáveis entre 1,7 a 2,4g, e o ferro absorvido e
armazenado sob forma de ferritina pelos macrófagos também é representativo,
entre 0,5 e 1,5g.
A incorporação do ferro através dos receptores de transferrina, as
reservas intracelulares de ferro em ferritina e a incorporação do ferro no anel
protoporfirínico para a síntese do heme nas mitocôndrias, são eventos coordenados
em resposta ao suprimento de ferro no nível de transcrição e de tradução, pela
presença de elementos responsivos ao ferro (ERF) localizados nas regiões
ascendentes não traduzidas dos RNA mensageiros (RNAm) para ferritina e para a
enzima eritróide heme sintética ácido delta-aminovulínico sintetase (ALA-S). Esse
processo biologicamente complexo do equilíbrio (ou homeostase) do ferro celular
tem na estrutura do ERF o seu ponto de compensação, ou seja, quando há grande
disponibilidade de ferro ocorre baixa afinidade entre ferro e ERF, resultando em
menor síntese do receptor da transferrina, e aumento da síntese de ferritina e ALAS. Por outro lado, quando o suprimento de ferro é baixo há o aumento de sua
ligação com o ERF, com o aumento da síntese do receptor da transferrina e a
redução na síntese de ferritina e ALA-S.
65
Situações que prejudicam a formação do grupo heme
Há
duas
situações
bem
específicas
que
tem
influência
no
desempenho da síntese do grupo heme. A primeira se deve à deficiência de
enzimas que participam das transformações químicas que ocorrem durante a
síntese do anel porfirínico, e em decorrência desse defeito ocorre a porfíria. A
segunda situação que causa prejuízo na formação do grupo heme se deve à
deficiência de ferro.
A porfíria constitui um conjunto de doenças, geralmente hereditárias,
causadas por alterações que ocorrem durante o processo de formação das
porfirinas (figura 34). As três porfirinas de importância clínica são: protoporfirina,
uroporfirina e coproporfirina. A protoporfirina está amplamente distribuída pelo
corpo e desempenha a função de precursor do grupo na composição da
hemoglobina e mioglobina, bem como da catalase e dos citocromos; participam
também do armazenamento e utilização de energia celular.
A
coproporfirina
e
a
uroporfirina,
que
são
precursoras
da
protoporfirina, são normalmente excretadas em pequenas quantidades pelas fezes
e urina. Os eritrócitos contém pequena concentração de protoporfirina e
coproporfirina.
Os portadores de porfírias se caracterizam pela fotossensibilidade,
dores abdominais agudas, neuropatias, excreção urinária aumentada de porfirinas e
de seus precursores.
As principais síndromes das porfírias são:
•
Porfíria eritropoiética – causa hereditária
•
Protoporfíria eritrocitária – causa hereditária
•
Porfíria hepática intermitente aguda (PIA) – causa hereditária
•
Porfíria hepática variegatta – causa hereditária
•
Porfíria hepática cutânea tardia – causa adquirida
•
Porfirinúria – causa decorrente de doenças malignas, infecções e
poliomielite
Os tipos, as características e a idade de manifestações clínicas e
laboratoriais das porfírias estão resumidas nas tabelas 9 e 10.
66
O ferro tem igual importância que as sínteses de porfirinas e de
globinas para compor a complexa molécula de hemoglobina. As principais situações
que causam as deficiências de ferro e, consequentemente, de hemoglobina se
devem a quatro condições: a) perda crônica de sangue, b) aumento de demanda, c)
mal absorção, e d) dieta com carência de ferro. Em países subdesenvolvidos, ou
mesmo nos bolsões de pobreza de países ou cidades desenvolvidas, a principal
causa da deficiência de ferro é de ordem alimentar. Em países desenvolvidos ou em
classes sociais com boas condições econômicas – que incluem moradia,
saneamento básico e cultura – a causa mais freqüente de deficiência de ferro se
deve à sua perda crônica, notadamente através do trato gastrointestinal e uterina.
Entretanto é importante ressaltar que a demanda de ferro durante a infância,
adolescência, gestação, lactação e ciclo menstrual, aumenta o risco de anemia pelo
balanço negativo de ferro. Finalmente, uma situação rara envolve conjuntamente o
uso de ferro na sua inserção no anel de protoporfirina, trata-se da anemia
sideroblástica. Esta anemia é do tipo refratária, ou seja, não responde ao
tratamento por suplementação de ferro, laboratorialmente se caracteriza pela
presença de eritrócitos hipocrômicos e elevada concentração de ferro nos
eritroblastos medulares, fato que originou o nome da anemia sideroblástica. A forma
mais comum de anemia sideroblástica se deve ao defeito na síntese das porfirinas
causada por mutação da enzima ácido-delta-aminolevulínico-sintetase (ALA-S), que
é sintetizada no cromossomo X. Por essa razão, a ação da enzima ferroquelatase
fica prejudicada e, consequentemente, o ferro não é inserido no anel porfirínico e o
grupo heme não é sintetizado (consultar figura 34).
Um resumo esquemático das principais causas que podem influenciar
na formação da hemoglobina, especialmente devido à síntese do grupo heme está
representada na figura 38.
67
A MOLÉCULA DA HEMOGLOBINA
A molécula de hemoglobina é estruturalmente composta por duas
globinas do tipo alfa e duas do tipo beta, compondo um tetrâmero com formato
globular (figura 39). As dimensões espaciais do tetrâmero são as mesmas nas
hemoglobinas embrionárias (Gower-1, Gower-2 e Portland), e nas hemoglobinas
Fetal, A e A2, com diâmetro de aproximadamente 5,5nm configurando-lhes um
modelo globular e discretamente achatado. O peso molecular das hemoglobinas
humanas é próximo de 64.500 daltons, com pequenas variações entre os diferentes
tipos. Todas as moléculas de hemoglobinas das fases embrionária, fetal e pósnascimento tem 574 aminoácidos, dos quais 282 estão na composição das duas
globinas tipo alfa (141 aminoácidos por globina tipo alfa) e 292 na composição das
duas globinas tipo beta (146 aminoácidos por globina tipo beta). Os graus de
semelhanças estruturais, calculado com base na similaridade da composição de
aminoácidos entre os tipos de globina são variáveis com maior identidade entre as
globinas beta e delta (96% de semelhança), seguida da beta e gama (71%), e com
menores similitudes entre alfa e beta (42%), e alfa e gama (39%). Essa identidade
química é possível ser explicada por meio da suposição genética sobre a origem e
evolução da hemoglobina, apresentada no início desse capítulo.
A
estabilidade
das
moléculas
de
hemoglobinas,
quer
sejam
embrionárias, Fetal, A ou A2, é dependente do arranjo estrutural que ocorre entre a
composição das globinas do tipo alfa com as do tipo beta. As estruturas
tridimensionais desses dois grupos de globinas são muito parecidas, apesar de
suas seqüências de aminoácidos serem diferentes, conforme apresentado acima. A
conformação globular da molécula de hemoglobina se deve à extensa disposição
helicoidal dos polipeptídeos que compõe as globinas dos tipos alfa e beta (figura
39), que representa 75% do total da sua estrutura. Os trabalhos realizados por
Perutz e Kendrew em 1959 utilizando o método de cristalografia de proteínas por
meio da difração de raio-X, mostraram algumas particularidades físico-químicas da
molécula de hemoglobina definitiva ou adulta (Hb A). A Hb A possui um rearranjo
tetraédrico devido a conformação pareada de duas globinas alfa (α2) e duas beta
(β2). Essa disposição tetramérica α2 β2 somente é possível devido às ligações físico-
68
químicas de diferentes intensidades que possibilitam a movimentação da molécula
durante a oxigenação. Para tornar mais fácil o entendimento dessas ligações e das
suas relações com a fisiologia da hemoglobina, denominou-se o tetrâmero químico
α2 β2 em α1 α2 / β1 β2 (figura 40), devido aos contatos intermoleculares que ocorrem
entre globinas alfa e beta.
Pela disposição do tetrâmero da hemoglobina (figuras 39 e 40)
observa-se que as globinas alfa e beta se situam diagonalmente, de tal forma que
os contatos entre os aminoácidos da globina α1 com a globina β2 (α1 β2) são iguais
aos que ocorrem entre as globinas α2 β1. Da mesma forma os contatos
intermoleculares entre α1 β1 são iguais aos α2 β2. Os contatos entre as globinas α1
β2 e α2 β1 envolvem um total de 38 aminoácidos (6,6% do total de aminoácidos da
molécula). Esses contatos α1β2 e α2 β1, que se dispõe horizontalmente no modelo
molecular da figura 40, promovem movimentos de deslizamento das globinas alfa e
beta, fato que facilita a oxigenação dos quatro grupos heme da molécula. Os
contatos intermoleculares entre as globinas α1 β1 e α2 β2 são mais extensos pois
participam 68 aminoácidos (11,8% do total de aminoácidos da molécula) que se
dispõe verticalmente no modelo molecular da figura 40. Esses contatos α1 β1 e α2 β2
são os que mantém a integridade físico-química do tetrâmero, dando-lhe
estabilidade molecular. Os contatos α1 α2 ocorrem somente na forma desoxigenada
da hemoglobina, e tem influência na interação entre os grupos heme, no efeito Bohr
e no transporte de CO2. Os contatos β1 β2 ocorrem nas formas oxi e desoxigenadas,
e são responsáveis pela acomodação da molécula de 2,3
difosfoglicerato (2,3
DPG) durante a desoxigenação da hemoglobina.
Os estudos seqüentes sobre a configuração estrutural da molécula de
hemoglobina demonstraram que as globinas dos tipos alfa e beta tem duas regiões
específicas, a interna e a externa. As regiões internas, são compostas por
aminoácidos não-polares e hidrofóbicos localizados em 75% da molécula, incluindo
os helicóides e o grupo de aminoácidos que envolve o grupo heme. As regiões
externas são bem menos extensas pois compreendem apenas em 25% do
conteúdo molecular, e são formadas por aminoácidos polares e hidrofílicos que se
dispõe nas partes não helicoidais da molécula, fazendo contato com a água. A
tabela 11 mostra os aminoácidos hidrofóbicos e hidrofílicos.
69
CROMOSSOMO 16 – GENES DO TIPO ALFA
40.000 bases nitrogenadas
5'
3'
RCG
ζ
ψζ
ψ α1
α2
α1
Feto
PN
Feto
PN
Pseudogenes
Embrião
Região
Controladora
de genes
CROMOSSOMO 11 – GENES DO TIPO BETA
60.000 bases nitrogenadas
5'
3'
RCG
Região
Controladora
de genes
ε
Embrião
G
B
γ
γ
Feto
Feto
ψβ
Pseudogene
δ
β
PN
PN
Figura 32 – Esquema representativo do agrupamento de genes de globinas do
tipo alfa (cromossomo 16) e tipo beta (cromossomo 11), com
destaques para a Região Controladora de Genes (RCG) e o
tamanho de cada agrupamento caracterizado pelo número de
bases nitrogenadas. PN: pós-nascimento.
70
Tabela 8 – Relação entre os diferentes tipos de hemoglobinas, composições
estruturais e concentrações, com as fases de desenvolvimento
ontogênico.
Fase da
Hemoglobina
Estrutura
ontogênese
Embrionária
Fetal (*)
Pós – Nascimento
Concentração
(%)
Gower – 1
ζ2 ε2
20 – 40
Portland
ζ2 γ2
5 – 20
Gower – 2
α2 ε2
10 – 20
Fetal
α2 γ2
90 – 100
A
α2 β2
96 – 98
A2
α2 δ2
2–4
Fetal
α2 γ2
0–1
(*) Na fase fetal ocorre o início as síntese da Hb A, não excedendo 10% de
concentração
71
Figura 33 – Eletroforese de globinas obtidas de amostras de pessoa adulta e
recém-nascido. No adulto o fracionamento de globinas alfa e beta
se caracteriza visualmente pelo equilíbrio de suas concentrações.
No recém-nascido, além da globina alfa há duas outras globinas, a
γA e γG, que decrescem rapidamente após o nascimento. Após o
sexto mês de vida normalmente as duas globinas gama deixam de
ser sintetizadas para serem substituídas pela globina beta.
72
Piruvato
Acetil-Co A
Ácidos Graxos e esteróis
Glicose
Fenilpiruvato
Oxaloacetato
Citrato
Glutamina
Prolina
Arginina
Serina
α - cetoglutamato
Glicina
Glutamato
Malato
Cisteína
Aspartato
Fenilalanina
Asparagina
Purinas
Succinil – Co A
Tirosina
Triptofatano
Pirimidinas
Porfirinas
Figura 34 – Esquema sintético representativo do ciclo do ácido cítrico (Krebs).
Produtos intermediários desse ciclo, assinalados em retângulos,
participam da síntese do grupo heme.
73
GLICINA
SUCCINIL – Co A
ALA sintetase
ALA
PBG
PBG desaminase
PORFÍRIA INTERMITENTE
AGUDA
URO I
URO III cossintetase
PORFÍRIA ERITROPOIÉTICA
(Doença de Gunther)
URO III
URO descarboxilase
PORFÍRIA CUTÂNEA
COPRO
DEFICIÊNCIAS
ENZIMÁTICAS
COPRO oxidase
DOENÇAS
COPROPORFÍRIA
PROTO gene
PROTO gene oxidase
PORFÍRIA VARIEGATTA
PROTOPORFIRINA
PROTOPORFÍRIA
Ferroquelatase
ERITROPOIÉTICA
FERRO
HEME
Figura 35 – Síntese da molécula de porfirina e do grupo heme após a
incorporação do ferro, e a relação das deficiências enzimáticas
com doenças que causam as porfírias.
74
CH2
H
C
CH
CH3
CH3
N
CH
N
Fe
HC
N
CH2
CH
N
CH3
H3C
CH2
CH2
COOH
C
H
CH2
CH2
COOH
Figura 36 – O grupo heme composto pela molécula anelada de porfirina
e o ferro em sua região central.
75
Figura 37 – Representação da estrutura molecular do grupo heme inserido na
globina. No centro, a esfera maior representa o ferro circundado
pelo anel de porfirina. As estruturas carbonadas mais claras
indicam as posições dos aminoácidos hidrofóbicos que protegem
o grupo heme da água circundante. As estruturas escuras e
maiores são os aminoácidos hidrofílicos da superfície interna da
globina.
76
Tabela 9 – Principais características das porfírias eritropoiéticas.
Características
Herança
Idade
Prevalência
Fotossensibilidade
Anemia
Esplenomegalia
Lesão cutânea
PE
PPE
Autossômica recessiva
Autossômica dominante
0 a 5 anos
0 a 5 anos
Rara
Comum
Elevada
Baixa
Hemolítica
–
Presente
–
Vesiculares e
Dermatoses
ulcerativas
Urina
Prognóstico
Vermelha ou rosa
Normal
Ruim
Bom
PE: Porfíria eritropoiética; PPE: Protoporfíria eritropoiética
77
Tabela 10 – Principais características das porfírias hepáticas.
Herança
PIA
PV
CP
PC
Autossômica
Idem
Idem
Adquirida
Variável
Variável
dominante
Idade
15 a 40 anos 10 a 30 anos
Prevalência
Comum
Rara
Rara
Rara
Fotossenbilidade
Ausente
Ausência
Ausência
Intensa
Lesão cutânea
Ausente
Presente
Ausente
Presente
Dor abdominal aguda
Presente
Presente
Presente
–
Neuropatia
Presente
Presente
Presente
–
Hepatopatia
–
–
–
Presente
Vermelha e
(*)
–
–
Bom
Bom
Variável
Urina
escura
Prognóstico
Bom
(*) aumento de coproporfirina, uroporfirina e protoporfobilinogênio.
PIA: Porfíria intermitente aguda; PV: Porfíria Variegatta; CP: Coproporfíria
hereditária; PC: Porfíria cutânea tardia.
78
FERRO
PROTOPORFIRINA
Anemia Sideroblástica
• Deficiência de ferro
• Perda de ferro
HEME
+
GLOBINA
HEMOGLOBINA
Figura 38 – Esquema representativo de situações que interferem na síntese
do grupo heme.
79
Figura 39 – Modelo espacial do tetrâmero da molécula de hemoglobina
formado por duas globinas do tipo alfa e duas do tipo beta, com o
grupo heme inserido em cada uma das globinas.
80
β1
α2
α1
β2
Figura 40: Contatos intermoleculares entre as globinas alfa e beta. Os contatos
α1 β 1 e α2 β 2 têm importância na estabilidade da molécula. Os
contatos α1 β 2
e
α2
durante a oxigenação.
β1
atuam na movimentação da molécula
81
Tabela 11: Propriedades dos vinte aminoácidos naturais da hemoglobina.
Aminoácido
Sigla
Grupo R
Polarização
Hidrofóbico
PI
% em
proteínas
Glicina
Gly
Alifático
NP
Não
5,97
7,5
Alanina
Ala
Alifático
NP
Sim
6,01
9,0
Valina
Val
Alifático
NP
Sim
5,97
6,9
Leucina
Leu
Alifático
NP
Sim
5,98
7,5
Isoleucina
Ile
Alifático
NP
Sim
6,02
4,6
Prolina
Pro
Alifático
NP
Não
6,48
4,6
Fenilalanina
Phe
Aromático
NP
Sim
5,48
3,5
Tirosina
Tyr
Aromático
NP
Não
5,66
3,5
Triptofano
Trp
Aromático
NP
Não
5,89
1,1
Serina
Ser
Neutro
P
Não
5,68
7,1
Treonina
Thr
Neutro
P
Não
5,87
6,0
Cisteína
Cys
Neutro
P
Sim
5,07
2,8
Metionina
Met
Neutro
P
Sim
5,74
1,7
Asparagina
Asn
Neutro
P
Não
5,41
4,4
Glutamina
Gln
Neutro
P
Não
5,65
3,9
Aspartato
Asp
Negativo
P
Não
2,77
5,5
Glutamato
Glu
Negativo
P
Não
3,22
6,2
Lisina
Lys
Positivo
P
Não
9,74
7,0
Arginina
Arg
Positivo
P
Não
10,76
4,7
Histidina
His
Positivo
P
Não
7,59
2,1
NP: não polar; P: polar; pI: ponto isoelétrico; Neutro: não carregado eletricamente.
82
SÍNTESE E EQUILÍBRIO MOLECULAR
DAS HEMOGLOBINAS NORMAIS
Após a apresentação nesse capítulo das sínteses individualizadas das
globinas e do grupo heme, e também da composição estrutural da molécula de
hemoglobina, é importante destacar que todo esse processo ocorre de forma
sincrônica e simultânea dentro de cada eritroblasto. Assim, a síntese de moléculas
de hemoglobinas abrange a ação de genes de globinas α, β, δ e γ, de ribossomos e
mitocôndrias, que atuam em processos de mútua dependência biológica durante a
hemoglobinogênese que se desenvolve nos eritroblastos e reticulócitos (ver tabela
5, capítulo 2). Como resultado desse sincronismo biológico a síntese de globinas α,
β, δ e γ ocorre juntamente com os grupos heme que se inserem na estrutura
terciária dessas globinas e, em seguida, se dimerizam em α2, β2, δ2, γ2, para então
se tetramerizarem em moléculas de estrutura quaternária de α2 β2 (Hb A), α2 δ2 (Hb
A2) e α2 γ2 (Hb Fetal). Esse processo descrito para a fase pós-nascimento e que
será efetivado para toda a vida do indivíduo, acontece também nas fases fetal e
embrionária. Entretanto, para o fim de expor didaticamente o equilíbrio que se
verifica entre as globinas dimerizadas alfa e não-alfa (β, δ e γ), representaremos por
meio de figuração hipotética a formação de hemoglobinas A, A2 e Fetal após o
sexto mês de vida (figura 41). A importância visual do esquema que representa o
equilíbrio entre globinas é fundamental para entender as causas e conseqüências
das talassemias alfa e beta ocorrem por desequilíbrio de síntese entre essas duas
globinas. Se pudéssemos "encaixotar" as globinas alfa e não-alfa seria possível
construir modelos representativos do equilíbrio das globinas alfa e não-alfa das
hemoglobinas normais, e também do desequilíbrio que se verificam nas talassemias
alfa e beta (figura 42). Considerando que o volume de síntese das hemoglobinas A,
A2 e Fetal é proporcional às suas respectivas concentrações obtidas nas dosagens
eletroforéticas ou cromatográficas dessas frações, é também possível supor que em
condições normais essas três hemoglobinas compartilham do mesmo espaço –
obviamente com concentrações diferentes – dentro de um mesmo eritrócito.
Considera-se portanto hemoglobinas normais as três frações identificadas em
83
eletroforeses alcalina de hemoglobina em pessoas com idade superior a 6 meses
ou por métodos cromatográficos, com as seguintes concentrações:
Hb A:
96 a 98%
Hb A2:
2 a 4%
Hb Fetal:
0a
1%
HEMOGLOBINAS GLICOSILADAS
Após o nascimento, observa-se que além das hemoglobinas A, A2 e
Fetal, surgem outros cinco tipos de moléculas que constituem o grupo das
hemoglobinas glicosiladas: Hb A1a-1, Hb A1a-2, Hb A1b, Hb A1c e Hb A1d. O conjunto
dessas hemoglobinas que eletroforeticamente se posicionam um pouco à frente da
Hb A, sem que ocorra um fracionamento visível (figura 43), representa 5 a 8% da
concentração da Hb A. Todas essas hemoglobinas são derivadas da Hb A por
terem hexoses ligadas à região N-terminal do primeiro aminoácido da globina beta –
a valina. A glicolização ocorre por um processo lento com intermediação enzimática
durante a hemoglobinogênese. Assim, as hexoses permanecem ligadas à Hb A por
todo o tempo de vida do eritrócito, que é de 120 dias, em média. A Hb A1c por
apresentar maior concentração entre as hemoglobinas glicosiladas, atua como
sensível marcadora biológica da glicose sangüínea. A tabela 12 relaciona, suas
concentrações e os produtos específicos de glicolização.
84
Cromossomo 16
Cromossomo 11
Mitocôndria
α2
γ
α1
δ
β
Grupos heme
Globinas α (100%)
α2
α2
α2
α2
Globinas β (96 – 98%)
Globinas δ ( 2 – 4%)
Globinas γ (0 – 1%)
α2
β2
Dímeros de globinas α
α2
β2
β2
δ2
γ2
Dímeros de globinas β, δ, γ
β2
α2
α2
δ2
β2
α2
α2
β2
γ2
Figura 41 – Esquematização hipotética da formação equilibrada entre globinas
alfa e não-alfa (β
β, δ e γ) após o sexto mês de vida.
85
α
γ
α
δ
α
→ α2 γ2 :
Hb Fetal (0 – 1%)
→ α2 δ2 :
Hb A2
(2 – 4%)
→ α2 β2 :
Hb A
(96 – 98%)
β
Equilíbrio entre Globinas nas Hemoglobinas Normais
α
α
γ
δ
α
β
Talassemia Alfa
α
α
α
γ
δ
β
Talassemia Beta
Figura 42 – Esquematização do equilíbrio entre globinas na formação de
hemoglobinas normais, e dos desequilíbrios na talassemia alfa
(diminuição da síntese de globina α) e na talassemia beta
(diminuição da síntese de globina β ).
86
Grupo de Hb Glicosiladas
A
A2
Anidrase carbônica
1
2
3
Figura 43 – Eletroforese de hemoglobinas em acetato de celulose, tampão
alcalino (TEB pH 8,6). Nas três amostras observam-se à frente da
Hb A as frações difusas com as hemoglobinas glicosiladas. A
amostra 1 é de paciente com talassemia beta menor (Hb A2
aumentada) e as amostras 2 e 3 são normais.
Tabela 12 – Subtipos de HbA1
87
relacionados com suas concentrações e
glicolização.
Subtipo
Concentração
Glicolização
(%)
A1a – 1
0,2
Hexose – difosfato
Frutose – difosfato
Glicose, manose e galactose
difosfato
A1a – 2
0,2
Hexose – monofosfato
Glicose – 6 – fosfato
Glicose, manose e galactose
monofosfato
A1b
0,5
Hexose não – fosforilada
Glicose, manose, galactose
A1c
4–6
A1d
0,4
1 – deoxi – beta – D – frutose
Beta – D – glicopiranosil
88
FISIOLOGIA DA OXIGENAÇÃO DA HEMOGLOBINA
O sangue do ser humano transporta diariamente o equivalente a 600
litros de oxigênio dos pulmões aos tecidos, mas pouco deste oxigênio é
transportado no plasma sangüíneo porque ele é muito solúvel em soluções
aquosas. Quase todo o oxigênio transportado pelo sangue está ligado à
hemoglobina. Os eritrócitos ao passarem pelos pulmões tem suas moléculas de
hemoglobinas saturadas em 96% de oxigênio (oxiemoglobina do sangue arterial)
que serão gradualmente liberados para os tecidos. No sangue venoso que retorna
ao coração a hemoglobina está apenas 64% saturada de oxigênio. Assim,
o
sangue que passa através dos tecidos libera perto de um terço do oxigênio que
transporta.
As propriedades especiais da molécula de hemoglobina que a
transforma em um transportador tão eficiente podem ser entendidas pela
comparação das curvas de ligação do oxigênio, ou curvas de saturação do O2 da
hemoglobina e mioglobina (figura 44). Estas curvas mostram os graus de saturação
de oxigênio quando mioglobina e hemoglobina estão no sangue venoso e arterial. A
mioglobina tem maior afinidade pelo oxigênio que a hemoglobina. Ela está quase
100% saturada em pressões parciais de oxigênio medida em milímetros de
mercúrio (pO2 / mm Hg) quando o pO2 é de 15 mmHg ou 1,5 kPa, enquanto a
hemoglobina requer pO2 de 35 mmHg ou 3,5 kPa para obter 50% de saturação.
Quando o hemoglobina se oxigeniza no sangue arterial seu grau de saturação é de
95%, e à medida que começa a distribuição do oxigênio para as células teciduais o
faz de forma lenta até passar ao sangue venoso. No sangue venoso o
desprendimento do oxigênio é muito rápido e eficiente, fato que faz com que a
saturação de oxigênio de 75% em pO2 de 50 mmHg (do músculo em repouso)
diminui rapidamente para menos de 10% de saturação em pO2 de 15 mmHg, numa
curva tipo sigmóide. Assim, a curva sigmóide de saturação da hemoglobina revela
uma adaptação molecular para a sua função de transporte nos eritrócitos,
assegurando a ligação e a liberação do oxigênio para as células teciduais. Esse
fato indica que a mioglobina tem alta afinidade pelo oxigênio em comparação com a
hemoglobina. Conforme mostra a figura 44, o gráfico da curva de saturação da
89
mioglobina pelo oxigênio é do tipo hiperbólica simples, fato de corrente da ação de
massa do oxigênio no equilíbrio mioglobina + O2
Oxi Mb. Em contraste, a
afinidade da hemoglobina diminui rapidamente à medida que se transforma de
oxiHb → desoxiHb, fato que caracteriza a curva sigmóide que se acentua no
sangue venoso. O formato sigmóide tem uma explicação físico-química da
afinidade da hemoglobina pelo oxigênio. A figura 45 representa cada uma das
quatro subunidades de globinas (duas alfa ou α2 e duas beta ou β2) se ligando
independentemente com a molécula de oxigênio (O2). Assim, o processo fisiológico
da oxigenação da hemoglobina ocorre em quatro estágios seqüentes. No primeiro
estágio, a molécula está desoxigenada e a molécula de 2,3 – difosfoglicerato (2,3DPG) está inserida entre as duas subunidades de globina beta; no estágio seguinte,
inicia-se a oxigenação dos grupos heme das duas globinas alfa, primeiro um e
depois o outro; o terceiro estágio se caracteriza pelo ajustamento da conformação
tetramérica provocado pelo processo de oxigenação que, ao se completar nos
grupos heme das globinas alfa, começa a abranger as globinas beta. O movimento
de adaptação a esse processo é provocado pela aproximação entre as globinas
beta e a desacomodação do 2,3 DPG, que é expelido para fora. Finalmente, o
último estágio se deve pela oxigenação dos grupos heme das globinas beta,
inicialmente uma e depois a outra, completando a oxigenação da molécula de
hemoglobina.
A oxigenação da molécula de hemoglobina também depende do pH e
da concentração de CO2; o aumento de CO2 induz a liberação de oxigênio pela
hemoglobina, cujo processo é conhecido por efeito Bohr. Esse desempenho
bioquímico se deve quando a curva de dissociação de oxigênio (curva sigmóide)
em pO2 de 50 mmHg (ou P50) é afetada pelo metabolismo tecidual e pH sangüíneo.
Quando o metabolismo tecidual está aumentado são liberados produtos ácidos
capazes de causar a queda de pH (acidose) e assim a curva sigmóide é mudada à
direita, permitindo maior liberação de oxigênio para os tecidos. Por outro lado,
quando há elevação do pH sangüíneo (alcalose) a curva sigmóide se move para a
esquerda, diminuindo a liberação de oxigênio para os tecidos.
A curva de dissociação de oxigênio também varia em situações
específicas:
90
a) O 2,3-DPG, encontrado em grande quantidade nos eritrócitos e em pequenas
quantidades nos tecidos, desvia a curva para a direita, diminuindo a afinidade da
hemoglobina pelo oxigênio;
b) A afinidade da molécula isolada de Hb S pelo oxigênio é a mesma que a da Hb
A, porém os eritrócitos falciformes contém mais 2,3-DPG do que os normais e,
consequentemente, diminuem sua afinidade ao oxigênio.
c) A Hb Fetal tem maior afinidade pelo oxigênio do que a Hb A, provavelmente
devido ao fato do 2,3-DPG não se ligar às globinas gama;
d) A Hb H, constituída por quatro globinas beta, tem afinidade pelo oxigênio 12
vezes maior que a Hb A;
e) Há várias hemoglobinas variantes que apresentam afinidade aumentada pelo
oxigênio – Hb Bethesda, Hb Luton, entre outras – e Hb variantes que
apresentam baixa afinidade pelo oxigênio, como é o caso da Hb Kansas.
91
A
2,3
DPG
O2
O2
B
O2
C
2,3
DPG
O2
2,3
DPG
O2
D
O2
O2
E
O2
O2
2,3
DPG
O2
2,3
DPG
Figura 45: Seqüência dos estágios da oxigenação. A) molécula de
hemoglobina (Hb A) desoxigenada; B) início da oxigenação, com a
fixação de uma molécula de O2 para uma subunidade de globina
alfa; C) a outra globina alfa se oxigena; D) quando o O2 é fixado por
uma subunidade de globina beta inicia-se o deslocamento da
molécula de 2,3 DPG; E) a fixação do O2 por outra globina beta,
expulsa o 2,3 DPG da molécula de hemoglobina, que se torna
totalmente oxigenada.
92
pO2 do
sangue
venoso
100
Mb
Saturação
com O2
(%)
Hb
Músculo em
repouso
50
Músculo em
trabalho
pO2 (kPa)
0
1
5
10
13
0
10
50
100
130 pO2 (mmHg)
Figura 44: Curvas de saturação da mioglobina (Mb) e hemoglobina (Hb) pelo
oxigênio. A mioglobina tem uma afinidade muito maior pelo
oxigênio que a hemoglobina. Ela está 50% saturada em pressões
parciais de oxigênio (pO2) de apenas 0,15 a 0,30kPa, enquanto a
hemoglobina requer uma pO2 de 3,5kPa para uma saturação de
50%. Note que embora as duas, hemoglobina e mioglobina, estejam
mais que 95% saturadas na pO2 do sangue arterial que deixa os
pulmões (~13kPa), a hemoglobina está apenas cerca de 75%
saturada no músculo em repouso, onde a pO2 é cerca de 5kPa e
apenas 10% saturada no músculo em trabalho, onde a pO2 é
apenas 1,5kPa. Assim, a hemoglobina pode liberar o seu oxigênio
de forma muito eficiente no músculo e em outros tecidos
periféricos. A mioglobina, por outro lado, ainda está perto de 80%
saturada em uma pO2de 1,5kPa e, portanto, descarrega muito
pouco oxigênio, mesmo em situações de pO2 muito baixas. A curva
sigmóide de saturação da hemoglobina revela uma adaptação
molecular para a sua função de transporte nos eritrócitos,
assegurando a ligação e a liberação do oxigênio nos tecidos
apropriados.