Olimpíada de Química do Rio Grande do Sul – 2014
MODALIDADE EM1
Nº INSCRIÇÃO: ____________
Escrever o NÚMERO DE INSCRIÇÃO na grade de respostas e nas folhas de
respostas das questões descritivas.
Ao término da prova entregar somente a grade de respostas e as folhas de
respostas das questões descritivas.
A prova é constituída de 20 questões que devem ser respondidas com tinta
azul ou preta e sem rasuras.
As 15 primeiras questões são de escolha simples (escolher apenas uma
alternativa) e devem ter suas respostas marcadas na grade que se encontra na
folha de respostas, sem rasuras. Para cada questão CORRETA será atribuído 0,4
ponto.
As questões numeradas de 16 a 20 são descritivas e devem ser respondidas
na folha de respostas.
Amostra
Densidade (g/mL)
Ponto de Fusão
0
( C)
Ponto de Ebulição
0
( C) a 1 atm
Álcool comum
0,80
- 117
78,5
Pentano
0,65
- 130
36
CCl4
1,60
- 23
76,5
Fenol
1,07
41
182
Água pura
1,00
0
100
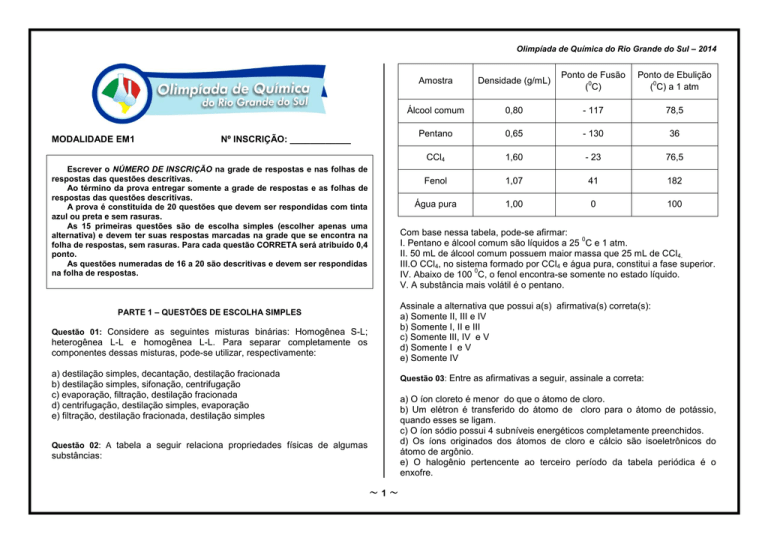
Com base nessa tabela, pode-se afirmar:
0
I. Pentano e álcool comum são líquidos a 25 C e 1 atm.
II. 50 mL de álcool comum possuem maior massa que 25 mL de CCl4.
III.O CCl4, no sistema formado por CCl4 e água pura, constitui a fase superior.
0
IV. Abaixo de 100 C, o fenol encontra-se somente no estado líquido.
V. A substância mais volátil é o pentano.
Assinale a alternativa que possui a(s) afirmativa(s) correta(s):
a) Somente II, III e IV
b) Somente I, II e III
c) Somente III, IV e V
d) Somente I e V
e) Somente IV
PARTE 1 – QUESTÕES DE ESCOLHA SIMPLES
Questão 01: Considere as seguintes misturas binárias: Homogênea S-L;
heterogênea L-L e homogênea L-L. Para separar completamente os
componentes dessas misturas, pode-se utilizar, respectivamente:
a) destilação simples, decantação, destilação fracionada
b) destilação simples, sifonação, centrifugação
c) evaporação, filtração, destilação fracionada
d) centrifugação, destilação simples, evaporação
e) filtração, destilação fracionada, destilação simples
Questão 03: Entre as afirmativas a seguir, assinale a correta:
a) O íon cloreto é menor do que o átomo de cloro.
b) Um elétron é transferido do átomo de cloro para o átomo de potássio,
quando esses se ligam.
c) O íon sódio possui 4 subníveis energéticos completamente preenchidos.
d) Os íons originados dos átomos de cloro e cálcio são isoeletrônicos do
átomo de argônio.
e) O halogênio pertencente ao terceiro período da tabela periódica é o
enxofre.
Questão 02: A tabela a seguir relaciona propriedades físicas de algumas
substâncias:
~1~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
.Questão 04: Na coluna da esquerda estão alguns compostos de sódio e, na
Questão 06: O ácido nítrico é forte, volátil à temperatura ambiente e oxidante
coluna da direita, algumas de suas aplicações importantes.
enérgico. É o segundo ácido mais fabricado e mais consumido na indústria
química, perdendo apenas para o ácido sulfúrico.
Suas principais aplicações são na produção de fertilizante agrícola, de
explosivos, de vernizes, resinas sintéticas, corantes, nylon, dentre outras.
Seus sais são os nitratos, destacando-se o nitrato de potássio, usado na
indústria de pólvora e o nitrato de amônio, na indústria de fertilizantes.
Modernamente, é produzido a partir do processo de Ostwald que consta,
basicamente, de três etapas:
1ª etapa: Queima da amônia, resultando no gás monóxido de nitrogênio.
2ª etapa: Reação do monóxido de nitrogênio com oxigênio, produzindo o
dióxido de nitrogênio.
3ª etapa: Reação do dióxido de nitrogênio com água, a alta pressão,
produzindo, por fim, esse ácido e, como subproduto, o monóxido de
nitrogênio.
Compostos
I – NaNO3
II- NaF
III- NaOH
IV- NaI
V- NaClO
Aplicações Importantes
(
(
(
(
(
) Fabricação de sabões
) Prevenção de cáries dentárias
) Desinfetante e alvejante
) Tratamento do bócio endêmico
) Explosivos e fertilizantes
Assinale a alternativa que relaciona corretamente cada composto com suas
respectivas aplicações.
a) III, II, V, IV, I
b) V, II, III, I, IV
c) III, IV, V, II, I
d) III, II, I, IV, V
e) I, II, V, IV, III
Baseado no texto acima, avalie as seguintes afirmações:
I- Na 1ª etapa, o número de oxidação do nitrogênio varia de 3+ para 2+.
II- A geometria molecular do gás produzido na 2ª etapa é linear.
III- No íon nitrato, o nitrogênio apresenta número de oxidação 5+.
IV- O grau de ionização do ácido nítrico é menor do que 50 %.
V- A soma dos menores coeficientes inteiros de todos os compostos
envolvidos na reação da 3ª etapa é igual a 7.
Questão 05: Sobre modelo atômico e elementos químicos são feitas as
seguintes afirmações.
I. Considerando os níveis de energia de um átomo, um salto quântico do
primeiro nível para o nível 3 é menos energético do que um salto quântico do
primeiro nível para o nível 2.
II. Ao voltar de um estado ativado para a sua posição fundamental, o elétron
recebe energia na forma de ondas eletromagnéticas.
III. Os elétrons são responsáveis pela maior parte da massa do átomo.
IV. Dois átomos que possuem o mesmo número de prótons pertencem ao
mesmo elemento químico.
V. Um elemento químico é identificado pelo seu número de massa.
Estão corretas:
a) Somente I, II, III e V
b) Somente II, III e IV
c) Somente I, IV e V
d) Somente II e IV
e) Somente III e V
Questão 07: Considere as três substâncias: HCl, HBr e HF. Das afirmativas
abaixo, assinale a correta:
Assinale a alternativa que possui a(s) afirmativa(s) correta(s):
a) A ordem crescente de ponto de ebulição é HF<HCl<HBr.
b) As três substâncias fazem ligações de hidrogênio.
c) Somente o HCl e o HBr fazem ligações de hidrogênio.
d) Todas as substâncias são moléculas polares.
e) O ácido com maior grau de ionização é o HF.
a) Somente II, III e IV
b) Somente I, II e III
c) Somente III, IV e V
d) Somente I, IV e V
e) Somente IV
~2~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
Questão 08: Em uma aula de laboratório de química o professor solicitou a um
Questão 10: Abaixo estão representados alguns materiais usados em um
grupo de alunos que produzissem um gás combustível, um gás nãocombustível e um sal insolúvel, nesta ordem, usando apenas uma solução
de ácido clorídrico.
Para isso, forneceu ao grupo, uma pequena amostra das seguintes
substâncias:
laboratório de química:
A- limalhas de ferro
B- solução de amoníaco
C- solução de nitrato de prata
D- bicarbonato de sódio, em pó
E- salmoura caseira
Assinale a alternativa cujas amostras que, ao reagirem com a solução do
ácido clorídrico, atendem a solicitação do professor.
a) B, D, E
b) A, D, C
c) D, A, C
d) B, A, E
e) A, D, B
Questão 09: Compostos contendo enxofre estão entre as principais impurezas
que existem em combustíveis derivados de petróleo, como óleo diesel e
gasolina.
Durante a queima industrial ou em veículos automotores desses
combustíveis, são lançados na atmosfera uma grande quantidade de dióxido
de enxofre, um dos principais responsáveis pela chuva ácida. Esse gás reage
com o oxigênio presente no ar, originando o trióxido de enxofre que, em
contato com a água, produz o ácido sulfúrico.
Baseado nessa última reação, um químico quer produzir 4,9 kg de ácido
sulfúrico. O volume de trióxido de enxofre, nas CNTP, que ele deve usar,
considerando rendimento da reação de 70 % é:
Assinale a alternativa que relaciona corretamente o material com a sua
respectiva aplicação.
(
) Para aquecimentos a seco (calcinações).
(
) Para medidas aproximadas de volumes de líquidos.
(
) Para separação de líquidos imiscíveis.
(
) Para dosagens precisas de líquidos, em análises volumétricas.
(
) Para preparar ou diluir soluções.
(
) Para condensar vapores em uma destilação.
(
) Para facilitar filtrações, por redução de pressão.
a) 784 L
b) 1600 L
c) 1120 L
d) 336 L
e) 3430 L
a) V, I, VI, VII, IX, III, X
b) VIII, IV, VI, VII, IX, X, III
c) II, VII, I, IV, VI, II, X
d) V, I, VI, IV, IX, II, III
e) V, IV, I, VII, VI, III, VIII
~3~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
Questão 11: Em uma aula de química inorgânica sobre os tipos de reações, o
HClO2- dá origem a sais que são usados para branqueamento de polpa de
celulose e papel e desinfecção de águas.
HClO- usado no tratamento de água potável e na produção de desinfetante
doméstico.
Sobre esses ácidos, são feitas as seguintes afirmações:
professor realizou dois experimentos.
No 1º experimento, ele misturou uma solução de nitrato de chumbo II com
uma solução de iodeto de potássio. Percebeu-se a formação de um sólido
insolúvel amarelo.
No 2º experimento, ele adicionou uma certa quantidade de solução de ácido
sulfúrico, em uma solução de carbonato de sódio. Percebeu-se uma certa
efervescência.
I- Todos são oxiácidos e fortes.
II- Os sais derivados do HClO2 são os cloritos.
III- Aquele em que o cloro apresenta menor nox é o ácido hipocloroso.
IV- O mais forte é o ácido clórico.
V- No ácido perclórico, o nox do cloro é 5+.
Ao questionar os alunos sobre esses experimentos, ele levantou as seguintes
afirmações:
Estão corretas:
a) Somente I, II e III
b) Somente II, IV e V
c) Somente II e III
d) Somente I e IV
e) Somente III e V
I- Em ambos os experimentos as reações são de dupla troca.
II- No 1º experimento, a reação é de dupla troca, mas no 2º experimento, é de
deslocamento.
III- O sólido insolúvel amarelo formado é o iodeto de chumbo II, de fórmula
química PbI2.
IV- A efervescência observada no 2º experimento foi causada pelo
desprendimento de um gás de caráter neutro.
V- Em ambos os experimentos, há formação de sais solúveis.
Estão corretas:
a) Somente I, III e V
b) Somente II, III e IV
c) Somente I e IV
d) Somente II e IV
e) Somente II e V
Questão 13: Tetracloreto de carbono (CCl4) é um líquido incolor, com cheiro
adocicado e característico, que pode ser detectado a baixas concentrações.
Foi muito usado como agente extintor e como agente refrigerante. Hoje a sua
produção e seu uso estão muito restritos, pois seus vapores destroem a
camada de ozônio e podem causar danos severos ao organismo humano,
principalmente no sistema nervoso central, pulmão, fígado e rins, além de
0
possuírem um potencial risco carcinogênico. À temperatura de 25 C, quais
substâncias abaixo são solúveis em tetracloreto de carbono?
Questão 12: O halogênio cloro, na sua forma diatômica, pura e nas CNTP, é
I- MgCl2
II- NH3
III- CO2
IV- I2
V- CS2
um gás de coloração amarelo-esverdeada, extremamente tóxico, odor
irritante e altamente reativo. Devido a essa alta reatividade, na natureza,
praticamente só é encontrado na forma combinada, destacando-se os
cloretos e cloratos. É o halogênio mais abundante da água do mar. É
empregado, principalmente, para potabilizar a água de consumo, como
desinfetante, branqueador e oxidante.
a) Somente I, II e V
b) Somente II, III e IV
c) Somente III, IV e V
d) Somente II e IV
e) Somente III e V
Seguem abaixo alguns ácidos de cloro e suas principais aplicações.
HClO4-oxidante poderoso, usado na fabricação de explosivos e herbicidas.
HClO3- dá origem a sais largamente usados na indústria, em pirotecnia,
fabricação de fósforo de segurança e produção de oxigênio.
~4~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
Questão 14: A tabela abaixo, mostra a solubilidade de gases em água pura,
gás clorídrico e o gás cianídrico, dentre outros. Sobre esses gases, são
feitas as seguintes afirmações:
I- O CO2 na forma de gelo seco apresenta-se sólido, devido às forças de van
der Waals existentes entre suas moléculas apolares.
II- O metano é uma substância composta, cuja molécula é polar e o oxigênio
do ar, é uma substância simples, que contém ligações covalentes polares.
III- O gás clorídrico e o gás cianídrico são substâncias polares e apresentam
geometria linear.
IV- O gás amônia apresenta geometria piramidal e em suas moléculas
ocorrem ligações de hidrogênio.
em g de soluto/10 g de água, a pressão de 1 atm.
0
Gás
Temperatura C
0
20
50
100
N2
0,0029
0,0019
0,0012
0
O2
0,0069
0,004
0,0027
0
CO2
0,335
0,169
0,076
0
SO2
22,8
10,6
4,3
1,8
NH3
89,9
51,8
28,4
7,4
Estão corretas:
a) Todas
b) Somente I, II e III
c) Somente I, III e IV
d) Somente III e IV
e) Somente II e III
Baseando-se nesta tabela, assinale a afirmativa INCORRETA:
QUESTÕES ANALÍTICO-EXPOSITIVA
a) Para todos os gases, quanto menor a temperatura, maior é a solubilidade.
b) Em todas as temperaturas, o gás de caráter básico é o que apresenta
maior solubilidade.
c) Na temperatura de ebulição da água, os gases de geometria linear são
totalmente insolúveis.
d) Na temperatura de congelamento da água, o principal constituinte do ar
atmosférico é o mais insolúvel.
e) Na temperatura de ebulição da água, os gases ácidos são totalmente
insolúveis.
Questão 16: O sulfato de alumínio é o mais tradicional agente coagulante
usado no tratamento de água para consumo humano. É empregado na etapa
de clarificação, onde provoca a aglutinação da matéria em suspensão,
formando flocos que ganham em densidade e sedimentam-se. Pode ser
obtido pela reação entre cloreto de alumínio e ácido sulfúrico.
a) Escreva a reação balanceada de obtenção desse composto.
b) Partindo-se de 534 g de sal, com 75 % de pureza, calcular a massa de
sulfato de alumínio obtida, considerando rendimento de 90 %.
c) Calcule a quantidade de matéria de enxofre existente em 855 g de sulfato
de alumínio puro.
d) Escreva a reação balanceada de obtenção do sulfato de alumínio,
substituindo o sal de alumínio por sua respectiva base.
Questão 15: A atmosfera terrestre é composta principalmente pelos gases
nitrogênio, oxigênio e argônio. Os demais gases, devido às suas
pequeníssimas quantidades, são referidos como traços, entre os quais estão
os gases do efeito estufa, como o gás carbônico, metano (CH4), ozônio e o
óxido nitroso. Vários poluentes industriais podem também estar presentes,
como o gás cloro, gases do enxofre (SO2 e SO3 principalmente), gás amônia,
~5~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
a) Faça a reação balanceada de decomposição do referido sal.
b) Qual o número de oxidação do bromo nos respectivos compostos da
reação?
c) Se forem adicionados 501 g de bromato de potássio na farinha, calcule o
volume, em L, de gás liberado, nas CNTP.
Questão 17: Considere as seguintes substâncias: cloreto de cobre II, trióxido
de enxofre, nitrato de prata, óxido de magnésio, tetrafluoreto de silício, ácido
sulfídrico, hidreto de fósforo e brometo de zinco.
a) Escreva a fórmula química das substâncias iônicas.
b) Escreva a fórmula química das substâncias moleculares.
c) Dê a geometria das substâncias moleculares.
d) Faça a reação balanceada entre nitrato de prata e brometo de zinco.
Questão 20: Deseja-se reaproveitar cada composto presente em um
determinado resíduo sólido de um laboratório de química.
A tabela abaixo fornece algumas propriedades físicas de cada componente
desse resíduo.
Questão 18: O elemento metálico X é não- magnético, bom condutor de calor
e muito usado em panelas de cozinha, latas, em papel para embalagem de
assados e em diversas ligas metálicas. O cátion de X é isoeletrônico do
cátion de outro elemento metálico Y, usado em pirotecnia e em folhas
fotográficas. Além disso, seu hidróxido é empregado na medicina como
antiácido e laxante. Os cátions de X e Y são também isoeletrônicos do ânion
do elemento Z, que apresenta 9 prótons.
Composto
Ponto de
O
Fusão ( C)
d (g/cm )
Solubilidade em
0
água, a 25 C
KNO3
334
---
Solúvel
Baseado no texto escreva:
MgCl2
714
---
Solúvel
a) O subnível mais energético do elemento X e do ânion do elemento Z.
b) O período e o grupo da tabela periódica do elemento Y.
c) As fórmulas químicas e o nome dos compostos formados pelos cátions X e
Y com o ânion Z.
d) A ordem crescente de raio atômico e de eletronegatividade, dos elementos
X, Y e Z.
BaSO4
----
4,5
Insolúvel
PEBD (polietileno de
baixa densidade)
----
0,91
Insolúvel
3
Baseado nos dados disponíveis, proponha um procedimento completo,
através de um fluxograma, que permita a recuperação de cada um desses
compostos.
Nesse fluxograma, deve constar o nome da operação de separação usada,
bem como, os componentes presentes em cada etapa.
Questão 19: Confirmado o uso de bromato em mistura para bolo. “O Ministério
da Agricultura (Mapa), coletou cinco amostras de mistura para bolo, para
analisar bromato. Dessas, quatro indicaram a presença da substância. O
bromato de potássio é potencialmente cancerígeno, sendo proibido seu uso
no Brasil. Ele é utilizado para melhorar o crescimento da massa.” (Correio do
Povo, 14 de junho de 2014).
O bromato de potássio é adicionado à farinha. Durante o processo de
aquecimento da massa resultante, ocorre a decomposição desse sal em seu
respectivo brometo, e a liberação de um gás, que é o responsável pela
obtenção de um pão de maior volume e de melhor textura.
Boa Prova!
Baseado no texto acima:
~6~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
GABARITO – QUESTÕES OBJETIVAS
ESPELHO QUESTÕES ANALÍTICO-EXPOSITIVAS
Questão 16 – RESPOSTA DO ESTUDANTE ALEXANDRE ANDREAS
QUESTÃO
01
02
03
04
05
06
07
08
09
10
11
12
13
14
15
PRIETO SAUERWEIN (COLÉGIO POLITÉCNICO DA UFSM)
ALTERNATIVA
CORRETA
a) 2 AlCl3 + 3 H2SO4 → Al2(SO4)3 + 6 HCl
A
D
D
A
E
E
D
B
B
A
A
C
C
E
C
b) 534 g de AlCl3 … 100 % de pureza
x
...... 75 %
x= 400,5 g
2 mols de AlCl3 = 267 g
1 mol de Al2(SO4)3 = 342 g
267 g de AlCl3.... 342 g de Al2(SO4)3
400,5 g
y
y..................... 100 % de rendimento
z ..................... 90 % de rendimento
z= 0,9 y= 0,9 x 400,5 x 342 x 1/267 = 461,1 g de sulfato de alumínio
c) 1 mol de Al2(SO4)3 ......342 g
y............................ 855 g
y= 2,5 mols
1 mol de Al2(SO4)3 …….. 3 mols de S
2,5 mols
Y
y= 7,5 mols de S
d) 2 Al(OH)3 + 3 H2SO4 → Al2(SO4)3 + 6 H2O
~7~
Olimpíada de Química do Rio Grande do Sul – 2014
Modalidade EM1
Questão 17 – RESPOSTA DO ESTUDANTE ARDEL EDNOR NUNES
Questão 19 –
JUNIOR (COLÉGIO MARISTA SÃO LUÍS DE SANTA CRUZ DO SUL)
a) 2 KBrO3 →2 KBr + 3 O2 ( por aquecimento)
a) CuCl2, AgNO3, MgO e ZnBr2
b) O nox do bromo no bromato é +5 e no brometo é -1
b) SO3, SiF4, H2S e PH3
c) SO3 – trigonal plana
piramidal
H2S – angular
SiF4 - tetraédrica
c) 2 KBrO3 → 3 O2
334 g
67,2 L
501
x
PH3 –
x= 100,8 L de O2
d) 2 AgNO3 + ZnBr2 → 2 AgBr + Zn(NO3)2
Questão 20 – RESPOSTA DO ESTUDANTE CASSIANO MOEHLECKE
Questão 18 – RESPOSTA DO ESTUDANTE IGOR WILBERT (FUNDAÇÃO
(FUNDAÇÃO ESCOLA TÉCNICA LIBERATO SALZANO VIEIRA DA
CUNHA DE NOVO HAMBURGO)
ESCOLA TÉCNICA LIBERATO SALZANO VIEIRA DA CUNHA DE NOVO
HAMBURGO)
a) X → 3p3
Solução aquosa de KNO3 + MgCl2 com BaSO4 no fundo e PEBD
flutuando. Decanta-se esse sistema e remove-se o PEBD da superfície
por raspagem com uma pá. Após, realiza-se uma filtração simples,
removendo o BaSO4 da solução. Aquece o sistema líquido até toda
água evaporar, sobrando apenas KNO3 e MgCl2. Coloca-se ambos os
sólidos em uma cápsula de porcelana e o sistema é aquecido até atingir
completa fusão do KNO3. Faz-se então, novamente, uma filtração
simples removendo o MgCl2 do KNO3, separando-se todos os
componentes.
Z - → 2p6
b) Terceiro período e grupo 2 ou grupo dos metais alcalino-terrosos.
c) XZ3 = AlF3 = fluoreto de alumínio
magnésio
e YZ2 = MgF2 = fluoreto de
d) ordem crescente de raio atômico F < Al < Mg ou Z < X < Y
ordem crescente de eletronegatividade: Mg < Al < F ou Y < X < Z
~8~












