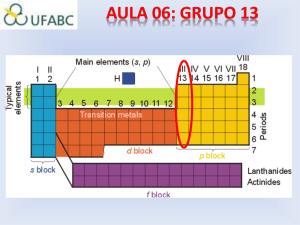
Elementos do Grupo 13 ou 3A
• O Grupo 13 (3A) da Tabela Periódica é formado pelos seguintes
metais: boro (B), alumínio (Al), gálio (Ga), índio (In) e tálio (Tl).
•Seus membros têm configuração eletrônica da camada de valência ns2np1 .
Logo, espera-se que seu número de oxidação máximo seja +3 .
•AlCl3 e GaCl3 são covalentes quando anidros, mas os elementos Al, Ga, In e
Tl formam íons em solução.
• Estado de Oxidação +1 (Efeito do Par Inerte)
Ga (I), In (I) e Tl (I)
• Os membros mais leves são encontrados na natureza em combinação com o
oxigênio, ou seja, na forma de óxidos.
Exemplos:
Na2B4O5(OH)4.8H2O Bórax
Al2O3.H2O Bauxita
BORO
• O boro não é encontrado livre na natureza, mas em jazidas
relacionadas a atividades vulcânicas, combinado com oxigênio e
sódio (BÓRAX).
Na2B4O5(OH)4.8H2O Bórax
Ponto de Fusão = 2079°C
Ponto de Ebulição = 2550 °C
Densidade = 2,37 g/cm3
• O boro é o único elemento da família 3A que pode ser considerado nãometálico.
• Há 13 isótopos do boro, no entanto, apenas 2 são estáveis:
B -10 : 19,85% de abundância
B -11: 80,2% de abundância
EXCEÇÃO À REGRA DO OCTETO
• B (Z = 5): 1s2 2s2 2p1 forma 3 ligações covalentes com outros elementos
não metálicos.
Isso resulta em uma camada de valência com somente 6 elétrons para o
Boro em seus compostos (2 a menos que o octeto).
Ex.: BF3
• Os compostos de Boro são bastante reativos. Boranos são compostos
contendo boro e hidrogênio.
BH3, B2H6
• O átomo de Boro pode acomodar um quarto par de elétrons, mas somente
quando esse par é fornecido por um outro átomo (ÁCIDO DE LEWIS).
• Moléculas ou íons com pares isolados de elétrons podem cumprir esse
papel (BASE DE LEWIS).
1. BF3 tem a maior parte de sua carga positiva no átomo do boro e sua carga
negativa localiza-se nos três átomos de flúor.
2. NH3 tem a maior parte de sua carga negativa localizado na região de pares de
elétrons livres (não ligantes).
3. Os elétrons livres ou não-ligantes da amônia atacam o átomo de boro do
trifluoreto de boro, preenchendo a camada de valência do boro.
Obtenção
2B
• Os tri-haletos de boro (BF3, BCl3 e BBr3) são ácidos de Lewis (possuem
afinidade por elétrons).
BF3 CL = 1,30 Å (menor que a soma dos raios covalentes: B = 0,80 Å , F =
0,72 Å).
• O principal composto com oxigênio é o B2O3 (sesquióxido).
• Um resfriamento rápido do B2O3 fundido conduz à formação de vidros de
borossilicatos (Pirex) que possui baixa dilatação térmica e não quebra
quando aquecido.
Ex: utensílios de cozinha e laboratório
O boro amorfo tem densidade igual a 2,34. O cristalino, mais puro, é muito
duro, tem brilho quase metálico e densidade igual a 3,3.
• O boro amorfo é usado em fogos de artifício, devido à coloração verde que
produz.
Compostos de Boro e Oxigênio
H3BO3 ou B(OH)3 ácido fraco (aceita íons OH-)
Ácido Ortobórico
ALUMÍNIO
• Há 23 isótopos de alumínio. Apenas 1 é estável: Al – 27
• Os demais são radioativos e possuem tempo de meia-vida da ordem de nanosegundos.
• O alumínio puro metálico não é encontrado na natureza. É encontrado combinado
principalmente com o oxigênio formando o óxido de alumínio (Al2O3) – BAUXITA
Obtenção
Hidrometalurgia do alumínio
•
O processo de Bayer:
– O minério triturado é dissolvido em NaOH 30% (em massa) a 150 - 230°C e alta
pressão (30 atm para impedir a ebulição).
– Al2O3 dissolve:
Al2O3.H2O(s) + 2H2O(l) + 2OH-(aq) → 2Al(OH)4-(aq)
– A solução de aluminato é separada através da redução do pH.
– A solução de aluminato é calcinada e reduzida para produzir o metal.
Eletrometalurgia do alumínio
• A célula de eletrólise do processo de Hall é usada para a produção do alumínio.
• O Al2O3 funde à 2000°C e não é prático fazer eletrólise no sal fundido.
• Hall: usa o Al2O3 purificado em criolita fundida (Na3AlF6, ponto de fusão
1012°C).
• Anodo: C(s) + 2O2-(l) → CO2(g) + 4e• Catodo: 3e- + Al3+(l) → Al(l)
• Os bastões de grafite são consumidos na reação.
• Processo de Bayer: a bauxita (~ 50 % de Al2O3) é concentrada para produzir
óxido de alumínio.
Eletrometalurgia do alumínio
•
•
•
•
•
Hall: usa o Al2O3 purificado em criolita fundida (Na3AlF6, ponto de fusão 1012°C).
Anodo: C(s) + 2O2-(l) → CO2(g) + 4eCatodo: 3e- + Al3+(l) → Al(l)
Os bastões de grafite são consumidos na reação.
Processo de Bayer: a bauxita (~ 50 % de Al2O3) é concentrada para produzir óxido de
alumínio.
Eletrometalurgia do alumínio
•
Para a produção de 1.000 kg de Al, precisamos de 4.000 kg de bauxita, 70
kg de criolita, 450 kg de anodos de C e 56 × 109 J de energia.
CORROSÃO
O alumínio em contato com a umidade e o ar reage rapidamente com o
oxigênio formando a uma fina capa de óxido que o protege de ataques
do meio ambiente.
Forma-se uma camada barreira que CORROSÃO protege o alumínio da
corrosão.
4 Al + 3 O2 → 2 Al2O3
Reações com ácidos e álcalis
Reações com oxigênio
Meio ácido
USOS DOS ELEMENTOS DO GRUPO 13
BORO. O composto de boro de maior importância econômica é o bórax,
empregado em grandes quantidades para a fabricação de fibras de vidro e
perborato de sódio.
O Boro é usado em reatores nucleares com a função de materiais de controle, é
usado para controlar e até mesmo finalizar a reação de fissão nuclear em cadeia,
pois o Boro é um ótimo absorvente de Nêutrons. Outros usos:
Fibras de boro são usadas em aplicações mecânicas especiais , como no âmbito
aeroespacial. Alcançam resistências mecânicas de até 3600 MPa.
O boro amorfo é usado em fogos de artifício devido a coloração verde que
produz.
ALUMÍNIO: O metal alumínio é moderadamente mole e fraco quando puro, mas
torna-se consideravelmente mais resistente quando combinado em ligas com outros
metais. Sua principal vantagem é seu baixo peso (densidade baixa, de 2,73 g.cm-3).
Algumas ligas são utilizadas para finalidades específicas: duralumínio, que contém
cerca de 4% de Cu, e diversos "bronzes de alumínio" (ligas e Cu e Al com outros
metais, como Ni, Sn e Zn). São muitos os usos do alumínio e de suas ligas:
• A maior parte da produção mundial destina-se às indústrias aeronáutica e
automobilística.
• Outra importante área de aplicação do alumínio é a fabricação do arame.
• Bom condutor de calor, o alumínio não tem gosto nem cheiro, por isso é usado em
utensílios de cozinha.
• Características de leveza (densidade cerca de 1/3 da do aço).
• Resistência mecânica (a resistência específica é o dobro ou o triplo da dos aços).
• Resistência à corrosão, ainda melhorada por tratamentos de superfície.
RECICLAGEM
• A reciclagem de latas é dividida em dez etapas, e se inicia com a
entrega da
latinha nos postos de coleta.
• Diferencial: poder ser usada para o mesmo fim, ao contrário das
garrafas
plásticas, que depois de recicladas não podem guardar alimentos.
AS CURIOSIDADES
Uma latinha de alumínio pesa apenas 14,5 gramas.
67 latinhas de alumínio correspondem a 1 kg.
Cada 1.000 kg de alumínio reciclado significa 5 mil kg de minério bruto (bauxita)
poupados.
O Brasil possui uma das três maiores reservas de bauxita do mundo.
Para reciclar o alumínio são gastos apenas 5% da energia utilizada na extração, ou
seja, uma economia suficiente para manter iluminadas 48 residências.
Todo o processo de reciclagem do alumínio no Brasil envolve mais de 2 mil
empresas.
No Brasil são consumidas 51 latas de alumínio por habitante por ano, enquanto
nos Estados Unidos esse número chega a 375 latas por habitante.
Uma lata de alumínio demora mais de 100 anos para se decompor na natureza.
GÁLIO, ÍNDIO E TÁLIO: Não há usos em grande escala desse elementos, mas pequenas
quantidades de Ga são empregadas para "dopar" cristais na fabricação de transistores.
A fabricação de semicondutores requer Ga de extrema pureza. O Ga é também usado
em outros dispositivos semicondutores. O arseneto de gálio, GaAs, é isoeletrônico com
o Ge, e é usado em diodos emissores de luz (LEDs=light emiting diodes) e diodos de
laser. O índio é usado para "dopar" cristais na fabricação de transistores p-n-p, e em
termistores (InAs e InSb). O índio também é utilizado em soldas de baixo ponto de
fusão (usadas comumente na solda de "chips" de semicondutores) e em outras ligas de
baixo ponto de fusão.