Priscilla Soares de Oliveira
Faculdade de Formação de Professores/UERJ
[email protected]
A DINÂMICA DOS NUTRIENTES NA ÁGUA E A SUA INFLUÊNCIA NO
PROCESSO DE EUTROFIZAÇÃO DO CANAL DO MANGUE.
INTRODUÇÃO
Os resíduos de substâncias de origem natural ou sintética constituem um dos mais
importantes fatores de degradação do meio ambiente pelo homem. Nesse sentido, os rios que
são elementos de suma importância na dinâmica da natureza, vêm sofrendo grandes impactos.
O rio Maracanã, situado no Estado do Rio de Janeiro recebe uma grande carga de
efluentes que são inseridos em suas águas de diversas maneiras, tendo como principal fonte o
esgoto, acabando por deposicionar grande quantidade de nutrientes e compostos químicos
ricos em fósforo e nitrogênio. Estes são elementos essenciais para vida dos organismos sendo
considerados nutrientes limitantes para a produtividade primária em sistemas de água doce.
Assim como o oxigênio, carbono, água, a dinâmica do nitrogênio e do fósforo na
natureza pode ser entendida através dos denominados ciclos biogeoquímicos que são
processos naturais de reciclagem de vários elementos em diferentes formas químicas do meio
físico para os organismos e vice-versa.
As aplicações industriais dos compostos de nitrogênio são bastante variadas:
fertilizantes, explosivos, medicamentos, cosméticos, pigmentos, nylon, entre outras. E embora
amplamente empregado e abundante na natureza sua obtenção em forma utilizável não é fácil.
Em relação ao ciclo do fósforo, se dá tipicamente de forma sedimentar. O fósforo é
liberado dos reservatórios - as rochas de fosfato, depósitos de guano (excremento de aves
marinhas) e depósitos de animais fossilizados - por erosão natural e filtração, e através da
mineração e do uso como adubo pelo homem. O fósforo geralmente está na presente na
natureza na forma de fosfato orgânico e inorgânico.
Os estudos sobre a dinâmica do fósforo em microbacias hidrográficas, bem como de
outros contaminantes, ajudam a estimar os impactos e suas conseqüências nos ecossistemas
aquáticos. O fósforo também pode ser considerado uma importante ferramenta que auxilia a
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
1
visibilizar as conseqüências do uso inadequado do solo. Nesse sentido, os rios, que são
elementos de suma importância na dinâmica da natureza, vêm sofrendo grandes impactos.
Nas áreas urbanas, os rios encontram-se degradados devido à ação antrópica que causa
transtornos ambientais e sociais. A cada ano se tornam mais eutrofizados.
O processo de eutrofização é o aumento da concentração de nutrientes,
particularmente fósforo e nitrogênio, nos ecossistemas aquáticos, que tem como conseqüência
o aumento de suas produtividades. Suas principais fontes são os efluentes domésticos;
efluentes industriais; escoamento superficial; chuvas. O Canal do Mangue, situado no Estado
do Rio de Janeiro recebe uma grande carga de efluentes que são inseridos em suas águas de
diversas maneiras, tendo como principal fonte o esgoto.
O objetivo deste presente trabalho é analisar como as altas taxas de nutrientes podem
contribuir para a diminuição do oxigênio no Canal do Mangue, situado na cidade o Rio de
Janeiro.
ÁREA DE ESTUDO
A Bacia do Canal do Mangue possui área de drenagem com cerca de 44,6 km², que
correspondendo aproximadamente 1% do total da área continental de contribuição à Baía de
Guanabara. Seu perímetro é da ordem de 32,9 km e sua altitude máxima, localizada no
Maciço da Tijuca, atinge 826 m.
É limitada, ao Norte, pela própria Baía de Guanabara; ao Sul, pela Serra da Carioca;
a Leste principalmente pelo Morro de Santa Tereza e a Oeste, pela Bacia do Canal do
Cunha. O Canal do Mangue tem como principal formador o rio Maracanã, cujas nascentes se
encontram na área do Parque Nacional da Tijuca, em cotas da ordem de 680 m, na parte Sul
da bacia. O talvegue principal da bacia, formado pelo rio Maracanã e o trecho do Canal do
Mangue, a jusante, se apresenta na direção SW-NE, com extensão de 11 km e sua bacia tem
formato intermediário entre o arredondado e o alongado.
A área está inteiramente abrigada pelo Município do Rio de Janeiro. A
desembocadura do Canal está a Sudoeste da Baía de Guanabara na região do Cais do Porto.
Este eixo principal apresenta três trechos distintos: trecho alto, de aproximadamente 1 km,
onde o desnível é da ordem de 400 m, o trecho médio, que apresenta declividade mais
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
2
branda, com 2,2 km de extensão e desnível de 200 m, onde já aparece a mancha urbana e o
trecho inferior com cerca de 8km de extensão e baixa declividade.
A bacia se encontra densamente ocupada, e ainda hoje sofre com pressões do
processo de expansão da mancha urbana sobre as poucas áreas que ainda restam com
cobertura vegetal. Preservam-se principalmente as áreas mais elevadas pertencentes ao
Parque Nacional da Tijuca. Diversos fatores afetam a área e geram zonas críticas: influência
da maré, cotas extremamente baixas, trechos onde o gradiente de declividade é baixo,
diversas obras hidráulicas inadequadas, assoreamento, ocupação de encostas e lixo. A
qualidade da água do Canal do Mangue e do seu principal formador, o Rio Maracanã,
continua sofrendo sérios impactos em virtude dos descartes domésticos e industriais
produzidos nesta região.
A Região que hoje abriga o bairro Maracanã fazia parte de uma das 21 freguesias ou
paróquias, que formavam o Rio de Janeiro no século XVIII, freguesias que eram divididas
sob aspecto eclesiástico. A freguesia de São Francisco Xavier do Engenho Velho foi criada
em 1762 e pertencia à Ordem dos padres Jesuítas, que utilizavam a área como lavoura de
diversas culturas como arroz, cacau, etc. A freguesia abrigava os antigos bairros do Andaraí
Grande e Andaraí Pequeno, Aldeia Campista, Fábrica das Chitas e Vila Isabel.
Posteriormente formaram a região da Grande Tijuca.
Em 1818 a 1823 foi feito o primeiro plano de captação de suas águas, com a
construção de um encanamento provisório até o Campo de Santana (atual Praça da
República).
O novo encanamento foi realizado na década de 50 do século XIX no baixo curso
do rio, onde o terreno era um alagadiço e devido ao elevado grau de urbanização ocorrido na
área gerou problemas antagônicos. Com isso, devido à urbanização relacionada à valorização
do solo, foi expandida a canalização do rio Maracanã em 1950, gerando freqüentes
inundações. Essas enchentes causadas pela impermeabilização dos solos juntamente com a
redução do espaço para o fluxo de água(diminuição na vazão regular do rio) aumentam o
volume dos rios que acabam transbordando.
A área da atual Grande Tijuca, onde está o bairro Maracanã, era nos primórdios da
colonização do Brasil um grande território pantanoso. O adensamento populacional do bairro
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
3
Maracanã, seu desenvolvimento urbano e seu processo de edificação foram condicionados
pelo leito do rio.
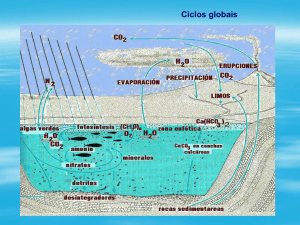
OS CICLOS BIOGEOQUÍMICOS
Segundo Braga (2002), os elementos que são essenciais a vida participam de uma
trajetória desde um meio inanimado, passando pelos organismos vivos e retornando ao meio
original. De acordo com ele um elemento essencial que seja disponível para todos os
produtores, em forma molecular ou iônica, recebe o nome de nutrientes. A partir disso
podemos classificar os nutrientes em dois grupos: macronutrientes, que participam em
quantidades superiores a 0,2 por cento do peso orgânico seco, e os denominados
micronutrientes, que participam em quantidades inferiores a 0,2 por cento do peso orgânico
seco de um ser vivo.
No grupo dos macronutrientes podemos citar: Carbono, Hidrogênio, Oxigênio,
Nitrogênio e o Fósforo. Já como micronutrientes podemos citar: o Alumínio, Boro, Cromo,
Zinco, Vanádio, entre outros. Esses elementos essenciais fazem parte de ciclos que recebem
o nome de biogeoquímicos. Bio, porque os organismos vivos interagem no processo de
síntese orgânica e decomposição dos elementos; Geo, porque o meio terrestre é a fonte dos
elementos, e químico, porque são ciclos de elementos químicos (Braga, 2002).
Ainda de acordo com Braga, 2002, o ciclo que foi relatado acima pode se distinguir
em três tipos, sendo dois tipos referindo-se ao ciclo dos elementos vitais – onde se encontram
os macros e micronutrientes – e o outro que se refere ao ciclo de um composto vital: a água.
Esses ciclos são chamados de ciclo hidrológico, sedimentares e gasosos. Portanto, nos ciclos
sedimentares (como por exemplo, do fósforo), o reservatório que supre os elementos e os
recebe de volta é a litosfera, ao passo que nos ciclos gasosos (como por exemplo, do
nitrogênio), o reservatório é a atmosfera.
OS MACRONUTRIENTE – O FÓSFORO E O NITROGÊNIO
NITROGÊNIO - O nitrogênio, que compõe 78% das partículas do ar, é incolor, inodoro e
principalmente inerte em condições ambientais, o que garante que o oxigênio (O2) disperso
na atmosfera não incendeie a vegetação do planeta. O Nitrogênio é um dos elementos mais
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
4
importantes no metabolismo de ecossistemas aquáticos, graças à sua participação na
formação de proteínas, um dos componentes básicos dos seres vivos. Quando presente em
baixas concentrações pode atuar como fator limitante na produção primária dos lagos e
reservatórios.
As principais fontes naturais de N são: a chuva, material orgânico e inorgânico de
origem externa e a fixação biológica no lago por bactérias e algas cianofíceas. O Nitrogênio
apresenta-se sob várias formas: nitrato (NO3-), nitrito (NO2-), amônia (NH3), íon amônio
(NH4+), óxido nitroso (N2O), nitrogênio molecular(N2), nitrogênio orgânico dissolvido
(peptídeos, purinas, aminas, aminoácidos, etc.), nitrogênio orgânico particulado (bactérias,
fitoplâncton, zooplâncton e detritos), etc.
O nitrogênio, mesmo ocorrendo em grande quantidade na atmosfera, não pode ser
aproveitado diretamente pelos vegetais e animais. Entretanto, algumas bactérias e alguns azuis
(cianofíceas) podem fixar e utilizar o nitrogênio atmosférico nos solos e na água. Nas raízes
das leguminosas, por exemplo, encontramos nódulos que abrigam um número imenso destas
bactérias que vivem em simbiose com a hospedeira.
FÓSFORO - O ciclo deste elemento é tipicamente sedimentar. O fósforo é liberado dos
reservatórios - as rochas de fosfato, depósitos de guano (excremento de aves marinhas) e
depósitos de animais fossilizados - por erosão natural e filtração, e através da mineração e do
uso como adubo pelo homem. O fósforo geralmente está presente na natureza na forma de
fosfato orgânico e inorgânico. As plantas usam o fosfato inorgânico para produzir compostos
orgânicos necessários para a vida. O fósforo inorgânico é absorvido pelos vegetais sob a
forma de ortofosfato. E os animais recebem esse elemento ao ingerir as plantas.
O fósforo no ecossistema aquático
Este elemento é essencial para a vida dos organismos, sendo considerado como um dos
principais limitantes da produtividade primária do sistema de água doce. A produção dos
fictoplânctos em ecossistemas de água doce é comumente limitada pelo fósforo e menos
comumente pelo nitrogênio e sílica.
A interação qualitativa e quantitativa entre os sedimentos e a água é o fator que determina
a disponibilidade do fósforo na água. As quantidades e formas de fósforo presente no
escoamento e no deflúvio superficial são dependentes, das fontes de poluição, dos
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
5
mecanismos de transferência de sedimentos e fósforo, das transformações que ocorrem
durante a sua trajetória.
O fósforo no sistema aquático esta sob a forma de fosfato, sendo o ortofosfato a
forma mais comum e a mais utilizada pelos vegetais. Tais compostos estão em quantidades
muito pequenas na água, porém constituindo um importante elemento componente da
substância viva (nucleoproteínas), além de estar ligado ao metabolismo respiratório e
fotossintético.
Portanto, assim como o nitrogênio, o fósforo deve ser continuamente removido da
água pela plantas, competindo com o solo, onde o mesmo (fósforo) é fortemente adsorvido,
fixando-se no fundo em formas relativamente indisponíveis.
Em meio alcalino, águas ricas em cálcio forma-se o fosfato de cálcio que se precipita
no sedimento, e em águas com ferro e alumínio o fosfato é liberado para as águas quando em
condições redutoras. Quando de elevado teor de oxigênio, águas ricas em ferro fazem
precipitar a forma fosfato ferroso insolúvel, juntamente com o hidróxido férrico que se forma
sob as mesmas condições, portanto um fator considerável para redução do elemento fósforo
é a oxigenação das águas.
Os estudos sobre a dinâmica do fósforo em microbacias hidrográficas, bem como de
outros contaminantes, ajudam a estimar os impactos e suas consequências nos ecossistema
aquáticos. O fósforo também pode ser considerado uma importante ferramenta que auxilia a
visibilizar as conseqüências do uso inadequado do solo.
As fontes geradoras de fósforo, podem tanto ser de ordem natural, artificiais e
antropogênicas. Por tanto, as principais fontes, não só deste nutriente para a água, como
pode-se observar na figura abaixo são: minerais fosfáticos, (apatitas); despejos domésticos,
industriais, fezes de animais, decomposição da matéria orgânica, entre outros, sendo que
na natureza ele não aparece em estado puro, por ser muito reativo em contato com o ar
(com o oxigênio explode, formando o fosfato –PO4), a não ser dentro de alguns meteoritos
ou quando produzido em laboratórios armazenado sem presença de oxigênio.
O PROCESSO DE EUTROFIZAÇÃO DOS SISTEMAS AQUÁTICOS
Eutrofização é o enriquecimento das águas de ecossistemas aquáticos através do
aumento da concentração de nutrientes, principalmente nitrogênio e fósforo. Esse
enriquecimento tem ligação direta com o aumento da produtividade do meio; e em
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
6
conseqüência desse processo o ambiente passa de um estado oligotrófico e mesotrófico para
a condição de eutrófico ou hipertrófico.
O processo de eutrofização pode ocorrer naturalmente ou ser induzido pela ação do
homem. Quando ocorre de forma natural o processo é considerado lento e é um resultado do
acúmulo de nutrientes trazidos pelas chuvas e águas superficiais. Quando esse processo é
induzido pelo homem ele acontece de maneira rápida e a eutrofização passa a ser uma doença
para os reservatórios de água doce.
A eutrofização artificial pode ser considerada como uma forma de poluição, pois ela
provoca inúmeras mudanças dentro de um ecossistema aquático. São várias as fontes
geradoras dessa eutrofização, mas a principal é o crescimento populacional e a falta de
educação ambiental da maioria das pessoas.
ESTEVES (1998) enumera como sendo fontes de eutrofização artificial os efluentes
domésticos, industriais, agropastoris e as chuvas. Ele afirma que essas fontes liberam
nutrientes, como fosfato e nitrogênio, que são compostos estimuladores da eutrofização.
Os efluentes industriais provocam grandes alterações nos níveis de fósforo e
nitrogênio dos lagos; entre as indústrias merece destaque as da área alimentícia, pois são as
principais fontes de efluentes orgânicos, ricos em fósforo e nitrogênio.
Entre as atividades agrícolas e pastoris a que tem mais efeitos sobre a eutrofização é a
atividade agrícola, essa interferência aumentou consideravelmente apartir da década de 40
com a introdução de superfosfatos como sendo uma forma de melhorar a produção agrícola.
As chuvas são os elementos principais na eutrofização natural mais também contribui
para a eutrofização artificial especialmente nas regiões de intensa poluição atmosférica.
ESTEVES (1998) relata que lagos localizados próximos a rodovias podem receber aporte
adicional de fosfato e nitrogênio, devido ao tráfego de veículos, principalmente nos períodos
de chuva. Todas essas interferências aos ambientes aquáticos trazem inúmeras conseqüências
e características que facilitam a identificação desses ambientes.
MÉTODO
Para a realização da metodologia executamos os seguintes processos: realização de
campo para coleta de 10 amostras de água e 10 amostras de sedimentos; no laboratório
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
7
foram realizadas análises do teor de matéria orgânica por queima da mesma com Peróxido
10% nos sedimentos; análises de oxigênio dissolvido em água través do método de Winkler e
a quantificação de nutrientes pelo método colorímetro de Denigés.
RESULTADOS PRÉVIOS
Como resultados prévios obtivemos as seguintes concentrações variando para, o PO4
no primeiro campo de 0,22 mg/L a 7,82 mg/L e no segundo variando de 0 (abaixo do limite
de detecção) a 151,68 mg/L; NO2 variando de 0,1 mg/L a 6,18 mg/L no primeiro campo e
no segundo de 2,18 mg/L a 12,44 mg/L. Em relação a matéria orgânica obtemos a seguinte
variação no primeiro campo, 0,41g a 4,35g e no segundo campo resultados variando de
0,01g a 1,21g. Já na concentração de oxigênio obtivemos valores entre 6,02 a 67,11 no
primeiro campo e 2,36 a 59,21 no segundo campo. O gráfico a baixo ilustra os dados
relatados acima.
Figura 3 - O gráfico acima demonstra os resultados das análises,
mostrando as porcentagens de: Fosfato, Nitrato, Matéria Orgânica e
Oxigênio.
Segundo o Art. 17, da resolução Conama 357/2005, as águas doces de classe 4
apresentarão as seguintes condições e padrões:
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
8
1.
2.
3.
4.
5.
6.
7.
Materiais flutuantes, inclusive
espumas não naturais: virtualmente
ausentes;
Odor e aspecto: não objetáveis;
Óleos e graxas: toleram-se
iridescencias;
Substancias facilmente
sedimentáveis que contribuam para
o assoreamento de canais de
navegação: virtualmente ausentes;
Fenóis totais (substancias que
reagem com 4 - aminoantipirina)
ate 1,0 mg/L de C6H5OH;
OD, superior a 2,0 mg/L O2 em
qualquer amostra;
pH: 6,0 a 9,0;
8. Fósforo total máximo de 0,05
mg/L
9. Nitrogênio total máximo de 10,0
mg/L;
10. Oxigênio superior a 2,0 mg/L em
qualquer amostra;
11. pH: 6,0 a 9,0.
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
9
Através das analises dos dados obtidos foi possível realizar uma correlação entre os
parâmetros medidos e a concentração dos poluentes estudados, assim como visualizar a
fração química destes, verificando seus comportamentos e processos de remobilização
visualizando assim a mobilidade e a biodisponilibilidade destes elementos para a biota deste
ecossistema. Como a pesquisa também está comprometida em outros tipos de análises que se
dão de forma sazonal, a mesma já se encontra em seu segundo estágio de coletas e análises
em laboratório.
CONSIDERAÇÕES FINAIS
Concentração de nutrientes: o aumento dos nutrientes em um ecossistema faz com
que o mesmo produza mais do que sua capacidade para consumir, esse desequilíbrio
traz conseqüências para o metabolismo do ecossistema. O tipo de nutrientes
acumulado depende da fonte de efluentes a que está exposto o ambiente.
Conseqüências para a comunidade fitoplanctônica: concentração de nutrientes
favorece o aumento da produção do fitoplâncton que por sua vez limita a produção
primária nas camadas inferiores devido às precárias condições de luminosidade.
Conseqüências sobre as comunidades de macrófitas aquáticas: no início da
eutrofização artificial ocorre o crescimento de diferentes grupos ecológicos de
macrófitas aquáticas. Porém no decorrer do processo esse crescimento diminui, uma
vez que a superfície da água fica espessa impedindo a entrada da luz, prejudicando o
crescimento tanto das macrófitas submersas quanto das emersas.
Conclui- se que a eutrofização causa grande desequilíbrio ecológico, com a diminuição do
número e quantidade das espécies aquáticas. Torna o meio impróprio para o lazer, o qual se
converte num local de disseminação de doenças e pode diminuir a atividade piscícola. Diante
dessa problemática faz-se necessário uma reflexão crítica das ações do homem sobre os
ecossistemas aquáticos, visando encontrar soluções para a minimização desse problema na
nossa realidade.
Bibliografia
AMADOR, E.S. 1997. Baia de Guanabara e ecossistemas periféricos - Homem e
Natureza. Rio de Janeiro, Retroarte Gráfica e Editora. 539 p.
ABESSA, D. M. 2002. Avaliação da Qualidade dos Sedimentos do Sistema
Estuarino de Santos, Tese de Doutorado, Instituto Oceanógrafo. Universidade de
São Paulo, 290 p
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
10
BAPTISTA NETO, J.A. 1996. Sedimentological evidence for human impact on a
nearshore sedimentary environment: Jurujuba Sound, Rio de Janeiro State, Brazil. 330
pp. (Ph.D. dissertation, The Queen’s University of Belfast, Irlanda do Norte/Reino
Unido).
BAPTISTA NETO, J.A. 1993. Sedimentologia e Geomorfologia da Enseada de
Jurujuba – Niterói (Baía de Guanabara) / RJ. Dissertação de Mestrado – Programa
de Pós graduação em Geologia e Geofísica Marinha/Departamento de Geologia –
Universidade Federal Fluminense, pp. 131
BRAGA, E. S. 1989. Estudo dos Nutrientes Dissolvidos nas Águas da Enseada das
Palmas, Ilha Anchieta (Ubatuba – São Paulo), com ênfase as formas nitrogenadas e
contribuição dos aportes terrestres e atmosféricos. Dissertação de Mestrado, Instituto
de Oceanografia. Universidade de São Paulo, 207 p.
BRAGA, E. S. 1995. Nutrientes Dissolvidos e Produção Primária do Fictoplancton
em Dois Sistemas Costeiros do Estado de São Paulo. Tese de Doutorado,
Universidade de São Paulo. Departamento de Oceanografia. Geologia 2 vol.
ESTEVES, F. A. 1998. Fundamentos de Limnologia, 2ª Edição. RJ, Editora
Interciência
FEEMA – Fundação Estadual de Engenharia do Meio Ambiente,1992: Coletânea de
Legislação federal e estadual de meio ambiente. Rio de Janeiro.
Relatório PDBG-FEEMA/ dezembro1997).
VON SPERLING, M. Introdução à Qualidade das Águas e ao Tratamento de
Esgotos, Desa-UFMG, 1996
Realizado de 25 a 31 de julho de 2010. Porto Alegre - RS, 2010. ISBN 978-85-99907-02-3
11