Nome:
Série:
Turma:
Data:
Questão 1 (Ufal - 2008)
A matéria existe, principalmente, em três estados físicos: sólido, líquido e gasoso. A
maior parte da matéria é constituída por mistura de substâncias. Cada substância possui
um conjunto único de propriedades físicas e químicas que pode ser utilizado para
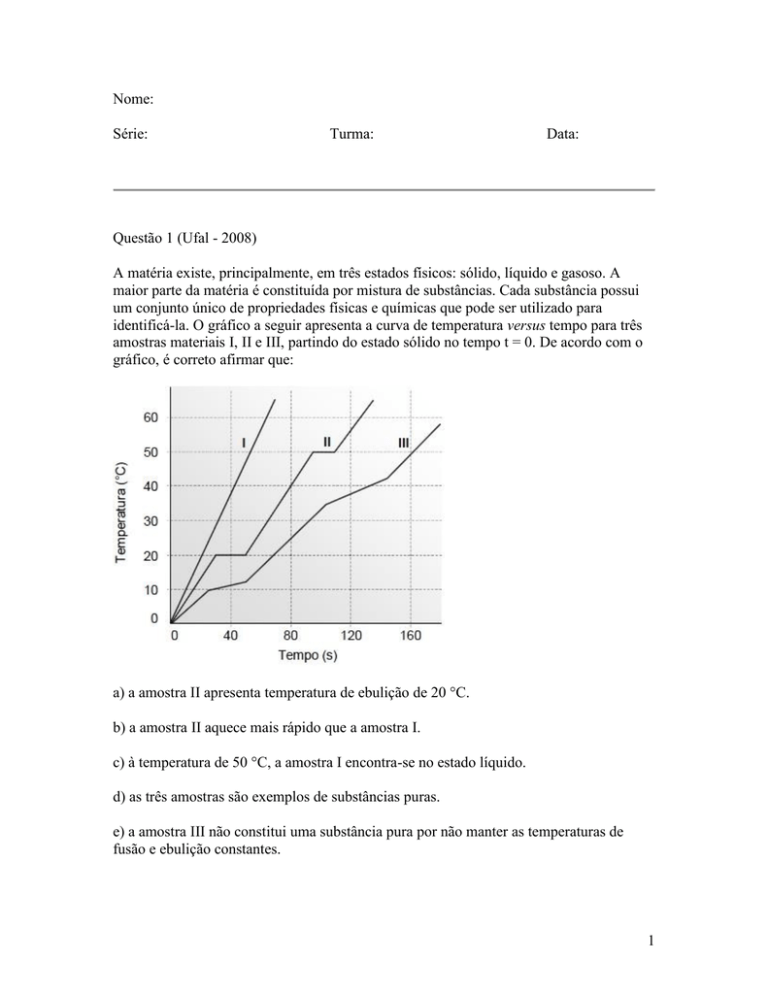
identificá-la. O gráfico a seguir apresenta a curva de temperatura versus tempo para três
amostras materiais I, II e III, partindo do estado sólido no tempo t = 0. De acordo com o
gráfico, é correto afirmar que:
a) a amostra II apresenta temperatura de ebulição de 20 °C.
b) a amostra II aquece mais rápido que a amostra I.
c) à temperatura de 50 °C, a amostra I encontra-se no estado líquido.
d) as três amostras são exemplos de substâncias puras.
e) a amostra III não constitui uma substância pura por não manter as temperaturas de
fusão e ebulição constantes.
1
Questão 2 (UFG - 2008)
Quando a água solidifica, a uma pressão constante e igual a 1,0 atm, sua densidade
diminui.
Já com o dióxido de carbono verifica-se que, a 73 atm, a solidificação resulta num sólido
de densidade maior que o líquido original. Considerando essas informações,
(A) esboce o diagrama de fases do dióxido de carbono, indicando o ponto triplo (217 K e
5 atm) e as constantes críticas (304 K e 74 atm);
(B) explique as diferenças entre as densidades desses materiais durante o processo de
solidificação.
Questão 3 (Unemat - 2010)
Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos
dados na tabela abaixo.
Substância
I
II
III
IV
Temperatura
de
fusão (°C)
42
1.530
–218
–63
Temperatura
de
ebulição (°C)
185
2.885
–183
91
Com bases nos dados da tabela, pode-se afirmar.
a. Num ambiente a –80 °C, nenhum dos compostos estará na sua forma gasosa.
b. O composto II estará na forma líquida a 550 °C.
c. A 100 °C, os compostos I e III estarão na forma gasosa.
d. Existe um valor de temperatura acima de 0 °C em que as quatro substâncias estarão na
forma sólida.
2
e. Numa temperatura de 25 °C, apenas os compostos I e II estarão na forma sólida.
Questão 4 (Uneb - 2008)
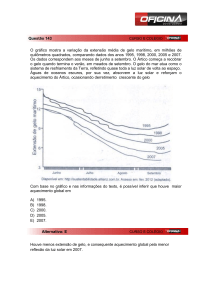
Cientista da Universidade do Colorado, nos EUA, afirma, com base no estudo de imagens
reveladas por dispositivos a bordo de satélites, como o F8, que a capa de gelo do mar
Ártico diminuiu 9% a cada década dos últimos 30 anos, e estudos revelam que, nos
últimos 20 anos, o aquecimento do oceano Ártico foi oito vezes maior do que a média
dos últimos séculos. Embora o derretimento
nessa região pouco chega a elevar o nível dos oceanos, é fator de incremento à tendência
de aquecimento global, uma vez que a camada glacial reflete com mais intensidade os
raios do Sol do que o mar aberto.
Associando-se o fenômeno de derretimento do gelo do oceano Ártico ao aquecimento do
planeta, tendo como referência os conhecimentos de química, é correto afirmar:
01) O derretimento do gelo do oceano Ártico vem aumentando a quantidade total de água
no planeta.
02) O calor absorvido durante a fusão de 1,0 ton de gelo é igual ao liberado durante a
solidificação de igual massa de água, nas mesmas condições.
03) O derretimento do gelo do oceano Ártico implica aumento da salinidade e da
densidade das águas oceânicas no Hemisfério Norte.
04) A passagem de água do estado sólido para o estado líquido tem como consequência o
aumento de ligação de hidrogênio entre moléculas de água.
05) A fusão de um bloco de 10,0 km3 de gelo do mar Ártico produz mais de 10,0 km3 de
água líquida, que é pouco significativa para elevar o nível dos oceanos.
Questão 5 (Uneb - 2008)
O gelo que antes ficava sobre a terra contribui para o nível global do mar tão logo
comece a flutuar. Um iceberg – com sua maior parte abaixo da superfície oceânica – já
está deslocando o mesmo volume de água que deslocaria caso liquefeito [...] Na
Antártida, baixas temperaturas, cerca de –34°C, em média, significam que o gelo
continental quase nunca se derrete. Isto pode mudar se o aquecimento global tornar-se
mais intenso na região; mas, atualmente, a Antártida só influi no nível dos oceanos
quando o gelo sólido – levado à orla marítima por geleiras costeiras ou por esteiras
transportadoras naturais, chamadas correntes de gelo – desprende-se ou adere às
3
plataformas de gelo existentes.
(GÉLlDAS Perspectivas, 2007, p. 30).
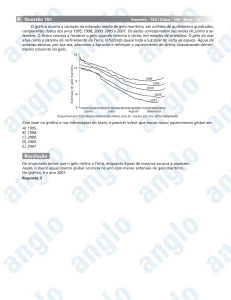
Uma análise dos efeitos das mudanças climáticas causadas sobre as capas glaciais
antárticas e da conclusão de que não é preciso que o gelo derreta para fazer subir o nível
dos oceanos permite afirmar:
1) A densidade dos icebergs é superior à das águas dos mares da Antártida.
2) A água dos oceanos congela abaixo de 0 ºC em razão da presença de inúmeros sais
dissolvidos.
3) O sistema, formado por iceberg e água do mar, possui dois componentes de iguais
tensões superficiais.
4) Os icebergs só contribuem para elevar o nível dos oceanos enquanto permanecerem
flutuando no mar.
5) O deslizamento do gelo por esteiras transportadoras naturais é consequência das
intensidades da força de atrito e do peso do gelo serem iguais.
Questão 6 (UFV - 2010)
A calda de caramelo utilizada em doces e pudins é preparada pelo aquecimento do açúcar
comercial (sacarose, C12H22O11). Considerando as propriedades físicas e químicas da
sacarose, assinale a afirmativa CORRETA:
a) Durante a fusão ocorre quebra de ligações químicas.
b) A interação entre as moléculas de sacarose é do tipo íon-dipolo.
c) Forças intermoleculares são rompidas em uma mudança de estado físico.
d) A sacarose é líquida na temperatura de 25 oC e 1 atm.
Questão 7 (UnB - 2010)
Composto
Nome
Fórmula
Propriedades (a 1 atm)
Ponto de
Ponto de
4
ácido
H2S
fusão (°C)
–82,3
ebulição (°C)
–60,3
sulfídrico
dióxido de carbono
CO2
–78,0
–57,0
metano
CH4
–182,5
–161,6
amônia
NH3
–77,7
–33,3
ácido
CH3CH2COOH
–20,5
141,2
propanoico
putrescina
H2N(CH2)4NH2
27
158
A partir dessas informações, julgue os itens a seguir (certo ou errado).
• Os dados da tabela permitem inferir que, na temperatura de 0 °C e à pressão de 1 atm,
as substâncias putrescina e ácido propanoico encontram-se no estado sólido, e as demais
da tabela, no estado gasoso.
• NH3 e CH4 são exemplos de moléculas com geometrias piramidal e tetraédrica,
respectivamente.
Questão 8 (PUC-Camp - 2010)
Marte é o futuro
1
Aos onze anos de idade, no final dos anos 1960, o
clímax do entusiasmo de qualquer menino era alcançado
com um foguete Saturno-5, que levou o homem à Lua em 20
5
de julho de 1969. Depois da Lótus verde de Jim Clark, claro,
que voava baixo nas pistas de automobilismo. Tudo de bom
5
ainda era “made in USA”, como as cobiçadas calças Lee
(pelas quais um adolescente brasileiro pagava os olhos da
cara junto a importadores clandestinos). Hoje as façanhas da
corrida espacial são produzidas na China, como quase tudo
10 mais. Prepara-se a Longa Marcha para a Lua e, talvez, Marte. A empreitada soa tão verossímil quanto a consagração do
vocábulo “taikonauta” no dicionário espacial, ao lado de
“astronauta” (Estados Unidos) e “cosmonauta” (Ex-União
Soviética).
15 Naquela noite de julho em Ubatuba, quarenta anos
atrás, foi preciso encontrar um aparelho de TV. Poucas casas de veraneio no bairro do Itaguá, do lado de lá do aeroporto
onde pousaram alguns DC-3 da Vasp, contavam com
esse eletrodoméstico de luxo. Pai e filho acabaram por
20 encontrá-lo no casebre de um dos moradores permanentes,
num arrabalde povoado por caiçaras. Foi uma grande decepção em preto e branco. Era péssima a qualidade da imagem
recebida pelo par de antenas em V, apesar dos suplicantes
chumaços de palha de aço nas pontas. Manchas e fantas25 mas se arrastavam pelo que bem poderia ser um cenário
montado com queijo suíço, como pronunciou um dos céticos
presentes. O feito se confirmaria depois com a publicação
das famosas fotos da câmera Hasselblad nas revistas ilustradas. Duvidava quem queria, e acreditava quem tinha
30 imaginação e fé na tecnologia. Revolução Verde, Guerra Fria
e Era Atômica iam de vento em popa.
O pouso na Lua não foi só o ápice da corrida espacial.
6
Foi também o passo inicial do turbocapitalismo que dominaria
as três décadas seguintes. Capitalismo avançado, sim,
35 mas dependente, porém, de matérias-primas do século 19:
aço, carvão, óleo. Lançar-se ao espaço implicava algum
reconhecimento dos limites da Terra. Ela era azul, como já
testemunhara o astronauta pioneiro Yuri Gagarin, mas finita.
Com o império da tecnociência ascendeu também sua
40 nêmesis*, representada pelo movimento ambiental. Fixar
Marte como objetivo para dentro de 20 ou 30 anos, hoje,
parece tão louco quanto chegar à Lua em dez, como determinou John F. Kennedy. Não há um imperialista visionário
como ele à vista, e isso é bom. A ISS (Estação Espacial
45 Internacional) representa a prova viva de que certas metas
só podem ser alcançadas pela humanidade como um todo,
não por nações forjadas no tempo das caravelas, ávidas por
constituir impérios duradouros e exercer uma hegemonia
política em nível planetário.
50 Uma missão a Marte trará outros benefícios para o
imaginário terráqueo. Se Neil Armstrong e Buzz Aldrin encontraram na Lua um satélite morto, cinzento, desértico e
coberto de cicatrizes, Marte serão outros quinhentos.
Antes de mais nada, vale lembrar que é um planeta de
55 verdade, não um apêndice. Mais vermelho do que cinza. Em
vez de crateras e mais crateras, algumas paisagens familiares aos humanos: vales, ravinas, dunas, montanhas. Um
mundo morto mais recentemente, quem sabe apenas moribundo, com resquícios de água e microrganismos.
7
60 Marte é o futuro da humanidade. Ele nos fornecerá a
experiência vívida e a imagem perturbadora de um planeta
devastado, inabitável. Destino certo da Terra em vários
milhões de anos. Ou, mais provável, em poucas décadas, se
prosseguir o saque a descoberto de tanta energia fóssil pelo
65 hipercapitalismo globalizado, inflando a bolha ambiental.
Todo sucesso, portanto, à Missão Planeta Vermelho. Ela nos
trará de volta ao Azul.
*Nêmesis = vingança exigida, retaliação necessária, tributo cobrado.
(Adaptado de Marcelo Leite, Folha de S.Paulo, 26 jul. 2009.)
Marte é permanentemente encoberto por calotas polares, em ambos os polos, compostas,
em sua maior parte, de dióxido de carbono. Durante o verão norte, o dióxido de carbono
sublima completamente, deixando uma camada residual de gelo de água.
Esse processo que ocorre no verão norte para o dióxido de carbono pode ser representado
graficamente por:
8
Questão 9 (UFPE - 2010)
Considere as seguintes transformações e identifique aquelas em que ocorrem reações
químicas.
1) A luz de uma lanterna enfraquece lentamente até que finalmente se extingue.
2) O suco de laranja congelado é reconstituído adicionando-se água.
3) Uma colher de sopa de açúcar se dissolve numa xícara de café.
4) O crescimento das plantas depende da energia solar em um processo chamado
fotossíntese.
5) A água ferve acima de 100 °C no topo da Serra das Russas.
6) Gelo seco (CO2) sublimando.
Estão corretas apenas:
A) 4, 5 e 6
B) 1 e 4
C) 2 e 3
D) 1, 4 e 5
E) 2, 3 e 6
Questão 10 (Unesp - 2011)
Alquimia subterrânea transforma mina de carvão em mina de hidrogênio
Em uma área de mineração de carvão localizada no sul da Polônia, um grupo de cientistas
está usando uma mina de carvão para avaliar experimentalmente um método alternativo
para a produção de energia limpa e, assim, oferecer uma utilização para pequenos
depósitos de carvão ou minas exauridas, que são tradicionalmente deixados de lado,
representando passivos ambientais.
Na teoria e no laboratório, a injeção de oxigênio e de vapor no carvão resulta na produção
de hidrogênio. No processo, oxigênio líquido é colocado em um reservatório especial,
localizado nas galerias da mina de carvão, onde se transforma em oxigênio gasoso,
começando o processo denominado de gaseificação de carvão.
(www.inovacaotecnologica.com.br. Adaptado.)
A passagem do oxigênio líquido para oxigênio gasoso é uma transformação física
(A) exotérmica, classificada como fusão.
(B) exotérmica, classificada como ebulição.
(C) endotérmica, classificada como liquefação.
(D) endotérmica, classificada como evaporação.
(E) espontânea, classificada como sublimação.
9
10