Colégio Saint Michel
Química – Professor Rafael – 2º ano EM.
Equilíbrio Químico, Funções Orgânicas – Revisão 3º bimestre P1
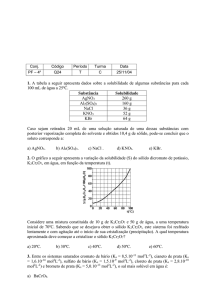
1) Dada a reação abaixo, verificou-se no equilíbrio, a
1000°C, que as concentrações em mols/L são [X2] = 0,20,
[Y2] = 0,20, [XY3] = 0,60. O valor da constante de equilíbrio
da reação química é: (valor 1,0)
6) (UFSCar-2007) Em 1912, o químico alemão Fritz Haber
desenvolveu um processo para sintetizar amônia diretamente
dos gases nitrogênio e hidrogênio. Este processo é muito
importante economicamente, porque a amônia é bastante
utilizada, por exemplo, na indústria de fertilizantes.
Considere a reação em equilíbrio químico num sistema
fechado
N2 (g) + 3 H2 (g) 2 NH3 (g)
Mantendo-se a temperatura constante, algumas modificações
podem ser realizadas nesse sistema:
I. introdução de N2 (g);
II. aumento da pressão do sistema;
III. adição de catalisador.
As modificações que irão provocar o deslocamento do
equilíbrio, favorecendo a formação de NH3, são:
a) I e II, apenas.
b) I e III, apenas.
c) III, apenas.
d) II e III, apenas.
e) I, II e III.
X2 + 3 Y2 2 XY3
2) (UNB-DF) O pentacloreto de fósforo é um reagente muito
importante em Química Orgânica. Ele é preparado em fase
gasosa através da reação:
PCl3 (g) + Cl2 (g) PCl5 (g)
Um frasco de 3,00L contém as seguintes quantidades de
equilíbrio, a 200oC: 0,120mol de PCl5; 0,600 mol de PCl3; e
0,0120 mol de Cl2. Calcule o valor da constante de
equilíbrio, em (mol/L)-1, a essa temperatura.
3) (UFRRJ) Adiciona-se uma solução de ácido cianídrico ao
hidróxido de amônio contidos num recipiente fechado. O
equilíbrio que se estabelece pode ser descrito pela equação
abaixo:
HCN + NH4OH NH4CN + H2O ΔH< O
Em relação a esse equilíbrio, para aumentar a quantidade de:
a) NH4CN pode-se adicionar H2O.
b) NH4OH pode-se diminuir a temperatura.
c) H2O pode-se adicionar NH4CN.
d) NH4CN pode-se diminuir a temperatura.
e) HCN pode-se adicionar NH4OH.
7) (UFMA) A amônia NH3(g) é uma importante matéria
prima para a obtenção de fertilizantes, corantes, explosivos,
etc. Sua obtenção é feita geralmente pelo método de HaberBosch, que envolve a seguinte reação:
N2 (g) + 3 H2 (g) 2 NH3 (g)
ΔH = - 46,2 kJmol-1
Com base nessas informações, marque a alternativa correta.
a) Ao se aumentar a pressão, o equilíbrio será deslocado no
sentido da reação inversa.
b) Ao se aumentar a concentração de amônia, o equilíbrio
será deslocado no sentido da reação direta.
c) Ao se aumentar a concentração de hidrogênio, o equilíbrio
será deslocado no sentido da reação inversa.
d) Ao se aumentar a temperatura, o equilíbrio será deslocado
no sentido da reação direta.
e) Ao se aumentar a concentração do nitrogênio, o equilíbrio
será deslocado no sentido da reação direta.
4) (UFPE) O ferro metálico pode ser extraído de seus
minérios, segundo o equilíbrio abaixo;
FeO (s) + CO (g) Fe (l) + CO2 (g) ΔH> O
O deslocamento da reação, no sentido da obtenção de ferro
metálico, pode ser feito através de:
a) aumento da quantidade de FeO.
b) aumento da pressão parcial de CO2.
c) resfriamento da mistura para solidificar o ferro líquido.
d) aumento da pressão parcial de CO.
e) agitação da mistura para liberar os gases formados.
8) (Mackenzie-SP) A concentração de íons hidrogênio num
suco de laranja que possui pH = 4,0 é: (valor 1,0)
5) (PUC-SP) Berthollet, enquanto servia à expedição de
Napoleão no Egito, observou que nas margens dos lagos
salgados havia, como resultado da evaporação da água da
solução salina, a presença de carbonato de sódio no
sedimento. Era perfeitamente conhecido o fato de que em
laboratório ocorria o processo espontâneo:
Na2CO3 + CaCl2 CaCO3 + 2 NaCl
que tendia a se completar devido à precipitação de CaCO3.
A explicação que surgiu para a ocorrência do processo
inverso foi a de que a inversão era causada:
a) pela presença de catalisadores, não conhecidos, no lago.
b) por variações na pressão barométrica nessa região.
c) pela pequena solubilidade do CaCl2 em água.
d) pelo grande excesso de NaCl no lago salgado.
e) pelas diminuições drásticas da temperatura durante a
noite.
a) 4 x 1014 mol/litro
b) 1 x 104 mol/litro
c) 1 x 10-4 mol/litro
d) 1 x 10-10 mol/litro
e) 4 x 10-10 mol/litro
1
9) (F.M. Pouso Alegre) Assinale a alternativa correta: Uma
solução de ácido acético (CH3COOH) é preparada de tal
modo que seja 0,004mol/L. O pH dessa solução aquosa,
sabendo que o ácido se encontra 25% ionizado, é:
15) (Unisa) O sal que, em solução aquosa, não produz efeito
sobre papel de tornassol é:
a) CuSO4
b) Na2CO3
c) NaCl
d) CH3COONa
e) NH4Cl
a) 1
16) (PUC-Campinas) as soluções aquosas e bem diluídas de
bicarbonato de sódio (NaHCO3) e carbonato de sódio
(Na2CO3) são respectivamente:
a) básica e ácida.
b) básica e básica.
c) ácida e básica.
d) ácida e ácida.
e) neutra e básica
b) 2
c) 3
d) 4
e) 5
10) (Mackenzie) Ao se colocar gelo seco (CO2 solidificado)
em água levemente alcalina, em presença de fenolftaleína,
verifica-se que a solução, inicialmente rósea, torna-se
incolor. Observa-se esse fato porque:
a) Ocorre o abaixamento da temperatura da água.
b) Ocorre vaporização da fenolftaleína.
c) O ácido carbônico formado é incolor.
d) o pH da solução aumenta.
e) o pH da solução diminui.
17) (UTFPR) A respeito da hidrólise salina, dizemos que ela
ocorre quando o cátion ou o ânion de um sal reage com a
água produzindo íons hidrogênio ou hidróxido, alterando,
desta forma, o pH do meio. Esta alteração de pH pode ser
observada adicionando-se um indicador adequado ao meio,
como o azul de bromotimol que apresenta coloração amarela
em meio ácido, verde em meio neutro e azul em meio
básico. Um estudante realizou um experimento para
comprovar a ocorrência da hidrólise em alguns sais e irá
preencher a tabela a seguir:
11) (Fuvest) Ao tomar dois copos de água, uma pessoa
diluiu seu suco gástrico (solução contendo ácido clorídrico),
de pH= 1, de 50ml para 500ml. Qual será o pH da solução
resultante logo após a ingestão da água?
a) 0
b) 2
c) 4
d) 6
e) 8
12) (Puccamp-SP) Uma solução aquosa tem [H+(aq)] = 1 x
10-2 molar; uma segunda solução aquosa tem [H+(aq)] = 1 x
10-5 molar. O pH da primeira solução é X, sendo mais Y do
que a segunda.
Completa-se corretamente a afirmação substituindo X e Y
por:
a)
b)
c)
d)
e)
X
10-2
2
2
12
12
Substância
(NH4)2Cl4
NaNO3
Na2S
KCN
FeCl3
Y
Ácida
Ácida
Básica
Básica
Ácida
Coloração
A sequência de cor, de cima para baixo, encontrada pelo
aluno, deverá ser:
a) azul, verde, amarelo, amarelo, azul.
b) azul, amarelo, verde, verde, azul.
c) amarelo, verde, azul, amarelo, azul.
d) verde, amarelo, azul, azul, amarelo.
e) amarelo, verde, azul, azul, amarelo.
13) (Uece 2008) O conceito de pH foi introduzido na
química pelo químico dinamarquês Soren Peter Lauritz
Sorensen, em 1909, para facilitar a caracterização da acidez
de uma substância. Assinale a alternativa que contém o pH
da solução que se obtém ao ser feita a dissolução de 5,6 g de
KOH em um litro de água. K= 39, O=16, H=1
a) 1,0
b) 3,0
c) 11,0
d) 13,0
18) Complete a tabela abaixo:
Substância
Suco de
tomate
Pasta de
dente
Lágrima
Água
sanitária
Leite de
magnésia
Cerveja
Suco
gástrico
14) (UFMA 2006) Dos sais abaixo, o único que não perturba
o equilíbrio hidrogeniônico da água
(2H2O H3O+ + OH-) é:
a) hipoclorito de sódio
b) acetato de sódio
c) cianeto de potássio
d) cloreto de amônio
e) cloreto de sódio
[H+]
pH
[OH-]
pOH
Classificação
10-3
8
10-7
12
10
10-6
10-13
19) Com base na tabela do exercício 21 responda: quantas
vezes o suco gástrico é mais ácido que a água sanitária:
2
24) Para a dissociação do trióxido de enxofre 2 SO3(g)
2 SO2(g) + O2(g) o valor de Keq é igual a 5, a uma certa
temperatura. Num recipiente de 10 L, a essa mesma
temperatura, verifica-se que estão presentes no equilíbrio 40
mols de SO2 e 50 mols de O2. Portanto, o número de mols de
SO3 não-dissociados é igual a:
a) 4
b) 5
c) 16
d) 20
e) 40
20) Calcule a constante de equilíbrio, em termos de
concentração, para a reação representada pela equação
química abaixo, sabendo que nas condições de temperatura e
pressão em que se encontra o sistema existem as seguintes
concentrações dos compostos presentes no equilíbrio: [SO 3]
= 0,2 mol/L; [O2] = 3 mol/L; [SO2] = 2 mol/L.
2 SO2 + O2 2 SO3
21) (UFPR-2009) A dureza da água é um problema que afeta
residências e indústrias por gerar acúmulo mineral nas
tubulações e dificultar a formação de espumas de sabão e
detergentes. Relacione os elementos da 1ª coluna, que
apresenta as constantes de produto de solubilidade de
carbonatos, com as afirmativas da 2ª coluna.
Kps
1. CaCO3 10–9
2. MgCO3 10–5
3. FeCO3 10–11
4. SrCO3 10–10
25) FUVEST) A altas temperaturas, N2 reage com O2
produzindo
NO,
um
poluente
atmosférico:
N2(g) + O2(g) 2NO(g)
à temperatura de 200 kelvin, a constante de equilíbrio acima
é igual a 4,0 x 10-4. Nessa temperatura, se as concentrações
de equilíbrio de N2 e O2 forem, respectivamente, 4,0 x 10 -3
e 1,0 x 10-3 mol/L, qual será a de NO?
( ) É o carbonato menos solúvel dos listados.
( ) Uma solução saturada possui concentração de 10 –5 mol.L–
1
do cátion e 10–5 mol.L–1 do ânion.
( ) Se a concentração do cátion é da ordem de 4,0 x 10 –3
mol.L-1, para ocorrer precipitação a concentração do
carbonato deve ser de pelo menos 2,5 x 10 –7 mol.L–1.
( ) Se a concentração do cátion é da ordem de 3,0 x 10 –3
mol.L-1, para ocorrer precipitação a concentração do
carbonato deve ser de pelo menos 3,4 x 10 –3 mol.L–1.
Assinale a alternativa que apresenta a numeração correta da
coluna da direita, de cima para baixo.
a) 3 – 4 – 1 – 2.
b) 3 – 2 – 1 – 4.
c) 4 – 2 – 3 – 1.
d) 3 – 1 – 4 – 2.
e) 2 – 4 – 1 – 3.
26) (UNIOESTE) O esmalte que cobre os dentes contém o
mineral hidroxiapatita, pouco solúvel em água, que se
dissolve em meio ácido em pH abaixo de 5,5, de acordo com
a reação:
Ca10(PO4)6(OH)2 (s) + 14 H+ (aq) → 10Ca2+ (aq) + 6 H2PO4(aq)+ 2 H2O (l)
O ácido lático, proveniente da degradação dos resíduos dos
alimentos por bactérias, presente na superfície dos dentes
diminui o pH para valores menores que 5.
Indique a resposta INCORRETA.
a) Uma alteração no pH no valor de uma unidade, indica
uma alteração de 10 vezes na concentração de íons H+.
b) Bochechar hidrogenocarbonato de sódio favorece o
equilíbrio no sentido da hidroxiapatita.
c) H2PO4-, que possui Ka = 6,2 x 10-8, é um ácido.
d) O pH 5,0 indica uma concentração de 1 x 10 -5 mol L-1 de
H+.
e)A concentração de H+ pode ser calculada pelo antilog do pH.
22) (UEM-PR) Considere um litro de uma solução, a 25 oC,
que contém 10-10 mol/l de Pb2+, 10-11 mol/l de Hg2+, 10-9
mol/l de Zn2+ e 10-8 mol/l de Bi3+. Quando se adiciona S2- à
solução, podem precipitar PbS (Kps a 25 o C = 10-28), HgS
(Kps a 25o C = 10-53), ZnS (Kps a 25o C = 10-21) e/ou Bi2S3
(Kps a 25o C = 10-97). De acordo com essas informações,
assinale o que for correto.
01) A concentração de S2- necessária para precipitar o
PbS(s) deve ser maior do que 10-26 mol/l.
02) Ao se adicionarem 10-14 mols de S2- o Bi2S3(s), o PbS(s) e
o HgS(s) irão precipitar-se, mas o ZnS(s) não se precipitará.
04) A expressão da constante do produto de solubilidade
para o HgS(s) é Kps = [Hg+]2[Pb2+].
08) Quando se adicionam 10-22 mols de S2-, nenhum
composto se precipitará.
16) A expressão da constante do produto de solubilidade
para o Bi2S3(s) é Kps = [Bi3+]2[S2-]3.
27) (FEPAR-PR) O composto abaixo apresenta os seguintes
grupos funcionais:
OH
H
O
O
C
C
a) álcool, aldeído, éster;
b) éter, cetona, álcool;
c) aldeído, fenol, éster;
d) aldeído, álcool, cetona.
e) éster, cetona, fenol.
23) Quantas vezes um cafezinho (pH=5) é mais ácido que a
água do mar (pH=8)?
3
O
CH3
28) (Fuvest-SP) A fórmula da vitamina K3 é dada a seguir.
Nela reconhece-se a função:
O
31) (Unitau-SP) As funções:
I. R
O
II. R
R'
CH3
R'
O
III. R
b) aldeído
e) cetona
c) éter
29) (CEFET-BA)
Funções orgânicas
C
OH
IV. R
C
O
C
R'
O
O
O
são respectivamente,
a) éter; cetona; ácido carboxílico; anidrido de ácido.
b) éter; cetona, ácido carboxílico; éster.
c) éster, cetona, ácido carboxílico; função mista cetonapoliol.
d) éster; éter; cetona – álcool; anidrido de ácido.
e) éter; éster; cetona; ácido carboxílico.
O
a) ácido
d) fenol
C
32) (UEM-PR) Dadas as seguintes fórmulas moleculares
assinale o que for correto:
Composto orgânico
OH
( )
(1) álcool
a) C3H8O
c) C2H6O
(2) ácido carboxílico
( ) CH3CHOHCH3
(3) aldeído
( ) CH3COOH
(4) fenol
( ) CH3CH2COH
Associando-se os compostos orgânicos às suas respectivas
funções, a ordem encontrada, de cima para baixo, é:
a) 4, 1, 2, 3
b) 1, 4, 2, 3
c) 4, 3, 2, 1
d) 2, 1, 3, 4
c) 1, 2, 4, 3
01) A fórmula B pode ser a propanona.
02) A função ácido carboxílico está presente, em pelo,
menos uma das fórmulas.
04) a fórmula C pode ser a etanamida.
08) a fórmula D pode ser o benzeno.
16) a função álcool não esta representada pelas fórmulas
moleculares a ou B.
32) a fórmula A pode ser o metoxi-etano.
30) (ITA-SP) Considere as seguintes substâncias:
33) (UFRJ) A cânfora, substância obtida da árvore de
mesmo nome, encontrada no Oriente e na América do sul, é
usada para fins medicinais e apresenta a seguinte fórmula
estrutural:
H3C
CH3
C
C O
H3C
C
H2C
C
CH2
CH2
H
a) Qual o grupamento funcional presente na cânfora?
b) Quantos grupos metila estão presentes na cânfora?
O
I)
H3C
CH2
C
H
O
II)
III)
H3C
CH2
C
CH3
H3C
CH2
O
CH3
O
IV)
H3C
CH2
C
O
b) C2H6O
d) C6H12
CH3
E as seguintes funções químicas:
a) ácido carboxílico
b) álcool
c) aldeído
d) cetona
e) éster
f) éter
34) (UFRGS) O composto comercialmente conhecido como
“aspirina” apresenta estrutura:
O
O C
A opção que associa corretamente as substâncias com as
funções químicas é:
CH3
COOH
Neste composto aparecem as funções:
a) Id; IIc; IIIe; IVf
b) Ic; IId; IIIe; IVa
c) Ic; IId; IIIf; IVe
d) Id; IIc; IIIf; IVe
e) Ia; IIc; IIIe; IVd
a) éster, cetona e álcool.
b) éster e álcool.
c) fenol e cetona
d) ácido carboxílico e éter
e) éster e ácido carboxílico
4
40) (FAFI-MG) O nome do composto a seguir e sua função
são, respectivamente:
grupo funcional
carbonila
radical
radical
35) (Unicamp-SP) O éster responsável pelo aroma do rum
tem a seguinte fórmula estrutural:
CH3
H
C
CH2
O
C
CH3
CH3
O
O
H3C
Escreva ás fórmulas estruturais do ácido e do álcool dos
quais o éster poderia ser formado.
) (FUVEST-SP) Pentanal, conhecido também como
valeraldeído apresenta a seguinte fórmula molecular:
a) C3H6O
d) C5H10O2
b) C4H8O
e)C5H10O
CO
CH2
C
CH3
a) benzoato de propila – éster;
b) benzopropilato de metanal – aldeído;
c) metil-propanona-fenil – cetona;
d) propil-benzil-cetona – cetona;
e) iso-propil-fenil-cetona – cetona.
c) C4H8O2
36) (UFRO) A fórmula
H3C
HC
41) (Mackenzie-SP) O nome do composto a seguir, que pode
ser usado para dar o sabor “morango” a balas e refrescos, é:
O
H3C CH2
CH2
C
O CH2
CH3
CH3
Corresponde ao composto:
a) ácido butanóico
b) butanol
c) butanal
d) butanona
e) etóxi-etano
37) (UCSal-BA) A acetona é um composto carbonílico com
3 átomos de carbono e cadeia saturada. Sua fórmula
molecular é:
a) etanoato de butila
b) butanoato de etila
c) ácido etil-n-propil-metanóico
d) propanoato de metila
e) butanoato de metila
a) C3H6O
d)C3H8O2
42) (FEI-SP) Escreva a fórmula estrutural do 2,4
pentadienal.
b) C3H7O
e) C3H8O3
c) C3H8O
38) (Makenzie-SP) O aldeído normal, de menor número de
átomos de carbono, apresenta fórmula molecular igual a:
a) C2H4O2
d) C3H8O2
b) CH2O2
e) CH2O
43) (UEMA) O nome do composto:
O
H3C CH2
CH2
C
O CH2
c) C2H6O
Que pode ser usado para dar sabor de morango a balas e
refrescos, é
39) (FEI-SP) A nomenclatura correta do composto cuja
fórmula é dada a seguir é:
CH3
H3C
CH
CH
CH2
C
CH3
a) Butanoato de metila.
b) Ácido etil-n-propil-metanóico.
c) Propanoato de metila
d) Butanoato de etila.
e) Etanoato de butila
CH3
O
CH3
44) (UNICAMP-SP) A substância 2-propanona
a) 3,4-dimetil-5-hexanona;
b) 3-metil-4-etil-2-pentanona;
c) 4,4-dimetil-2-hexanona;
d) 3-metil-2-etil-4-pentanona;
e) 3-sec-butil-2-butanona.
O
CH3
C CH3
Pode ser chamada simplesmente de propanona, já que não
existe um composto com o nome de 1-propanona. Explique
por quê.
5
45) (Puccamp-SP) Na manteiga rançosa, encontra-se a
substância
CH3 CH2 CH2 C OOH
49) (UFRN) O composto que é usado como essência de
laranja tem fórmula:
O
H3C C
O C8H17
O nome dessa substância é:
a) butanol
b) butanona
c) ácido butanóico
d) butanoato de metila
e) butanal.
O nome oficial desse composto é:
a) butanoato de metila;
b) butanoato de etila;
c) etanoato de n-octila;
d) etanoato de n-propila;
e) hexanoato de etila.
46) (FCC-BA) A formula do cloreto de vinila é H2C=CHCl
e a do ácido acético, CH3COOH. Logo, a fórmula do acetato
de vinila deve ser:
50) (UFSC) Selecione a(s) opção(ões) em que a fórmula
estrutural corresponde ao nome apresentado:
H
a) CH3 – COO – CH = CH2
b) CH3COOCH2CH3
c) CH3CO – CH3
d) CH3COCH = CH2
e) CH3COOCH3
01)
CH3
C
C
CH3
CH3
2-metil-2-buteno
47) (UTP-PR) O composto
O
CH3
CH2
C
O CH3
OH
02)
Denomina-se:
a) propanoato de metila;
b) propano di-metil;
c) propanóico di-metil;
d) metanoato de n-propil;
e) metanoato de etila.
CH3
Para-dimetil-benzeno
O
04)
CH3
48) (UNISINOS-RS) Recentemente, o Conselho Nacional
de Petróleo (CNP) autorizou a Petrobrás a aditivar a gasolina
o metil-terciobutil-éter (MTBE), tendo em vista a escassez
de álcool combustível. Qual a fórmula estrutural correta do
aditivo em questão?
H3C
O
a)
b)
CH
CH2
H3C
O
H3C
CH2
CH2
O
08)
CH2
CH3
CH2
CH2
CH3
OH
1-propanol
CH3
O
CH2
CH
CH2
16)
CH3
CH3
C
OH
Ácido metanóico
CH3
CH3
O
CH3
H3C
O
C
32)
H3C
CH2
CH3
CH2
CH2
C
CH3
H
1-butanol
CH3
e)
O
Etanoato de etila
CH3
c)
d)
C
O
CH2
CH2
CH3
CH3
64)
C
CH
CH
CH3
2,5-dimetil-2,4-hexadieno
6
C
CH3
CH3