Química Solucionada
9.9999.0111 / 9.8750.0050 / 9.9400. / 9.8126.0630
Título: Revisando (química elementar)
Data:
/
/ 2016
QS.1
EXERCÍCIOS DE REVISÃO
TEXTO PARA A PRÓXIMA QUESTÃO:
O ferro raramente é encontrado livre na crosta terrestre
e sim associado a outros elementos químicos constituindo um
minério.
Para extrair o ferro de seu minério é usado um
equipamento chamado alto-forno, no qual são introduzidos a
hematita (um tipo de minério de ferro), o coque (constituído
principalmente por carbono) e ar quente, que é injetado por
aberturas existentes na base do alto-forno.
A queima do coque libera energia térmica elevando a
temperatura até cerca de 1 500ºC e produz monóxido de
carbono, que irá interagir com o minério para formar o ferro-gusa.
O ferro-gusa é empregado na produção de aço, que é
um material essencial aos vergalhões utilizados na construção
civil.
No alto-forno também é introduzido calcário cuja função
é extrair as impurezas do minério de ferro, principalmente a
areia, formando um material chamado escória, o qual é usado na
produção de cimento e de tijolos especiais e na pavimentação de
rodovias.
1. (G1 - cps) Pela leitura do texto, conclui-se que na produção
do ferro-gusa,
a) o coque, além de ser matéria-prima, é o combustível utilizado
no alto-forno.
b) a maior quantidade do ferro encontrado na natureza está sob
a forma metálica, isto é, puro.
c) a escória é o resíduo formado no alto-forno e não apresenta
nenhum interesse comercial.
d) a hematita, o monóxido de carbono e a escória são as
matérias-primas introduzidas no alto-forno.
e) para aquecer o alto-forno é consumida grande quantidade de
energia elétrica, tornando o processo caro.
2. (G1 - cftsc) Um fenômeno químico é caracterizado pela
formação de novas substâncias; enquanto num fenômeno físico
as substâncias são “preservadas”, ou seja, não há formação de
novas substâncias. Assinale a alternativa que indica um
fenômeno físico.
a) Processo de produção da energia necessária para que o atleta
praticante de MMA (Mixed Martial Arts) Antônio Rodrigo
“Minotauro” Nogueira execute um golpe chamado “triângulo
de mão”.
b) Produção de papel a partir da celulose.
c) Liberação de gases, quando um comprimido efervescente de
vitamina C é colocado em água.
d) Oxidação de uma placa de vídeo do Playstation 3®.
e) Separação do lixo doméstico para coleta seletiva.
3. (G1 - cps) Considere o que se observa quando um
comprimido antiácido efervescente é acrescentado à água, ou
seja, a rápida produção de gás. Essa observação leva a concluir
o seguinte:
a) evaporando-se a solução aquosa obtida após a liberação de
gás, obtém-se o comprimido.
b) a mistura “comprimido efervescente e água” resultou em
transformação química.
c) o comprimido efervescente decompõe a água em seus dois
gases constituintes, H2 e O2.
d) o gás produzido é tóxico e a solução resultante não deve ser
ingerida se apresentar bolhas.
e) o comprimido fez com que houvesse liberação dos gases, que
estavam dissolvidos na água.
4. (G1 - cps) Da água do mar se obtém o sal de cozinha. Para
isso, é utilizado um processo de separação de misturas
conhecido como _________, que envolve a mudança de estado
físico da água denominado _________.
www.quimicasolucionada.com.br
As lacunas desse texto são corretamente preenchidas,
respectivamente, com
a) solidificação e ebulição.
b) solidificação e vaporização.
c) fusão fracionada e ebulição.
d) cristalização fracionada e vaporização.
e) cristalização fracionada e destilação fracionada.
5. (G1 - cps) As cores com as quais se compõem os magníficos
vitrais que ornamentam, por exemplo, catedrais famosas, podem
ser obtidas a partir de misturas de pigmentos, durante o processo
de fabricação dos vidros. Alguns exemplos são encontrados no
quadro a seguir:
Fórmula Química dos Pigmentos
Cor
MnO2
lilás
Co2O3
azul
Cr2O3
verde
As fórmulas apresentadas no quadro referem-se a
a) misturas homogêneas sólidas.
b) misturas heterogêneas líquidas.
c) misturas homogêneas líquidas.
d) substâncias compostas.
e) substâncias simples.
TEXTO PARA A PRÓXIMA QUESTÃO:
Redação do Site Inovação Tecnológica - 18/02/2010
Fontes de energia do futuro
Células a combustível alimentadas por hidrogênio e por energia
solar são as duas maiores esperanças para as fontes de energia
do futuro, por serem mais amigáveis ambientalmente e,
sobretudo, sustentáveis. A combinação das duas, então, é
considerada como particularmente limpa: produzir hidrogênio
para alimentar as células a combustível, quebrando moléculas de
água com a luz solar, seria de fato o melhor dos mundos. Esta é
a chamada fotossíntese artificial, que vem sendo alvo de
pesquisas de vários grupos de cientistas, ao redor do mundo.
Eletrodo fotocatalítico
Uma equipe liderada por Thomas Nann e Christopher Pickett, da
Universidade de East Anglia, no Reino Unido, criou um
fotoeletrodo eficiente, robusto, que pode ser fabricado com
materiais comuns e de baixo custo. O novo sistema consiste de
um eletrodo de ouro que é recoberto com camadas formadas por
nanopartículas de fosfeto de índio (InP). A esse eletrodo, os
pesquisadores adicionaram um composto de ferro-enxofre [Fe2S2
(CO)6] sobre as camadas. Quando submerso em água e
iluminado com a luz do Sol, sob uma corrente elétrica
relativamente fraca, este sistema fotoeletrocatalítico produz
hidrogênio com uma eficiência de 60%.
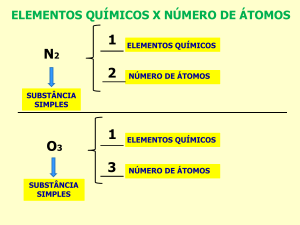
6. (Fatec) Considerando as substâncias químicas empregadas
na construção do eletrodo fotocatalítico, o qual permite a
realização da fotossíntese artificial, pode-se notar que há uma
substância simples, formada por átomos de um único elemento
químico, e substâncias compostas, formadas por átomos de mais
de um elemento químico.
A única substância simples empregada nesse eletrodo é
a) InP
b) H2O
c) Au
d) O2
e) Fe2S2 (CO)6
TEXTO PARA A PRÓXIMA QUESTÃO:
Suor não é sinônimo de queima de gordura... Para
muitas pessoas, correr debaixo do sol do meio-dia ou usar muita
[email protected] 1
Química Solucionada
roupa enquanto se pratica esporte é sinônimo de
emagrecimento, uma vez que acreditam que quanto mais
transpirarem, maior será a queima de gordura.
Acontece que suar não emagrece. Perdem-se apenas
água e sais minerais. Depois de uma sauna, por exemplo, a
pessoa normalmente vai perceber uma redução em seu peso
corporal, mas assim que ingerir o primeiro copo d’água, o líquido
perdido vai sendo reposto e o peso acaba voltando ao normal.
O organismo transpira para manter estável a
temperatura interna do corpo, transferindo o calor de dentro para
fora e, assim, mantendo a temperatura interna do organismo
entre 36 e 36,5ºC.
Se você deseja “queimar” aquelas incômodas
gordurinhas, já que com a transpiração não se perde peso, o
ideal é queimá-las de uma maneira gradativa e saudável. Cerca
de 30 minutos de atividade física moderada (caminhar, correr ou
andar de bicicleta), três vezes por semana, são ideais para isso.
Com esse ritmo de perda de calorias, você queimará um
quilograma de gordura por mês.
9.9999.0111 / 9.8750.0050 / 9.9400. / 9.8126.0630
9. (Ufg) Considere a descrição da seguinte técnica: O minério
pulverizado é recoberto com óleo, água e detergente; nessa
mistura, é borbulhado ar. Essa descrição refere-se a um método
de separação de misturas muito utilizado em indústrias
metalúrgicas. Qual é essa técnica?
a) Decantação
b) Flotação
c) Cristalização
d) Destilação
e) Sublimação
10. (G1 - cftmg) O derramamento de petróleo no Golfo do
México, após a explosão da plataforma Deepwater Horizon,
trouxe uma consequência, dentre outras, a mistura de
componentes oleosos na água do mar. Um método utilizado para
separar o óleo dessa água é a
a) filtração.
b) levigação.
c) sublimação.
d) decantação.
7. (G1 - cps)
Sobre a transpiração e as substâncias que compõem o suor, é
válido afirmar que
a) a água e os sais minerais, no suor, formam uma mistura
heterogênea.
b) a água sofre vaporização absorvendo calor do corpo, durante
a transpiração.
c) o sal cloreto de sódio é obtido nas salinas unicamente por
processo químico.
d) a água e o sal cloreto de sódio são formados pelo mesmo
número de átomos.
e) a substância água é formada por duas moléculas de
hidrogênio ligadas a uma molécula de
oxigênio.
8. (Ufu) Sobre os procedimentos químicos da destilação de uma
solução aquosa de sal de cozinha e suas aplicações, assinale a
alternativa correta.
a) O sal de cozinha entra em ebulição ao mesmo tempo da água
e é colhido no erlenmeyer.
b) O condensador possui a função de diminuir a temperatura dos
vapores produzidos pelo aquecimento e, assim, liquefazer a
água.
c) A temperatura de ebulição do sal de cozinha é menor que a
temperatura de ebulição da água.
d) A eficiência do método de destilação é pequena para separar
o sal da água.
www.quimicasolucionada.com.br
11. (Enem) Ainda hoje, é muito comum as pessoas utilizarem
vasilhames de barro (moringas ou potes de cerâmica não
esmaltada) para conservar água a uma temperatura menor do
que a do ambiente. Isso ocorre porque:
a) o barro isola a água do ambiente, mantendo-a sempre a uma
temperatura menor que a dele, como se fosse isopor.
b) o barro tem poder de "gelar" a água pela sua composição
química. Na reação, a água perde calor.
c) o barro é poroso, permitindo que a água passe através dele.
Parte dessa água evapora, tomando calor da moringa e do
restante da água, que são assim resfriadas.
d) o barro é poroso, permitindo que a água se deposite na parte
de fora da moringa. A água de fora sempre está a uma
temperatura maior que a de dentro.
e) a moringa é uma espécie de geladeira natural, liberando
substâncias higroscópicas que diminuem naturalmente a
temperatura da água.
12. (Enem) Quando definem moléculas, os livros geralmente
apresentam conceitos como: "a menor parte da substância capaz
de guardar suas propriedades". A partir de definições desse tipo,
a ideia transmitida ao estudante é a de que o constituinte isolado
(moléculas) contém os atributos do todo.
É como dizer que uma molécula de água possui densidade,
pressão de vapor, tensão superficial, ponto de fusão, ponto de
ebulição, etc. Tais propriedades pertencem ao conjunto, isto é,
manifestam-se nas relações que as moléculas mantêm entre si.
O texto evidencia a chamada visão substancialista que ainda se
encontra presente no ensino da Química. A seguir estão
relacionadas algumas afirmativas pertinentes ao assunto.
I. O ouro é dourado, pois seus átomos são dourados.
II. Uma substância "macia" não pode ser feita de moléculas
"rígidas".
III. Uma substância pura possui pontos de ebulição e fusão
constantes, em virtude das interações entre suas moléculas.
IV. A expansão dos objetos com a temperatura ocorre porque os
átomos se expandem.
Dessas afirmativas, estão apoiadas na visão substancialista
criticada pelo autor apenas
a) I e II.
b) III e IV.
c) I, II e III.
d) I, II e IV.
e) II, III e IV.
TEXTO PARA A PRÓXIMA QUESTÃO:
Produtos de limpeza, indevidamente guardados ou manipulados,
estão entre as principais causas de acidentes domésticos. Leia o
relato de uma pessoa que perdeu o olfato por ter misturado água
sanitária, amoníaco e sabão em pó para limpar um banheiro:
A MISTURA FERVEU E COMEÇOU A SAIR UMA FUMAÇA
ASFIXIANTE. Não conseguia respirar e meus olhos, nariz e
garganta começaram a arder de maneira insuportável. Saí
correndo à procura de uma janela aberta para poder voltar a
[email protected] 2
Química Solucionada
respirar.
13. (Enem) Entre os procedimentos recomendados para reduzir
acidentes com produtos de limpeza, aquele que deixou de ser
cumprido, na situação discutida no texto, foi:
a) Não armazene produtos em embalagens de natureza e
finalidade diferentes das originais.
b) Leia atentamente os rótulos e evite fazer misturas cujos
resultados sejam desconhecidos.
c) Não armazene produtos de limpeza e substâncias químicas
em locais próximos a alimentos.
d) Verifique, nos rótulos das embalagens originais, todas as
instruções para os primeiros socorros.
e) Mantenha os produtos de limpeza em locais absolutamente
seguros, fora do alcance de crianças.
14. (Fatec) Considere as seguintes propriedades dos metais
estanho e chumbo:
Metal
Temperatura de fusão (ºc)
Densidade (g/cm3)
estanho
232
7,3
chumbo
327
11,4
Certa liga de solda utilizada na fixação de componentes em
circuitos eletrônicos contém 63% de estanho e 37% de chumbo
(porcentagens em massa). Com base nessas informações,
afirma-se que tal liga
I. apresenta maior temperatura de fusão do que o estanho puro;
II. apresenta densidade igual a 9,4 g/cm3;
III. é boa condutora de corrente elétrica.
É correto o que se afirma somente em
a) I.
b) II.
c) III.
d) I e III.
e) II e III.
15. (Enem cancelado) O controle de qualidade é uma exigência
da sociedade moderna na qual os bens de consumo são
produzidos em escala industrial. Nesse controle de qualidade são
determinados parâmetros que permitem checar a qualidade de
cada produto. O álcool combustível é um produto de amplo
consumo muito adulterado, pois recebe adição de outros
materiais para aumentar a margem de lucro de quem o
comercializa. De acordo com a Agência Nacional de Petróleo
(ANP), o álcool combustível deve ter densidade entre 0,805
g/cm3 e 0,811 g/gm3.
Em algumas bombas de combustível a densidade do álcool pode
ser verificada por meio de um densímetro similar ao desenhado
abaixo, que consiste em duas bolas com valores de densidade
diferentes e verifica quando o álcool está fora da faixa permitida.
Na imagem, são apresentadas situações distintas para três
amostras de álcool combustível.
A respeito das amostras ou do densímetro, pode-se afirmar que
a) A densidade da bola escura deve ser igual a 0,811 g/cm3.
b) a amostra 1 possui densidade menor do que a permitida.
c) a bola clara tem densidade igual à densidade da bola escura.
d) a amostra que está dentro do padrão estabelecido é a de
número 2.
e) o sistema poderia ser feito com uma única bola de densidade
entre 0,805 g/cm3 e 0,811 g/cm3.
16. (Unesp)
Os hidrocarbonetos aromáticos simples são
provenientes de duas fontes principais: carvão e petróleo. A
decomposição do carvão por aquecimento na ausência de ar
conduz à formação de compostos voláteis (gases), um líquido
viscoso (alcatrão da hulha) e um resíduo sólido (coque). A partir
da destilação fracionada do alcatrão da hulha obtêm-se diversas
www.quimicasolucionada.com.br
9.9999.0111 / 9.8750.0050 / 9.9400. / 9.8126.0630
substâncias aromáticas, dentre essas, benzeno, tolueno, p-xileno
e o bifenilo.
Temperatura de
Temperatura de
Substância
fusão (°C)
ebulição (°C)
benzeno
5,5
80
tolueno
-95
111
p-xileno
13
138
bifenilo
70
255
Baseando-se nas propriedades físicas apresentadas na tabela à
pressão de 1 atm, assinale a alternativa correta, considerando
que todos os processos citados ocorram nesta pressão.
a) O bifenilo é um líquido a 25 °C.
b) Durante a destilação fracionada do alcatrão da hulha, o
composto obtido primeiro é o benzeno, e a seguir vem o
tolueno.
c) Durante a destilação fracionada do alcatrão da hulha, o
composto obtido primeiro é o tolueno, e a seguir vem o
benzeno.
d) O p-xileno é gasoso a 100 °C.
e) O bifenilo sublima-se acima de 255 °C.
TEXTO PARA A PRÓXIMA QUESTÃO:
A estrutura tridimensional de uma proteína determina sua função
biológica. Como exemplo, pode-se citar a queratina, a proteína
que constitui os cabelos, rica em cisteína e estabilizada por
numerosas ligações dissulfeto (S – S).
17. (Ufg) Os processos de alisamento e enrolamento artificiais
dos cabelos utilizam substâncias químicas redutoras e altas
temperaturas para o rompimento das ligações dissulfeto.
O rearranjo dessas ligações na -hélice da queratina do cabelo
remove, ou introduz, tensões na fibra, surgindo assim o efeito
estético do cabelo liso ou crespo. A propriedade física que as
ligações dissulfeto conferem à queratina do cabelo é
a) refletividade.
b) densidade.
c) condutividade térmica.
d) resistência mecânica.
e) volume.
18. (Uff) Um Universo em expansão, como o nosso, é um
Universo com uma história. E o que aprendemos ao estudar essa
história é que, à medida que o Universo se expande, a matéria
se resfria. Esse resfriamento gradual permitiu que partículas,
inicialmente livres, eventualmente formassem estruturas cada
vez mais complexas: núcleos atômicos, átomos de hidrogênio e
hélio, estrelas e planetas. Mas para que a vida seja possível,
hidrogênio e hélio não bastam. Faltam os outros elementos:
Carbono, Oxigênio, Ferro, Ouro... Eles são formados durante os
momentos finais da vida de estrelas, em eventos conhecidos
como explosões de supernova.
Em relação aos elementos H, C, O e He e seus compostos,
pode-se afirmar que são utilizados, respectivamente, em:
a) confecção de diamantes; eletrodos; ozonização; filtros para
água e ar.
b) produção de diamantes; solda oxi-acetilênica; produção de
margarina; filtros para água e ar.
c) produção de margarina; filtros para água e ar; balões
meteorológicos; ozonização.
d) combustível de foguete; eletrodos; ozonização de água;
balões meteorológicos.
e) combustível de foguete; ozonização de água; produção de
margarina; balões meteorológicos.
19. (Ufrgs) Fabricantes de pigmentos para tatuagens deverão
brevemente obter registro de seus produtos junto aos órgãos
oficiais. A preocupação com as normas para essas tintas decorre
do fato de muitos pigmentos apresentarem derivados de metais
pesados, o que pode provocar efeitos adversos à saúde.
Atualmente, pode ser encontrado HgS no pigmento vermelho,
PbCrO4 no amarelo e Cr2O3 no verde.
Assinale a propriedade compartilhada pelos metais Hg
(mercúrio), Pb (chumbo) e Cr (cromo).
a) Apresentam altos valores de potenciais de ionização.
b) Têm seus elétrons distribuídos em um mesmo número de
camadas eletrônicas.
[email protected] 3
Química Solucionada
c) Reagem vigorosamente com a água, formando óxidos.
d) Apresentam elevados valores de eletronegatividade.
9.9999.0111 / 9.8750.0050 / 9.9400. / 9.8126.0630
e) Podem apresentar mais de um estado de oxidação.
20. (Enem 2ª aplicação) O Brasil é um dos países que obtêm melhores resultados na reciclagem de latinhas de alumínio. O esquema
a seguir representa as várias etapas desse processo:
A temperatura do forno em que o alumínio é fundido é útil também porque
a) sublima outros metais presentes na lata.
b) evapora substâncias radioativas remanescentes.
c) impede que o alumínio seja eliminado em altas temperaturas.
d) desmagnetiza as latas que passaram pelo processo de triagem.
e) queima os resíduos de tinta e outras substâncias presentes na lata.
Gabarito:
Resposta da questão 1:
[A]
O carvão coque, além de ser matéria-prima, é o combustível utilizado
no alto-forno.
Resposta da questão 2:
[E]
A separação do lixo doméstico para coleta seletiva é um processo
físico, pois não ocorre rearranjo atômico no mesmo.
Resposta da questão 3:
[B]
Observamos que a mistura “comprimido efervescente e água”
resultou em transformação química, ou seja, formação de gás
carbônica.
Resposta da questão 4:
[D]
Da água do mar se obtém o sal de cozinha. Para isso, é utilizado um
processo de separação de misturas conhecido como cristalização
fracionada, que envolve a mudança de estado físico da água
denominado evaporação (vaporização).
Resposta da questão 5:
[D]
As fórmulas apresentadas no quadro referem-se a substâncias
compostas (formadas por mais de um elemento químico).
Resposta da questão 6:
[C]
O novo sistema consiste de um eletrodo de ouro (substância simples)
que é recoberto com camadas formadas por nanopartículas de
fosfeto de índio (InP - substância composta).
Resposta da questão 7:
[B]
Análise das afirmativas:
a) Afirmativa incorreta. A água e os sais minerais, no suor, formam
uma mistura homogênea.
www.quimicasolucionada.com.br
b) Afirmativa correta. A água sofre vaporização absorvendo calor do
corpo, durante a transpiração mudando do estado líquido para o
gasoso.
c) Afirmativa incorreta. O sal cloreto de sódio é obtido nas salinas por
processo físico (evaporação).
d) Afirmativa incorreta. A água (moléculas com 3 átomos cada) e o
sal cloreto de sódio (2 elementos; atomicidade indefinida) não são
formados pelo mesmo número de átomos.
e) Afirmativa incorreta. A substância água é formada por moléculas
que apresentam dois átomos de hidrogênio ligados a um de oxigênio.
Resposta da questão 8:
[B]
Alternativa [A] está incorreta, pois o sal de cozinha entra em ebulição
em temperaturas muito mais altas que a água e, na destilação, ele
permanece no balão. A água é recolhida no erlenmeyer.
Alternativa [B] está correta. No sistema de destilação, a água do
balão que evapora, em contato com as paredes mais frias do
condensador, condensa e escorre até ser recolhida no erlenmeyer.
Alternativa [C] está incorreta. A temperatura de ebulição do sal de
cozinha é muito maior que a temperatura de ebulição da água e é
esta diferença que permite que os dois sejam separados por
destilação.
Alternativa [D] está incorreta, pois a diferença nas temperaturas de
ebulição da água e do sal faz com que a destilação seja um método
eficiente para separá-los.
Resposta da questão 9:
[B]
A flotação utiliza a diferença de densidade na separação sólidolíquido. No caso do exercício, as partículas foram recobertas com
óleo, que é imiscível com a água e então borbulha-se ar para que o
minério pulverizado se liguem as bolhas de ar e se separem do
líquido, e então se acumule na superfície.
Resposta da questão 10:
[D]
Na decantação o óleo se separa da água devido à diferença de
polarização (óleo = apolar, água = polar) e de densidade.
Resposta da questão 11:
[C]
[email protected] 4
Química Solucionada
9.9999.0111 / 9.8750.0050 / 9.9400. / 9.8126.0630
O barro é poroso, permitindo que a água passe através dele. Parte
dessa água evapora ( H2O( ) calor H2O(v) ), absorvendo
calor da moringa e do restante da água, que são assim resfriadas.
Resposta da questão 12:
[D]
Análise das afirmativas:
I. Apoiada na visão substancialista: o ouro é dourado, pois seus
átomos são dourados (a ideia transmitida ao estudante é a de que
o constituinte isolado (átomo de ouro) contém os atributos do
todo).
II. Apoiada na visão substancialista: uma substância "macia" não
pode ser feita de moléculas "rígidas" (a ideia transmitida ao
estudante é a de que o constituinte isolado (molécula) contém os
atributos do todo).
III. Não apoiada na visão substancialista: uma substância pura possui
pontos de ebulição e fusão constantes, em virtude das interações
existentes entre suas moléculas (forças intermoleculares).
IV. Apoiada na visão substancialista: a expansão dos objetos com a
temperatura ocorre porque os átomos se expandem (a ideia
transmitida ao estudante é a de que o constituinte isolado (átomos)
contém os atributos do todo, se expandem individualmente, o que
não é verdade).
Resposta da questão 13:
[B]
Devemos evitar misturas de componentes desconhecidos que podem
reagir produzindo substâncias tóxicas.
Resposta da questão 14:
[C]
Gabarito Oficial: [D]
Gabarito SuperPro®: [C]
O Gabarito oficial da FATEC para esta questão é a alternativa [D],
pois na resolução levou-se em consideração a não existência da
mistura eutética, ou seja, a temperatura de fusão da mistura deveria
estar entre as temperaturas de fusão dos dois metais constituintes da
liga (232C TF 327C).
Porém, na composição aproximada de 63% de estanho e 37% de
chumbo, a liga se comporta como uma substância pura, com uma
temperatura de fusão de 183C, ou seja, trata-se de uma mistura
eutética.
A partir dos dados da tabela, vem:
Densidade
Temperatura de
Metal
3
fusão (C)
(g/cm )
estanho
chumbo
232
327
7,3
11,4
63 % de es tanho 63 g
Para 100 g de mistura
37 % de chumbo 37 g
m
des tanho
V
63
7,3
Ves tanho
dliga
m
Ves tano Vchumbo
Ves tano Vchumbo 8,63 3,25 11,88 cm3
100
dliga
8,42 g / cm3
11,88
8,42 g / cm3 9,4 g / cm3
Ligas metálicas são excelentes condutoras de corrente elétrica
devido à ligação metálica.
Conclusão: é correto o que se afirma somente em [I] e [III].
Fonte: Solda estanho - chumbo, aplicações na eletrônica de E. A. C.
Aranha Neto, UFPR.
Resposta da questão 15:
[D]
De acordo com a Agência Nacional de Petróleo (ANP), o álcool
combustível deve ter densidade entre 0,805 g/cm 3 e 0,811 g/gm3.
Duas bolas com valores de densidade diferentes devem ficar
afastadas no teste, ou seja, as densidades relativas serão diferentes.
Resposta da questão 16:
[B]
Análise das alternativas:
[A] Incorreta. A 25°C o bifenilo é sólido, pois sua temperatura de
fusão é de 70°C.
[B] Correta. O benzeno é obtido primeiro, pois sua temperatura de
ebulição (80°C) é menor do que a do tolueno (111°C).
[C] Incorreta. O benzeno é obtido primeiro, pois sua temperatura de
ebulição (80°C) é menor do que a do tolueno (111°C).
[D] Incorreta. O p-xileno é líquido a 100°C, pois ele funde a 13°C e
entra em ebulição a 138°C.
[E] Incorreta. O bifenilo estará no estado gasoso acima de 255°C.
Resposta da questão 17:
[D]
A propriedade física que as ligações dissulfeto conferem à queratina
do cabelo é a resistência mecânica.
Resposta da questão 18:
[D]
Os elementos H, C, O e He e seus compostos são utilizados em:
combustível de foguete; eletrodos; ozonização de água; balões
meteorológicos.
Resposta da questão 19:
[E]
A propriedade compartilhada pelos metais Hg (mercúrio), Pb
(chumbo) e Cr (cromo) é que podem apresentar mais de um estado
de oxidação: Hg2+, [Hg2]2+; Pb2+, Pb4+; Cr2+, Cr3+.
Resposta da questão 20:
[E]
A temperatura do forno em que o alumínio é fundido é útil também
porque queima os resíduos de tinta e outras substâncias presentes
na lata, pois as tintas e outros produtos químicos são eliminados
durante a fusão a 400 oC – 700 oC.
Ves tanho 8,63 cm3
m
V
37
dchumbo
11,4
Vchumbo
Vchumbo 3,25 cm3
Cálculo da densidade da liga a partir dos volumes e da massa total:
www.quimicasolucionada.com.br
[email protected] 5