LISTA DE EXERCÍCIOS – 2ª SÉRIE DO EM
PROFESSOR NETO
Questão 01)
O homem utiliza o fogo para moldar os mais
diversos utensílios. Por exemplo, um forno é
essencial para o trabalho do ferreiro na confecção
de ferraduras. Para isso, o ferro é aquecido até
que se torne moldável.
Considerando que a massa de ferro empregada
na confecção de uma ferradura é de 0,5 kg, que a
temperatura em que o ferro se torna moldável é
de 520 ºC e que o calor específico do ferro vale
0,1 cal/g ºC, assinale a alternativa que fornece a
quantidade de calor, em calorias, a ser cedida a
essa massa de ferro para que possa ser
trabalhada pelo ferreiro.
Dado: temperatura inicial da ferradura: 20 ºC.
a)
b)
c)
d)
e)
25
250
2500
25000
250000
Questão 02)
Certo estudante, em um laboratório de Física, na
Inglaterra, realizou uma experiência que envolvia
trocas de calor. Durante uma parte do trabalho,
teve de aquecer um corpo de massa 1,00 kg,
constituído de uma liga de alumínio, cujo calor
específico é c = 0,215 cal/(g.ºC). A temperatura
do corpo variou de 212 ºF até 392 ºF.
Considerando que 1 caloria = 4,2 J, a energia
térmica
recebida
por
esse
corpo
foi
aproximadamente
a)
b)
c)
d)
e)
160 kJ
90 kJ
40 kJ
16 kJ
9 kJ
Questão 03)
A existência da água em seus três estados
físicos, sólido, líquido e gasoso, torna nosso
Planeta um local peculiar em relação aos outros
Planetas do Sistema Solar. Sem tal peculiaridade,
a vida em nosso Planeta seria possivelmente
inviável. Portanto, conhecer as propriedades
físicas da água ajuda a melhor utilizá-la e assim
contribuir para a preservação do Planeta.
Na superfície da Terra, em altitudes próximas ao
nível do mar, os estados físicos da água estão
diretamente relacionados à sua temperatura
conforme mostrado no Gráfico ao lado. Esse
Gráfico representa o comportamento de uma
massa de 1,0 g de gelo a uma temperatura inicial
de – 50ºC, colocada em um calorímetro que,
ligado a um computador, permite determinar a
temperatura da água em função da quantidade de
calor que lhe é cedida.
Observando-se o Gráfico, pode-se concluir que a
quantidade de calor necessária para liquefazer a
massa de 1,0g de água e elevar sua temperatura
de 0ºC até 100ºC é, respectivamente,
a)
b)
c)
d)
105 cal e 80 cal.
105 cal e 100 cal.
80 cal e 105 cal.
100 cal e 105 cal.
Questão 04)
Uma das medidas adotadas para resfriar o reator
superaquecido da usina nuclear de Fukushima foi
usar um canhão d'água. Ao evaporar 1,0 tonelada
de água, inicialmente a 10 ºC, a energia térmica,
em joules, retirada das paredes do reator, foi de:
Dados:
Calor latente da água: 80 cal/g
Calor específico da água: 1,0 cal/gºC
1 cal 4,0 J
a)
b)
c)
d)
e)
5
3,6x10
5
1,7x10
5
6,8x10
8
3,6x10
8
6,8x10
Questão 05)
Em uma experiência no laboratório de Física,
observa-se que um bloco metálico de 0,15 kg de
massa, ao receber 1530 cal, varia sua
temperatura de 68ºF para 122ºF. O calor
específico da substância que constitui esse corpo
é
a)
b)
c)
0,19 cal/(g.ºC)
0,23 cal/(g.ºC)
0,29 cal/(g.ºC)
d)
e)
0,34 cal/(g.ºC)
0,47 cal/(g.ºC)
Questão 06)
O gráfico mostra a temperatura de 20 gramas de
o
um líquido, inicialmente a 0 C, em função da
quantidade de calor absorvida.
a)
b)
c)
d)
e)
1,00 cal/g °C
0,75 cal/g °C
1,25 cal/g °C
1,50 cal/g °C
3,75 cal /g °C
Sabendo-se que o calor específico do líquido é
0,6
cal
o
, é correto afirmar que o calor latente de
g. C
vaporização para esse líquido, em cal/g, é igual a
a)
b)
c)
d)
e)
100
200
300
400
500
Questão 07)
Uma bolsa térmica com 500 g de água à
temperatura inicial de 60 ºC é empregada para
tratamento da dor nas costas de um paciente.
Transcorrido um certo tempo desde o início do
tratamento, a temperatura da água contida na
bolsa é de 40 ºC. Considerando que o calor
específico da água é 1 cal/(g·ºC), e supondo que
60% do calor cedido pela água foi absorvido pelo
corpo do paciente, a quantidade de calorias
recebidas pelo paciente no tratamento foi igual a
a)
b)
c)
d)
e)
2 000.
4 000.
6 000.
8 000.
10 000.
Questão 08)
Ao colocar sobre a placa que atinge maiores
temperaturas um corpo sólido de 75g, foi
detectada uma variação de temperatura em
função do tempo conforme se ilustra no gráfico
abaixo. Considerando que a placa libera energia
a uma potência constante de 150 cal/min, é
correto afirmar que o corpo sólido tem calor
específico de:
Questão 09)
A tabela abaixo mostra apenas alguns valores,
omitindo outros, para três grandezas associadas a
cinco diferentes objetos sólidos:
–
–
–
massa;
calor específico;
energia recebida ao sofrer um aumento de
temperatura de 10 ºC.
objetos m(g) c(cal g 1 º C 1
I
II
Q(cal)
0,3
300
0,2
400
III
150
IV
150
0,4
450
V
100
0,5
A alternativa que indica, respectivamente, o objeto
de maior massa, o de maior calor específico e o
que recebeu maior quantidade de calor é:
a)
b)
c)
d)
I, III e IV
I, II e IV
II, IV e V
II, V e IV
Questão 10)
Em um dia ensolarado, uma criança brinca com
uma lupa de diâmetro de 10 cm e resolve derreter
uma pequena pedra de gelo de massa 1g,
focalizando a luz solar. Considere que a pedra de
gelo está inicialmente a uma temperatura de -14
ºC, que o valor da irradiação solar incidente é de
2
420 W/m e que o gelo absorve 80% dessa
energia.
Dados:
1 cal 4,2 J
Calor latente de fusão do gelo: 80 cal/g
Calor específico do gelo: 0,50 cal/g ºC
3
para que toda a energia fornecida seja absorvida
pelo gelo apenas para fundi-lo é:
Considerando os dados apresentados, calcule:
a)
b)
a quantidade de energia em calorias para
derreter completamente a pedra de gelo;
o tempo, em segundos, que a criança irá
esperar até a pedra de gelo derreter-se
completamente,
sendo,
nesse
caso,
desprezado o calor do meio ambiente.
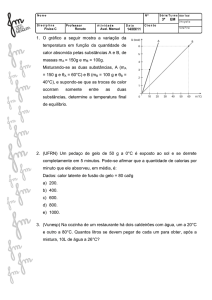
Questão 11)
Um estudante, no laboratório de Física de sua
escola, forneceu calor a um corpo de massa 50 g,
utilizando uma fonte térmica de potência
constante. Com as medidas obtidas, construiu o
gráfico ao lado, que representa a quantidade de
calor Q recebida pelo corpo em função de sua
temperatura t. Analisando o gráfico, pode-se
afirmar que o calor específico, no estado sólido e
o calor latente de vaporização da substância que
constitui o corpo, valem, respectivamente,
a)
b)
c)
d)
e)
5,0 min
3,0 min
1,5 min
8,0 min
10 min
Questão 14)
Energia térmica, obtida a partir da conversão de
energia solar, pode ser armazenada em grandes
recipientes isolados, contendo sais fundidos em
altas temperaturas. Para isso, pode-se utilizar o
sal nitrato de sódio (NaNO3), aumentando sua
temperatura de 300 ºC para 550 ºC, fazendo-se
assim uma reserva para períodos sem insolação.
Essa energia armazenada poderá ser recuperada,
com a temperatura do sal retornando a 300 ºC.
Para armazenar a mesma quantidade de energia
que seria obtida com a queima de 1 L de gasolina,
necessita-se de uma massa de NaNO3 igual a
Podercaloríficoda gasolina 3,6 107 J/L
Calor específico do NaNO3 1,2 103 J/kg º C
a)
b)
c)
d)
e)
a)
b)
c)
d)
e)
0,6 cal/(g.ºC) e 12 cal/g
0,4 cal/(g.ºC) e 12 cal/g
0,4 cal/(g.ºC) e 6 cal/g
0,3 cal/(g.ºC) e 12 cal/g
0,3 cal/(g.ºC) e 6 cal/g
Questão 12)
Considerando que os calores específico e latente
de vaporização da água são respectivamente c =
4190 J/kg.K e L = 2256 kJ/kg, a energia mínima
necessária para vaporizar 0,5 kg de água que se
encontra a 30ºC, em kJ, e aproximadamente:
4,32 kg.
120 kg.
240 kg.
4
3 × 10 kg.
4
3,6 × 10 kg.
Questão 15)
Considere que o calor específico de um material
presente nas cinzas seja c = 0,8 J/gºC . Supondo
que esse material entra na turbina a –20ºC , a
energia cedida a uma massa m = 5 g do material
para que ele atinja uma temperatura de 880ºC é
igual a
a)
b)
c)
d)
220 J.
1000 J.
4600 J.
3600 J.
GABARITO:
1) Gab: D
a)
b)
c)
d)
645
1275
1940
3820
Questão 13)
Coloca-se 1,50 kg de gelo, à temperatura de 0 ºC,
no interior de um forno de micro-ondas de
potência 1,0 kW. O tempo de funcionamento a
que se deve programar o forno de micro-ondas
2) Gab: B
3) Gab: B
4) Gab: E
5) Gab: D
6) Gab: A
7) Gab: C
8) Gab: A
9) Gab: D
10) Gab:
a) Q = 87 cal
b) t = 145 s
11) Gab: B
12) Gab: B
13) Gab: D
14) Gab: B
15) Gab: D