XV SEMANA
VI CONGRESSO IBÉRICO
Transferência de metais tóxicos no sistema solo-planta e sua
complexação no Juncus effusus L.
Toxic metals transference in the soil-plant system and its
complexation on Juncus effusus L.
1
Durães, N. ; Bobos, I.
1,2
; Ferreira da Silva, E.
3
1
2
GIMEF - Centro de Geologia, Universidade do Porto, Rua do Campo Alegre 687, 4169-007 Porto
e-mail: [email protected]
Departamento de Geologia, Faculdade de Ciências, Universidade do Porto, Rua do Campo Alegre 687, 4169-007
Porto
3
ELMAS - Departamento de Geociências, Universidade de Aveiro, Campus de Santiago, 3810-193 Aveiro
Abstract
The bioaccumulation of metals by plants is important in the remediation (fitoremediation) of contaminated sites.
However the transport and accumulation mechanisms of metals in plants are even very few studied.
The soil mineralogy where the plant growed was studied by X ray diffraction. Clay minerals, hydrate Fe oxides,
gypsum, carbonates, quartz and sulphides minerals were identified. The chemical analyse of this soil showed high toxic
-1
-1
-1
-1
metals contents: Cu (146-192 mg.Kg ); Pb (139-173 mg.Kg ); Zn (232-1123 mg.Kg ) e Cd (38-74 mg.Kg ).
The chemical analyse of Juncus effusus L. roots and stems showed that metals contents were here too high. The
-1
-1
-1
-1
-1
roots had metals levels of Cu (110 mg.Kg ), Pb (34 mg.Kg ), Zn (265 mg.Kg ), Cd (2.5 mg.Kg ), Fe (12771 mg.Kg ) e
-1
-1
-1
-1
-1
Mn (183 mg.Kg ). In stems this levels were: Cu (24 mg.Kg ), Pb (4 mg.Kg ), Zn (348 mg.Kg ), Cd (12 mg.Kg ), Fe
-1
-1
(224 mg.Kg ) e Mn (784 mg.Kg ). This values proves that this plant have a high capacity of metals sorption.
The study by FT-IR spectrometry of plant allowed the identification of organic (C-O; C=O) and inorganic (S-O; Si-O)
complexes in roots and stems. In the roots still occurs Me-O type complexes, while in the stems occurs Al-OH and Ca2SO4 type complexes. The type of complexes presents indicated the precipitation of a group of inorganic complexes
associated with mineral structures (clay minerals, gypsum, etc) with which metals can be complexated in plant.
Keywords: FT-IR, metal, bioaccumulation, complexation
Resumo
A capacidade de bioacumulação de metais pelas plantas é um assunto que tem despertado interesse no que
concerne à remediação (fitoremediação) de zonas contaminadas. Contudo, os mecanismos que presidem ao transporte
e a acumulação dos metais nas plantas são ainda pouco estudados.
Foi realizado o estudo mineralógico, por difractometria de raios X, do solo onde se encontrava a planta, onde foi
possível identificar minerais argilosos, óxidos de ferro hidratados, gesso, carbonatos, quartzo e sulfuretos. Na análise
-1
-1
química do solo determinaram-se teores elevados em metais tóxicos: Cu (146–192 mg.Kg ); Pb (139–173 mg.Kg ); Zn
-1
-1
(232–1123 mg.Kg ) e Cd (38–74 mg.Kg ).
A análise química das raízes e dos caules do Juncus effusus L. demonstrou que os teores em metais eram também
-1
-1
-1
-1
elevados. As raízes apresentavam teores em Cu (110 mg.Kg ), Pb (34 mg.Kg ), Zn (265 mg.Kg ), Cd (2.5 mg.Kg ),
-1
-1
-1
-1
Fe (12771 mg.Kg ) e Mn (183 mg.Kg ). Nos caules os valores registados foram: Cu (24 mg.Kg ), Pb (4 mg.Kg ), Zn
-1
-1
-1
-1
(348 mg.Kg ), Cd (12 mg.Kg ), Fe (224 mg.Kg ) e Mn (784 mg.Kg ). Estes teores sugerem que a esta planta
apresenta uma grande capacidade de sorção dos metais.
O estudo realizado por espectrometria de FT-IR na planta permitiu a identificação de um conjunto de complexos
orgânicos (C-O; C=O) e inorgânicos (S-O; Si-O) nas raízes e nos caules. Nas raízes ocorrem ainda complexos do tipo
2Me-O, enquanto que nos caules surgem complexos do tipo Al-OH e Ca-SO4 . Este tipo de complexos são indicativos
da precipitação de um conjunto de complexos inorgânicos associados a estruturas minerais (minerais argilosos,
sulfatos, etc) com os quais os metais se poderão complexar na planta.
Palavras-chave: FT-IR, metal, bioacumulação, complexação
9. Biogeoquímica/ Biogeochemistry
|| 422
XV Semana – VI Congresso Ibérico de Geoquímica
Introdução
Os mecanismos de interacção solo-planta
são ainda pouco estudados. Contudo, a
capacidade
de
algumas
plantas
para
absorverem,
acumularem
ou
mesmo
decomporem contaminantes que se encontram
nos solos, tem despertado atenções, no sentido
da sua utilização na remediação de zonas
contaminadas.
Vários factores são determinantes até que o
metal se encontre em condições de poder ser
assimilado pelas raízes da planta. Estes
factores podem estar relacionadas: 1) com o
solo (pH, potencial redox, volume de matéria
orgânica, tipo de minerais argilosos e óxidos de
Fe e Mn e a interacção entre diferentes iões); 2)
com a planta (espécie e idade da planta); 3)
com a própria interacção planta-metal (Adriano,
2001).
A segregação de exsudações pelas raízes
ou pelas micorrizas, para a rizosfera, tem um
contributo importante no sentido de facilitar a
tolerância e o transporte dos metais nas plantas,
através da variação do pH ou das condições
redox. Em geral, no caso de catiões, a
acidificação tende a provocar uma maior
solubilidade
destes
(Pilon-Smits,
2005;
Robinson et al., 2006), enquanto que para
aniões, a solubilidade aumenta como o aumento
do pH (Robinson et al., 2006).
Vários autores têm-se dedicado ao estudo
da tolerância de espécies de plantas a metais
pesados. Deng et al. (2004) estudaram a
acumulação de Pb, Zn, Cu e Cd em 12 espécies
de plantas. Em Portugal, Freitas et al. (2004)
estudaram a capacidade de tolerância de
elementos traço em plantas e em solos
contaminados da mina de S. Domingos. Por
outro lado, Batista et al. (2007) estudaram os
mecanismos biogeoquímicos e a transferência
de metais para a planta Cistus Ladanifer L. na
região mineira de Neves Corvo.
No presente trabalho pretende-se fornecer
dados químico-mineralógicos relativamente à
rizosfera e os tipos de complexos que ocorrem
nos Juncus effusus L..
Materiais e Métodos
Amostras de solos e plantas foram
recolhidas nas zonas contaminadas com metais
tóxicos, aferentes à zona de oxidação da mina
do Lousal (Faixa Piritosa Ibérica). Os solos da
região correspondem, predominantemente, a
litossolos (solos esqueléticos), resultantes da
alteração de xistos e grauvaques.
Os valores de pH e condutividade eléctrica
determinaram-se numa suspensão de 1/5 (p/p)
de solo/água. A análise mineralógica dos solos
efectuou-se por difractrometria de raios X das
fracções inferiores a 2mm, com recurso a um
aparelho da marca Philips X’Pert MPD, radiação
de CuKα. A análise química dos solos realizouse por espectrometria de fluorescência de raios
X.
Das amostras de plantas procedeu-se à
separação das raízes e das partes aéreas. Após
lavagem em água destilada, as plantas foram
colocadas a secar numa estufa ventilada numa
temperatura nunca superior a 45 ºC, durante um
período mínimo de 48 horas. Posteriormente, as
raízes foram moídas a uma granulometria
inferior a 150μm. Deste material, uma parte foi
separada para análise química e uma outra
parte para Espectrometria de Infravermelho (FTIR).
A análise química foi realizada por
espectrometria
de
absorção
atómica.
Previamente foi feita uma decomposição da
amostra seca numa mistura ácida (HCl – HNO3
– HF – HClO4), aquecida numa placa de
aquecimento até à total evaporação. Ao resíduo
final foi adicionada uma quantidade de HNO3 e
H2O.
A
análise
por
espectrometria
de
Infravermelho (FT-IR) foi efectuada com recurso
a um espectrómetro de Infravermelho com
Transformada Fourier, da marca Bruker Tensor27, numa frequência de 4000-400 cm -1.
Resultados
Mineralogia do solo
As fracções silto-argilosas dos solos contêm
minerais argilosos, óxidos de ferro hidratados,
gesso, carbonatos, quartzo e sulfuretos. Na
amostra superficial do solo (S1) predominam o
gesso, as micas, o quartzo e os FeO(OH),
enquanto na amostra inferior de solo (S2)
identificaram-se clorites,
micas,
quartzo,
sulfuretos e FeO(OH). Esta análise sugere que
os sulfuretos, devido à sua elevada densidade,
encontram-se preferencialmente sedimentados
em profundidade no perfil do solo, enquanto que
à superfície ocorrem os minerais resultantes dos
processos de oxidação, ou minerais com
densidade mais baixa.
Geoquímica de solos e plantas
Das várias amostras de plantas recolhidas,
fez-se uma selecção de uma amostra (Juncus
effusus L.) com base nos teores elevados de
metais que apresentava.
A análise dos resultados dos teores em Cu,
Pb, Zn, Fe, Mn e Cd nas amostras de solo e na
planta (Tabela1) permite-nos constatar que a
acumulação dos metais é bastante elevada.
Para o caso dos solos a acumulação é maior na
camada inferior do solo que na camada
superfícial. Contudo, o aspecto mais relevante a
salientar, está relacionado com a acumulação
de metais na planta que é muito superior à
acumulação no solo onde se encontrava.
Quando se comparam os valores dos metais
presentes nas raízes e nos caules, verifica-se,
que contrariamente ao que seria de esperar,
para o caso do Zn, Cd e Mn existe uma maior
acumulação no caule do que nas raízes.
9. Biogeoquímica/ Biogeochemistry
|| 423
XV Semana – VI Congresso Ibérico de Geoquímica
2.5
Caule
Transmitância%
2
1.5
Ca-SO42Al-OH
1
Raíz
0.5
Me-O
0
3900
3400
2900
2400
1900
1400
900
Me-O400
-1
Frequência cm
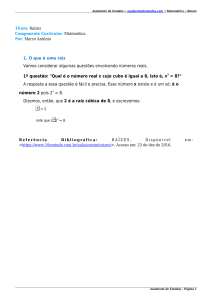
Fig. 1 – Espectros de FT-IR das amostras de raízes e caules da planta Juncus effusus L.
Os valores de Zn no solo são elevados,
nomeadamente, na amostra S2, enquanto que
os valores de Cu e Pb são, de um modo geral,
mais baixos. No caso do Zn as massas do
minério apresentavam teores de 1,4%, maiores
que o Cu e Pb, com teores de 0,7% e 0,8%,
respectivamente (Matzke, 1971).
A bioacumulação do Zn, Cd e do Mn é maior
nos caules que nas raízes, o que indica que
estes elementos são facilmente translocados na
planta. Em contraste, a bioacumulação do Cu,
Pb e Fe ocorre preferencialmente nas raízes.
Espectroscopia de infravermelho
-1
Tabela 1 – Teores de metais (mg.Kg ) das amostras
de raízes e caules do Juncus effusus L. (valores
referentes a Kg de amostra seca) e do respectivo solo.
Amostra
S1
S2
Raíz
Caule
Cu
146
192
110
24
Pb
139
173
34
4
Zn
232
1123
265
348
Cd
38
74
2.5
12
Fe
ND
ND
12771
224
Mn
ND
ND
183
784
ND – Não determinado
Tabela 2 – Medidas de pH e condutividade do solo
Amostra
pH
Solo
4.70
Condutividade
(μS.cm -1)
3800
Os resultados químicos sugerem que o
Juncus effusus L. apresenta um potencial de
bioacumulação elevado para o Zn, Fe e o Mn.
Caso semelhante ocorre para o Cd, que embora
apresente teores significativamente mais baixos,
do
que
os
elementos
considerados
anteriormente, estes valores são muito
elevados, atendendo a que os teores médios em
-1
solos são de 0.01–1mg.Kg . Contudo, embora
os níveis de toxicidade deste elemento para as
plantas tenda a ser baixo, estas, em regra, têm
uma grande permissividade ao Cd (Varennes,
2003).
As amostras de raízes e de caules foram
estudadas por espectrometria de infravermelho.
Os resultados obtidos confirmam a presença de
complexos orgânicos (C-O; C=O) e complexos
inorgânicos (S-O; Si-O) presentes nas raízes e
nos caules (Fig.1). Nas raízes ocorrem ligações
do tipo Me-O (bandas de absorção 532 – 435
-1
cm ). Nos caules ocorrem ligações do tipo Al-1
OH (banda de absorção 918 cm ) e ligações do
2
tipo Ca-SO4 (bandas de absorção 669 cm-1, 602
-1
cm ).
Discussão e Conclusão
Quando os níveis de toxicidade são
elevados, as plantas podem adoptar estratégias
de precipitação dos metais na rizosfera,
tornando-os, deste modo, menos biodisponiveis
(Pilon-Smits, 2005).
O Juncus effusus L. apresenta tolerância a
ambientes contaminados com metais pesados.
Os resultados obtidos da análise química do
solo e da planta permitem afirmar que o Juncus
effusus L. tem a capacidade de extrair os metais
do solo, de os bioacumular e, para o caso de
alguns desses metais, de os translocar
eficientemente para as partes aéreas da planta.
A análise dos espectros de infravermelho
permitiu detectar a presença de compostos
orgânicos que poderão participar na quelatação
dos metais.
9. Biogeoquímica/ Biogeochemistry
|| 424
XV Semana – VI Congresso Ibérico de Geoquímica
A quelatação dos elementos contaminantes
a compostos de carbono segregados pelas
plantas, é importante na sequestração e
transporte dos metais da rizosfera para a planta,
na translocação destes das raízes para as
partes aéreas, assim como, na tolerância a
esses mesmos contaminantes (Pilon-Smits,
2005).
A presença de compostos de S-O, Si-O, Al2
OH e Ca-SO4 , indicam a precipitação de um
conjunto de complexos inorgânicos associados,
supostamente, a um conjunto de estruturas
minerais (minerais argilosos, sulfatos, etc), com
os quais os metais se poderão complexar na
própria planta. As bandas Me-O comprovam
também a presença de Fe na planta, tal como
demonstrado pelas análises químicas.
Contudo, estes estudos carecem de mais
dados para uma melhor compreensão dos
mecanismos de complexação e precipitação dos
metais nas plantas.
Varennes, A., 2003. Produtividade dos solos e
ambiente. Escolar Editora, Lisboa, 409pp.
Agradecimentos
O primeiro autor agradece à Fundação para
a Ciência e a Tecnologia o apoio concedido no
âmbito
da
bolsa
de
doutoramento
(SFRH/BD/22413/2005).
Referências
Adriano, D.C., 2001. Trace Elements in
Terrestrial Environments: Biogeochemistry,
Bioavailability and Risks of Metals. 2nd ed..
Springer-Verlag, New York, 866pp.
Batista, M.J., Abreu, M.M, Serrano Pinto, M.,
2007. Biogeochemistry in Neves Corvo
mining region, Iberian Pyrite Belt, Portugal.
Journal of Geochemical Exploration 92, 159176.
Deng, H., Ye, Z.H., Wong, M.H., 2004.
Accumulation of lead, zinc, copper and
cadmium by 12 wetland plant species
thriving in metal-contaminated sites in China.
Environmental Pollution 132, 29-40.
Freitas, H., Prasad, M.N.V., Pratas, J., 2004.
Plant community tolerant to trace elements
growing on the degraded soils of São
Domingos mine in the south east of Portugal:
environmental implications. Environmental
Pollution 30, 65-72.
Matzke, K., 1971. Mina do Lousal. Principais
jazigos minerais do sul de Portugal. LivroGuia nº4, I Congresso Hispano-LusoAmericano de Geologia Económica, Lisboa,
pp.25-32.
Pilon-Smits, E., 2005. Phytoremediation. Annu.
Rev. Plant Biol 56, 15-39.
Robinson, B., Bolan, N., Mahimairaja, S.,
Clothier, B., 2006. Solubility, Mobility, and
Bioaccumulation of Trace Elements: Abiotic
Processes in the Rizosphere. In: Prasad,
M.N.V., Sajwan, K.S., Naidu, R. (Ed.), Trace
Elements
in
the
Environment:
Biogeochemistry,
Biotechnology,
and
Bioremediation, CRC Press Taylor and
Francis, New York, pp. 97-110.
9. Biogeoquímica/ Biogeochemistry
|| 425