PRÉ-VEST
AMANDA
06-07-2015
QUÍMICA
SIMULADO DE QUÍMICA
1 - Observe os gráficos abaixo, que registram o aquecimento
e o resfriamento da água pura.
d) maior do que 1 g, pois o ferro é mais denso do que o
oxigênio.
e) maior do que 1 g, pois átomos de oxigênio se ligam aos de
ferro.
4 - Um aluno encontrou em um laboratório três frascos
contendo três misturas binárias, conforme descrito a seguir.
1.a mistura: heterogênea, formada por dois sólidos.
2.a mistura: heterogênea, formada por dois líquidos.
3.a mistura: homogênea, formada por dois líquidos cujos
pontos de ebulição diferem em 20 °C.
Marque a alternativa que indica os processos de separação
mais adequados para recuperar as substâncias originais na
1.a, 2.a e 3.a misturas, respectivamente.
As etapas (I), (II), (III) e (IV) correspondem, respectivamente,
às seguintes mudanças de estados físicos:
a) fusão, ebulição, condensação e solidificação.
b) condensação, solidificação, fusão e ebulição.
c) solidificação, condensação, fusão e ebulição.
d) fusão, ebulição, solidificação e condensação.
e) ebulição, condensação, solidificação e fusão.
2 - As equações abaixo representam transformações que
ocorrem na natureza:
Gelo → água líquida
Mármore + chuva ácida (ácido sulfúrico) → gesso + água + gás
carbônico
Madeira + ar → carvão + gás carbônico + água
Sobre essas transformações, é correto afirmar que:
a) a transformação física apresentada ocorre com liberação
de energia.
b) a transformação química requer energia para que ocorra; a
física, não.
c) a formação de gases evidencia a ocorrência de reação
química.
d) a água líquida é obtida apenas a partir de transformação
química.
3 - Quando se aquece uma porção de esponja de aço,
constituída principalmente por ferro (Fe), em presença de
oxigênio do ar, ela entra em combustão, formando óxido de
ferro (III) como único produto. Logo, se 1 g de esponja de aço
for aquecido e sofrer combustão total, a massa do produto
sólido resultante será:
a) menor do que 1 g, pois na combustão forma- se também
CO2(g).
b) menor do que 1 g, pois o óxido formado é muito volátil.
c) igual a 1 g, pois a massa se conserva nas transformações
químicas.
a) Filtração, decantação e destilação simples.
b) Evaporação, destilação simples e decantação.
c) Decantação, destilação simples e destilação fracionada.
d) Sublimação, decantação e destilação fracionada.
5 - As massas atômicas são essenciais para os cálculos da
química. Se uma nova escala de massas atômicas médias
fosse definida, baseada na suposição da massa de um átomo
de carbono-12 (12C) ser exatamente 1 u, qual seria a massa
atômica média do neônio? (Massa atômica média do neônio
na escala atual = 20,18 u)
a) 20,18/ 12 u
b) 12 u
c) 20,18 u
d) 20,18 × 12 u
e) 12 / 20,18 u
6 - Analise as afirmações em relação a duas moléculas de
ácido ascórbico (vitamina C) C6H8O8.
I. Contém 6 átomos de carbono, 8 átomos de hidrogênio e 8
átomos de oxigênio.
II. Contêm 12 átomos de carbono, 16 átomos de hidrogênio e
16 átomos de oxigênio.
III. Sua massa corresponde a 208 g.
É (são) correta(s):
a) apenas III.
b) apenas I.
c) apenas II.
d) I e II.
e) I e III.
7 - O enxofre é uma substância simples cujas moléculas são
formadas pela união de 8 átomos; logo, sua fórmula
molecular é S8 . Quando no estado sólido, ele forma cristais
do sistema rômbico ou monoclínico, conforme figura abaixo.
Rua Lúcio José Filho, 27 Parque Anchieta Tel: 3012-8339
10 microgramas por decilitro de sangue já causa efeitos
adversos para o aprendizado e o comportamento, segundo o
site da OMS.
Adaptado de Sahabi Yahaya, Reuters/Nigéria.
A respeito do enxofre rômbico e do enxofre monoclínico é
correto afirmar que eles se constituem em:
a) formas alotrópicas do elemento químico
fórmula é S8.
b) átomos isótopos do elemento químico
símbolo é S.
c) átomos isótopos do elemento químico
fórmula é S8.
d) formas alotrópicas do elemento químico
símbolo é S.
e) formas isobáricas da substância química
símbolo é S.
enxofre, cuja
enxofre, cujo
enxofre, cuja
enxofre, cujo
enxofre, cujo
8 - Um átomo do elemento químico x, usado como corante
para vidros possui número de massa igual a 79 e número de
nêutrons igual a 45. Considere um elemento y, que possua
propriedades químicas semelhantes ao elemento x.
Na Tabela de Classificação Periódica, o elemento y estará
localizado no seguinte grupo:
De acordo com o texto e com os seus conhecimentos
específicos a respeito do chumbo, é correto afirmar que:
a) o elemento químico chumbo (Pb) é um metal alcalino.
b) os íons Pb2+, contidos em uma solução, não poderiam ser
precipitados pela ação de íons cloreto, pois o PbCl 2 é muito
solúvel em meio aquoso.
c) o chumbo é um metal que apresenta somente um estado
de oxidação.
d) segundo o site da OMS, o chumbo, ao atingir a
concentração de 1∙10–4 g/L no sangue, causa efeitos adversos
para o aprendizado e para o comportamento.
e) à temperatura ambiente, o metal chumbo encontra-se no
estado líquido.
11 - O aspartame é um dipeptídeo cristalino, inodoro, de
baixa caloria e com uma doçura de 180 a 200 vezes à da
sacarose, que é um dissacarídeo formado por glicose e
frutose.
Abaixo estão representadas as fórmulas estruturais da
sacarose e do aspartame.
a) 7
b) 9
c) 15
d) 16
9- A que família e período pertence o átomo que apresenta
os seguintes números quânticos para o elétron diferencial.
n=4
L= 1
m= +1 s = -1/2
a) Família 5A e 4º período
b) Família 3A e 4º período
c) Família 4A e 3º período
d) Família 5A e 5º período
e) Família 5A e 3º período
10 - ENVENENAMENTO POR CHUMBO MATA 163 PESSOAS
NA NIGÉRIA
Pelo menos 163 nigerianos morreram desde março, a maioria
crianças, devido ao envenenamento por chumbo, causado por
garimpeiros clandestinos. O epidemiologista chefe do
Ministério da Saúde da Nigéria, Henry Akpan, disse à Agência
Reuters que já foram notificados 355 casos, em seis
localidades remotas do Estado de Zamfara, norte do país, e
que 111 dos mortos eram crianças, muitas delas menores de
cinco anos. Segundo ele, há uma incidência excepcional de
dores abdominais, vômitos, náuseas e, eventualmente,
convulsões e que muitas vítimas morreram após entrar em
contato com ferramentas, terra ou água com concentrações
elevadas de chumbo em torno da área onde estão escavando
ouro.
O excesso desse metal no organismo pode afetar vários
órgãos, incluindo o sistema nervoso e reprodutivo e os rins,
sendo especialmente nocivo para crianças pequenas e para
grávidas. Estudos sugerem que uma concentração a partir de
A respeito dessas moléculas, considere as afirmações I, II, III,
IV e V abaixo.
I. O aspartame possui os grupos funcionais: ácido carboxílico,
amina, cetona e éster.
II. A sacarose possui uma ligação peptídica unindo a glicose e
a frutose.
III. Na molécula do aspartame, existe somente um átomo de
carbono terciário.
IV. A sacarose é um hidrocarboneto de fórmula molecular
C12H22O11.
V. A molécula do aspartame possui atividade óptica.
Estão corretas, somente,
a) I, III e V.
b) I, IV e V.
c) I, II e III.
d) II, III e IV.
e) III e V.
12 - Certa solução aquosa de bicarbonato de sódio, NaHCO3,
apresenta pH = 8,3 a 25oC. Tal solução é:
Rua Lúcio José Filho, 27 Parque Anchieta Tel: 3012-8339
a) básica e terá seu pH diminuído, se a ela for acrescentada
uma porção de ácido clorídrico, HCl.
b) ácida e terá seu pH aumentado, se a ela for acrescentada
uma porção de soda cáustica, NaOH.
c) básica e terá seu pH diminuído, se a ela for acrescentada
uma porção de soda cáustica, NaOH.
d) ácida e terá seu pH diminuído, se a ela for acrescentada
uma porção de ácido clorídrico, HCl.
e) básica e terá seu pH aumentado, se a ela for acrescentada
uma porção de ácido clorídrico HCl.
13- O titânio e seus compostos são amplamente empregados
tanto na área metalúrgica como na produção de cosméticos e
fármacos. No Brasil, são extraídos os minérios na forma de
óxidos, rutilo (TiO2) e ilmenita (FeTiO3). O titânio apresenta o
mesmo estado de oxidação nesses dois minérios. O número
de oxidação do titânio e a configuração eletrônica da camada
de valência do ferro (26Fe) no estado de oxidação em que se
encontra na ilmenita são, respectivamente,
a) +2 e 3d6 4s2.
b) +2 e 3d4 4s2.
c) +3 e 3d5.
d) +4 e 3d6.
e) +4 e 3d4
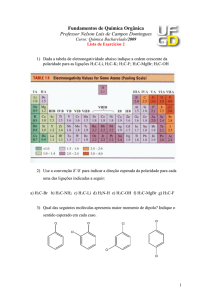
14 - Na tabela a seguir, é reproduzido um trecho da
classificação periódica dos elementos.
A partir da análise das propriedades dos elementos, está
correto afirmar que:
a) a afinidade eletrônica do neônio é maior que a do flúor.
b) o fósforo apresenta maior condutividade elétrica que o
alumínio.
c) o nitrogênio é mais eletronegativo que o fósforo.
d) a primeira energia de ionização do argônio é menor que a
do cloro.
e) o raio do íon Al3+ é maior que o do íon Se2-.
15 - Os metais alcalino terrosos, como o estrôncio, pertencentes ao grupo 2 da tabela periódica, têm a tendência de
perder dois elétrons para a formação de sais com os
halogênios pertencentes ao grupo 17, como o iodo.
Considerando o isótopo, assinale a alternativa em que todas
as informações estão corretas.
16 - O que diferencia uma ligação iônica de uma ligação
covalente é:
a) a quantidade de elétrons existente nas eletrosferas dos
átomos que participam da ligação.
b) o fato de em uma delas ocorrer compartilhamento de um,
dois ou três pares de prótons entre os átomos que
participam da ligação.
c) a quantidade de nêutrons existente nos núcleos dos
átomos, que determina a carga dos íons formados.
d) o fato de em uma delas existir força de repulsão entre íons
com cargas opostas.
e) o fato de em uma delas ocorrer transferência de elétrons
da eletrosfera de um átomo para a eletrosfera de outro.
17 - Assinale a opção que contém, respectivamente, a geometria das moléculas AsH3 e SiCl4 no estado gasoso.
a) Plana, plana.
b) Piramidal, plana.
c) Plana, tetragonal.
d) Piramidal, piramidal.
e) Piramidal, tetragonal.
18 - planejar suas pesquisas para fins de obtenção de produtos específicos, muitos materiais de nobres utilidades para
o homem foram descobertos de maneira acidental. O teflon,
por exemplo, foi descoberto em 1938 por Roy Plunkett,
quando pesquisava as propriedades do gás tetrafluoretileno
(C2F4), o qual originou um polímero sólido, de cor branca,
bastante resistente ao calor. Com relação ao
tetrafluoretileno, é correto afirmar que suas ligações
químicas são respectivamente:
Dados: C (Z = 6); F (Z = 9); H (Z = 1)
a) todas covalentes apolares do tipo pi (π).
b) iônicas (C–F) e eletrovalentes (C–C).
c) todas covalentes apolares do tipo sigma (σ).
d) covalentes polares (C–F) e apolares (C–C).
e) covalentes polares (F–F) e apolares (C–F).
19 - Existem três diferentes diclorobenzenos, C6H4Cl2, dependendo da localização dos átomos de cloro:
Sobre esses compostos, pode-se dizer que:
( ) todos têm o mesmo momento de dipolo, pois sua
composição química é a mesma.
( ) o mais polar é o composto (2).
( ) o composto (1) é mais solúvel em solventes apolares.
( ) os compostos (2) e (3) são polares.
( ) nenhum deles é polar porque o anel benzênico é
perfeitamente simétrico nos três casos.
20 - Para responder à questão, numere a Coluna B, que
contém algumas fórmulas de substâncias químicas, de acordo
com a Coluna A, na qual estão relacionados tipos de atrações
intermoleculares.
Rua Lúcio José Filho, 27 Parque Anchieta Tel: 3012-8339
Coluna A
1. Ligações de hidrogênio
2. Dipolo induzido-dipolo induzido
3. Dipolo-dipolo
d) interações dipolo permanente-dipolo permanente.
Coluna B
( ) HF
( ) Cl2
( ) CO2
( ) NH3
( ) HCl
( ) SO2
( ) BF3
( ) CCl4
21 - Estudos recentes têm indicado que o uso inapropriado
de lubrificantes ordinários, normalmente encontrados em
farmácias e drogarias, tais como loções oleosas e cremes,
que contêm vaselina, óleo mineral ou outros derivados de
petróleo, acarretam danificações nos preservativos
masculinos (camisinhas), os quais são feitos, geralmente,
de um material denominado látex (poli-1,4-isopreno),
cujo momento dipolar é aproximadamente igual a zero (μ
≈ 0), e cuja estrutura da unidade monomérica é dada a
seguir:
Tais danificações, geralmente, constituem-se de microrupturas das camisinhas, imperceptíveis a olho nu, que
permitem o fluxo de esperma através das mesmas,
acarretando gravidez indesejável, ou a transmissão de
doenças sexualmente transmissíveis, particularmente a aids.
Assinale a alternativa correta.
a) Substâncias apolares seriam mais adequadas como
lubrificantes dos preservativos.
b) Óleos lubrificantes bastante solúveis em tetracloreto de
carbono (CCl4), geralmente, não interagem com o látex.
c) Os óleos que provocam danificações nos preservativos são,
geralmente, de natureza bastante polar.
d) Substâncias, cujas forças intermoleculares se assemelham
às presentes no látex, seriam mais adequadas como
lubrificantes dos preservativos.
e) Substâncias com elevados valores de momento de dipolo
seriam mais adequadas como lubrificantes dos
preservativos.
23 - Alguns compostos, quando solubilizados em água,
formam soluções que conduzem eletricidade. Dados os
compostos abaixo:
I. K2SO4
II. Cl2
III. NaNO3
IV. KCl
V. CH3CH2OH
Quais formam soluções condutoras de eletricidade?
a) I, III, IV
b) III e IV
c) I, III, IV e V
d) I e IV
e) III, IV e V
24 - O leite de magnésia nada mais é do que uma suspensão
de hidróxido de magnésio em água e é utilizado como
antiácido estomacal, nas azias, e como laxante intestinal. Se
uma pessoa tomar essa solução, ocorrerá qual das reações
químicas abaixo no estômago?
a) Mg (OH)2 + 2 HNO3 → Mg(NO3)2 + 2 H2O
b) Mg (OH)2 + HCOOH → MgHCOOH + H2O
c) MgO + 2 HCl → MgCl2 + H2O
d) Mg (OH)2 + 2 HCl → MgCl2 + 2 H2O
e) MgO + 2 HClO → Mg(ClO)2 + H2O
25 - A água destilada (pH = 7,0), em contato com o ar, dissolve o dióxido de carbono (CO2), levando à formação de um
composto que a deixa levemente ácida (pH = 6,0). Nas
grandes cidades, a queima de combustíveis fósseis produz
gases, como os óxidos de nitrogênio e de enxofre, que
reagem com a água produzindo compostos ainda mais ácidos.
A precipitação dessas soluções aquosas denomina-se chuva
ácida. Os gases como o dióxido de carbono, os óxidos de
nitrogênio e o trióxido de enxofre, presentes no ar das
grandes cidades, reagem com a água podendo formar,
respectivamente, os ácidos:
a) carboxílico, nítrico e sulfídrico.
b) acético, muriático e nítrico.
c) carbônico, nítrico e sulfúrico.
d) carbônico, sulfúrico e nítrico.
e) clorídrico, nítrico e sulfúrico.
22 - Analise este quadro, em que está apresentada a temperatura de ebulição de quatro substâncias:
Considerando-se os dados desse quadro, é correto afirmar
que, à medida que a cadeia carbônica aumenta, se tornam
mais fortes as:
a) ligações covalentes.
b) interações dipolo instantâneo-dipolo induzido.
c) ligações de hidrogênio.
Rua Lúcio José Filho, 27 Parque Anchieta Tel: 3012-8339