ENRIQUECIMENTO DE NITROGÊNIO-15 PELO SISTEMA NITROX. PARTE I
COLUNA DE CONTRACORRENTE ENTRE SOLUÇÃO DE ÁCIDO NÍTRICO E ÓXIDOS DE NITROGÊNIO NA
FASE GASOSA
Carlos Ducatti*, José Aurélio Bonassi** & Eichii Matsui**
* Departamento de Física e Biofísica do Instituto de Biociências - UNESP
Caixa Postal 510
18618-000 Botucatu/SP - Brasil
** Centro de Energia Nuclear na Agricultura - CENA/USP
Caixa Postal 96
13416-000 Piracicaba/SP - Brasil
RESUMO
Neste trabalho, descreve-se o modo operacional, a nível de laboratório, de uma coluna de contracorrente
entre solução de ácido nítrico e óxidos de nitrogênio (Sistema Nitrox), para a produção de ácido nítrico na
concentração de 5 átomos % de 15N.
.
I. INTRODUÇÃO
Sistema Nitrox é um sistema químico utilizado
internacionalmente para o enriquecimento de nitrogênio15, na solução de ácido nítrico e óxidos de nitrogênio na
fase gasosa, em fluxo de contracorrente.
O nitrogênio-15 tem sido separado e
concentrado por uma variedade de métodos [1] [2] e,
dentre eles, os mais utilizados são: troca química,
termodifusão, destilação a baixa temperatura, troca
iônica, fotoquímica e absorção contínua.
Normalmente, os sistemas de troca química
entre duas fases, líquido e gás, são os mais utilizados em
relação aos demais métodos, particularmente devido à
rápida troca entre as formas químicas utilizadas. Estes
métodos têm mostrado serem os mais satisfatórios na
separação dos isótopos, para a maioria dos elementos
leves[3].
Especificamente, o sistema de troca isotópica
entre solução de ácido nítrico e monóxido de nitrogênio
torna-se o mais atrativo, devido ao seu alto fator de
fracionamento (α = 1,055).
O objetivo reside no desenvolvimento, a nível
de laboratório, de uma coluna de enriquecimento de
nitrogênio-15, em fluxo de contracorrente de solução de
ácido nítrico e óxidos de nitrogênio na fase gasosa. Visa,
também, à obtenção de nitratos com concentração da
ordem de 5 átomos% 15N.
II. MATERIAL E MÉTODOS
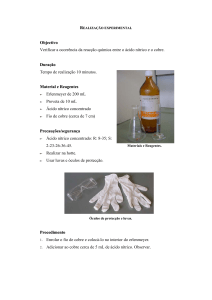
Coluna de Enriquecimento. O diagrama da Figura 1
ilustra as principais unidades operacionais, a principal
reação de troca isotópica e as principais reações químicas
do sistema HNO3/NO.
O sistema, genericamente, consta de
três
unidades operacionais principais. O Refluxador Principal,
onde o ácido nítrico, na presença de dióxido de enxofre,
dissocia-se em óxidos de nitrogênio, sendo que, o dióxido
de nitrogênio, na presença da água, regenera-se a ácido
nítrico e, como conseqüência destas reações, ocorre a
formação de ácido sulfúrico como sub-produto. A Coluna
Isotópica, na qual o nitrogênio-15 acumula-se, lentamente,
no ácido nítrico e nos óxidos de nitrogênio, a partir da base
da coluna. Por último, o Refluxador Secundário, no qual o
monóxido de nitrogênio, na presença da água e oxigênio,
regenera-se a ácido nítrico como sub-produto.
As principais desvantagens deste sistema
resumem-se no largo consumo de dióxido de enxofre e na
produção de uma tonelada de ácido sulfúrico como subproduto, para cada átomo grama de 15N puro obtido [4].
A coluna de Troca Isotópica, consiste em um tubo
único de aço inox, de 390cm de comprimento e 1,8cm de
diâmetro interno, preenchida com unidades de tela de aço
inox de 60 mesh, de dimensões (∅ 0,4 x h 0,4)cm,
enroladas na forma aproximada da letra maiúscula G [5].
O Refluxador Principal, consiste em uma peça
única de vidro, tipo pyrex no 7740, de 110 cm de
comprimento e 4 cm de diâmetro interno, preenchido com
unidades de vidro, denominadas de miçangas, de 0,2 cm
de diâmetro, 0,15 cm de espessura, com furo de 0,08 cm
de diâmetro[5].
O Refluxador Secundário, consiste em uma peça
única de vidro, tipo pyrex no 7740 de 137 cm de
comprimento e 2 cm de diâmetro interno, preenchido com
miçangas de vidro[5].
HNO3
Principais Reações
H2O
Refluxador Secundário
NO
Refluxador Secundário
O2
Coluna de
Troca
Isotópica
2NO + O2 →2NO2
(1)
3NO2 + H2O → 2HNO3 + NO
(2)
HNO3 Sub-produto
Coluna de Troca Isotópica
Amostrador de Produto:
Líquido ou Gás
HNO3
NO
retirou-se lentamente um volume aproximado de 2 cm3
diário de ácido nítrico enriquecido.
No segundo experimento, o equilíbrio do sistema
foi mantido durante o período de vinte e sete dias.
Durante a manutenção do patamar de equilíbrio isotópico,
(1,723 ±
0,042) átomo% 15N, referente ao período de três dias
15
NO + H14NO3
14
NO + H15NO3
(3)
Refluxador Principal
H2O
3SO2 + 2HNO3 + 2H2O→ 3H2SO4 + 2NO
(4)
SO2 + 2HNO3
→ H2SO4 + 2NO2
(5)
3NO2 + H2O
→ 2HNO3+ NO
(6)
Zona de Reação
SO2
Refluxador principal
H2SO4
Sub-Produto
Figura
1.
Diagrama Das Principais Unidades
Operacionais, e as Principais Reações no
Sistema HNO3/NO. [2], [5], [6].
Preparo da Amostra: O ácido nítrico é reduzido a
nitrogênio molecular sob temperatura (350oC) e em
presença de cobre metálico. A análise do 15N é feita por
espectrometria de massa [5]. O sistema de preparo e a
análise fornecem um desvio padrão de 0,3%, para
amostras de concentração da ordem de 5 átomos% 15N.
III. RESULTADOS E DISCUSSÃO
Mantendo-se o sistema HNO3/NO em equilíbrio
dinâmico, realizou-se três experimentos. No primeiro
experimento, o equilíbrio dinâmico foi mantido durante
o período de vinte e dois dias consecutivos em regime de
vinte e quatro horas, sendo que, durante o período
inicial dos nove primeiros dias, o sistema HNO3/NO
apresentou-se em fase de enriquecimento. No patamar
de equilíbrio isotópico característico, (5,188 ± 0,161)
átomo% 15N, alcançado durante sete dias consecutivos,
consecutivos, retirou-se 10 cm3 de ácido nítrico diários.
Após esta fase, o sistema entrou em novo equilíbrio
isotópico (1,057 ± 0,056) átomo% 15N, durante o período
de três dias consecutivos, no qual retirou-se 20 cm3 de
ácido nítrico diários.
No terceiro experimento, manteve-se o sistema
HNO3/NO sob equilíbrio dinâmico durante o período de
vinte e nove dias. Repetiu-se a sistemática de retirada
para as coletas de 5, 10 e 15 cm3 de ácido nítrico diários,
correspondentes aos patamares de equilíbrio isotópico de
(2,606 ± 0,029) átomo% 15N (três dias consecutivos);
(1,833 ± 0,039) átomo% 15N (nove dias consecutivos);
(1,489 ± 0,029) átomo % 15N (sete dias consecutivos),
respectivamente, com a ressalva de que, coletava-se,
lentamente, a metade do volume na parte da manhã, e a
outra metade na parte da tarde, obedecendo a um intervalo
mínimo de nove horas entre as duas coletas da amostra
considerada.
Neste terceiro experimento, acoplou-se o
Refluxador Secundário no topo da Coluna de Troca
Isotópica, para regenerar os óxidos de nitrogênio a ácido
nítrico.
Os dados destes experimentos estão mostrados
na Tabela 1.
Através da Tabela I, percebe-se que a Coluna de
troca isotópica empregada, permite enriquecer o ácido
nítrico de concentração (0,369 ± 0,001) a (5,188 ± 0,161)
átomo% de 15N. De forma simples e prática, é possível
coletá-lo pelo uso do sistema de dreno, utilizado no
Refluxador Principal.
Nota-se, também, que a concentração de ácido
nítrico enriquecido em nitrogênio-15 é da mesma ordem
de grandeza das obtidas pelas colunas de enriquecimento
citadas na Tabela 2.
Devido ao grande número de placas teóricas (s)
requeridas para aumentar a concentração em átomo% de
15
N, torna-se importante o tipo de enchimento
empregado, que resulte em um pequeno valor para a
altura equivalente de uma placa teórica (HETP).
Utilizando-se destes parâmetros como elementos
comparativos, percebe-se, da Tabela 2, que o tipo de
enchimento utilizado, Espiral de Gauze, apresenta uma
pequena desvantagem em relação ao enchimento
Helipack ≠ 3013.
O uso do Refluxador Secundário permite a
reutilização dos óxidos de nitrogênio liberados no topo
da coluna principal, os quais foram regenerados na
forma de ácido nítrico como sub-produto. Alguns
resultados do terceiro experimento estão mostrados na
Tabela 1.
A determinação simultânea do número de placas
teóricas (s) da Coluna de Troca Isotópica e do fator de
fracionamento (α) do sistema HNO3/NO foi efetuada
através da função s = f (α, No, Np, P, L), por método
gráfico[4].
Nesta função, No e Np referem-se à
concentração média de 15N, no ácido nítrico da
alimentação e do produto, respectivamente. L e P
referem-se às vazões médias da mistura isotópica no
ácido nítrico da alimentação e do produto,
respectivamente, em mol de nitrogênio por unidade de
tempo.
Tomando-se a amostragem na base da coluna,
os valores médios dos três experimentos realizados
forneceram os seguintes valores
na temperatura
ambiente: s = 45,3 ± 7,1 e α = 1,062 ± 0,001.
Por outro lado, utilizando-se os valores médios
nos equilíbrios isotópicos dinâmicos, em átomo% de 15N
de ácido nítrico da alimentação e de ácido nítrico subproduto obtido no Refluxador Secundário, Tabela 1, e
pela própria definição de fator de fracionamento[8] α =
[(N/1 - N) fase líquida] / [(n/1 - n) fase gasosa] obtém-se
o valor de α = 1,065 ± 0,004, ou seja, ao longo da
Coluna de Troca Isotópica, entre o ponto de retirada e o
ponto de alimentação, o fator de fracionamento do
sistema HNO3/NO mantém-se praticamente constante em
cada placa teórica, durante o equilíbrio isotópico
dinâmico.
Estes valores indicam que, no equilíbrio
isotópico dinâmico, as concentrações em átomo% de 15N
entre as fases gasosa e líquida diferem uma da outra,
sendo levemente maior na fase líquida.
Neste sentido, visando à construção de um
segundo estágio de contracorrente, para um maior
enriquecimento de 15N no ácido nítrico, e tomando-se,
como parâmetro, as concentrações das fases líquida e
gasosa, torna-se indiferente utilizar-se o ácido nítrico
enriquecido, na fase líquida, ou os óxidos de nitrogênio
na fase gasosa, como substâncias primárias, para a
alimentação do segundo estágio.
[6] Spindel, W., Taylor, T.I. Separation of nitrogen
isotopes by chemical exchange betwen NO and
HNO3.. J. Chem. Phys. 23: 981-982, 1955.
[7] Abrudean, M., Axente, D., Bâldea, S. Enrichment
of 15N and 18O by chemical exchange reaction between
nitrogen oxides (NO, NO2) and aqueous nitric acid.
Isotopenpraxis, 17 (1): 377-382, 1981.
[8] Ducatti., Matsui, E. Fundamentos Teóricos da
Separação Isotópica em coluna de contracorrente.
Piracicaba, CENA, 1988. 37p. (BT - 011).
ABSTRACT
IV. CONCLUSÕES
Foi possível enriquecer o ácido nítrico de
concentração (0,369 ± 0,001) a (5,188 ± 0,161) átomo%
15
N, nas condições de trabalho empregadas na Coluna de
Troca Isotópica. De forma simples e prática, torna-se
possível coletar o ácido nítrico produto, através do
sistema de dreno e registro de teflon utilizados
AGRADECIMENTOS
À Fundação Banco do Brasil, Processo no 10/443421FBB,pelo apoio recebido, e à secretária, Srta. Silvia
Helena Ramos, pelos serviços prestados.
REFERÊNCIAS
[1] Krell, E. Zur entwicklung der 15N - Production in
der DDR. Isotopenpraxis, 12(5): 188-193, 1976.
[2] Taylor, T.I., Spindel, W. Preparation of highy
enriched nitrogen - 15 by chemical exchange of NO
with HNO3. In: Symposium on isotope separation.
Amsterdan, 1957. Cap. 10, p. 158-177. Proceedings
[3] Johns, T.F. Chemical Exchange. In: London, H., ed.
Separation of isotopes. London, George Newnes, 1961.
cap. 5. pg. 95-100.
[4] Krell E., Jonas, C. Industrial plants for production
of highly enriched nitrogen - 15. In: IAEA. Stable
Isotopes in the Life Sciences, Vienna, IAEA, 1977, p.5968.
[5] Ducatti, C. Análise teórica e experimental do
enriquecimento isotópico de nitrogênio-15, do sistema
monóxido de nitrogênio e ácido nítrico. São Carlos,
1985. 188p. (Doutorado - Instituto de Física e Química
de São Carlos/USP.
In this paper is described the operational mode of
countercurrent column of aqueous nitric acid and
nitrogen oxides (Nitrox System) for the production of
nitric acid in the concentration of 5% atoms of 15N in
laboratory.