Resumo – Fisiologia (Neuro)
Barbra Rafaela XLI
Cap. 5 – Potenciais de Membrana e Potencial de Ação
A concentração de K é maior do lado interno da membrana da fibra nervosa, existindo
uma tendência para que este se difunda para fora (considerando a membrana permeável
só a esse único íon); quando o faz, cria eletropositividade do lado externo da membrana
(carrega íons +).
O potencial de difusão (diferença de potencial entre as partes interna e externa), em
cerca de um milissegundo, torna-se grande o suficiente (−94 milivolts nos mamíferos) e
bloqueia a difusão do K.
O mesmo fenômeno ocorre com o Na, no entanto, o mesmo encontra-se concentrado do
lado externo da membrana e tem um potencial de difusão de +61 mV.
Conclusão: as diferenças entre as concentrações iônicas nos dois lados de uma membrana
seletivamente permeável, podem criar um potencial de membrana.
Potencial de Nernst: nível do potencial de difusão em toda a membrana que se opõe
exatamente ao da difusão efetiva de um íon particular através da membrana;
determinado pela proporção entre as concentrações desse íon nos dois lados da
membrana.
EMF (milivolts) = + 61 log Concentração interna
Concentração externa
EMF: força eletromotiva
(+) se o íon (difundindo-se de dentro para fora) for negativo
(−) se for positivo
Quanto maior a proporção, maior a tendência para que o íon se difunda e, com isso,
maior deve ser o potencial de Nernst para evitar uma difusão efetiva adicional.
O potencial elétrico medido no lado externo da membrana é zero (potencial do líquido
extracelular); na camada do dipolo elétrico (área de variação da voltagem na membrana
celular), o potencial passa para −90 mV.
Um número ínfimo de íons precisa ser transferido através da membrana para estabelecer
o potencial de repouso (−90 mV) ou inverter o potencial para o máximo (+35 mV); essa
alternância de íos causa os sinais nervosos.
O potencial dentro da fibra é 90 mV mais negativo do que o potencial no líquido
extracelular, do lado de fora.
A bomba de Na+-K+ é eletrogênica, pois, mais cargas positivas são bombeadas para fora
que para dentro (3 Na+ saem/2 K+ entram), deixando um déficit de íons positivos na parte
de dentro (gera potencial negativo dentro).
Os íons atravessam a membrana nervosa através de canais protéicos (canais de
extravasamento de potássio-sódio), que são muito mais permeáveis ao K que ao Na (100
vezes mais).
Se o único movimento de íons através da membrana fosse o de K, este geraria um
potencial de repouso de −94 mV; se o mesmo ocorresse com o Na, o potencial seria de
+61 mV; a interação entre os dois, gera um potencial de −86 mV e, com a interação da
bomba, que gera um grau adicional de negatividade do lado interno de −4 mV, é
produzido o potencial de membrana efetivo de −90 mV.
Potenciais de ação: rápidas alterações do potencial de membrana que se propagam com
grande velocidade por toda a membrana da fibra nervosa, transmitindo os sinais
nervosos. Apresenta estágios sucessivos:
Estágio de Repouso: potencial de repouso da membrana, antes do início do potencial
de ação (membrana polarizada - −90 mV).
1
Estágio de Despolarização: a membrana fica permeável aos íons Na, os quais se
difundem para o interior do axônio (membrana despolarizada - potencial + nas fibras
de maior calibre (overshoot) e próximo a zero nas delgadas).
Estágio de Repolarização: os canais de Na se fecham e os de K se abrem muito,
levando a uma rápida difusão de íons K para o exterior (membrana repolarizada –
potencial de repouso negativo).
Juntamente com a bomba e os canais de extravasamento, atuam os canais de Na e K
regulados pela voltagem; nesse sentido, o canal de Na é o principal agente na
repolarização e despolarização das membranas durante o potencial de ação.
O canal de Na tem duas comportas: de ativação (perto da abertura externa) e de
inativação (perto da abertura interna); quando o potencial aumenta (se torna menos
negativo), o canal se abre (estado ativado) e se fecha pouquíssimo tempo depois (estado
inativado), abrindo-se novamente só após a repolarização da fibra.
O canal de K permanece fechado no estado de repouso e se abre quando o potencial de
membrana aumenta; devido a um pequeno retardo, eles se abrem ao mesmo tempo em
que os canais de Na estão se fechando, acelerando o processo de repolarização.
A tetrodotoxina, aplicada na parte externa da membrana celular, bloqueia os canais de Na
e o íon tetraetilamônio, quando aplicado no interior da fibra, bloqueia os canais de K.
A variação da condutância mostra a abertura abrupta dos canais de Na (que se fecham
automaticamente) e lenta dos de K (que permanecem abertos durante todo o potencial).
Outros íons, além de Na e K, participam da geração de potencial, como os ânions
negativos, responsáveis pela carga negativa dentro da fibra, quando existe déficit de íons
positivos, e os íons Cálcio, que apresentam uma bomba, semelhante à de Na, que
transfere os íons para o exterior da membrana; além disso, existem canais de Ca
regulados por voltagem que são ligeiramente permeáveis aos íons Na (canais de Ca++-Na+
).
Os canais de Ca são canais lentos (muito numerosos nos músculos cardíaco e liso) e
necessitam de muito mais tempo para serem ativados que os canais de Na, que são
canais rápidos.
Quando existe déficit de íons Ca, os canais de Na são abertos por pequeno aumento do
potencial de membrana; devido a isso, a fibra nervosa fica muito excitável, descarregando
repetidamente sem qualquer estímulo, o que pode levar a uma tetania muscular (pode ser
letal, se afetar os músculos respiratórios).
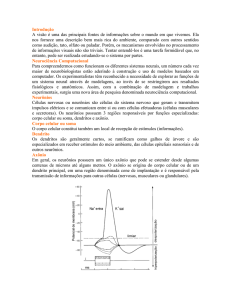
Qualquer evento capaz de provocar um aumento inicial do potencial de membrana (de
−90 a zero), leva à abertura de vários canais de Na provocada pela própria alteração da
voltagem; o influxo rápido de íons Na aumenta o potencial de membrana, abrindo mais
canais regulados por voltagem e permitindo a entrada de mais íons (círculo vicioso de
feedback positivo).
O potencial de ação só ocorre quando o número de íons Na que entra na fibra fica maior
que o número de íons K que saem, sendo −65 mV o limiar para a estimulação.
Um potencial de ação provocado em qualquer parte de uma membrana excitável (porção
adjacente ou central) resulta num potencial propagado por toda a membrana (impulso
nervoso ou muscular).
O potencial de ação se propaga para todos os trafega em todas as direções para longe do
estímulo, não tendo direção única.
Princípio do Tudo ou Nada: se as condições forem adequadas o processo de
despolarização trafega por toda a membrana, após a geração do potencial de ação; se
não, não se propaga de maneira nenhuma.
Fator de segurança: para que ocorra propagação contínua de um impulso, a proporção
entre o potencial de ação e o limiar de excitação deve ser sempre maior que 1.
O restabelecimento das concentrações de Na e K na fibra é realizado pela bomba Na +-K
membrana se ATPase, que tem sua atividade estimulada pelo acúmulo de Na no interior
da fibra muscular, consumindo energia (produzindo calor) a medida que a freqüência dos
impulsos aumenta.
2
No músculo cardíaco pode ocorrer uma demora na repolarização da fibra, o que forma um
platô perto do pico do potencial; isso pode ocorrer devido à morosidade na abertura dos
canais lentos de Ca ou mesmo dos do K.
Descargas repetitivas espontâneas são importantes em processos como o do batimento
ritmado do coração, peristaltismo rítmico dos intestinos e controle ritmado da respiração,
sendo que quase todos os tecidos excitáveis podem sofrer esse processo se limiar de
excitabilidade dos tecidos for reduzido (fibras estáveis como as nervosas e musculares
esqueléticas o fazem quando colocadas em solução contendo veratrina ou quando a
concentração de Ca cai muito – aumento da permeabilidade da membrana ao Na).
Se a membrana for bastante permeável aos íons Na (ou Ca), não apresentará voltagem
negativa suficiente para manter os canais totalmente fechados; dessa forma, íons Na e Ca
fluem para dentro, aumentando ainda mais a permeabilidade da membrana, gerando o
potencial de ação e a repolarização da membrana; após um mínimo retardo, a
excitabilidade espontânea causa nova despolarização e um novo potencial (ciclo – leva à
excitação rítmica).
Próximo ao término de cada potencial de ação, a membrana torna-se muito permeável ao
K, deixando o interior da fibra muito negativo, o que leva a uma hiperpolarização da
membrana; quando esse estado desaparece, novo potencial de ação é desencadeado.
As fibras nervosas calibrosas são mielinizadas e as mais delgadas são amielinizadas, as
quais constituem a maioria nos troncos nervosos.
Uma fibra mielinizada típica contém: axônio (cerne central da fibra), cuja membrana
conduz o potencial de ação; axoplasma (preenche o axônio na parte central); bainha de
mielina (em volta do axônio); nodo de Ranvier (a cada 1 a 3 mm de bainha); células de
Schwann (depositam a bainha de mielina em torno do axônio); esfingomielina (substância
isolante elétrica das células de Schwann).
Já que os íons não podem fluir através da bainha de mielina, eles passam através dos
nodos de Ranvier (áreas não isoladas), gerando potenciais de ação transmitidos por
condução saltatória.
Essa condução, além de ser bem mais rápida, conserva energia para o axônio, pois,
somente os nodos se despolarizam e, ainda reduz a capacitância da membrana, o que
permite que a repolarização ocorra com transferência muito pequena de íons.
Qualquer fator que promova a entrada de Na na célula, pode provocar a abertura desses
canais, como: distúrbio mecânico (pressão que excita terminações sensoriais nervosas na
pele), efeitos químicos (neurotransmissores que transmitem sinais de um neurônio a
outro) e passagem de eletricidade (transmissão de sinais entre as sucessivas células do
coração).
Em laboratório, um nervo ou músculo é excitado por eletrodos, cuja corrente negativa
diminui a voltagem fora da membrana, até um valor próximo ao potencial de dentro,
permitindo a abertura dos canais de Na e resultando num potencial de ação.
Estímulos fracos podem não desencadear potenciais de ação, mas, provocam alterações
locais do potencial da membrana (potenciais locais agudos); o potencial só será
efetivamente produzido quando o potencial local atingir o nível limiar necessário.
Período refratário absoluto: período durante o qual um segundo potencial de ação não
pode ser produzido, enquanto a membrana ainda estiver despolarizada (os canais de Na
e/ou Ca estão inativos).
Existem substâncias capazes de diminuir a excitabilidade nervosa (fatores estabilizadores
da membrana), como íons Ca (sua alta concentração no líquido extracelular diminui a
permeabilidade para o Na) e os anestésicos locais (procaína e tetracaína – atuam
dificultando a abertura dos canais de Na, até que a excitabilidade da membrana diminua a
tal ponto que o fator de segurança seja menor do que 1).
Cap. 6 – Contração do Músculo Esquelético
O corpo é composto em 40% por músculo esquelético, composto por inúmeras fibras,
sendo cada uma delas formada por subunidades ainda menores.
3
A composição das fibras musculares inclui:
Sarcolema: membrana celular da fibra muscular; constituído por uma membrana
plasmática e um revestimento de material polissacarídeo contendo delgadas fibrilas
colágenas, que, na extremidade da fibra, fundem-se com uma fibra de tendão, a qual,
por sua vez, se agrupa em feixes, formando os tendões, que vão se inserir nos ossos.
Miofibrilas (actina/miosina): existem centenas de miofibrilas em cada fibra muscular,
sendo que cada uma delas é formada 1500 filamentos de miosina e 1300 filamentos de
actina (proteínas responsáveis pela contração muscular; a actina constitui filamentos
em faixas claras, chamados de faixa I (isotrópicas à luz polarizada), já a miosina
constitui filamentos em faixas escuras, chamadas de faixas A (anisotrópicas à luz
polarizada); projeções laterais dos filamentos de miosina (pontes cruzadas) interagem
com os filamentos de actina causando as contrações; do chamado disco Z (composto
por proteínas e que cruza as miofibrilas, conectando-as), os filamentos de actina se
estendem e se interdigitam com os filamentos de miosina; o segmento da miofibrila
(ou da fibra) entre dois discos Z é chamado sarcômero.
Sarcoplasma: líquido intracelular que preenche os espaços entre as miofibrilas e
contem grande quantidade de K, Mg, fosfato, enzimas protéicas e mitocôndrias.
Retículo Sarcoplasmático: contem uma organização especial para o controle da
contração muscular e circunda as miofibrilas de cada fibra muscular.
Os filamentos de actina e miosina são mantidos lado a lado por moléculas filamentares de
uma proteína chamada titina, cuja flexibilidade atua como arcabouço que mantém os
filamentos em seus lugares.
A contração muscular apresenta as seguintes etapas:
1. Os potencias de ação vão pelo nervo motor, até às terminações nas fibras musculares;
2. O nervo secreta acetilcolina em cada terminação;
3. A acetilcolina age na membrana abrindo canais regulados por ela;
4. Íons Na se difundem para o interior da membrana, desencadeando o potencial de
ação;
5. O potencial de ação se propaga pela membrana da fibra muscular (tal como no nervo);
6. O potencial despolariza a membrana e sua eletricidade flui pelo centro da fibra
muscular, fazendo com que o retículo sarcoplasmático libere muitos íons Ca;
7. Os íons Ca provocam atração entre os filamentos de actina e miosina, que deslizam
um ao lado do outro (processo contrátil);
8. Os íons de Ca são bombeados de volta ao retículo (bomba de Ca) e a contração cessa.
Quando os íons Ca são liberados, ativam as forças entre os filamentos, geradas pela
interação das pontes cruzadas, fazendo com que a contração se inicie e se mantenha pelo
fornecimento de energia da quebra das moléculas de ATP.
Os filamentos de actina são formados por 3 componentes protéicos:
Actina
Tropomiosina: recobrem os locais ativos do filamento de actina, durante o repouso,
impedindo a contração.
Troponina: tem 3 subunidades – TI (afinidade com actina), TT (afinidade com
tropomiosina) e TC (afinidade com íons Ca), cuja interação com o Ca, provavelmente,
desencadeia o processo de contração.
Os íons Ca se ligam à TC alternado sua conformação pelo deslocamento das moléculas de
tropomiosina, deixando os locais ativos da actina descobertos (permitindo a atração das
pontes cruzadas e, com isso, a contração) – mecanismo hipotético.
No memento em que não existe sobreposição dos filamentos de actina e miosina, a
tensão desenvolvida pelo músculo é nula; a medida que o sarcômero encurta e os
filamentos começam a se sobrepor, a tensão aumenta progressivamente.
O músculo em repouso se contrai com força máxima quando ativado, no entanto, o
aumento dessa tensão ativa durante a contração diminui com o estiramento do músculo
além de seu comprimento normal.
4
Quando é aplicada uma carga ao músculo, a velocidade da contração fica cada vez menor
à medida que a carga aumenta; se a carga for igual à força máxima que o músculo pode
exercer, a velocidade de contração é zero.
A energia para a contração muscular vem da quebra das moléculas de ATP em ADP; o ATP
é reconstituído no próprio músculo, através de algumas fontes, como (em ordem de uso):
fosfocreatina, glicogênio e metabolismo oxidativo.
A quantidade de energia fornecida ao músculo (vinda dos nutrientes), que pode ser
convertida em trabalho é de, no máximo, 25%, sendo o restante transformado em calor;
a metade da energia dos nutrientes é perdida na formação do ATP e a maioria dela não
poderá ser convertida em trabalho.
Quanto aos tipos de contração muscular, tem-se a isométrica (quando o músculo não
encurta durante a contração) e a isotônica (quando encurta mas sua tensão permanece
constante por toda a contração.
A contração muscular varia de acordo com o tamanho e a função do músculo, por
exemplo: músculo ocular (1/40 segundo – movimentos rápidos), m. gastrocnêmio (1/15
s. – velocidade moderadamente alta) e m. sóleo (1/3 s. – contração lenta).
Os músculos que reagem rapidamente são compostos, em sua maior parte, por fibras
rápidas (grandes; retículo sarcoplasmático extenso; muitas enzimas glicolíticas; menor
suprimento sanguíneo; menor número de mitocôndrias) e os músculos que respondem
lentamente, com contração prolongada, tem mais fibras lentas (menores; fibras nervosas
pequenas; maior suprimento sanguíneo; muitas mitocôndrias; muita mioglobina – que
confere a cor e o nome a esse músculo de músculo vermelho, tal como o músculo rápido,
chamado músculo branco).
Unidade Motora: formada por todas as fibras musculares inervadas por uma só fibra
nervosa.
Cada motoneurônio que sai da medula espinhal inerva múltiplas fibras musculares, sendo
que a quantidade de fibras depende do tipo do músculo: músculos pequenos, de reação
rápida, tem mais fibras nervosas que musculares (laringe); grandes músculos, que não
precisam de controle fino, tem muitas fibras musculares para uma única unidade motora
(sóleo).
Somação: soma das contrações individuais para aumentar a intensidade da contração
total; pode ocorrer por dois meios:
1. Somação por Fibras Múltiplas: pelo aumento do número de unidades motoras que se
contraem ao mesmo tempo.
2. Somação por Freqüência e Tetanização: pelo aumento da freqüência de contração, que
pode levar à tetanização.
Quando um músculo começa a se contrair, a partir do repouso, sua força é pequena, mas,
vai aumentando até atingir um platô (efeito de escada ou treppe); acredita-se que isso
seja causado pelo aumento de Ca no citosol, devido à liberação intensa pelo retículo.
Tônus Muscular: tensão mantida no músculo em repouso, resultante da baixa freqüência
de impulsos nervosos da medula espinhal.
Fadiga Muscular: incapacidade contrátil provocada por contrações musculares fortes (por
tempo prolongado) que levam à depleção do glicogênio muscular.
Todos os movimentos do corpo são causados por contrações simultâneas dos músculos
agonistas e antagonistas nos lados opostos da articulação (coativação).
Hipertrofia Muscular: quando a massa muscular total aumenta, como resultado do
aumento do número dos filamentos de actina e miosina em cada fibra muscular; quando o
músculo trabalha contra uma carga num processo contrátil, a intensidade das fibras
contráteis no músculo é bem maior; do contrário, quando a massa muscular diminui
(redução das proteínas contráteis) o processo é chamado atrofia muscular.
Quando os músculos são estirados excessivamente, novos sarcômeros são adicionados às
extremidades das fibras musculares, podendo desaparecer no caso contrário, quando o
músculo permanece continuamente encurtado.
Hiperplasia da Fibra: rara condição (geração de força muscular extrema) em que o
número de fibras musculares aumenta.
5
Um músculo privado de seu suprimento nervoso deixa de receber sinais contráteis
necessários para manter suas dimensões normais; nesse caso, o processo de atrofia se
desenvolve rapidamente levando a mudanças degenerativas e, com o tempo, e à
destruição das fibras musculares, substituídas por tecido fibroso e gorduroso.
Contratura: tendência do tecido fibroso, formado na desnervação, de se encurtar
progressivamente, o que pode provocar debilidades e deformidades.
Na poliomielite, com a destruição de muitas fibras nervosas, as fibras remanescentes se
ramificam para formar novos axônios, que vão inervar muitas fibras musculares
paralisadas; as unidades motoras formadas são chamadas unidades macromotoras (não
oferecem a eficiência do controle muscular, mas, permite os movimentos voluntários).
Rigidez Cadavérica: estado de contratura em que o corpo entra algumas horas após a
morte, resultante da perda de ATP, necessário para a separação das pontes cruzadas dos
filamentos, no relaxamento; a rigidez desaparece quando as proteínas musculares
degeneram, devido à autólise pelas enzimas lisossômicas.
Cap. 7 – Excitação do Músculo Esquelético: Transmissão Neuromuscular e
Acoplamento Excitação-Contração
Grandes fibras nervosas mielinizadas que se originam nos grandes neurônios motores
(cornos anteriores da medula espinhal), inervam as fibras musculares esqueléticas.
Junção Neuromuscular: junção da terminação nervosa com a fibra muscular, em sua
porção média (quase sempre uma por fibra – exceto em 2% das fibras musculares);
através da micrografia eletrônica, podem ser vistos:
Goteira Sináptica (canaleta sináptica): membrana invaginada.
Fenda Sináptica (espaço sináptico): espaço entre o terminal e a membrana da fibra.
Fendas Subneurais: pequenas e numerosas dobras da membrana muscular, que
aumentam a área de superfície na qual o transmissor sináptico pode agir.
Placa Motora: complexo de terminais nervosos ramificados da fibra nervosa, que se
invaginam na superfície extracelular da fibra muscular; a estrutura é recoberta por uma
ou mais células de Schwann que a isolam dos líquidos circunjacentes.
Mitocôndrias, no terminal axonal, fornecem ATP para a síntese de acetilcolina, transmissor
excitatório que excita a membrana da fibra muscular, sendo sintetizada no citoplasma do
terminal, absorvida por vesículas sinápticas e, rapidamente, destruída pela enzima
acetilcolinesterase, no espaço sináptico.
Cada impulso nervoso que atinge a junção neuromuscular libera cerca de 125 vesículas de
acetilcolina dos terminais no espaço sináptico.
Canais de cálcio controlados por voltagem: partículas protéicas que penetram na
membrana neural (de cada lado de uma barra densa).
O potencial de ação que se propaga para o terminal abre os canais e permite que os íons
cálcio se difundam do espaço sináptico para o interior do terminal nervoso.
Os íons Ca atraem as vesículas de acetilcolina, puxando-as para a membrana neural
adjacente às barras densas; onde se fundem com a membrana e esvaziam a acetilcolina
no espaço sináptico (exocitose).
Canais iônicos controlados pela acetilcolina: receptores de acetilcolina na membrana da
fibra muscular, próximos às aberturas das fendas subneurais (abaixo das áreas de barras
densas); são moléculas protéicas que formam um canal tubular, que se abre após a
ligação de duas moléculas de acetilcolina ao mesmo, permitindo a passagem de íons
positivos (Na, K, Ca), porém impedindo a passagem de íons negativos (cloreto) por
repulsão.
Potencial de Placa Motora: alteração potencial local positiva no interior da membrana da
fibra muscular provocada pela entrada, através dos canais colinérgicos, de Na, o qual leva
com ele muitas cargas positivas; esse potencial deflagra o potencial de ação, que se
propaga pela membrana muscular, causando a contração.
6
A acetilcolina é removida do espaço sináptico de duas maneiras: destruída pela
acetilcolinesterase e difundindo-se para fora do espaço sináptico, excitando a fibra
muscular; a rápida remoção impede que a acetilcolina reexcite o músculo enquanto este
se recupera de seu potencial de ação inicial.
Alguns potenciais de placa motora são muito fracos para desencadear um potencial de
ação, produzindo fracas alterações locais de voltagem; essa baixa amplitude do potencial
pode ser causada por venenos como:
Curare: droga que bloqueia o efeito controlador da acetilcolina sobre os canais
colinérgicos competindo pelos receptores da mesma.
- Drogas curariformes: impedem a passagem dos impulsos da terminação nervosa para
o músculo (D-tubocurarina: bloqueia a ação da acetilcolina nos receptores da fibra,
evitando um aumento na permeabilidade dos canais de membrana muscular suficiente
para iniciar o potencial de ação.
Toxina Botulínica: veneno bacteriano que diminui a quantidade de acetilcolina liberada
pelos terminais nervosos.
Cada impulso que chega à junção neuromuscular provoca um potencial de ação três vezes
maior que o necessário para estimular a fibra musular (fator de segurança), no entanto,
com a diminuição das vesículas de acetilcolina, os impulsos não são mais transmitidos
(fadiga da junção neuromuscular).
A formação e a liberação da acetilcolina seguem as seguintes etapas:
1. Pequenas vesículas são formadas pelo aparelho de Golgi, no corpo celular do neurônio
motor (medula espinhal), e transportadas, pelo axoplasma, através do núcleo do
axônio, desde o corpo celular até a junção neuromuscular (terminações das fibras
nervosas periféricas).
2. A acetilcolina é sintetizada no citosol do terminal da fibra nervosa e armazenada nas
vesículas (10.000 moléculas em cada vesícula).
3. O potencial que chega ao terminal nervoso abre canais de Ca na membrana, fazendo
com que a concentração desse íon aumente a fusão das vesículas, liberando
acetilcolina no espaço sináptico, que é posteriormente clivada (íon acatato + colina) e
reabsorvida pelo terminal neural (para formar novas moléculas).
4. Após cada potencial ter terminado pequenas invaginações aparecem na membrana do
terminal nervoso (ação da proteína contrátil clatrina) e se transformam em novas
vesículas.
Substâncias como a metacolina, o carbacol e a nicotina tem o mesmo efeito que a
acetilcolina sobre o músculo, mas são destruídas lentamente (não pela colinesterase),
prolongando sua ação e, consequentemente, gerando vários potenciais de ação que
podem levar a um espasmo muscular.
Drogas conhecidas inativam a acetilcolinesterase nas sinapses e esta não mais hidrolisa
acetilcolina, fazendo com que, a cada impulso nervoso, ela se acumule mais na fibra
muscular, causando espasmo; são elas:
Neoestigmina e Fisoestigmina: combinam-se à acetilcolinesterase, inativando-a por até
várias horas.
Fluorofosfato de diisopropil: gás venenoso para os nervos, inativando a
acetilcolinesterase por semanas (letal).
Miastenia Gravis: causa paralisia muscular devido a incapacidade de as junções
neuromusculares transmitirem sinais suficientes das fibras nervosas para as fibras
musculares (os potenciais de placa motora que ocorrem nas fibras musculares sçao muito
fracos para estimulá-las); acredita-se que seja uma doença auto-imune (imunidade contra
os próprios canais iônicos colinérgicos); pode ser melhorada por várias horas de
administração de neostigmina (ou de outras droga anticolinesterásica), que provoca um
acúmulo de acetilcolina no espaço sináptico.
Diferenças quantitativas entre os potencias das fibras musculares em ralação às nervosas:
1. Potencial de repouso da membrana: de −80 a −90mV (igual às fibras mielinizadas).
2. Duração do potencial de ação: 1 a 5ms (5 vezes mais prolongado que nos nervos).
3. Velocidade de condução: 3 a 5m/s (1/13 das fibras mielinizadas).
7
Na fibra muscular esquelética a corrente tem que penetrar profundamente (até perto das
miofibrilas) para causar o máximo de contração muscular; os potenciais se propagam,
então, através dos túbulos transversos (túbulos T), que penetram a fibra muscular.
Os túbulos T são extensões internas da membrana celular, comunicando-se com o líquido
extracelular da fibra e tendo, eles mesmos, líquido em seus lumens; isso permite que o
potencial se propague, através deles, para o interior da fibra muscular.
Retículo Sarcoplasmático: composto pelas cisternas terminais, que fazem contato com os
túbulos T e pelos túbulos longitudinais, que circundam a superfície das miofibrilas; em seu
interior há um excesso de íons Ca, que são liberados pelo potencial de ação.
Nas paredes do retículo existe uma bomba de Ca que bombeia esses íons para longe das
miofibrilas (de volta aos túbulos sarcoplasmáticos).
Cap. 45 – Organização do Sistema Nervoso Central, Funções Básicas das
Sinapses e “Substâncias Neurotransmissoras”
Diferentes tipos de neurônios têm desde centenas até milhares de conexões sinápticas
aferentes, no entanto, o sinal eferente, do mesmo neurônio, trafega por um único axônio,
o qual possui ramificações distintas que se dirigem para outras regiões do sistema
nervoso ou da periferia do corpo.
O sinal, nas sinapses, em sua maioria, se propaga apenas na direção anterógrada (do
axônio de um neurônio precedente para os dendritos localizados em neurônios
subseqüentes).
Receptores sensoriais (visuais, auditivos, táteis, etc.) recebem os estímulos vindos do
corpo e transmitem essas informações ao sistema nervoso central, através dos nervos
periféricos, de onde são conduzidas para áreas sensoriais múltiplas localizadas na medula
espinhal, na formação reticular da medula oblonga, ponte e mesencéfalo, no cerebelo, no
tálamo e em áreas do córtex cerebral; cada área executa sua própria função, sendo as
regiões inferiores responsáveis pelas respostas musculares automáticas (estímulos
sensoriais) e as superiores pelos movimentos musculares complexos.
O SN controla as atividades do corpo através da contração dos músculos esqueléticos e da
musculatura lisa dos órgãos internos e da secreção de substâncias químicas pelas
glândulas; essas atividades são chamadas funções motoras e os músculos e glândulas
funcionam como efetores (executam as funções ditadas pelos sinais nervosos).
Uma das principais funções do SN é a de processar informações aferentes para que sejam
efetuadas respostas motoras e mentais apropriadas.
Quando uma informação sensorial importante excita nossa mente, ela é canalizada para
regiões integrativas e motoras do cérebro para provocar a resposta; a canalização e o
processamento da informação são chamados funções integrativas do SN.
Desta forma, não percebemos as partes do corpo que estão em contato com nossa
vestimenta (mais de 99% das informações sensoriais são descartadas pelo cérebro como
irrelevantes), mas, afastamos, imediatamente, a mão de um fogão quente.
A sinapse é o ponto de confluência entre um neurônio e outro e determina as direções em
que os sinais nervosos vão se distribuir através do SN.
A transmissão sináptica pode ser controlada por sinais facilitatórios e inibitórios vindos de
diferentes áreas do SN, algumas vezes abrindo as sinapses para a transmissão e outras
vezes fechando-as.
As sinapses executam uma ação seletiva, bloqueando sinais fracos e permitindo que sinais
fortes passem, ou amplificando sinais fracos e transmitindo-os a muitas direções.
Uma pequena parte das informações sensoriais provoca resposta motora imediata; a
maioria é armazenada no córtex cerebral (e uma parte no encéfalo e na medula) para
futuro controle das atividades motoras e uso em processos cognitivos; esse processo é
chamado de memória.
A memória é uma função, também, executada pelas sinapses, de forma que quanto mais
os sinais passam através dessas sinapses, mais elas se tornam capazes de transmitir o
mesmo sinal em outra oportunidade; é o processo da facilitação.
8
As informações armazenadas no sistema nervoso são processadas no cérebro sob a forma
de pensamento, sendo futuramente comparado com novas experiências sensoriais a fim
de ajudar na seleção de uma nova informação, transmiti-la à área apropriada e provocar
respostas.
Níveis principais do SNC possuem características funcionais específicas:
1. Nível da Medula Espinhal: circuitos neuronais intrínsecos da medula podem ser
responsáveis por movimentos de marcha, reflexos que afastam parte do corpo de
objetos que causam dor ou enrijecem as pernas para que sustentem o corpo contra a
gravidade ou mesmo que controlam os vasos sanguíneos locais, movimentos
gastrointestinais ou secreção urinária.
2. Nível Cerebral Inferior ou Subcortical: controla muitas das atividades subconscientes
do corpo, como pressão arterial e respiração (medula oblonga e ponte), equilíbrio
(cerebelo, bulbo, ponte, mesencéfalo), reflexos alimentares (m. oblonga, ponte,
mesencéfalo, amígdala e hipotálamo) e padrões emocionais.
3. Nível Cerebral Superior ou Cortical: essencial para a maior parte de nossos processos
do pensamento, porém não funciona sozinho, sendo as estruturas subcorticais as
responsáveis pela ativação das funções corticais.
Funções sinápticas dos neurônios: bloqueio da transmissão do impulso nervoso de um
neurônio a outro, transformação de um impulso único em impulsos repetitivos, integração
de impulsos vindos de outros neurônios para gerar padrões complexos em neurônios
sucessivos.
Tipos de sinapses:
Químicas: o primeiro neurônio secreta, no seu terminal, um neurotransmissor
(acetilcolina, norepinefrina, epinefrina, estamina, ácido gama-aminobutírico (GABA),
glicina, serotonina, glutamato) que irá atuar em proteínas receptoras presentes na
membrana do neurônio subseqüente, para promover excitação, inibição ou
sensibilidade.
Elétricas: caracterizadas por canais que conduzem eletricidade de uma célula para a
próxima, sendo as principais estruturas as junções comunicantes (gap), que permitem
o movimento livre de íons do interior de uma célula para outra.
Princípio da Condução Unidirecional: as sinapses químicas sempre transmitem os sinais
em uma única direção, a partir do neurônio pré-sináptico que secreta o neutransmissor
para o neurônio pós-sináptico, no qual o neurotransmissor age.
O mecanismo de condução unidirecional permite que os sinais sejam direcionados para
alvos específicos, diferentemente da condução por sinapses elétricas, que, geralmente,
transmitem os sinais em ambas as direções.
Um neurônio motor anterior típico (medula espinhal) é composto por três partes
principais: corpo celular ou soma (constitui a maior parte do neurônio), axônio (se
estende a partir do corpo celular e incorpora-se aos nervos periféricos) e dendritos
(projeções ramificadas do soma que se estendem à áreas adjacentes da medula).
Na superfície dos dendritos (maioria) e do corpo celular encontram-se milhares de botões
sinápticos chamados terminais pré-sinápticos, que são as porções terminais de
ramificações de axônios de diversos outros neurônios (podem ser excitatórios ou
inibitórios).
Os neurônios apresentam diferenças de acordo com as partes do SN em que estão
presentes, como: comprimento de dendritos e axônios e número de terminais.
Terminais pós-sinápticos podem ser chamados botões terminais, pés terminais ou botões
sinápticos, devido à sua forma, sendo separados do neurônio pós-sináptico pela fenda
sináptica e possuindo estruturas importantes como as mitocôndrias e as vesículas
transmissoras (contém a substância transmissora, que pode excitar ou inibir o neurônio,
dependendo do tipo de receptor encontrado).
O potencial de ação que chega ao terminal pré-sináptico e despolariza a membrana, que
faz com que as vesículas liberem neurotransmissores na fenda, alterando a
permeabilidade da membrana neuronal pós-sináptica e, consequentemente, excitando ou
inibindo neurônio pós-sináptico.
9
A membrana pré-sináptica possui um grande número de canais de Ca dependentes de
voltagem, os quais se abrem e permitem a passagem desses íons para dentro do terminal
pré-sináptico, quando um potencial despolariza a membrana, liberando substância
transmissora na fenda.
Os íons Ca que entram se ligam a moléculas de proteínas da superfície interna da
membrana pré-sináptica, chamadas sítios de liberação, que se abrem e permitem a
liberação de neurotransmissores pelas vesículas.
A membrana do neurônio pós-sináptico contem proteínas receptoras, cujas moléculas tem
dois componentes importantes:
Componente de ligação: se exterioriza a partir da membrana, na fenda, se ligando ao
neutransmissor vindo do terminal pré-sináptico.
Componente ionóforo: atravessa a membrana pós-sináptica até alcançar o interior do
neurônio pós-sináptico; pode ser de dois tipos:
1. Canal iônico: permite a passagem de íons específicos pela membrana; são
geralmente catiônicos (revestidos com cargas negativas, permitindo a passagem de
Na e, as vezes, K e/ou Ca) e aniônicos (cloreto e outros); esses canais se fecham
rapidamente, sendo incapazes de provocar mudanças prolongadas no neurônio.
2. Ativador de Segundo Mensageiro: molécula que se projeta para o citoplasma da
célula, ativando substâncias no interior do neurônio pós-sináptico, sendo essas
substâncias responsáveis por provocar efeitos prolongados no neurônio; um dos
tipos mais comuns de segundos mensageiros utiliza a proteína G, que pode
provocar abertura de canais iônicos específicos na membrana da célula póssináptica, ativação de AMPc ou GMPc na célula neuronal, ativação de uma ou mais
enzimas extracelulares ou da transcrição gênica.
Os diferentes mecanismos utilizados por receptores para induzir excitação ou inibição são:
Excitação:
1. Abertura dos canais de Na, permitindo o fluxo de um grande número de cargas
elétricas positivas para o interior da célula pós-sináptica: aumenta o potencial
intracelular da membrana no sentido de atingir o limiar para a excitação.
2. Condução reduzida através dos canais de cloreto e/ou potássio: torna o potencial
interno da membrana mais positivo que o normal.
3. Mudanças no metabolismo interno do neurônio pós-sináptico: excitam a atividade
celular, aumentam o número de receptores excitatórios e diminuem os inibitórios.
Inibição:
1. Abertura de canais de íon cloreto na membrana neuronal pós-sináptica: difusão de
cargas negativas para o interior do neurônio, causando inibição.
2. Aumento na condutância de íons K para fora dos neurônios: íons positivos se
difundem para o meio extracelular, aumentando a negatividade interna.
3. Ativação de enzimas receptoras: inibem as funções metabólicas celulares,
aumentando os receptores sinápticos inibitórios ou diminuindo os excitatório.
Muitas substâncias atuam como transmissores sinápticos, divididas em dois grupos:
1. Neurotransmissores de moléculas pequenas e de ação rápida: induzem respostas
mais agudas do SN, como a transmissão de sinais sensoriais para o encéfalo e dos
sinais motores do encéfalo para os músculos; são sintetizados no citosol do
terminal pré-sináptico e entram nas vesículas sinápticas (que são continuamente
recicladas e reutilizadas) por transporte ativo; os principais transmissores são:
Acetilcolina: secretada por neurônios em diversas áreas do SN, possuindo efeito
excitatório e, em algumas terminações nervosas parassimpáticas periféricas,
inibitório (inibição do coração pelo nervo vago).
Norepinefrina: secretada por terminais de diversos neurônios do tronco cerebral e
hipotálamo e, mais especificamente, no locus ceruleus (ponte), o qual envia fibras
nervosas para áreas encefálicas, auxiliando, por exemplo, no nível de vigília; liga-se
mais a receptores excitatórios que inibitórios.
Dopamina: secretada por neurônios que se originam na substância negra e que se
projetam para os gânglios da base, tendo efeito geralmente inibitório.
Glicina: secretada nas sinapses da medula espinhal; atua sempre como inibitório.
10
GABA (ácido gama-aminobutírico): secretado por terminais nervosos da medula
espinhal, do cerebelo, dos gânglios da base e diversas áreas do córtex; tem sempre
efeito inibitório.
Glutamato: secretado por terminais pré-sinápticos em muitas vias sensoriais
aferentes e em diversas áreas do córtex cerebral; tem efeito sempre excitatório.
Serotonina: secretada por núcleos que se originam no tronco cerebral e vão para
diversas áreas encefálicas, da medula espinhal e do hipotálamo; age como inibidor
das vias da dor na medula, no controle do humor e provocando sono quando age
nas regiões superiores do SN.
Óxido Nítrico: secretado por terminais nervosos em áreas encefálicas responsáveis
por comportamentos de longo prazo e memória; diferentemente dos outros
neurotransmissores, não é armazenado em vesículas, mas, produzido quase
instantaneamente conforme sua necessidade, não induzindo grandes alterações no
potencial de membrana, mas alterando a excitabilidade do neurônio.
2. Neurotransmissores peptídicos de ação lenta ou fatores de crescimento:
neuropeptídeos que provocam ações mais prolongadas, como mudanças do número
de receptores neuronais, abertura e fechamento de canais iônicos e mudanças do
número e tamanho das sinapses; quantidades bem menores são liberadas em
relação aos outros transmissores, uma vez que possuem um método laborioso de
formação, sendo sintetizados como parte de moléculas protéicas pelos ribossomos
do corpo celular do neurônio; tem uma potência 1000 vezes maior que os outros e
produzem efeitos que podem durar dias, meses ou até anos.
O corpo celular do neurônio motor apresenta um potencial de repouso da membrana de
−65mV, voltagem baixa que tem importância no controle da excitabilidade do neurônio e,
ainda, atua na repulsão de íons cloreto do corpo celular.
Baseando-se no potencial de Nernst, pode-se calcular o potencial de membrana que irá se
opor ao movimento dos íons (Na, K e cloreto) através dos canais.
Qualquer alteração no potencial, em qualquer parte do corpo celular, induz uma alteração
quase igual no potencial em todos os outros pontos do corpo celular (sem haver
potencial), devido ao fato de o neurônio conter o líquido intracelular, de alta condutividade
e apresentar um grande diâmetro, não oferecendo resistência à condução da corrente.
Potencial excitatório pós-sináptico (PEPS): aumento positivo (para um valor menos
negativo) na voltagem a partir do potencial normal da membrana em repouso; se este
potencial aumentar até o limite na direção positiva, irá provocar um potencial de ação no
nuerônio pós-sináptico, excitando-o; se o potencial aumentar de −65 para −45mV (limiar
para a excitação do neurônio), o PEPS será de +20mV, ou seja, 20mV mais positivo que o
valor de repouso.
O potencial de ação causado pelo aumento do PEPS é deflagrado no segmento inicial do
axônio, onde existe uma concentração muito maior de canais para Na que no corpo
celular.
As sinapses inibitórias induzem a abertura de canais de cloreto, permitindo a passagem
desses íons para o líquido intracelular e levando o potencial de membrana a −70mV.
O influxo de cloreto, aliado ao efluxo de K, aumentam o grau de negatividade intracelular
(hiperpolarização).
Potencial inibitório pós-sináptico (PIPS): causado pela hiperpolarização, que inibe o
neurônio pela grande negatividade do potencial de membrana (maior que o potencial
intracelular normal) no estado de repouso; se o potencial de membrana diminuir de −65
para −70mV, o PIPS será de −5mV, ou seja, 5mV mais negativo que o normal.
Inibição pré-sináptica: ocorre nos terminais pré-sinápticos, antes que o sinal neural
alcance a sinapse; causada pela liberação de uma substância inibitória (geralmente GABA)
sobre os terminais nervosos pré-sinápticos, que abre os canais aniônicos, permitindo a
difusão de cloreto no terminal nervoso, inibindo o efeito excitatório dos íons Na.
Somação Espacial: efeito de somação dos PEPS simultâneos pela ativação de múltiplos
terminais em diversas áreas na membrana neuronal, uma vez que a excitação de um
único terminal pré-sináptico sobre um neurônio quase nunca excita a célula (pequena
quantidade de substância transmissora liberada).
11
Somação Temporal: acontece quando descargas sucessivas de um único terminal présináptico ocorrem rápido o suficiente para se somar a potenciais anteriores, aumentando
o potencial total.
Um PIPS e um PEPS agindo simultaneamente podem se anular completa ou parcialmente.
Facilitação: quando o potencial de membrana fica mais próximo do limiar de disparo
devido à somação de sinais pós-sinápticos.
A grande maioria dos terminais pré-sinápticos do neurônio motor anterior terminam em
dendritos, o que facilita o compartilhamento de excitação, embora a maioria dos dendritos
não transmita potenciais de ação, apenas correntes eletrotônicas em direção ao corpo
celular.
Condução Decremental: redução do potencial de membrana, à medida que se propaga
eletrotonicamente através dos dendritos em direção ao corpo celular, devido ao tamanho
dos dendritos e o “vazamento” da corrente celular pela membrana.
Existem muitos diferentes tipos de neurônios com diferentes respostas para realizar as
diversas funções do SN, apresentando baixo ou alto limiar de excitação, mínima ou
máxima freqüência de disparo.
Fadiga da transmissão sináptica: ocorre quando as sinapses excitatórias são
repetidamente estimuladas numa velocidade alta, o que faz com que a taxa de disparo
diminua progressivamente; é causada, principalmente, pelo esgotamento dos
neurotransmissores e é importante para conter processos de superexcitação, como as
convulsões eplépticas.
De modo geral, a alcalose aumenta a excitabilidade neuronal (convulsão) e a acidose
deprime essa atividade (coma); além disso, a hipóxia também provoca uma drástica
diminuição na atividade neuronal.
Diversas drogas atuam na excitabilidade dos neurônios:
Aumentando: cafeína, teofilina (chá) e teobromina (cacau) reduzem o limiar de
excitação dos neurônios; estricnina inibe a ação de algumas substâncias transmissoras
inibitórias (glicina na medula espinhal).
Diminuindo: anestésicos aumentam o limiar para excitação da membrana neuronal.
Retardo Sináptico: período mínimo requerido (em torno de 0,5ms) para que todos os
processos envolvidos na transmissão do sinal neuronal de um neurônio pré-sináptico para
um pós-sináptico ocorram.
Cap. 46 – Receptores Sensoriais e Circuitos Neuronais para o Processamento
das Informações
Há 5 tipos básicos de receptores sensoriais:
1. Mecanorreceptores: detectam a compressão mecânica ou o estiramento do receptor e
dos tecidos adjacentes a ele.
2. Termorreceptores: detectam alterações de temperatura, alguns frio, outros calor.
3. Nociceptores (receptores da dor): detectam danos nos tecidos, físicos ou químicos.
4. Eletromagnéticos: detectam luz que incide na retina dos olhos.
5. Quimiorreceptores: detectam gosto, cheiro, nível de oxigênio no sangue arterial,
osmolaridade dos líquidos corpóreos, concentração de dióxido de carbono e outros.
Os tipos diferentes de receptores detectam diferentes estímulos por sensibilidades
diferenciadas, ou seja, cada receptor é altamente sensível a um tipo de estímulo para o
qual é especializado e insensível a outros.
Os principais tipos de sensibilidade (dor, tato, visão, som, etc.) são chamados de
modalidade de sensação, sendo transmitidas por diferentes fibras nervosas.
Cada trato nervoso termina em uma área específica do SNC e o tipo de sensação
percebida quando uma fibra nervosa é estimulada é determinado pela região do SN para o
qual as fibras se dirigem.
Princípio das vias rotuladas: é representado pela especificidade da fibra para transmitir
apenas uma modalidade de sensação (se uma fibra dolorosa for estimulada, o indivíduo
percebe dor, independendo do estímulo que excita a fibra – elétrico, compressão, etc.).
12
Potencial receptor: efeito imediato de mudança de potencial elétrico da membrana do
receptor quando um estímulo o excita (característica de todos os receptores).
Os receptores podem ser estimulados de várias maneiras, causando o potencial receptor:
1. Por deformação mecânica do receptor, distendendo a membrana do mesmo e abrindo
os canais iônicos.
2. Pela aplicação de uma substância química na membrana, abrindo os canais iônicos.
3. Pela alteração da temperatura da membrana, alterando sua permeabilidade.
4. Pelos efeitos da radiação eletromagnética que altera as características da membrana
do receptor e permite que íons fluam através dos canais da mesma.
De maneira geral, a causa básica da geração do potencial (de amplitude máxima de
100mV) é a alteração do potencial transmembrana.
O corpúsculo de Pacini, um tipo de receptor, apresenta uma fibra nervosa central
amielínica (tornando-se mielinizada pouco antes de entrar num nervo sensorial periférico)
e múltiplas camadas capsulares concêntricas sobre elas.
Uma pequena área da fibra terminal deformada pela compressão do corpúsculo, abre os
canais iônicos da membrana, permitindo que íons Na se difundam para o interior da fibra,
que tem sua positividade aumentada, constituído o potencial receptor, o qual gera um
fluxo de corrente (circuito local) que se distribui ao longo da fibra; ao atingir o primeiro nó
de Ranvier, o fluxo despolariza a membrana da fibra neste nó, desencadeando os
potenciais de ação típicos, transmitidos pela fibra ao SNC.
A estimulação muito intensa do receptor provoca aumentos cada vez menores aos
potencias de ação, permitindo que o receptor seja sensível a experiências sensoriais muito
fracas, sendo capaz de não atingir a freqüência máxima de disparo até que a experiência
sensorial seja extrema (faz com que receptor tenha uma ampla gama de respostas).
Todos os receptores se adaptam parcial ou completamente a qualquer estímulo constante
depois de um tempo, sendo que esse estímulo se inicia com alta freqüência, diminuindo-a
progressivamente até que os impulsos cessem.
Todos os mecanorreceptores acabam se adaptando, embora alguns demorem a fazê-lo
(chamados receptores que não se adaptam); alguns barorreceptores (como dos corpos
carotídeos e aórticos) levam dois dias para se adaptar; quimiorreceptores e receptores
para dor provavelmente nunca se adaptem completamente.
Os mecanismos de adaptação são diferentes para cada receptor; no olho, os bastonetes e
cones se adaptam modificando as concentrações de substâncias químicas sensíveis à luz;
dos mecanorreceptores, o exemplo é o corpúsculo de Pacini, que apresenta duas formas:
Quando uma força de compressão é aplicada em um dos lados é transmitida pelo
componente viscoso do corpúsculo (estrutura viscoelástica) para o mesmo lado da
fibra nervosa central, desencadeando um potencial receptor; o líquido, no entanto, em
pouco tempo se redistribui, inibindo o potencial receptor.
Mesmo quando a fibra nervosa continua a ser distorcida, a terminação da mesma
gradualmente se acomoda ao estímulo, resultando da inativação progressiva dos
canais de Na na membrana da fibra.
Os receptores de adaptação lenta (receptores tônicos) continuam a transmitir impulsos
para o SNC enquanto o estímulo estiver presente, mantendo-o sempre informado do
estado do corpo em relação ao meio ambiente; incluem: fusos musculares, aparelhos
tendinosos de Golgi, receptores da mácula no aparelho vestibular, receptores da dor, etc.
Os receptores de adaptação rápida (receptores de transição do estímulo/de
movimento/fásicos) são estimulados apenas quando a força do estímulo se altera,
reagindo fortemente enquanto uma alteração está acontecendo de fato; conhecendo-se a
velocidade com que ocorre alguma alteração do organismo, pode-se predizer quais serão
as condições algum tempo depois (corredor entrando numa curva).
Quanto maior o diâmetro das fibras, maior a velocidade de condução do sinal, sendo que
as mesmas são classificadas em tipos, uma classificação geral:
A: fibras mielinizadas grandes e médias dos nervos espinhais, sendo subdivididas em
α, β, γ e δ.
C: fibras fina e amielínicas, que conduzem impulsos de baixa velocidade, dos nervos
periféricos e fibras autônomas pós-ganglionares.
13
Há ainda uma classificação das fibras, usada por fisiologistas:
Grupo Ia: fibras das terminações anuloespirais dos fusos musculares – tipo Aα.
Grupo Ib: fibras dos órgãos tendinosos de Golgi – tipo Aα.
Grupo II: fibras dos receptores táteis cutâneos mais discretos e das terminações
secundárias dos fusos musculares – Aβ e Aγ.
Grupo III: fibras que conduzem a sensibilidade térmica, do tato grosseiro e a
sensibilidade dolorosa em picada – Aδ.
Grupo IV: fibras amielínicas de condução das sensações de dor, coceira, temperatura e
tato grosseiro – C.
Somação espacial: fenômeno em que o aumento da intensidade do sinal é transmitido
usando progressivamente uma quantidade maior de fibras, ou seja, quando as
terminações nervosas livres para dor são estimuladas num campo receptivo da pele,
sendo o número de terminações grande no centro e menor na periferia, quanto mais
intensos os sinais, mais fibras são atingidas.
Somação temporal: é o aumento da freqüência dos impulsos nervosos em cada fibra.
O SNC é composto por muitos agrupamentos neuronais, uns com mais outros com menos
neurônios, sendo que cada agrupamento apresenta sua própria organização especial,
fazendo com que processe os sinais de uma maneira própria e única.
Cada fibra eferente de um grupamento neuronal se ramifica gerando terminações que se
distribuem, fazendo sinapse e gerando uma área neuronal estimulada chamada campo
estimulatório.
Se uma fibra aferente tem uma quantidade suficiente de terminações para induzir uma
descarga num neurônio, o estímulo é dito excitatório (supralimiar) e o local, zona de
descarga (excitada ou limiar), se os estímulos não forem suficientes para induzir uma
excitação, mas contribuem com terminais, eles são ditos sublimiares (neurônios em
estado facilitado) e o local, zona facilitada (ou zona inibitória, dependendo da fibra).
Divergência: fenômeno em que os sinais fracos que entram em um agrupamento neuronal
promovem a excitação de um grande número de fibras nervosas que deixam esse
agrupamento; possui dois tipos principais:
1. Amplificadora: um sinal aferente se espalha para um número cada vez maior de
neurônios a medida que passa por ordens sucessivas de neurônios no seu trajeto
(característica da via corticoespinhal – uma única célula piramidal no córtex motor é
capaz de excitar muitas fibras musculares).
2. Em múltiplos tratos: o sinal é transmitido em duas direções a partir do agrupamento
neuronal (no tálamo – as informações sensoriais são retransmitidas para estruturas
ainda mais profundas do tálamo ou para regiões discretas do córtex cerebral).
Convergência: sinais de aferências múltiplas excitam um único neurônio, fornecendo
somação espacial suficiente para trazer o neurônio ao limiar necessário à descarga; pode
também resultar de sinais aferentes (excitatórios ou inibitórios) de múltiplas fontes
(interneurônios da medula espinhal – recebem sinais convergentes das fibras nervosas
periféricas que entram na medual, das fibras proprioespinhais que passam de um
segmento da medula para outro, fibras corticoespinhais do córtex cerebral e de várias
outras vias descendentes longas do encéfalo para a medula espinhal, sendo que todos
convergem sobre os neurônios motores anteriores para controlar a função muscular).
Circuito de inibição recíproca: um sinal aferente para um grupamento neuronal gera um
sinal excitatório eferente em uma direção e, ao mesmo tempo, um sinal inibitório em
outra (circuito característico do controle de todos os pares de músculos antagonistas).
Pós-descarga sináptica: quando as sinapses excitatórias incidem no neurônio desenvolvese um potencial elétrico pós-sináptico que dura um tempo, podendo continuar a excitar o
neurônio, fazendo com que ele transmita uma seqüência contínua de impulsos aferentes.
Circuito reverberante (oscilatório): causado por retroalimentação positiva dentro do
circuito neuronal, em que um estímulo retorna excitando novamente uma aferência
daquele circuito, podendo ser constituído por um único ou muitos neurônios.
A intensidade do sinal eferente geralmente aumenta para um valor alto no início da
reverberação, diminuindo para um valor crítico, cessando rápida e completamente.
14
Alguns circuitos neuronais emitem continuamente sinais eferentes, mesmo na ausência de
sinais aferentes excitatórios, por dois mecanismos:
1. Descarga neuronal contínua intrínseca: muitos neurônios do cerebelo a maioria dos
interneurônios da medula espinhal têm o potencial de membrana elevados o suficiente
para fazer com que eles emitam impulsos continuamente.
2. Sinais reverberantes contínuos: se a fadiga não for o suficiente para impedir a
reverberação, o circuito se torna uma fonte de impulsos contínuos.
Muitos circuitos neuronais emitem sinais eferentes rítmicos (sinal respiratório rítmico que
se origina nos centros respiratórios da medula oblonga e da ponte), que são resultados de
circuitos reverberantes, que fornecem sinais excitatórios ou inibitórios.
Como quase todas as áreas do encéfalo se conectam a outras regiões, poderia haver uma
um ciclo contínuo de excitações, sendo o SN inundado por sinais reverberantes sem
controle (como ocorre em áreas encefálicas nas convulsões epilépticas).
Para evitar que isso ocorra todo o tempo, o SNC apresenta dois mecanismos básicos:
1. Circuitos inibitórios: existem dois tipos em áreas encefálicas extensas:
1.1) Circuitos inibitórios de retroalimentação que retornam das terminações nervosas
das vias de volta para os neurônios excitatórios iniciais das mesmas vias.
1.2) Alguns agrupamentos neuronais exercem um controle inibitório grosseiro sobre
amplas áreas do encéfalo (núcleos da base exercem influências inibitórias sobre os
sistemas de controle da motricidade).
2. Fadiga das sinapses: significa que a transmissão sináptica se torna progressivamente
mais fraca quanto mais prolongado e mais intenso for o período de excitação.
As sensibilidades das sinapses podem ser alteradas pelo aumento do número de
receptores de proteínas nos sítios sinápticos, quando houver hipoatividade, e pela redução
do número de receptores, quando houver hiperatividade.
O mecanismo envolvido é que os receptores de proteínas são constantemente formados
pelo sistema complexo de Golgi/retículo endoplasmático, sendo inseridos na membrana
sináptica do neurônio receptor; quando as sinapses são superutilizadas muitos desses
receptores são inativados e removidos da membrana sináptica.
Os controles automáticos normalmente reajustam as sensibilidades dos circuitos para
faixas controláveis de reatividade, quando os circuitos estão muito ativos ou deprimidos.
Cap. 48 – Sensações Somáticas: II. Dor, Cefaléia e Sensações Térmicas
A dor é um mecanismo protetor e ocorre sempre que qualquer tecido é lesionado, fazendo
com que o indivíduo reaja para remover o estímulo doloroso; por isso, pessoas que
perderam a sensação de dor (lesão na medula espinhal) apresentam graves problemas.
A dor é classificada em dois tipos principais:
Dor rápida (pontual, em agulhada, aguda, elétrica): sentida dentro de 0,1s após a
aplicação do estímulo doloroso, é a dor de uma agulhada, facada, queimadura ou
choque elétrico; desencadeada por estímulos dolorosos mecânicos e térmicos, que são
transmitidos nos nervos periféricos para a medula espinhal por fibras de velocidades
entre 6 e 30m/s.
Dor lenta (em queimação, persistente, pulsátil, nauseante, crônica): começa somente
após 1s ou mais, aumentando lentamente durante vários segundos ou até minutos,
estando associada à destruição tecidual; pode levar a um sofrimento prolongado e
insuportável, ocorrendo na pele, órgãos ou tecidos; desencadeada por estímulos
dolorosos mecânicos, térmicos e químicos (principalmente), transmitidos para a
medula espinhal através de fibras com velocidade entre 0,5 e 2m/s.
Os receptores para dor são terminações nervosas livres espalhados nas camadas
superficiais da pele e em tecidos internos (periósteo, paredes das artérias, superfícies
articulares, foice e tentório).
Estímulos dolorosos químicos são desencadeados por substâncias como: bradicinina,
serotonina, histamina, íons potássio, ácidos, acetilcolina e enzimas proteolíticas;
prostaglandinas e a substância P aumentam a sensibilidade das terminações nervosas,
15
sem, contudo, excitá-las; além disso, o aumento da concentração de íons K e de enzimas
proteolíticas estimulam a dor por tornarem as membranas mais permeáveis a íons.
Receptores para dor praticamente não se adaptam, possibilitando que a pessoa esteja
ciente de um estímulo lesivo.
Hiperalgesia: aumento da sensibilidade dos receptores para dor devido à progressiva
excitação das fibras dolorosas (dor lenta-persistente-nauseante).
A intensidade da dor está relacionada à velocidade do dano tecidual e não ao dano total
que já ocorreu.
A isquemia causa dor devido ao acúmulo de grandes quantidades de ácido láctico nos
tecidos (metabolismo anaeróbico), além da formação, nesses locais, de bradicinina e
enzimas proteolíticas, que estimulam as terminações para dor.
O espasmo muscular causa dor pela estimulação de receptores para dor
mecanossensíveis, pela compressão de vasos sanguíneos (levando à isquemia) ou pelo
aumento do metabolismo do tecido (liberação de substâncias químicas indutoras da dor).
Ao entrarem na medula espinhal, oriundas das raízes espinhais dorsais, as fibras da dor
terminam em neurônios-relé nos cornos dorsais e tomam dois caminhos para o encéfalo:
1. Trato neoespinotalâmico (para dor rápida): as fibras dolorosas (Aδ) terminam na
lâmina I (marginal) dos cornos dorsais e excitam os neurônios de segunda ordem, os
quais dão origem a fibras longas que cruzam para o lado oposto da medula e
ascendem ao encéfalo; algumas fibras terminam em áreas reticulares do tronco
cerebral, mas a maioria segue até o tálamo, terminando no complexo ventrobasal, se
onde são transmitidas ao encéfalo e córtex somatossensorial.
A dor rápida é localizada com muito mais precisão do corpo que a lenta, para isso, no
entanto, é preciso que os receptores táteis sejam estimulados.
O glutamato é o mais provável neurotransmissor secretado na dor rápida (fibras Aδ).
2. Trato paleoespinotalâmico (para dor crônica lenta): via muito mais antiga que
transmite os impulsos por fibras periféricas crônicas lentas do tipo C (algumas Aδ),
que terminam nas lâminas II e III (substância gelatinosa) dos cornos dorsais; os
sinais, então, atravessam neurônios de fibras curtas e entram na lâmina V, no mesmo
corno, de onde os últimos neurônios dão origem a longos axônios que se unem às
fibras para dor rápida, cruzam a medula e vão em direção ao encéfalo (via anterolateral).
O glutamato e a substância P são os mais prováveis neurotransmissores dessa via,
sendo que, o primeiro atua instantaneamente e o segundo é liberado mais lentamente,
tendo sua concentração aumentada como o tempo; a sensação dupla –
rápida/duradoura – de dor (agulhada) talvez seja causada pela presença de ambos.
A maioria das fibras de dor lenta não chegam ao tálamo terminando no tronco
cerebral, mais especificamente nos núcleos reticulares da medula oblonga ou na área
tectal do mesencéfalo (colículos) ou na região cinzenta periaquedutal (circunda o
aqueduto de Sylvius); animais que tiveram o cérebro seccionado acima do
mesencéfalo demonstram sofrimento devido a estas regiões.
A dor transmitida por essa via não pode ser especificamente localizada (conectividade
multissináptica difusa).
O animal não perde a capacidade de perceber a dor pela remoção das áreas
somatossensoriais do córtex cerebral, devido ao fato de que impulsos dolorosos que
penetram na formação reticular do tronco cerebral, tálamo e outras regiões inferiores do
encéfalo causam uma percepção consciente de dor.
As áreas onde terminam os estímulos de dor lenta (áreas reticulares do tronco cerebral e
dos núcleos intralaminares do tálamo) têm um forte efeito de alerta sobre a atividade
neural do encéfalo (não dormimos em caso de dor grave).
Para uma pessoa com uma dor grave e intratável, existem mecanismos de alívio, como o
corte das vias neurais em vários pontos:
Dor na parte inferior do corpo: cordotomia da região torácica da medula espinhal
(corte do quadrante ântero-lateral, no lado oposto ao da dor, para interromper a via
sensorial antero-lateral) – pode não ser eficiente, pois: muitas fibras não são cruzadas
e dor pode retornar por ter sensibilizado outras vias.
16
Dor crônica: cauterização de áreas dolorosas específicas nos núcleos intralaminares do
tálamo (mantém intacta a dor aguda – mecanismo protetro).
Sistema de analgesia: capacidade do encéfalo em suprimir as aferências de sinais
dolorosos para o SN; consiste em três grandes componentes:
1. Áreas periventricular e da substância cinzenta periaquedutal
2. Núcleo magno da rafe e núcleo reticular paragigantocelular
3. Complexo inibitório da dor nos cornos dorsais da medula espinhal
Muitos neurotransmissores estão envolvidos no sistema de analgesia, como a encefalina
(causa inibição pré e pós-sináptica das fibras de dor aferentes dos tipos C e Aδ, em suas
sinapses nos cornos dorsais) e a serotonina.
A injeção de morfina no núcleo periventricular ao redor do terceiro ventrículo e na
substância cinzenta periaquedutal no tronco cerebral causam extrema analgesia.
O SN possui opióides naturais, neurotransmissores que atuam nos receptores para
morfina, os quais são derivados de três moléculas: pró-opiomelanocortina, proencefalina e
prodinorfina, que tem como produtos principais a β-endorfina (hipotálamo e hipófise), a
metencefalina, a leuencefalina e a dinorfina (tronco cerebral e medula espinhal).
A estimulação das fibras sensoriais (Aβ) com origem nos receptores táteis periféricos pode
reduzir a transmissão dos sinais de dor vindos da mesma área – inibição lateral local na
medula espinhal (mecanismo das massagens, linimentos e acupuntura).
Eletrodos colocados na pele, implantados na medula espinhal (estimulam as colunas
sensoriais dorsais) ou colocados em núcleos intralaminares do tálamo e nas áreas
periventricular ou periaquedutal do diencéfalo, são utilizados para suprimir a dor.
Dor Referida: dor sentida em uma parte do corpo que fica distante do tecido causador da
dor (dor visceral referida na superfície do corpo); seu mecanismo consiste em ramos das
fibras para dor visceral fazerem sinapse na medula espinhal nos mesmos neurônios de
segunda ordem (1 e 2) que recebem os sinais dolorosos da pele, com isso, os sinais
dolorosos das vísceras são conduzidos por alguns dos mesmos neurônios da pele.
As vísceras geralmente possuem receptores sensoriais exclusivos para dor e danos
viscerais localizados raramente causam dor grave (corte das alças intestinais), ao
contrário de uma estimulação difusa das terminações nervosas para dor, que podem
causar dor grave (isquemia em uma grande área do intestino).
Estímulos que excitam as terminações nervosas para a dor em áreas difusas das vísceras
podem causar dor visceral e dores que se originam nas cavidades torácica e abdominal
(transmitidas por fibras C) causam dor crônica-persistente.
Causas de dor visceral (verdadeira):
Isquemia: formação de produtos finais metabólicos ácidos ou produtos degenerativos
dos tecidos (bradicinina, enzimas proteolíticas), que estimulam as terminações de dor.
Estímulos químicos: substâncias nocivas podem escapar do trato gastrintestinal para a
cavidade peritoneal (suco gástrico através de úlcera rompida), causando dor.
Espasmo de uma víscera oca: o espasmo de uma alça intestinal, vesícula e ducto biliar,
ureter ou qualquer outra víscera oca pode causar dor por estimulação mecânica das
terminações nervosas ou diminuição do fluxo sanguíneo (cólicas).
Distensão excessiva de uma víscera oca: preenchimento excessivo que pode
interromper vasos sanguíneos, causando dor isquêmica.
Vísceras insensíveis: poucas áreas viscerais são insensíveis à dor; entre elas estão o
parênquima do fígado e os alvéolos pulmonares.
Uma dor visceral geralmente se dissemina para peritônio, pleura e pericárdio parietal,
superfícies parietais supridas (assim como a pele) com extensa inervação dolorosa vinda
dos nervos espinhais periféricos; essa dor é diferente da dor visceral verdadeira.
A dor visceral é difícil de ser localizada por uma falta de reconhecimento do paciente da
existência de diferentes órgãos e por as sensações (de abdome e tórax) serem
transmitidas através de duas vias ao SNC:
1. Via visceral verdadeira: a dor é transmitida através das fibras sensoriais para dor nos
feixes nervosos autônomos, sendo as sensações referidas para a superfície do corpo.
A dor referida é geralmente localizada no segmento dermatomal de origem do órgão
visceral no embrião e não no local de atuação do mesmo. Ex: coração – origem no
17
dermátomo do pescoço e da região superior do tórax, onde a dor é sentida; estômago
– origem entre o sétimo e o nono segmentos torácicos do embrião, por isso a dor é
referida ao epigástrio anterior (áreas supridas pelos seguimentos torácicos de 7 a 9).
2. Via parietal: as sensações são conduzidas diretamente para os nervos espinhais locais
a partir do peritônio parietal, pleura ou pericárdio e se localizam sobre a área dolorosa.
A dor das vísceras frequentemente se localiza em duas áreas corporais ao mesmo
tempo (dupla transmissão – via visceral referida e via parietal direta).
Hiperalgesia: hipersensibilidade à dor, causada por uma via dolorosa excessivamente
excitável, que pode resultar de sensibilidade excessiva dos receptores para dor
(hiperalgesia primária – pele queimada de sol) ou de uma facilitação da transmissão
sensorial (hiperalgesia secundária – lesões na medula espinhal ou no tálamo).
Herpes Zoster (cobreiro): causado pela infecção de um gânglio da raiz dorsal pelo
herpesvíus, gerando dor grave no segmento dermatomal suprido pelo gânglio.
Tique Doloroso (neuralgia do trigêmeo ou do glossofaríngeo): dor semelhante a choques
elétricos súbitos que ocorre sobre um dos lados da face na área de distribuição sensorial
(ou em parte dela) do quinto ou nono nervo craniano; é desencadeada por áreas
disparadoras excessivamente sensíveis na superfície da face, boca ou orofaringe; pode ser
bloqueada pelo corte cirúrgico do nervo periférico que inerva a área hipersensível.
Síndrome de Brown-Séquard: ocorre pela secção da medula espinhal em somente um dos
lados, bloqueando todas as funções motoras abaixo do nível da transecção do lado
seccionado; as sensações de dor, calor e frio (via espinotalâmica) são perdidas no lado
oposto (dermátomos de 2 a 6 segmentos abaixo do nível de transecção); sensações de
posição, cinestésicas, de vibração, de localização discreta e discriminação de dois pontos
são perdidas do lado da transecção, em todos os dermátomos abaixo da mesma; o tato
fino fica prejudicado no lado da transecção, já o tato grosseiro, mal localizado, persiste.
Cefaléia: tipo de dor referida para a superfície da cabeça a partir de estruturas profundas
da mesma, resultando de estímulos dolorosos de dentro do crânio ou de fora (seios
nasais, por exemplo).
Os tecidos encefálicos são quase insensíveis à dor, ao contrário, a distensão dos seios
venosos em torno do encéfalo, lesões do tentório ou a distensão da dura na base do
encéfalo podem causar cefaléia; além disso, estímulos traumatizantes, esmagamentos ou
distensão dos vasos sanguíneos das meninges (especialmente a artéria meníngea média)
causam dor.
A estimulação dos receptores acima do tentório desencadeia impulsos dolorosos na porção
cerebral do quinto nervo, causando cefaléia na metade frontal da cabeça; impulsos
dolorosos vindos da região abaixo do tentório entram no SNC pelos nervos glossofaríngeo,
vago e segundo cervical, causando cefaléia occipital (parte posterior da cabeça).
Tipos de cefaléia intracraniana:
Cefaléia da meningite: dor em toda a cabeça causada pela inflamação das meninges.
Cefaléia causada por baixa pressão do líquido cefalorraquidiano: a remoção de uma
pequena parte do líquido já dificulta a flotação do cérebro, levando o encéfalo a
distender-se e distorcer as superfícies durais, causando dor.
Enxaqueca: conseqüência de fenômenos vasculares anormais como as tensões
prolongadas que causam um vasoespasmo reflexo de artérias da cabeça (incluindo as
encefálicas), produzindo isquemia de porções do encéfalo, o que provoca os sintomas
prodrômicos (náusea, perda de parte do campo visual, aura visual, etc.); a isquemia
torna os vasos sanguíneos flácidos e a pressão arterial os faz dilatarem-se e pulsarem,
causando dor; existem outras teorias, mas a predisposição genética é certa.
Cefaléia alcoólica: o álcool, com seus efeitos tóxicos, irrita diretamente as meninges.
Cefaléia causada por constipação: resulta da absorção de produtos tóxicos ou de
alterações no sistema circulatório, resultante da perda de líquido no intestino.
Tipos de cefaléia extracraniana:
Cefaléias resultantes de espasmo muscular: provocados por tensão emocional, que
torna espásticos os músculos ligados ao couro cabeludo e músculos cervicais ligados
ao osso occipital.
18
Cefaléias resultantes da irritação nasal e de estruturas nasais acessórias: uma infecção
ou outros processos irritativos nas estruturas nasais se somam, causando cefaléia.
Cefaléias causadas por distúrbios visuais: a contração excessiva dos músculos ciliares
ou o espasmo reflexo de músculos faciais (ambos mecanismos para focar a imagem),
causam cefaléia, gerada, também, pela exposição à irradiação excessiva ou pela
irritação actínica da conjuntiva.
As graduações térmicas (frio congelante, gelado, frio, indiferente, morno, quente, muito
quente) são discriminadas por três tipos de receptores sensoriais: receptores para frio,
calor e dor (frio congelante e calor extremo – sensações parecidas).
Os receptores para frio e calor estão imediatamente abaixo da pele, tendo os primeiros 10
vezes mais pontos que o último; esses pontos (nos receptores de frio) diferem em
número em regiões diferentes (20/cm2 nos lábios e 4/cm2 nos dedos da mão).
As terminações nervosas livres para calor não são comprovadamente distintas (sinais
transmitidos por fibras nervosas do tipo C); o receptor para frio, no entanto, já foi
identificado como um tipo especial de terminação nervosa mielinizada fina do tipo Aδ (e
algumas fibrasC).
Os receptores térmicos se adaptam, mas, não totalmente, tendo sua estimulação
diminuída, e respondem acentuadamente às alterações na temperatura (respondendo,
também, a estados de temperatura constante).
Tanto os receptores para frio, quanto para calor são estimulados por alterações de suas
taxas metabólicas, já que a temperatura altera a velocidade das reações químicas.
Quando uma grande área da pele é estimulada, os sinais térmicos de toda a área se
somam, sendo detectados, no entanto, uma enorme alteração na temperatura de uma
pequena área da pele pode não ser detectada.
Os sinais térmicos, geralmente, são transmitidos nas vias paralelas às da dor; ao entrar
na medula espinhal, os sinais cursam pelo trato de Lissauer, terminando nas lâminas I, II
e III dos cornos dorsais; posteriormente, os sinais trafegam fibras que cruzam para o
trato sensorial ântero-lateral oposto e terminam em áreas reticulares do tronco cerebral e
no complexo ventrobasal do tálamo, o qual pode retransmitir ao córtex somatossensorial.
Cap. 49 – O olho: I. Óptica da Visão
O índice refrativo de uma substância transparente é a razão da velocidade da luz no ar
(300.000 Km/s) para a velocidade na substância; o índice refrativo do ar é 1.
Quando raios luminosos atingem uma interface perpendicularmente, não se desviam,
porém sua velocidade é alterada; se a interface for angulada e os índices refrativos dos
dois meios diferentes, os raios se curvam, sendo esse fenômeno conhecido como refração,
cujo grau aumenta em função da razão dos dois índices refrativos e do grau de angulação.
Tipos de lente:
Convexa: converge o raios luminosos, que atingem uma face angulada, cada vez mais
em direção ao centro, podendo incidir exatamente no ponto focal.
Côncava: diverge os raios que incidem na face angulada.
Cilíndrica: curva os raios de luz a partir dos dois lados da lente, mas não de cima para
baixo, ocorrendo, portanto, curvatura em apenas um plano; os raios se curvam
formando uma linha focal.
Duas lentes cilíndricas cruzadas em ângulos retos entre si realizam a mesma função que
uma lente esférica de mesmo poder refrativo.
Distância Focal: distância além de uma lente convexa em que raios paralelos convergem
para um ponto focal comum; pode ser obtida pela seguinte relação:
1=1+1
f
a
b
f: distância focal
a: distância da fonte de luz à lente
b: distância da lente ao foco
Quando os raios de luz que já estão divergindo entram numa lente convexa, a distância
de foco no outro lado da lente é a maior em relação à lente do que a distância focal da
19
lente para raios paralelos, embora tanto raios paralelos quanto divergentes possam ser
focalizados à mesma distância se a convexidade da lente for ajustada.
Objetos alinhados em frente a uma lente produzirão imagens sobre o foco da mesma, no
entanto em posição invertida.
O poder refrativo de uma lente (capacidade de curvar raios de luz) é medido em dioptrias
(1/distância focal), sendo + para lentes convexas e − para côncavas.
O olho humano é opticamente equivalente à câmera fotográfica comum: tem um sistema
de lentes, uma abertura variável (a pupila) e uma retina que corresponde ao filme.
Os sistema de lentes é composto por 4 interfaces refrativas:
1. Entre o ar e a superfície anterior da córnea
2. Entre a superfície posterior da córnea e o humor aquoso
3. Entre o humor aquoso e a superfície anterior do cristalino
4. Entre a superfície posterior do cristalino e o humor vítreo
O índice interno do ar é 1; o da córnea é 1,38; o do humor aquoso é 1,33; o do cristalino
(em média) é 1,4 e o do humor vítreo é 1,34.
O olho tem um poder refrativo de 59 dioptrias quando o cristalino está acomodado para
visão à distância; esse poder é fornecido pela superfície anterior da córnea, já que seu
índice refrativo é muito diferente do índice do ar.
Imagens são focalizadas na retina, tal como no filme da câmera, e, embora essas imagens
estejam invertidas, o cérebro as interpreta como normais.
O cristalino pode mudar sua forma de uma lente moderadamente convexa para uma
muito convexa, sofrendo o processo de acomodação, que pode ser de 14 dioptrias em
uma criança (indo de 20 a 34 dioptrias).
No jovem, o cristalino é composto de cápsula elástica forte cheia de líquido viscoso,
proteináceo, transparente; relaxado, tem forma quase esférica (retração elástica da
cápsula), já tenso, tem suas bordas puxadas por cerca de 70 ligamentos suspensores em
direção ao círculo externo do globo ocular, tornando-o relativamente plano.
Também nas fixações laterais dos ligamentos do cristalino ao globo ocular, há o músculo
ciliar, que tem dois conjuntos separados de fibras de músculo liso, da seguinte forma:
Fibras meridionais (radiais): se estendem das extremidades periféricas dos ligamentos
suspensores para a junção cornoescleral e quando se contraem as inserções periféricas
dos ligamentos do cristalino são puxadas medialmente em direção às bordas da
córnea, liberando a tensão.
Fibras circulares: se dispõem circularmente à volta das fixações de ligamentos e
quando se contraem diminui o diâmetro do círculo das fixações com ligamentos
(esfíncter), permitindo que os ligamentos façam menos tração sobre o cristalino.
O músculo ciliar é controlado por pelo SNP, o qual provoca a contração dos conjuntos de
fibras, que relaxam os ligamentos do cristalino, fazendo com que fique mais “bojudo” e
aumente seu poder refrativo (focalização de objetos próximos).
Presbiopia: dificuldade na acomodação do cristalino devido ao fato de este se tornar
maior, mais espesso e menos elástico (desnaturação das proteínas) com o avançar da
idade (2 dioptrias aos 50 e 0 aos 70).
A íris aumenta a quantidade de luz que entra no olho (escuridão) e a diminui (luz), a qual
entra através da pupila, que pode diminuir (1,5mm) ou aumentar (8mm) seu diâmetro.
A abertura pupilar determina a profundidade de foco, que torna mais nítidas as imagens
mesmo com a retina deslocada do plano focal (é máxima quanto menor está a pupila).
Erros de refração:
Emetropia (visão normal): raios de luz paralelos de objetos distantes apresentam-se
em foco nítido na retina com o músculo ciliar totalmente relaxado.
Hipermetropia (visão boa para longe): se deve a um globo ocular curto demais ou a
um sistema de lentes muito fraco; os raios de luz paralelos não são curvados o
suficiente para chegar ao foco quando alcançam a retina (se cruzam atrás dela);
correção pelo uso de lentes convergentes (convexas).
Miopia (visão boa para perto): se deve a um globo ocular longo demais ou de
demasiado poder refratário no sistema de lente; com o músculo ciliar relaxado, os
20
raios de luz vindos de objetos distantes são focalizados antes da retina; correção pelo
uso de lentes divergentes (côncavas).
Astigmatismo: erro refrativo do olho que faz com que a imagem visual num plano
focalize numa distância diferente daquela do plano em ângulos retos, resultando de
uma curvatura da córnea grande demais em um plano do olho (ovo); neste caso, cada
um dos dois planos exige um grau diferente de acomodação, que pode não ser
compensado naturalmente; correção pela associação de uma lente esférica com uma
cilíndrica adicional.
Lentes de contato (vidro ou plástico) podem ser introduzidas na superfície anterior da
córnea, sendo mantidas por líquido lacrimal, o qual apresenta um índice refrativo quase
igual ao da córnea, substituindo a refração da mesma; a lente tem muitas vantagens:
Corrige erros refrativos causados por córnea de formato anormal (ceratocone).
A lente gira com o olho, promovendo uma visão mais ampla e clara.
Têm pouco efeito sobre o tamanho dos objetos que a pessoa vê.
Catarata: área(s) nublada ou opaca no cristalino, causada pela desnaturação de fibras do
próprio cristalino que coagulam e tomam o lugar das fibras protéicas transparentes; a
correção é feita pela remoção do cristalino, substituído por uma lente convexa poderosa.
A luz de uma fonte, quando focalizada na retina, apresenta uma mancha de, cerca de,
11μm, que é mais nítida no centro (brilhante), com bordas sombreadas.
Se dois pontos estão separados de seus centros até 2μm da retina (pouco maior que a
largura da fóvea – 1,5μm), a pessoa pode distingui-los, uma vez que a acuidade visual do
olho humano é de 25s de arco, o que significa que uma pessoa com acuidade visual
normal, olhando para duas manchas a 10m, mal pode diferenciar duas imagens a 1,5 ou
2mm de distância uma da outras.
A acuidade visual se torna cada vez pior quanto mais afastada da fóvea.
Percebemos a distância por 3 meios principais:
1. Tamanho das imagens de objetos conhecidos na retina: o cérebro sabe calcular a
distância a partir do tamanho de objetos conhecidos.
2. Fenômeno da paralaxe de movimento: se uma pessoa movimenta a cabeça olhando
para um objeto bem próximo (2,5cm), as imagens também se movimenta, ao
contrário de objetos distantes (60m), cujas imagens não se movimentam
perceptivelmente; deste modo pode-se determinar as distâncias relativas de objetos
diferentes, mesmo com apenas um olho.
3. Fenômeno da estereopsia: objetos a 2,5cm do nariz formam imagens do lado esquerdo
da retina do olho esquerdo e do lado direito da retina do direito, enquanto, se estão a
6m, tem suas imagens formadas em pontos correspondentes da retina (centro); é uma
paralaxe binocular que dá a pessoa com dois olhos uma capacidade maior de julgar
distâncias relativas de objetos próximos.
O olho está preenchido com um líquido intra-ocular, que mantém pressão no globo ocular
suficiente para conservá-lo distendido; é dividido em duas partes:
Humor Aquoso: se situa à frente do cristalino; é um líquido de fluxo livre; está
continuamente sendo formado e reabsorvido e esse equilíbrio regula o volume e a
pressão do líquido intra-ocular.
- Formado numa taxa média de 2 a 3μm/min e secretado pelos processos ciliares, que
tem área de 6cm2 disposta em dobras e com muitas células epiteliais secretoras, as quais
secretam o humor pelo transporte de íons Na (puxam cloreto e bicarbonato – neutralidade
elétrica), que causam osmose de água dos capilares sanguíneos e a solução resultante
banha os espaços dos processos ciliares (câmara anterior do olho); outros nutrientes (AA,
ácido ascórbico, glicose) são transportados através do epitélio.
- Após ser formado, o humor flui através da pupila e entra na câmara anterior do olho, de
onde flui na direção anterior ao cristalino e entra no ângulo entre a córnea e a íris e,
depois, através de uma tela de trabéculas para finalmente entrar no canal de Schlemm
(veia aquosa), que desemboca em veias extra-oculares.
Humor Vítreo: fica entre a superfície posterior do cristalino e a retina; é uma massa
gelatinosa (corpo vítreo) unida por fibras e proteoglicanos; água e substâncias
dissolvidas podem difundir-se por ele, porém pouco.
21
A pressão intra-ocular normal média é de cerca de 15mmHg (entre 12 e 20), medida por
um tonômetro, sendo determinada pela resistência à saída do humor aquoso da câmara
anterior para o canal de Schlemm (2,5μL/min), ocasionada pelas trabéculas.
Nas superfícies das placas trabeculares (e em outros locais) há grande número de células
fagocitárias que mantém os espaços trabeculares limpos de debris (fragmentos) que
podem se juntar após hemorragias ou infecções.
Glaucoma: doença em que a pressão intra-ocular se torna patologicamente alta (chega a
70mmHg), podendo causar cegueira rapidamente, uma vez que pressões acima de 25 a
30mmHg já são perigosas; a medida que a pressão se eleva, os axônios do nervo óptico
são comprimidos no ponto de saída do globo ocular no disco óptico, resultando na morte
de fibras (falta de nutrição) do nervo óptico que levam o fluxo axonal ao cérebro; a
pressão alta, nesse caso, pode ser resultado da resistência à saída de líquidos para o
canal de Schlemm (junção iridocórnea); pode ser tratado por colírios que reduzem a
secreção ou aumentem a absorção do humor aquoso ou por cirurgias para abrir os
espaços das trabéculas ou permitir que o líquido flua diretamente para o espaço
subconjuntival.
Cap. 50 – O Olho: II. Funções Receptora e Neural da Retina
A retina é a parte sensível à luz do olho e contém cones (responsáveis pela visão em
cores) e bastonetes (responsáveis pela visão em preto-e-branco em baixa luminosidade),
os quais, quando excitados, transmitem sinais pelos neurônios da própria retina,
propagando-se para as fibras do nervo óptico e para o córtex.
Os componentes funcionais da retina se dispõem em camadas, de fora para dentro:
1. Camada pigmentar
2. Camada de bastonetes e cones que se projeta na camada pigmentar
3. Camada nuclear externa contendo os corpos celulares de bastonetes e cones
4. Camada plexiforme externa
5. Camada nuclear interna
6. Camada plexiforme interna
7. Camada ganglionar
8. Camada de fibras do nervo óptico
9. Membrana limitante interna
A luz, após atravessar o sistema de lentes, atravessa o humor vítreo e entra na retina por
sua camada mais interna (camada ganglionar–plexiforme–nuclear...cones e bastonetes).
A fóvea, área com pouco mais de 1mm2 no centro da retina, possui visão acurada e
detalhada; a fóvea central é composta quase totalmente por cones, os quais são
diferentes (têm corpos celulares longos e delgados) dos da periferia da retina.
Na região da fóvea, vasos sanguíneos, células ganglionares, camada nuclear interna e
plexiforme, são deslocados do topo dos cones, permitindo a passagem da luz até eles.
Os fotorreceptores (cones e bastonetes) apresentam como segmentos funcionais:
Segmento externo: é quem diferencia morfologicamente cones e bastonetes;
apresenta muitas dobras de membrana celular (discos) contendo a substância
fotoquímica sensível à luz (rodopsina nos bastonetes e pigmento coloridos nos cones),
que é uma proteína conjugada incorporada à membrana (transmembrana) que
constitui 40% da massa do segmento.
Segmento interno: contém citoplasma com organelas, principalmente a mitocôndria.
Núcleo
Corpo sináptico: se liga às células horizontais e bipolares.
A melanina (pigmento negro) na camada pigmentar impede a reflexão da luz por todo o
globo ocular; está ausente em albinos, fazendo com que a luz que invade a retina seja
refletida em todas as direções no globo ocular pelas superfícies sem pigmentação da
retina e pela esclera subjacente, diminuindo muito a acuidade visual.
A camada pigmentar armazena grande quantidade de vitamina A, que se difunde pelas
membranas celulares dos seguimentos externos.
22
A artéria central da retina entra no globo ocular pelo centro do nervo óptico e se divide
para suprir a superfície retiniana interna, cujas camadas internas terão, então, seu próprio
suprimento sanguíneo independente.
As camadas externas da retina dependem da difusão a partir dos vasos da coróide (onde
a camada externa da retina está aderida) para sua nutrição e oxigenação.
Descolamento da retina: a retina neural pode se descolar do epitélio pigmentar devido a
lesões no globo ocular (acúmulo de líquido/sangue entre a retina e o epitélio pigmentar) e
por contratura das fibrilas de colágeno do humor vítreo (puxa a retina em direção ao
interior do globo).
A rodopsina (púrpura visual) é uma combinação da proteína escotopsina e o pigmento
carotenóide 11-cis retinal (retineno).
Quando a rodopsina absorve energia luminosa esta tem seus elétrons fotoativados e
começa a se decompor: a forma cis do retinal muda para uma forma toda-trans, que se
afasta da escotopsina; o produto da combinação do retinal todo-trans com a escotopsina é
a batorrodopsina, que cai para lumirrodopsina, que cai para metarrodopsina I, depois para
metarrodopsina II (rodopsina ativada – provoca alterações elétricas nos bastonetes) e,
finalmente, para os produtos de degradação completos.
O retinal todo-trans é convertido em 11-cis retinal, pela ação da enzima retinal isomerase,
o qual se recombina com a escotopsina para formar novamente a rodopsina, que
permanece estável até absorver energia luminosa e se decompor novamente.
Há uma segunda via de conversão do retinal todo-trans em 11-cis retinal, pela conversão
do retinal todo-trans primeiro em retinol todo-trans (forma de vitamina A), que é
convertido em 11-cis retinol, sob a influência da isomerase, sendo este transformado em
11-cis retinal, que se combina com a escotopsina para formar a nova rodopsina.
A vitamina A está no citoplasma dos bastonetes e na camada do pigmento da retina,
sempre disponível para formar novo retinal (que pode, quando em excesso, ser convertido
de volta em vitamina A).
Cegueira noturna: ocorre quando existe deficiência de vitamina A, o que diminui a
formação de retinal e rodopsina, dificultando a visão com pouca luz.
O potencial receptor resultante da exposição do bastonete à luz é diferente, uma vez que
sua excitação causa aumento da negatividade do potencial de membrana
(hiperpolarização); isso ocorre porque a rodopsina decomposta diminui a condutância da
membrana dos bastonetes para íons Na no segmento externo.
O segmento externo do bastonete é diferente do interno (bombeia Na de dentro para
fora), se tornando muito permeável aos íons Na na escuridão, os quais neutralizam muita
da negatividade dentro da célula (−40mV); a rodopsina exposta a luz se decompõe e
diminui a condutância de membrana, aumentando a eletronegatividade.
A única diferença entre as substâncias fotoquímicas é que as porções protéicas (opsinas),
chamadas de fotopsinas nos cones, são diferentes das escotopsina dos bastonetes.
Cada cone só tem um tipo de pigmento colorido, chamados pigmento sensível ao azul, ao
verde e ao vermelho, com comprimentos de onda de 445, 535 e 570nm,
respectivamente; a absorção para a rodopsina dos bastonetes tem um pico de 505nm.
Adaptação à luz: a exposição por longo período de tempo à luz converte grande parte das
substâncias fotoquímicas a retinal e opsinas (o retinal dos cones se converte em
viatminaA) e isso faz com que a sensibilidade do olho à luz se reduza; o contrário também
ocorre, ou seja a adaptação ao escuro.
Todos os fenômenos químicos da visão, inclusive a adaptação, ocorrem cerca de 4 vezes
mais rapidamente nos cones que nos bastonetes, no entanto, a sensibilidade à escuridão
nos bastonetes é muito maior (adaptação mais lenta).
Além da adaptação por alterações das concentrações das substâncias fotoquímicas, o olho
possui outros mecanismos de adaptação à luz e ao escuro, como a alteração do tamanho
pupilar e a adaptação neural, que consiste na diminuição da transmissão dos sinais no
circuito neural e ocorre com muita rapidez.
O registro de imagens pela retina exige detecção de manchas escuras e claras na imagem
e, por isso, se torna essencial que a retina seja ajustada de modo que os receptores
respondam às áreas mais claras, mas não às mais escuras.
23
O SN interpreta as sensações de cores através de proporções de estímulo, da seguinte
forma: a luz monocromática laranja, com comprimento de onda de 580nm, estimula os
cones vermelhos até um valor de estímulo de 99 (99% da estimulação máxima) e os
cones verdes a 42 e não estimula os cones azuis, sendo a proporção 99:42:0 interpretada
pelo sistema nervoso como a sensação de laranja.
A estimulação igual de cones vermelhos, verdes e azuis dá a sensação de branco.
Uma pessoa pode ter um grupo de cones receptivos à cor faltando, sendo incapaz de
distinguir algumas cores de outras; se um cone vermelho (protanopia) ou verde
(deuteranopia) estiver faltando, a pessoa tem cegueira para vermelho-verde.
A cegueira para cores (daltonismo) é um distúrbio genético exclusivamente do sexo
masculino (ligado ao cromossomo X), sendo que raramente faltam cones azuis, embora
eles possam ser sub-representados, num estado genético chamado fraqueza para o azul.
Os diferentes tipos celulares neuronais da retina são:
1. Fotorreceptores: cones e bastonetes, que transmitem sinais para a camada plexiforme
externa, onde fazem sinapse com células bipolares e horizontais.
2. Células horizontais: transmitem os sinais horizontalmente na camada plexiforme
externa, a partir de bastonetes e cones, para células bipolares.
3. Células bipolares: transmitem sinais verticalmente dos bastonetes, cones e células
horizontais para a camada plexiforme interna, onde fazem sinapse com as células
ganglionares e amácrinas.
4. Células amácrinas: transmitem sinais de células bipolares para ganglionares ou,
horizontalmente, dentro da camada plexiforme interna, dos axônios das células
bipolares aos dendritos das células ganglionares ou outras células amácrinas.
5. Células ganglionares: transmitem sinais eferentes da retina através do nervo óptico
para o cérebro.
6. Células plexiformes: transmitem sinais na direção retrógrada a partir da camada
plexiforme interna para a externa; esses sinais são inibitórios e seu papel pode ser
controlar o grau de contraste da imagem visual.
A retina tem um tipo antigo de visão baseado nos bastonetes e um mais recente baseado
nos cones, sendo que os neurônios e fibras neurais que conduzem os sinais visuais para a
visão dos cones são bem maiores que os dos bastonetes e os sinais conduzidos ao cérebro
duas a cinco vezes mais rapidamente; os sistemas são representados da seguinte forma:
A via visual da fóvea da retina representa o sistema mais recente e mais rápido dos
cones, com 3 neurônios: cones – células bipolares – células ganglionares; as células
horizontais transmitem sinais inibitórios lateralmente na camada plexiforme externa e
as amácrinas transmitem sinais lateralmente na camada plexiforme interna.
As conexões neurais para a retina periférica apresentam, para a visão pura de
bastonetes, 4 neurônios: bastonetes – células bipolares – células amácrinas – células
ganglionares (células horizontais e amácrinas fornecem conectividade lateral); há
ainda um circuito para cones e bastonetes, passando diretamente às células
ganglionares ou medialmente pelas células amácrinas.
Existem alguns neurotransmissores não muito conhecidos na retina, como o glutamato,
liberado por cones e bastonetes em suas sinapses com as células bipolares, o ácido gamaaminobutírico, a glicina, a dopamina, a acetilcolina e a indolamina, secretados pelas
células amácrinas, entre outros.
Todos os neurônios da retina transmitem seus sinais visuais por condução eletrotônica,
que significa o fluxo direto de corrente elétrica (não potenciais de ação) no citoplasma
neuronal e axônios nervosos desde o ponto de excitação em todo o trajeto até as sinapses
de eferência; quando ocorre a hiperpolarização em resposta à luz no seguimento externo,
o mesmo grau de hiperpolarização é conduzido por fluxo de corrente elétrica, sem
necessidade de potencial de ação, o que permite uma condução graduada, o que faz com
que a hiperpolarização esteja relacionada com a intensidade luminosa e não com tudo ou
nada, como seria para o potencial de ação.
As saídas das células horizontais são sempre inibitórias (inibição lateral), o que ajuda a
assegurar a transmissão de padrões visuais com contraste adequado, uma vez que
interrompem o sinal excitatório transmitindo bordas de contraste na imagem visual.
24
Dois tipos de células são bipolares são responsáveis por sinais opostos excitatórios e
inibitórios na via visual, a célula bipolar despolarizante e a hiperpolarizante, o que pode
ser explicado pelo fato de as duas serem diferentes ou receberem excitação diferente
(uma de cones e bastonetes e a outra de uma célula horizontal, que é inibitória).
Mais de 30 tipos de células amácrinas foram identificadas, com funções diferentes, como:
Parte da via direta para visão dos bastonetes.
Respondendo fortemente no início de um sinal visual contínuo.
Sinalizando mudança na iluminação.
Respondendo ao movimento de uma mancha pela retina (sensíveis à direção).
Cada retina contém 100 milhões de bastonetes e 3 milhões de cones e as células
ganglionares em 1,6 milhão (60 bastonetes e 2 cones convergem em cada célula; próximo
à fóvea, no entanto, menos cones e bastonetes convergem em cada fibra óptica, ficando,
também, mais delgados e, na fóvea central há somente cones delgados, sem bastonetes.
A retina periférica tem uma sensibilidade muito maior à luz fraca, resultante da presença
de muitos bastonetes (200 em uma única fibra do nervo óptico), que somam seus sinais.
Há 3 tipos de células ganglionares na retina, cada qual com uma função diferente:
Células W: constituem 40% das células ganglionares; recebem a maior parte de sua
excitação por bastonetes; são sensíveis para detectar movimento direcional no campo
visual e são importantes para a visão mais grosseira (escuridão).
Células X: são as mais numerosas (55%); seus sinais representam localizações
distintas na retina; transmitem os detalhes finos da imagem visual (visão colorida).
Células Y: são as menos numerosas (5%), mas as maiores de todas; notificam o SNC
quase instantaneamente quando ocorre um novo evento visual, mas sem precisão.
As células ganglionares transmitem seus sinais por meio de potenciais de ação repetitivos
e são excitadas, muitas vezes, por alterações na intensidade luminosa.
Uma única célula ganglionar pode ser estimulada por vários cones ou apenas por alguns;
quando todos os tipos estimulam a mesma célula, ela não detecta a diferença das cores
(recebe um sinal branco); cada tipo de célula ganglionar é excitada por uma cor e inibida
pela cor “oponente”, evidenciando que a análise das cores começa na retina.
Cap. 51 – O Olho: III. Neurofisiologia Central da Visão
Os sinais visuais saem das retinas através dos nervos ópticos, cujas fibras das metades
nasais cruzam, no quiasma óptico, para os lados opostos, onde se unem às fibras das
retinas temporais opostas para formar os tratos ópticos; as fibras de cada trato fazem
sinapse no núcleo geniculado dorsolateral do tálamo e daí projetam-se, por meio da
radiação óptica (trato geniculocalcarino), para o córtex visual primário.
As fibras visuais também se projetam para áreas mais antigas do cérebro:
1. Do quiasma óptico para os núcleos supraquiasmáticos do hipotálamo (controlam os
ritmos circadianos).
2. Para os núcleos pré-tectais no mesencéfalo (desencadeiam movimentos reflexos dos
olhos para focalizar objetos e ativar o reflexo fotomotor).
3. Para o colículo superior (controla movimentos direcionais rápidos dos olhos).
4. Para o núcleo geniculado ventrolateral do tálamo e regiões adjacentes (ajuda a
controlar funções comportamentais do corpo).
Desta forma, as vias visuais podem ser divididas em um sistema antigo (mesencéfalo e
áreas prosencefálicas basais), usado por muitos animais primitivos e um novo (para o
córtex visual nos lobos occipitais), em seres humanos.
O núcleo geniculado dorsolateral retransmite informações visuais do trato óptico para o
córtex visual por meio da radiação óptica (ponto a ponto) e “represa” (controla quanto é
permitido passar) a transmissão dos sinais para o córtex visual, recebendo sinais das
fibras corticofugais (de projeção direta do córtex visual primário para o núcleo geniculado
lateral) e de áreas reticulares do mesencéfalo; ambos os sinais são inibitórios.
Esse núcleo é composto por 6 camadas nucleares, sendo que as camadas II, III e V
recebem sinais da metade lateral da retina ipsilateral e as camadas I, IV e VI, da metade
medial da retina do olho contralateral; podendo ser dividido de outro modo: camadas
25
magnocelulares (I e II) com neurônios grandes , recebendo aferência das células Y da
retina (via de condução rápida e com transmissão apenas de preto-e-branco) e fibras
parvocelulares (camadas III e VI) com muitos neurônios pequenos e médios, recebendo
suas aferências das células X (condução moderada, ponto a ponto e colorida).
O córtex visual (nos lobos occipitais) se divide em duas partes:
1. Córtex visual primário (área visual I/córtex estriado): situa-se na área da fissura
calcarina (á frente, a partir do pólo occipital); é a região terminal dos sinais visuais
diretos, sejam da área macular da retina (próximo ao pólo occipital) ou da retina mais
periférica (lobo occipital medial); a fóvea (com muita representação no córtex)
transmite seus sinais para a grande área da mácula.
2. Áreas visuais secundárias do córtex (áreas de associação visual): situam-se lateral,
anterior, superior e inferiormente ao córtex primário; sinais secundários são
transmitidos a essas áreas para análise dos significados visuais.
A área ao redor do córtex primário (área 18 de Broadmann) é para onde, virtualmente, os
sinais são projetados, sendo chamada área visual II (V-2) e outras áreas visuais
secundárias são designadas V-3, V-4, até mais de 12 áreas.
O córtex visual primário tem 6 camadas distintas, sendo que as fibras geniculocalcarinas
terminam na camada IV, organizada em subdivisões:
IVcα: recebe os sinais das células Y e os retransmitem verticalmente em direção à
superfície cortical ou a níveis mais profundos.
IVa e IVcβ: recebem os sinais das células X e os retransmitem verticalmente em
direção à superfície do córtex e para camadas mais profundas.
O córtex visual é organizado em milhões de colunas verticais, cada uma com 1000 ou
mais neurônios; após terminarem na camada IV, os sinais são processados e enviados às
camadas I, II e III, que transmitem sinais para as distâncias curtas, V e VI, para
distâncias maiores.
Colunas (Blobs) de cores: áreas semelhantes à colunas, entremeadas entre colunas
visuais primárias e algumas secundárias, que são ativadas por sinais coloridos (áreas
primárias para decifrar cores).
A camada IV é entrelaçada com faixas de colunas neuronais, assim, os sinais de um olho
projetam-se para colunas alternadas, alternando-se com sinais vindos do outro olho.
Após sair do córtex visual primário, a informação visual é analisada em duas vias
principais nas áreas visuais secundárias:
1. Posição em 3D, forma grosseira e movimento de objetos: diz onde os objetos estão em
cada instante e se há movimento; os sinais dessa via são originados das células
ganglionares Y da retina, rápidos e em preto-e-branco.
2. Detalhes visuais e cor: referente a características visuais, como reconhecimento de
letras e textura de superfícies, leitura, além da determinação de cores detalhadas dos
objetos e descoberta de qual objeto e seu significado.
O sinal visual no córtex visual primário refere-se principalmente a contrastes na cena
visual e não a áreas não contrastantes (áreas de máxima excitação ocorrem ao longo das
bordas nítidas do padrão visual).
Além de detectar a presença de linhas e bordas nas diferentes áreas da imagem da retina,
o córtex também detecta a direção de orientação de cada linha ou borda (vertical,
horizontal ou com certo grau de inclinação).
Para cada uma das orientações de uma linha, são estimuladas células neuronais
específicas (células simples), encontradas na camada IV do córtex visual primário; longe
dessa camada, são encontradas células (células complexas) que detectam pequenas
alterações de distância das linhas, desde que na mesma direção.
À medida que se avança na via analítica do córtex visual (neurônios situados nas camadas
mais externas) são decifradas cada vez mais características de cada cena visual (bordas,
comprimentos, formas anguladas, etc.).
A cor é detectada do mesmo modo que as linhas, por contraste de cores, ou seja, uma cor
contrastando sobre outra, chamada cor oponente (uma área vermelha costuma ser
contrastada com uma área verde) ou as cores contrastando contras uma área branca.
26
A remoção do córtex visual primário humano causa perda da visão consciente (cegueira),
no entanto, pessoas assim conseguem, por vezes, reagir subconscientemente (virar os
olhos, por exemplo) a alterações da intensidade luminosa, movimento da cena visual e,
raramente, a algum aspecto grosseiro da visão, talvez por essa visão ser mediada por
vias neuronais que passam dos tratos ópticos para os colículos superiores e outras partes
do sistema visual mais antigo.
Campo visual: área visual vista por um olho num dado instante, sendo a área vista no
lado nasal campo visual nasal e a área vista na parte lateral campo visual temporal.
Perimetria: processo em que um utilizado um gráfico para diagnosticar cegueira em
partes específicas da retina, sendo que em todos os gráficos é encontrada uma mancha
cega, causada por falta de bastonetes e cones na retina sobre o disco óptico (15 graus
lateralmente ao ponto central da visão).
A perimetria pode diagnosticar patologias como os escotomas, que soa manchas cegas em
partes do campo visual (exceto no disco óptico), causadas por lesão do nervo óptico,
glaucoma, reações alérgicas na retina ou patologias tóxicas e retinite pigmentosa, em que
partes da retina degeneram e dão lugar a depósitos de melanina.
Lesões na via óptica:
A destruição do nervo óptico causa cegueira no olho afetado.
A destruição do quiasma óptico causa cegueira na metade nasal de cada retina, o que
significa cegueira no campo visual temporal para cada olho (a imagem do campo visual
é invertida na retina) – hemianopsia bitemporal.
A interrupção de um trato óptico desnerva a metade correspondente de cada retina no
mesmo lado que a lesão, fazendo com que nenhum dos olhos poça ver objetos do lado
oposto da cabeça – hemianopsia homônima.
Os movimentos oculares são controlados por três pares de músculos: retos medial e
lateral (contraem-se para movimentar os olhos lado a lado), retos superior e inferior
(contraem-se para movimentar os olhos para cima e para baixo) e oblíquos superior e
inferior (rodam os globos oculares e mantêm os campos visuais na posição vertical).
Cada um dos 3 conjuntos de músculos para cada olho é inervado reciprocamente, de
modo que um músculo do par relaxa enquanto o outro se contrai.
Movimentos importantes dos olhos são os que fazem com que eles se fixem numa parte
distinta do campo visual, sendo controlados por dois mecanismos neuronais:
1. Mecanismo de fixação voluntária: permite que uma pessoa movimente os olhos
voluntariamente para encontrar o objeto em que ela quer fixar a visão; uma lesão nas
regiões corticais pré-motoras dos lobos frontais torna difícil para a pessoa destravar os
olhos de um ponto e move-los para outro.
2. Mecanismo de fixação involuntária: mantém os olhos firmemente no objeto, uma vez
que ele tenha sido encontrado; uma lesão nas áreas visuais secundárias no córtex
occipital (ou destruição dos colículos superiores) torna difícil para o animal manter os
olhos direcionados a um ponto de fixação.
Os olhos têm 3 tipos de movimentos contínuos, imperceptíveis: tremor pela contração dos
músculos oculares, deslocamento lento dos globos oculares e movimentos rápidos
controlados pelo mecanismo de fixação involuntária.
Movimentos optocinéticos: ocorrem quando uma cena está se movendo continuamente
diante dos olhos, fazendo com que os olhos se fixem num destaque após o outro no
campo visual, aos saltos (sacadas).
Durante uma leitura ou a observação de uma pintura, a pessoa faz movimentos sacádicos
dos olhos para cada linha ou de um destaque da pintura para outro.
Movimento de perseguição visual: os olhos se mantém fixos num objeto em movimento,
através de um mecanismo altamente desenvolvido, que detecta o trajeto do movimento e
rapidamente desenvolve um trajeto semelhante para os olhos.
Se o córtex visual primário for destruído, mas, os colículos superiores estiverem intactos.
Uma pessoa é capaz de responder a perturbações visuais, evidenciando que esses
colículos desempenham um papel global na orientação dos olhos, cabeça e corpo com
respeito aos distúrbios externos visuais, auditivos e somáticos.
27
As imagens visuais se fundem nos pontos correspondentes das retinas para tornar as
percepções visuais mais significativas.
O mecanismo celular neuronal para estereopsia (percepção de profundidade) se baseia no
fato de que algumas das vias de fibras das retinas para o córtex visual organizam-se
considerando um a dois graus a cada lado da via central.
Estrabismo: falta de fusão adequada do eixo visual dos olhos em uma ou mais das
coordenadas visuais (horizontal, vertical, rotacional) causada por um ajuste anormal do
mecanismo de fusão do sistema visual (a criança fixa os olhos de maneira errada, estes
se tornam anormalmente ajustados e as imagens dos olhos jamais se fundem).
Se apenas um olho, no estrábico, é usado o tempo todo, o outro fica reprimido, perdendo
acuidade visual; pode se desenvolver, caso o olho dominante fique cego, com o
desenvolvimento apropriado das conexões sinápticas.
As fibras pré-ganglionares parassimpáticas do olho originam-se no núcleo de EdingerWestphal e passam no terceiro nervo até o gânglio ciliar, onde as fibras fazem sinapse
com neurônios parassimpáticos pós-ganglionares, os quais enviam fibras através dos
nervos ciliares para o globo ocular; esse nervos excitam o músculo ciliar (controla o foco
do cristalino) e o esfíncter da íris (causa constrição da pupila).
A inervação simpática do olho se origina nas células do corno intermediolateral do
primeiro segmento torácico da medula espinhal, de onde as fibras simpáticas entram na
cadeia simpática e sobem para o gânglio cervical superior, fazendo sinapse com neurônios
pós-ganglionares, cujas fibras se propagam ao longo das superfícies da artéria carótida e
outras (até chegar no olho); ali as fibras inervam as fibras radiais da íris (aumentam o
diâmetro pupilar), bem como vários músculos extra-oculares do olho.
A acomodação do cristalino é regulada por um mecanismo de feedback negativo que
automaticamente ajusta o poder refrativo do mesmo para obter o grau mais alto de
acuidade visual.
A focalização rápida e precisa do olho tem algumas características conhecidas, como:
1. Quando os olhos mudam subitamente a distância do ponto de fixação, o cristalino
muda seu poder de convergência na direção apropriada numa fração de segundo.
2. Diferentes indícios ajudam a mudar a forma do cristalino na direção apropriada:
2.1) Aberração cromática: os olhos são capazes de detectar qual raio de luz, vermelho ou
azul, por exemplo, que focalizam em regiões distintas, está no melhor foco, modificando o
poder de convergência do cristalino.
2.2) Os olhos fixados num objeto próximo se convergem, causando um sinal simultâneo
para regular a forma do cristalino.
2.3) A nitidez de foco na fóvea (mais aprofundada que o restante da retina) é diferente da
nitidez de foco das margens, alterando a força do cristalino.
2.4) O grau de acomodação do cristalino oscila todo o tempo, alterando a clareza da
imagem visual, o que faz com que o cristalino tenha que alterar sua força para focalizar.
A estimulação dos nervos parassimpáticos excita o músculo esfíncter da pupila, causando
miose (fechamento) e a estimulação dos nervos simpáticos excita as fibras radiais da íris,
causando midríase (dilatação).
Reflexo fotomotor: contração da pupila quando a luz brilha nos olhos; quando a luz invade
a retina, alguns dos impulsos resultantes passam dos nervos ópticos para os núcleos prétectais, de onde impulsos secundários passam para o núcleo de E.W. e voltam pelos
nervos parassimpáticos para contração do esfíncter; na escuridão o reflexo torna-se
inibido (a pupila se dilata).
Algumas doenças do SN, como sífilis do SNC, alcoolismo e encefalite, danificam a
transmissão nervosa dos sinais visuais das retinas para o núcleo de E.W., bloqueando,
algumas vezes, os reflexos pupilares; como as fibras do núcleo de E.W. são
principalmente inibitórias, com seu efeito perdido, o núcleo se torna cronicamente ativo
fazendo as pupilas continuarem contraídas, podendo responder à acomodação (pupila de
Argyll Robertson).
Síndrome de Horner: interrupção dos nervos simpáticos do olho na cadeia simpática
cervical, que provoca contração persistente da pupila, queda da pálpebra, dilatação
28
constante dos vasos sanguíneos e ausências de sudorese no lado da face e cabeça afetado
(exige estimulação simpática).
Cap. 52 – O Sentido da Audição
O cabo do martelo está fixado à membrana timpânica e sua outra parte se liga à bigorna
por minúsculos ligamentos, fazendo com que a mesma se mova sempre que o martelo se
move; em sua extremidade oposta, a bigorna articula-se com a base do estribo, cuja
placa se situa contra o labirinto membranoso da cóclea, na abertura da janela oval.
O ponto de fixação do martelo ao centro da membrana timpânica é constantemente
puxado pelo músculo tensor do tímpano, permitindo a passagem do som pelos ossículos.
A articulação bigorna/estribo faz com que este empurre para frente a janela oval e o
líquido coclear no outro lado da mesma, quando a membrana timpânica se move para
dentro, e puxe de volta o líquido quando o martelo se movimenta para fora.
A amplitude de movimento da placa do estribo com cada vibração sonora tem ¾ da
amplitude do cabo do martelo; os ossículos, suspensos por ligamentos,atuam como
alavanca única, aumentando a força de movimento cerca de 1,3 vezes (a superfície da
membrana timpânica tem 55mm2 , enquanto a do estribo tem 3,2mm2 – esta diferença de
17 vezes multiplicada por 1,3 causa 22 vezes mais força total exercida sobre o líquido da
cóclea em relação à exercida pelas ondas sonoras na membrana timpânica).
A membrana timpânica e o sistema ossicular proporcionam equalização das impedâncias
entre as ondas sonoras no ar e as vibrações sonoras no líquido da cóclea, sendo que, na
ausência destes, o som ainda pode trafegar pelo ar, mas com sensibilidade diminuída.
Reflexo de atenuação: quando sons intensos são transmitidos através do sistema ossicular
para o SNC, ocorre contração do estapédio (puxa o estribo para fora) e do tensor do
tímpano (puxa o cabo do martelo para dentro) e essas forças opostas aumentam a
rigidez, diminuindo a condução de baixa freqüência; esse mecanismo tem dupla função:
1. Proteger a cóclea de vibrações prejudiciais (sons intensos).
2. Mascarar sons com baixa freqüência em ambientes com som intenso (remove ruídos).
Além disso, esse sistema diminui a sensibilidade auditiva da pessoa à sua própria fala.
A cóclea está mergulhada no labirinto ósseo (cavidade do osso temporal) o que faz com
que as vibrações do crânio causem vibrações no líquido da própria cóclea.
O órgão de Corti, situado na membrana basilar,contem as células ciliadas, que são os
órgãos receptores finais que geram impulsos nervosos em resposta às vibrações sonoras.
As vibrações sonoras entram na rampa vestibular a partir da placa do estribo, a qual se
conecta a janela oval por um ligamento frouxo (permite o movimento com as vibrações
sonoras), movimentando o líquido para a rampa vestibular e média (ou pra trás).
A membrana basilar (separa a rampa média da timpânica) contém as fibras basilares, que
são curtas e rígidas perto da janela oval da cóclea (vibram melhor numa frequência muito
alta) e longas e menos rígidas próximo ao helicotrema (ressonância de baixa freqüência).
Uma onda sonora que entra pela janela oval, faz com que a membrana basilar curve-se
na direção da janela redonda (que precisa estar abaulada, já que a cóclea é delimitada
por paredes ósseas), criando uma tensão elástica nas fibras, iniciando a onda de líquido
que trafega ao longo da membrana basilar em direção ao helicotrema.
Toda onda é relativamente fraca a princípio, tornando-se forte quando chega à parte da
membrana basilar que tem freqüência de ressonância natural igual à respectiva freqüência
do som, sendo que a freqüência da onda é inversamente proporcional à distância que ela
alcança na membrana basilar.
As ondas trafegam rapidamente na parte inicial da membrana, tornando-se cada vez mais
lentas quando se afastam em direção à cóclea, devido à perda progressiva dos
coeficientes de elasticidade das fibras basilares.
O órgão de Corti, situado na superfície das fibras basilares, é o órgão que gera impulsos
nervosos em resposta à vibração da membrana basilar, cujos receptores sensoriais são as
células ciliadas internas e externas, as quais estimulam fibras nervosas que levam axônios
gânglio espiral de Corti e daí para o nervo coclear.
29
A excitação das fibras nervosas auditivas se faz pela ação dos estereocílos, que emergem
da membrana tectorial, os quais se curvam despolarizando (ou hiper) as células ciliadas.
As fibras nervosas são estimuladas principalmente pelas células internas, embora as
externas controlem a sensibilidade das mesmas para diferentes tons (afinação do sistema
receptor).
Potencial endonuclear: potencial elétrico de cerca de +80mV existente entre a endolinfa
(líquido secretado pela estria vascular que preenche a rampa média) e a perilinfa (líquido
com composição semelhante a do líquido cefalorraquidiano presente nas rampas
vestibular e timpânica), com positividade no interior da rampa média e negatividade fora.
A endolinfa contém alta concentração de K e baixa de Na, exatamente o oposto da
perilinfa, sendo o potencial gerado por secreção de K para a rampa média.
Princípio do lugar: é o principal método usado pelo SNC para detectar diferentes
freqüências sonoras, baseado nas posições da membrana que são mais estimuladas.
Disparo em surto (princípio de freqüência): baixas freqüências (entre 20 e 2000 ciclos/s)
podem causar surtos de impulsos nervosos sincronizados transmitidos aos núcleos
cocleares do cérebro, os quais distinguem as diferentes freqüências.
A intensidade do som é determinada pelo sistema auditivo de 3 modos:
1. Quando o som se torna mais intenso, a amplitude de vibração da membrana basilar e
das células ciliadas também aumenta, de modo que estas últimas excitam as
terminações nervosas em freqüências mais rápidas.
2. A amplitude de vibração aumentando faz com que mais células ciliadas fiquem
estimuladas, causando somação espacial dos impulsos (transmissão por muitas fibras).
3. Só uma vibração da membrana basilar de alta intensidade estimula significativamente
as células ciliadas, notificando o SN que o som é intenso.
A orelha interpreta grandes diferenças de nível sonoro, desde o mais suave até o mais
intenso, e essa sensação muda em proporção à raiz cúbica da intensidade real do som, ou
seja, a escala de intensidade é comprimida pelos mecanismos de percepção sonora do
sistema auditivo, permitindo a interpretação da intensidade sonora numa ampla faixa.
Um jovem ouve numa faixa normal de 20 a 20.000 ciclos por segundo, já na idade
avançada, esta faixa é encurtada para 50 a 8.000 ciclos por segundo.
Vias auditivas: as fibras nervosas do gânglio espiral de Corti entram nos núcleos cocleares
dorsal e ventral (parte superior do bulbo), onde fazem sinapse com neurônios de segunda
ordem e passam principalmente para o lado oposto do tronco cerebral, terminando no
núcleo olivar superior, daí a via sobe pelo leminisco lateral, terminando nele ou se
desviando ao colículo inferior, fazendo sinapse, a via passa então núcleo geniculado
medial, onde todas as fibras fazem sinapse e, finalmente, segue para a radiação auditiva
até o córtex auditivo (giro superior do lobo temporal).
As vias são transmitidas de ambos os lados do cérebro, havendo cruzamento delas em
pelo menos 3 lugares: corpo trapezóide, comissura entre os núcleos do lemnisco medial
lateral e comissura que liga os dois colículos inferiores.
Além do córtex auditivo primário, excitado diretamente por projeções do corpo geniculado
medial, existe o córtex auditivo secundário (córtex de associação auditiva), excitado por
impulsos do córtex primário ou projeções das áreas de associação talâmicas.
Cada uma das áreas do córtex auditivo disseca uma característica específica dos sons,
fazendo com que existam seis mapas tonotópicos para o mesmo, os quais evidenciam que
sons de baixa freqüência são reconhecidos anteriormente e os de alta, posteriormente.
O córtex auditivo é importante na discriminação de padrões sonoros tonais e seqüenciais,
sendo que sua remoção não impede o animal de detectar sons ou reagir a eles.
A destruição dos córtices auditivos primários no ser humano reduz a sensibilidade auditiva
e a destruição de um lado apenas reduz a audição da orelha oposta, não provocando
surdez devido às conexões cruzadas, mas afetando a capacidade de localização de uma
fonte de som (são necessários sinais comparativos nos dois córtices).
Lesões em áreas de associação auditivas não diminuem a audição ou a capacidade de
diferenciar tons, mas de interpretar o significado do som ouvido (lesões na área de
Wernicke fazem com que a pessoa ouça, mas não saiba o significado das palavras).
A pessoa determina a direção horizontal da qual vem o som de duas maneiras:
30
1. O intervalo de tempo entra a entrada de som numa orelha e na outra (funciona melhor
em frequências mais baixas, sendo mais eficaz).
2. A diferença entre as intensidades de sons nas duas orelhas (funciona melhor em
frequências mais altas).
A destruição do córtex auditivo nos dois lados causa perda da capacidade de detectar a
direção de onde vem o som, relacionada ao núcleo olivar superior, da seguinte forma:
Núcleo olivar superior lateral: detecta a direção da qual vem o som por comparação
entre as diferentes intensidades que chegam às orelhas.
Núcleo olivar superior medial: detecta o intervalo de tempo entre sinais acústicos que
entram nas duas orelhas, através de neurônios com dois dentritos principais que se
projetam para a direita e para a esquerda, sendo cada um estimulado de uma forma,
permitindo a detecção.
Existem fibras retrógradas em cada nível do SN auditivo, sendo inibitórias (a estimulação
direta de pontos do núcleo olivar inibe áreas do órgão de Corti, reduzindo sua
sensibilidade sonora) e responsáveis pela direção da atenção a um som específico.
Existem dois tipos de surdez:
1. Causada por comprometimento do nervo auditivo (surdez nervosa); pode ter alguns
padrões, como:
- Surdez para sons de baixa freqüência: causada por exposição a sons intensos, que tem
a freqüência mais baixa, sendo prejudiciais aos órgãos de Corti.
- Surdez para todas as freqüências: causada por sensibilidade dos órgãos de Corti a
algumas drogas e antibióticos (estreptomicina, canamicina e cloranfenicol).
2. Causada por comprometimento das estruturas físicas da orelha (surdez de condução)
que podem ser causados por:
- Fibrose na orelha média após infecção repetida.
- Fibrose por doença hereditária chamada otosclerose.
- Hipercrescimento ósseo até as bordas da janela oval, fazendo com que a placa do
estribo fique anquilosada.
Cap. 54 – Funções Motoras da Medula Espinhal; os Reflexos Espinhais
A informação sensorial gera respostas que tem início na medula espinhal, com reflexos
musculares simples, estende-se ao tronco cerebral com respostas mais complexas e,
finalmente, vai ao prosencéfalo, onde as habilidades musculares são controladas.
Sem os circuitos neuronais especiais da medula, mesmo os sistemas se controle motor
mais complexos no encéfalo não poderiam gerar qualquer movimento muscular
intensional – o encéfalo simplesmente envia sinais de comando à medula espinhal para
iniciar o processo de movimento (andar, por exemplo).
O encéfalo gera os programas que controlam as atividades seqüenciais da medula –
promovendo movimentos finos, inclinando o corpo para frente na aceleração, etc.
Animal espinhal: a medula é transeccionada, geralmente aos níveis cervicais, de modo
que a maior parte da mesma permanece funcional; a maioria das funções abaixo da
transecção fica gravemente diminuída, sendo que após algum tempo, a maior parte das
funções intrínsecas retorna a um padrão quase normal.
Animal descerebrado: o tronco cerebral é transeccionado no nível médio ou inferior do
mesencéfalo; os sinais inibitórios normais dos centros de controle superiores do encéfalo
para os núcleos pontinos e vestibulares de controle muscular são bloqueados; isso faz
com que esses núcleos se tornem tonicamente ativos, transmitindo sinais facilitatórios
para a maior parte dos circuitos de controle motor da medula espinhal, tornando os
reflexos motores espinhais muito excitáveis, sendo ativados mesmo pelos mais fracos
sinais sensoriais aferentes para a medula espinhal.
A substância cinzenta da medula espinhal é a área integrativa para os reflexos espinhais,
sendo que os sinais entram na medula através das raízes sensoriais posteriores,
trafegando então por duas vias: um ramo do nervo sensorial termina na substância
cinzenta, provocando os reflexos espinhais segmentares locais e outro ramo transmite
sinais para níveis superiores na própria medula e para o tronco cerebral (ou córtex).
31
Cada segmento da medula espinhal possui milhões de neurônios, de dois tipos:
1. Neurônios motores anteriores: localizados nos cornos anteriores da substância cinzenta
medular, dão origem às fibras nervosas que deixam a medula através das raízes
ventrais e inervam as fibras musculares esqueléticas – tipos α e γ.
1.1) α: dão origem às fibras nervosas motoras grandes (tipo Aα), que se ramificam no
músculo e inervam as grandes fibras musculares esqueléticas; a estimulação de
uma fibra nervosa α excita muitas fibras musculares esqueléticas, sendo esse
conjunto chamado unidade motora.
1.2) γ: localizam-se nos cornos anteriores da medula espinhal e transmitem impulsos
através das fibras nervosas motoras (tipo Aγ), que inervam as fibras musculares
esqueléticas especiais (fibras intrafusais), que constituem o centro do fuso
muscular, que auxilia no tônus muscular básico.
2. Interneurônios: presentes em todas as áreas da substância cinzenta medular,
apresentam muitas interconexões entre si e muitas delas fazem sinapse diretamente
com os neurônios motores anteriores, sendo essas conexões responsáveis pela maioria
das funções integrativas da medula espinhal.
Poucos sinais sensoriais aferentes provenientes dos nervos espinhais ou sinais do encéfalo
terminam diretamente sobre os neurônios motores anteriores; quase todos são
transmitidos primeiramente aos interneurônios, onde são processados.
Células de Renshaw: neurônios localizados na medula espinhal em associação com
neurônios motores, transmitindo sinais inibitórios aos mesmos (inibição lateral), os quais
possibilitam a transmissão do sinal na direção desejada, suprimindo seu escape lateral.
Fibras proprioespinhais: maioria das fibras ascendentes e descendentes da medula,
utilizadas nos reflexos multissegmentares, incluindo os reflexos que coordenam os
movimentos simultâneos dos membros superiores e inferiores.
O controle da função muscular requer não só a excitação do músculo, mas também a
retroalimentação contínua da função sensorial de cada um deles para a medula espinhal,
indicando seu estado funcional a cada instante; para fornecer essas informações, os
músculos são supridos com dois tipos de receptores sensoriais.
1. Fusos musculares: estão distribuídos no ventre do músculo e enviam informações para
o SN sobre o comprimento do músculo ou a velocidade de mudança do comprimento.
Constituído de 3 a 12 fibras intrafusais, ligadas às extrafusais, funcionando a região
central desta, que não se contrai (sem actina e miosina), como um receptor sensorial,
que pode ser excitado por aumento do comprimento do músculo (estiramento da
região central) e por contração das regiões terminais das fibras intrafusais
(estiramento da região central).
Existem dois tipos de terminações sensoriais, os primários (receptor anuloespiral), que
são fibras nervosas do tipo Ia e os secundários, fibras tipo II, que se espalham mais.
Há dois tipos de fibras intrafusais no fuso muscular: fibras musculares com saco
nuclear, nas quais os núcleos da fibra muscular estão reunidos em sacos expandidos
até a área receptora e fibras com cadeia nuclear, que tem os núcleos alinhados em
cadeia através da área receptora.
As terminações primárias são excitadas por ambas as fibras, já as secundárias,
somente pelas fibras com cadeia nuclear.
Resposta estática: aumento do número de impulsos transmitidos às terminações
quando a região receptora do fuso é estirada lentamente, significando que ambas as
terminações continuam a transmitir seus sinais, enquanto o fuso estiver estirado.
Resposta dinâmica: quando o comprimento do fuso aumenta rapidamente, a
terminação primária é estimulada forte e seletivamente; se o comprimento pára de
aumentar, a freqüência de descarga de impulsos retorna ao nível normal e, se o fuso
encurta, ocorrem sinais opostos.
Os neurônios motores γ são divididos em dois tipos: γ-dinâmico, que excita as fibras
intrafusais com saco nuclear e o γ-estático, que excita as fibras com cadeia nuclear.
Reflexo de estiramento muscular: sempre que um músculo é estendido rapidamente, a
excitação dos fusos causa a contração reflexa das fibras musculares esqueléticas
extrafusais do próprio músculo e dos sinérgicos relacionados.
32
Uma via monossináptica (com uma fibra do tipo Ia), no reflexo de estiramento,
possibilita que o sinal reflexo retorne ao músculo, com o menor atraso possível, após a
excitação do fuso; já as fibras tipo II terminam em interneurônios, ao quais
transmitem sinais com um retardo para os neurônios motores anteriores.
O reflexo de estiramento pode ser dividido em dois componentes: reflexo de
estiramento dinâmico, causado por estiramentos ou encurtamentos rápidos, mandando
um sinal forte à medula espinhal e o reflexo de estiramento estático, mais fraco, que
continua por tempo prolongado após o término do dinâmico, mantendo o grau de
contração constante.
A principal função do reflexo de estiramento é a de amortecimento, suavisando as
contrações musculares, mesmo que os sinais primários sejam bruscos (pró-mediação).
Co-ativação: sempre que os sinais são transmitidos do córtex ou outras áreas do
encéfalo pra os neurônios motores alfa, os neurônios motores gama são estimulados
simultaneamente, fazendo com que as fibras intra e extrafusais se contraiam ao
mesmo tempo, impedindo a alteração do comprimento da função receptora do fuso (
impedindo que o reflexo do mesmo se oponha à contração muscular) mantendo a
função de amortecimento do fuso muscular.
O sistema eferente gama é estimulado por sinais provenientes da região facilitatória
bulborreticular do tronco cerebral e, secundariamente, por impulsos transmitidos para
a área bulborreticular a partir do cerebelo, gânglios da base e córtex cerebral.
O sistema do fuso muscular estabiliza a posição do corpo durante qualquer ação
motora tensa; para isso, sinais excitatórios são transmitidos através das fibras
nervosas gama para as fibras musculares intrafusais, encurtando as terminações dos
fusos e estirando as regiões receptoras centrais, aumentando seu sinal de saída.
Um método usado para determinar a sensibilidade dos reflexos de estiramento é
provocar um reflexo patelar, o qual estira o quadríceps, ativando o reflexo de
estiramento dinâmico, projetando a perna para frente.
Os abalos musculares são utilizados para avaliar o grau de facilitação dos centros da
medula espinhal, sendo que grandes lesões nas áreas motoras corticais (provocadas
por derrames e tumores cerebrais) provocam reflexos de estiramento muscular
exagerados no lado oposto do corpo.
Clônus: abalo muscular que oscila em certas condições; ocorre quando o reflexo de
estiramento está muito sensibilizado pelos impulsos facilitatórios provenientes do
cérebro; num animal descerebrado, o clônus se desenvolve rapidamente (os reflexos
de estiramento estão muito facilitados).
2. Órgãos tendinosos de Golgi: localizados nos tendões musculares, transmitindo
informações sobre a tensão do tendão ou a velocidade de alteração nessa tensão.
São receptores sensoriais encapsulados, através dos quais passam fibras tendinosas
musculares, sendo estimulados quando essas fibras são tensionadas pela contração ou
pelo estiramento do músculo.
A principal diferença entre a excitação deste órgão e a do fuso é que o fuso detecta o
comprimento do músculo e as alterações no seu comprimento, enquanto o órgão
tendinoso detecta a tensão do músculo refletida no próprio tendão.
Quando os órgãos tendinosos de Golgi de um tendão muscular são estimulados por um
aumento da tensão em um músculo relacionado, os sinais são transmitidos para a
medula espinhal produzindo os efeitos reflexos no respectivo músculo, sendo os
mesmos inibitórios, o que previne o desenvolvimento de uma tensão excessiva.
Reação de alongamento: quando a tensão no tendão torna-se extrema, o efeito
inibitório do órgão tendinoso pode ser muito grande e levar a um relaxamento
instantâneo do músculo (previne o rompimento de músculos e tendões).
Tanto os fusos quanto os órgãos tendinosos informam os centros de controle motor
superiores das alterações instantâneas que ocorrem nos músculos.
Reflexo flexor: contração dos músculos flexores de um membro estimulado, provocando a
retirada deste do objeto estimulador (quase todos os estímulos sensoriais cutâneos
provocam esse reflexo do animal espinhal ou descerebrado).
33
Esse reflexo é mais provocado pela estimulação das terminações para dor (reflexo
nociceptivo/reflexo à dor), no entanto a estimulação dos receptores para tato também
podem provocá-lo, embora mais fraco e menos prolongado.
Circuito do reflexo flexor: circuitos diversos para propagar o reflexo para os músculos
necessários para a retirada – circuitos para a inibição dos músculos antagonistas (circuitos
de inibição recíproca) – circuitos que promovem a pós-descarga após o fim do
estiramento (duram frações de segundo depois).
Reflexo extensor cruzado: extensão do membro oposto pouco tempo após o estímulo
provocar um reflexo flexor em um membro, podendo empurrar todo o corpo para longe do
estímulo doloroso ao membro.
Muitos interneurônios estão envolvidos no circuito entre os neurônios sensoriais aferentes
e os neurônios motores do lado oposto, responsáveis pela extensão cruzada (justifica o
tempo envolvido entre o reflexo flexor e o extensor).
Reação de suporte positivo (sustentação positiva): uma pressão aplicada no coxim plantar
de um animal descerebrado faz com que o membro se estenda contra a pressão, sendo a
reação suficiente para enrijecer os membros de modo que suportem o peso do corpo; tal
reação envolve um circuito complexo de interneurônios e ajuda a impedir que o animal
caia (reação magnética).
Reflexo espinhal de endireitamento: quando um animal espinhal é deitado sobre um dos
lados do corpo, ele fará movimentos não coordenados tentando ficar em pé,
demonstrando que alguns reflexos relativamente complexos associados à postura são
interados na medula espinhal.
Animais espinhalizados podem realizar funções de marcha individuais em cada membro, o
que pode resultar dos circuitos de inibição mutuamente recíprocos dentro da matriz da
medula espinhal, oscilando entre neurônios que controlam os agonistas e antagonistas.
Reflexo de tropeço: se o topo do pé encontra uma obstrução durante um impulso para a
frente, parará por um tempo e, numa sequência rápida, o pé será erguido mais alto e
seguirá para a frente para ser colocado sobre a obstrução.
Reflexo da marcha: se um animal espinhalizado é colocado acima do chão com as pernas
pendentes, o estiramento dos membros pode levar a uma marcha diagonal entre os
membros anteriores e posteriores (manifestação da inervação recíproca).
Reflexo de galope: ocorre no animal espinhalizado, fazendo com que os membros
anteriores se movam para trás e, em harmonia, os membros posteriores se movam para
frente; ocorre quando estímulos de pressão e estiramento quase iguais são aplicados aos
membros de ambos os lados do corpo ao mesmo tempo.
Reflexo de coçar: deflagrado pela sensação de coceira ou cócega e envolve duas funções:
a sensação de posição que possibilita que a pata encontre o local exato da irritação sobre
a superfície do corpo e o movimento de vaivém de coçar (inervação recíproca).
Alguns espasmos musculares são observados em humanos, devido à dor localizada:
Resultante de um osso quebrado: resulta de impulsos dolorosos iniciados nas bordas
quebradas do osso, o que faz com que os músculos que envolvem a área se contraiam
tonicamente (podem ser abrandados com anestésicos, permitindo o retorno do osso).
Do músculo abdominal na peritonite: resulta da irritação do peritônio parietal,
ocorrendo, igualmente, durante operações cirúrgicas abdominais (impulsos de dor
fazem com que os músculos abdominais de contraiam); diminuído com o alívio da dor.
Cãibra muscular: qualquer fator irritante local ou anormalidade metabólica de um
músculo (frio intenso, ausência de fluxo sanguíneo, excesso de exercício) pode
provocar dor ou outros sinais sensoriais transmitidos do músculo à medula espinhal,
levando a contração do músculo por retroalimentação reflexa.
Reflexo em massa: a medula espinhal pode tornar-se rápida e excessivamente ativa,
provocando uma descarga maciça em grandes porções da mesma, sendo o estímulo
desencadeante uma dor forte na pele ou o enchimento excessivo de uma víscera; os
efeitos são: espasmo flexor de importantes músculos esqueléticos do corpo, evacuação do
cólon e esvaziamento vesical, aumento da pressão arterial, sudorese intensa; resulta da
ativação de circuitos reverberantes, se assemelhando a convulsões epiléticas.
34
Choque espinhal: a transecção abrupta da medula espinhal nos níveis cervicais altos
diminui imediatamente as funções da mesma, incluindo os reflexos espinhais, devido á
dependência dos neurônios pela excitação tônica contínua das descargas das fibras.
Os neurônios espinhais retomam sua excitabilidade após um tempo aumentando a sua
própria para suprir parcialmente a perda; nos humanos essa função pode nunca ser
recuperada ou a recuperação pode ser excessiva, resultando em hiperexcitabilidade de
algumas funções da medula, como:
A pressão arterial, que cai drasticamente, retorna ao normal em poucos dias.
Os reflexos musculares esqueléticos podem tornar-se hiperexcitáveis, sendo os
primeiros a retornar os reflexos de estiramento, seguidos pelos mais complexos
(flexores, antigravitacionais posturais e remanescentes dos de marcha).
Os reflexos sacrais para o controle da evacuação do cólon e esvaziamento da bexiga
são suprimidos, mas acabam retornando.
Cap. 55 – Controle Cortical e do Tronco Cerebral sobre a Função Motora
A maioria dos movimentos voluntários iniciados pelo córtex cerebral é obtida quando ele
ativa padrões de função armazenados nas áreas cerebrais inferiores (medula, tronco,
núcleos da base e cerebelo), os quais enviam sinais de controle específicos aos músculos.
Para alguns tipos de movimento (movimentos finos e com a destreza de mãos e dedos) o
córtex tem quase uma via direta dirigida aos neurônios motores anteriores da medula.
O córtex é dividido em 3 subáreas, cada uma com sua representação e função:
1. Córtex motor primário: mais da metade dele está relacionada ao controle dos
músculos das mãos e da fala, tendo, também representações topográficas da região da
face e da boca (fissura de Sylvius), braço e mão (parte média), tronco (ápice) e perna
e pé (fissura longitudinal).
2. Área pré-motora: os sinais neurais gerados nessa área causam padrões muito mais
complexos de movimento que no córtex primário, desenvolvendo primeiro uma
imagem motora do movimento a ser realizado e, posteriormente, excitando o padrão
de atividade muscular; a organização topográfica é praticamente a mesma do córtex
primário, com as áreas da boca e face mais lateralmente e, indo em direção caudal,
são encontradas áreas da mão, braço, tronco e perna.
3. Área motora suplementar: as contrações desencadeadas por estimulação dessa área
costumam ser bilaterais (agarrar com ambas as mãos); funciona em conjunto com a
área pré-motora gerando movimentos responsáveis pela postura corporal, movimentos
de fixação de seguimentos do corpo e de posição da cabeça e olhos.
Regiões altamente especializadas no córtex humano controlam funções específicas:
Área de broca: área pré-motora de formação das palavras; sua lesão não impede a
vocalização, mas torna o indivíduo incapaz de falar palavras inteiras.
Campo de movimentos oculares voluntários: localizado acima da área de broca,
também controla movimentos de piscar; lesões impedem a movimentação voluntária
dos olhos (tendem a travar em objetos específicos).
Área de rotação da cabeça: acima da área de movimentos oculares, relacionando-se
diretamente a eles, está esta área, que direciona a cabeça em direção a objetos.
Área para habilidades manuais: quando essa área é lesada, os movimentos manuais
ficam sem coordenação e sem propósito (apraxia motora).
Os sinais motores são transmitidos diretamente do córtex para a medula, por duas vias:
1. Trato corticoespinhal (piramidal): é a via de saída mais importante do córtex,
atravessando o ramo posterior da cápsula interna, descendo pelo tronco cerebral
(formando as pirâmides da medula oblonga); a maior parte das fibras cruza, então, na
parte inferior do bulbo para o lado oposto e desce pelos tratos corticoespinhais laterais
da medula, terminando nos interneurônios da substância cinzenta da medula ou em
neurônios sensoriais de segunda ordem no corno dorsal; algumas fibras não cruzam,
passando ipsilateralmente, formando os tratos corticoespinhais ventrais da medula;
muitas dessas fibras cruzam, podendo estar relacionadas ao controle de movimentos
posturais bilaterais pelo córtex motor suplementar; algumas fibras grandes e
35
mielinizadas originam-se nas células piramidais gigantes (células de Betz) e
transmitem impulsos nervosos à medula numa velocidade de 70m/s, a maior
velocidade de transmissão de qualquer sinal do cérebro.
2. Outras vias: o córtex dá origem a muitas fibras adicionais que vão para regiões
subcorticais telencefálicas e do tronco cerebral, incluindo:
2.1) Axônios das células de Betz – enviam sinais colaterais curtos de volta ao córtex.
2.2) Fibras que se dirigem ao núcleo caudado e putame – controlam músculos posturais.
2.3) Fibras motoras para os núcleos rubros – a partir deles, fibras descem para a
medula pelo trato rubroespinhal.
2.4) Fibras motoras para a substância reticular e núcleos vestibulares do tronco – daí
sinais vão para a medula pelos tratos reticulo e vestibuloespinhal e, para o
cerebelo, pelos tratos reticulo e vestibulocerebelar.
2.5) Fibras motoras que fazem sinapse na ponte – dão origem às fibras
pontocerebelares, que carregam sinais aos hemisférios cerebelares.
2.6) Colaterais que terminam nos núcleos Olivares inferiores – daí fibras
olivocerebelares secundárias transmitem sinais para o cerebelo.
O córtex motor recebe a informação e opera em associação com os núcleos da base e
cerebelo para dar seguimento ao curso da ação motora, por meio de vias aferentes:
1. Fibras subcorticais de regiões adjacentes do córtex cerebral (áreas somatossensoriais
do córtex parietal, áreas adjacentes do córtex frontal, córtices visual e auditivo).
2. Fibras subcorticais que chegam através do corpo caloso provenientes do hemisfério
cerebral oposto; conectam áreas homotópicas.
3. Fibras somatossensoriais que chegam diretamente do complexo ventrobasal do
tálamo; retransmitem sinais táteis cutâneos e sinais articulares e musculares.
4. Tratos dos núcleos ventrobasal e ventroanterior do tálamo que recebem sinais do
cerebelo e dos núcleos da base.
5. Fibras dos núcleos intralaminares do tálamo; controlam o nível de excitabilidade do
córtex motor e da maioria das outras regiões.
O núcleo rubro funciona em associação ao trato corticoespinhal, recebendo grande
número de fibras diretas do córtex motor (trato corticorrubral) e seguindo o trajeto à
medula espinhal (trato rubroespinhal), terminando na substância cinzenta da mesma.
A via corticorrubroespinhal serve como rota acessória para a transmissão de sinais
discretos do córtex motor para a medula espinhal, sendo que na destruição das fibras
corticoespinhais alguns movimentos discretos são mantidos (punho).
Os tratos cortico e rubroespinhais são chamados sistema motor lateral da medula,
distinguindo-se do sistema vestibulorreticuloespinhal (sistema motor medial da medula).
Sistema extrapiramidal: denota as partes do cérebro e do tronco que contribuem para o
controle motor, sem fazer parte do sistema corticoespinhal-piramidal direto (vias pelos
núcleos da base, formação reticular do tronco, núcleos vestibulares e núcleo rubro).
As células do córtex motor são organizadas em colunas verticais de células, sendo que
cada uma estimula um grupo de músculos sinérgicos ou apenas um; esta disposição
permite uma amplificação para estimular um grande número de fibras.
Se um sinal forte for enviado a um músculo para contração rápida, um sinal contínuo mais
fraco pode manter a contração por longos períodos; para isso cada coluna de células
excita duas populações de neurônios, estáticos (lentos) e dinâmicos (rápidos).
Quando os sinais neuronais do córtex motor causam uma contração muscular, sinais
somatossensoriais (originados nos fusos, órgãos tendinosos dos tendões e receptores
táteis da pele) retornam o caminho da região ativada do corpo para os neurônios no
córtex motor, causando retroalimentação positiva da contração muscular (intensificam).
Acidente Vascular Cerebral: o chamado derrame pode lesar o sistema de controle motor
por uma ruptura de vaso que sangra no cérebro ou por trombose de uma artéria principal
deste; o resultado é a perda da irrigação para o córtex ou trato corticoespinhal, no ponto
que atravessa a cápsula interna entre o núcleo caudado e o putame.
A remoção de uma parte do córtex motor primário causa graus variáveis de paralisia nos
músculos representados; se o núcleo caudado subjacente e as áreas motoras
suplementares adjacentes não forem lesadas, ainda poderão ocorrer movimentos
36
posturais grosseiros e fixação de extremidades, embora haja perda do controle voluntário
de movimentos discretos dos segmentos distais das extremidades (mãos e dedos).
Hipotonia: remoção do efeito estimulador tônico e contínuo que o córtex primário exerce
sobre os neurônios motores da medula espinhal.
O tronco cerebral (formado por bulbo, ponte e mesencéfalo) é como uma extensão da
medula, realizando funções motoras sensoriais do mesmo modo que ela, porém é
responsável por muitas funções especiais, controlando a respiração, o sistema
cardiovascular, a função gastrointestinal (parcialmente), movimentos estereotipados do
corpo, equilíbrio e movimentos oculares.
Dois grupos de núcleos reticulares funcionam de maneira antagônica:
1. Sistema reticular pontino: os núcleos transmitem sinais excitatórios descendentes para
a medula espinhal através do trato reticuloespinhal pontino, terminado em neurônios
motores anteriores que excitam músculos axiais (que sustentam o corpo – da coluna
vertebral e extensores das extremidades.
2. Sistema reticular bulbar: os núcleos transmitem sinais inibitórios aos mesmos
neurônios motores anteriores antigravitários pelo trato reticuloespinhal bulbar.
Os núcleos vestibulares funcionam em associação aos núcleos reticulares pontinos para
controlar os músculos antigravitários, através da transmissão de fortes sinais excitatórios
por meio dos tratos vestibuloespinhais lateral e medial.
Rigidez de descerebração: ocorre em músculos antigravitários (do pescoço e extensores
da pata), devido ao bloqueio da interferência para os núcleos reticulares bulbares a partir
do córtex, núcleos rubros e da base.
Sistema vestibular: órgão sensorial que detecta sensações de equilíbrio, estando
encerrado num sistema de tubos e câmaras ósseas, localizado na parte petrosa do osso
temporal (labirinto ósseo), englobando um sistema de tubos e câmaras membranosos
(labirinto membranoso).
Mácula: localizada dentro de cada utrículo (plano horizontal), determina a orientação da
cabeça quando em posição ereta, e dentro de cada sáculo (plano vertical), onde sinaliza a
orientação da cabeça quando o indivíduo está deitado.
As máculas são cobertas por estatocônias (cristais de carbonato) e por células ciliadas,
com muitos estereocílios ligados a um grande quinocílio, de modo que quando este se
curva, os estereocílios fazem o mesmo, abrindo muitos canais na membrana celular
neuronal, conduzindo íons positivos para o interior da célula, causando despolarização da
membrana do receptor (o movimento ao contrário gera hiperpolarização).
Os ductos semicirculares (anterior, posterior e lateral) são dispostos em ângulos retos
entre si, de modo que, quando a cabeça da pessoa gira em qualquer direção, a inércia do
líquido (endolinfa) em um ou mais ductos semicirculares faz com que o mesmo
permaneça estacionário, enquanto o ducto gira; assim, o líquido flui, atravessa a ampola,
deforma a cúpula para um lado, orientando os quinocílios da mesma forma e causando a
despolarização das células (ou hiperpolarização, se para o lado oposto); sinais são então
enviados das células ciliadas ao SNC (pelo nervo vestibular), informando sobre a mudança
da rotação da cabeça e a velocidade com que isso ocorreu.
Quando o corpo é subitamente empurrado para frente, as estatocônias caem para trás
nos cílios das células ciliadas e a informação de desequilíbrio é enviada aos centros
nervosos (sente como se estivesse caindo para trás), fazendo com que o indivíduo se
incline para frente (até que o equilíbrio se restabeleça).
Quando a rotação da cabeça pára, a endolinfa continua a circular, enquanto o ducto pára.
O mecanismo do ducto circular prediz se o desequilíbrio vai ocorrer, fazendo com que os
centros do equilíbrio realizem ajustes preventivos antecipatórios apropriados.
A remoção dos lobos floculonodulares do cerebelo impede a detecção normal de sinais do
ducto (perda do equilíbrio dinâmico durante alterações rápidas de movimento), embora
tenha pouco efeito em detectar sinais maculares.
Quando a cabeça é rodada subitamente, sinais dos ductos fazem com que os olhos rodem
numa direção igual e oposta à rotação da cabeça, resultando em reflexos transmitidos
pelos núcleos vestibulares e fascículo longitudinal medial aos núcleos oculomotores.
37
Quando a cabeça está inclinada numa direção por curvatura do pescoço, impulsos dos
proprioceptores cervicais impedem os sinais originados no aparelho vestibular de dar à
pessoa um senso de desequilíbrio (ao contrário de quando todo o corpo se vira).
Se o aparelho vestibular é destruído ou ocorre perda das informações proprioceptivas, o
indivíduo pode ainda usar os mecanismos visuais para manter o equilíbrio, uma vez que o
movimento corporal muda as imagens visuais da retina, transmitindo as informações aos
centros do equilíbrio (de olhos fechados, o equilíbrio é imediatamente perdido).
Anencefalia: ocorre quando um bebê nasce sem estruturas cerebrais acima da região
mesencefálica, sendo capaz (por meses) de realizar movimentos estereotipados
(integradas no tronco cerebral) para alimentar-se (suga, expulsa alimento desagradável,
chupa os dedos), podendo bocejar, esticar-se, seguir objetos com olhos, chorar e se
esforçar para sentar.
Cap. 56 – Contribuições do Cerebelo e dos Núcleos da Base para o Controle
Motor Global
Além do córtex cerebral, duas outras áreas são essenciais para a função motora normal:
cerebelo e núcleos (gânglios) da base, funcionando em associação com outros sistemas.
Cerebelo:
Chamado área silenciosa do cérebro por não ter qualquer reação consciente à excitação
elétrica, contudo sua remoção torna os movimentos corporais anormais.
É especialmente vital na coordenação motora de atividades musculares rápidas (correr,
digitar, tocar piano e conversar), embora sua perda não cause paralisia muscular; não
causa contração, mas faz ajustes corretivos nas atividades motoras corporais.
Recebe, a partir de áreas de controle motor, informações sobre a sequência de contrações
musculares desejada e informações sensoriais das partes periféricas do corpo, informando
sobre mudanças sequenciais da situação de cada parte do corpo (posição, velocidade,
movimento, forças que atuam sobre ele), então compara os movimentos reais com os
originalmente programados pelo sistema motor; se houver discrepância, sinais corretivos
são enviados de volta às estruturas envolvidas no controle motor.
Ajuda o córtex, também, a planejar o próximo movimento seqüencial, enquanto o
movimento atual ainda está sendo executado, aprendendo com os erros, ou seja, se o
movimento não sai como o planejado ele aprende a fazer mais forte ou fraco da próxima
vez, através de alterações na excitabilidade de neurônios cerebelares apropriados,
fazendo contrações musculares subseqüentes correspondendo ao movimento pretendido.
Divide-se em 3 lobos: anterior, posterior e floculonodular, sendo este último a parte mais
antiga, atuando no controle do equilíbrio corporal; possui uma faixa estreita abaixo do
centro chamada vérmis, onde estão localizadas as funções para movimentos musculares
do corpo axial, pescoço, ombros e quadris; ao lado do vérmis estão a zona intermediária
(controle das contrações de mãos, dedos, pés e artelhos) e a zona lateral (se une ao
córtex no planejamento global de movimentos motores sequenciais).
As grandes partes laterais não têm representações topográficas do corpo, recebendo seus
sinais aferentes do córtex e desempenhando papéis importantes no planejamento e
coordenação das atividades musculares sequenciais rápidas do corpo.
Via corticopontocerebelar: se origina nos córtices motor e pré-motor cerebrais e no córtex
somatossensorial cerebral; passa por núcleos pontinos e tratos pontocerebelares para as
divisões laterais dos hemisférios cerebelares contralaterais às áreas cerebrais.
Tratos aferentes importantes se originam a cada lado do tronco encefálico:
1. Trato olivocerebelar: origina-se na oliva superior e dirige-se a todas as partes do
cerebelo, sendo ativado na sua origem por fibras do córtex motor cerebral, dos
gânglios da base e várias regiões da formação reticular e medula espinhal.
2. Fibras vestibulocerebelares: se originam no aparelho vestibular e núcleos vestibulares
do tronco encefálico, terminando no lobo floculonodular e núcleo fastigial do cerebelo.
3. Fibras reticulocerebelares: se originam em diferentes porções da formação reticular do
tronco encefálico e terminam nas áreas medianas cerebelares (vérmis).
38
Recebe sinais sensoriais importantes das partes periféricas do corpo, principalmente
através dos tratos espinocerebelar dorsal e ventral, sendo que os sinais do dorsal
notificam o cerebelo sobre condições momentâneas de contração muscular, grau de
tensão sobre os tendões, posições e velocidades de movimento das diferentes partes do
corpo e forças que agem sobre a superfície do mesmo; já o ventral é excitado
principalmente por sinais motores que chegam aos cornos anteriores da medula vindos do
encéfalo e medula (cópia de eferência).
Os núcleos cerebelares profundos (dentado, interpósito e fastigial) recebem sinais do
córtex cerebelar e dos tratos sensoriais profundos aferentes para o cerebelo.
Os sinais que chegam ao cerebelo sempre seguem duas direções: para os núcleos
profundos ou para uma área correspondente do córtex cerebelar que recobre um núcleo,
sendo que todos acabam terminando nos núcleos profundos.
As grandes vias aferentes que levam sinais efetores do cerebelo são:
1. Via que se origina no vérmis, passa pelos núcleos fastigiais e vai para regiões bulbares
e pontinas do tronco: controle do equilíbrio e postura.
2. Via que segue o caminho – zona intermediária – núcleo interpósito – núcleos
ventrolateral e ventroanterior do tálamo – córtex cerebral – linha média do tálamo –
núcleos da base – núcleo rubro e formação reticular do tronco: contração recíproca de
agonistas e antagonistas nas extremidades.
3. Via que começa no córtex cerebelar da zona lateral, passa aos núcleos dentado,
ventrolateral e ventroanterior do tálamo, terminando no córtex cerebral: coordena
atividades motoras seqüenciais iniciadas pelo córtex cerebral.
O córtex cerebelar tem três grandes camadas: molecular, de células de Purkinje e de
células granulosas, sendo que abaixo delas estão os núcleos profundos que enviam sinais
de saída, que partem de uma célula nuclear profunda e aferem ao cerebelo por fibras
trepadeiras (chegam à camadas externas do córtex cerebelar) e musgosas (vão até as
células granulosas do córtex, as quais enviam axônios à camada molecular externa dele).
A estimulação direta das células nucleares profundas pelas diferentes fibras provoca sua
excitação, já os sinais que chegam às células de Purkinje as inibem; esse mecanismo de
feedback impede que o movimento muscular ultrapasse a dimensão programada.
Outras células são ainda encontradas no cerebelo: em cesto e estreladas, situadas na
camada molecular do córtex, causando inibição lateral das células de Purkinje.
O cerebelo ajuda a emitir sinais rápidos de ligar para músculos agonistas e de desligar
recíproco para antagonistas no início do movimento, sendo que no fim do mesmo, os
sinais são emitidos de maneira oposta (os mecanismos desse processo são especulativos).
Quando um novo ato motor é realizado, o grau de realce motor pelo cerebelo no início das
contrações e a temporização das mesmas são quase sempre incorretos para o
desempenho preciso do movimento, no entanto, após o ato se repetir muitas vezes, os
eventos se tornam cada vez mais precisos.
As fibras em trepadeira enviam sinais de erro ao cerebelo, alternado a sensibilidade das
células de Purkinje, o que faz com que a temporização e outros aspectos do controle
cerebelar dos movimentos se aproximem da perfeição.
O SN usa o cerebelo para coordenar funções de controle motor em 3 níveis:
1. Vestibulocerebelo: consiste em pequenos lobos floculonodulares e proporciona circuitos
neurais para a maioria dos movimentos associados ao equilíbrio do corpo.
Importante para controlar movimentos rápidos e que envolvem alteração de direção;
sinais da periferia permitem a ele calcular antecipadamente o próximo movimento,
fazendo a correção antecipatória dos sinais motores posturais.
2. Espinocerebelo: consiste na maior parte do vérmis e zonas intermediárias adjacentes,
fornecendo circuitos para a coordenação dos movimentos das extremidades distais.
Responsável por comparar os movimentos realizados com as intenções dos níveis mais
altos do sistema de controle motor.
3. Cerebrocerebelo: formado pelas zonas laterais, funcionando em um modo de feedback
com o sistema sensoriomotor cortical para planejar movimentos voluntários
seqüenciais do corpo e extremidades (desenvolvimento de imagens motoras).
39
Faz o planejamento dos movimentos seqüenciais e a temporização dos mesmos além
de temporizar movimentos eventos que não os movimentos do corpo, como as taxas
de progressão de fenômenos auditivos e visuais (a pessoa pode predizer, pela
alteração da cena visual, com que rapidez pode se aproximar de um objeto).
Tremor de ação (tremor intencional): uma pessoa cujo cerebelo tenha sido destruído tem
uma tendência a passar do alvo durante os movimentos pendulares (do braço, por
exemplo), o que leva os centros conscientes do telencéfalo a iniciar um movimento na
direção oposta, fazendo com que o braço oscile, para frente e para trás, passando do
movimento pretendido por vários ciclos antes de finalmente se fixar em sua marca.
Sistema de amortecimento: se o cerebelo estiver intacto, sinais subconscientes param o
movimento precisamente no ponto pretendido, impedindo a ultrapassagem do alvo e o
tremor.
Movimentos balísticos: a maioria dos movimentos rápidos do corpo (movimento dos dedos
ao digitar) tem de ser inteiramente pré-planejados antes de serem colocados em
execução, já que são rápidos demais para receber informações de feedback.
Quando o cerebelo é retirado ocorrem alterações nos movimentos balísticos: têm
desenvolvimento lento, sem onda de início extra, a força desenvolvida é fraca e há uma
demora para desligar os movimentos, permitindo que passem além do alvo pretendido.
As lesões cerebelares causam falha na progressão suave dos movimentos, fazendo com
que movimentos complexos (escrever, correr, conversar) fiquem sem coordenação.
A destruição de até metade do córtex cerebelar lateral não afeta as funções motoras do
animal, desde que os núcleos cerebelares profundos sejam mantidos e os movimentos
sejam realizados de forma lenta; algumas anormalidades cerebelares são:
Dismetria e Ataxia: movimentos sem coordenação, que passam da marca pretendida,
são chamados ataxia, os quais são compensados excessivamente na direção oposta,
pela parte consciente do cérebro, resultando em dismetria; podem resultar de lesões
nos tratos espinocerebelares.
Passar do ponto: o cerebelo inicia a maior parte dos sinais motores que terminam o
movimento depois que ele é começado, portanto se este estiver ausente, a pessoa
movimenta a mão ou outras partes do corpo além do ponto de intenção.
Deficiências de progressão:
1. Disdiadococinesia – série de movimentos fracionados e atrapalhados em lugar de
movimentos coordenados normais de pronação e supinação, devido a incapacidade
do controle motor de predizer onde as diferentes partes do corpo estarão num dado
momento (perde-se a percepção das partes durante movimentos rápidos), não
ocorrendo a progressão do movimento de forma organizada.
2. Disartria – falha de progressão ao falar, porque a formação de palavra depende de
uma sucessão rápida e organizada de movimentos musculares individuais na
laringe, boca e sistema respiratório, causando vocalização confusa.
Tremor intencional: resulta de ultrapassagem cerebelar do alvo e falha desse sistema
em amortecer os movimentos, quando uma pessoa que perdeu o cerebelo tenta fazer
um movimento voluntário (os mesmos oscilam).
Nistagmo cerebelar: tremor do globo ocular que ocorre geralmente quando se tenta
fixar os olhos numa cena num dos lados do campo visual, resultando em rápidos e
trêmulos dos olhos (falha do amortecimento pelo cerebelo); ocorre após lesões nos
lobos floculonodulares, associando-se, por isso, à perda de equilíbrio (disfunção das
vias dos ductos semicirculares que passam por essa região).
Hipotonia: diminuição do tônus da musculatura corporal periférica no lado da lesão
cerebelar (perda dos núcleos profundos, especialmente o dentado e o interpósito),
resultante da perda da facilitação cerebelar do córtex motor e dos núcleos motores do
tronco por sinais tônicos provenientes de núcleos cerebelares profundos.
Gânglios da Base:
Os núcleos da base constituem outro sistema motor acessório, que funciona em
associação com o córtex cerebral e com o sistema de controle motor corticoespinhal.
A cada lado do encéfalo os núcleos consistem em núcleo caudado, putâmen, globo pálido,
substância negra e núcleo subtalâmico.
40
Quase todas as fibras nervosas motoras e sensoriais, que ligam o córtex à medula,
atravessam o espaço entre o núcleo caudado e o putâmen, chamado cápsula interna.
Um dos principais papéis dos gânglios da base é, em associação ao sistema
corticoespinhal, controlar padrões complexos de atividade motora, como: escrever, cortar
com tesoura, bater pregos, arremessar uma bola, tirar sujeira com uma pá, vocalizar, etc.
Entre todos os circuitos neuronais dos gânglios da base, dá-se ênfase a dois:
1. Circuito do putâmen: as vias começam nas áreas pré-motora e suplementar do córtex
motor e nas somatossensoriais do córtex sensorial, seguem para o putâmen, globo
pálido e núcleos de retransmissão do tálamo, retornando finalmente ao córtex motor
primário e às áreas associadas a ele.
Quando uma parte do circuito é lesada ou bloqueada, alguns movimentos tornam-se
anormais, como:
- Lesões no globo pálido levam a movimentos de contorção espontâneos e muitas vezes
contínuos de uma mão, um braço, pescoço ou face (atetose).
- Uma lesão no subtálamo leva a movimentos súbitos e em bloco de uma extremidade
inteira (hemibalismo).
- Múltiplas pequenas lesões no putâmen levam a movimentos rápidos e abruptos de curta
extensão nas mãos, face e outras partes do corpo (coréia).
- Lesões na sibstância negra levam à rigidez, acinesia e trmores (doença de Parkinson).
2. Circuito do caudado: depois eu os sinais passam do córtex ao núcleo caudado, eles são
transmitidos ao globo pálido interno e depois aos núcleos de retransmissão do tálamo,
voltando, então às áreas do córtex (vão para regiões motoras acessórias, pré-motoras
e suplementares – responsáveis por padrões seqüenciais de movimento); recebe
grandes quantidades de suas aferências das áreas de associação do córtex cerebral,
que estão sobre ele.
O núcleo caudado desempenha papel importante no controle cognitivo da atividade
motora (ações motoras como consequência de pensamentos); são as funções
cognitivas que determinam subconscientemente quais padrões de movimento serão
usados para atingir um objetivo (fugir de um leão).
O córtex parietal posterior é uma área cortical especialmente importante, por ser o local
das coordenadas espaciais para controle motor de todas as partes do corpo e para a
relação deste e de suas partes com tudo que está em torno; a pessoa que não possui essa
área pode praticamente ignorar a existência da parte oposta do corpo (se não tem o lado
esquerdo, desconhece o direito).
Vários neurotransmissores específicos funcionam nos gânglios da base, como:
Dopamina – vias da substância negra para o núcleo caudado putâmen.
GABA – do núcleo caudado e putâmen para o globo pálido e substância negra.
Acetilcolina – do córtex para o núcleo caudado e putâmen.
Norepinefrina, serotonina, encefalina e outros – múltiplas vias gerais do tronco.
Glutamato – transmite sinais excitatórios que equilibram os muitos sinais inibitórios
(transmitidos pelo GABA, serotonina e dopamina).
Doenças importantes resultam de lesões em estruturas dos gânglios da base:
Doença de Parkinson: conhecida como paralisia agitante, é resultado da destruição da
pars compacta da substância negra, que envia fibras nervosas secretoras de dopamina
para o núcleo caudado e o putâmen; se caracteriza por rigidez muscular, tremor
involuntário das áreas envolvidas, mesmo em repouso (3 a 6 ciclos por segundo) e
dificuldade intensa de iniciar movimentos (acinesia); a causa dos efeitos motores pode
estar relacionada a destruição dos neurônios dopaminégicos (a dopamina é inibitória),
permitindo que núcleo caudado e putâmen ficassem muito ativos, excitando o sistema
de controle motor corticoespinhal.
- Tratamento com L-Dopa: é convertida no cérebro em dopamina (não atravessa a
barreira hematoencefálica), restaurando o equilíbrio normal entre os núcleos e
melhorando os sintomas de rigidez e acinesia.
- Tratamento com L-deprenil: inibe a monoamina oxidase, responsável pela destruição da
maior parte da dopamina depois de ser secretada, além de tornar mais lenta a destruição
dos neurônios secretores de dopamina (combinado com a L-Dopa é mais eficaz).
41
- Tratamento com células dopaminérgicas fetais transplantadas: é eficiente, porém por
curto período de tempo (as células vivem apenas alguns meses).
- Tratamento por destruição de parte do circuito de feedback nos gânglios da base:
tentativas de tratamento por bloqueio dos sinais anormais dos gânglios (lesões no núcleo
subtalâmico podem gerar bons resultados).
Doença de Huntington (Coréia de Huntington): distúrbio hereditário que começa a
causar sintomas a partir dos 30 anos e caracteriza-se por movimentos rápidos em
músculos individuais e depois movimentos graves progressivos de distorção do corpo
inteiro, além de causar demência grave; os movimentos anormais podem ser causados
pela perda de corpos celulares secretores de GABA (núcleo caudado e putâmen) e de
acetilcolina (muitas parte do cérebro), uma vez que esses neurônios inibem parte do
globo pálido e substância negra; a demência pode ser resultado da perda de neurônios
colinérgicos (córtex).
Existem diferentes níveis de controle para o controle global dos movimentos:
1. Nível espinhal: exibem padrões locais de movimento para todas as áreas musculares
do corpo (reflexos de retirada); e padrões complexos de movimentos rítmicos (andar).
2. Nível Rombencefálico: a ponte e o bulbo são responsáveis por manter o tônus axial do
corpo (postura em pé) e pela modificação do tônus nos músculos (equilíbrio).
3. Nível do córtex motor: fornece sinais motores ativadores para a medula, podendo
modificar a intensidade dos padrões ou modificar sua programação e características.
O cerebelo funciona com todos os níveis de controle muscular:
Medula espinhal: aumenta o reflexo de estiramento (resistência à cargas).
Tronco cerebral: contribui com movimentos posturais, principalmente os rápidos.
Córtex cerebral: dá força motora extra para iniciar a contração; ativa antagonistas.
Cerebelo: ajuda a programar as contrações musculares.
Os núcleos da base auxiliam no controle motor ajudando o córtex a executar padrões de
movimentos aprendidos e a planejar padrões paralelos e sequenciais de movimento.
Cap. 59 – Estados de Atividade Cerebral – Sono, Ondas Cerebrais, Epilepsia,
Psicoses
Estamos atentos a diferentes estados de ativação cerebral, como sono, alerta,
excitamento extremo e até estados de humor, como alegria, depressão e medo.
Sono:
Definido como um estado de inconsciência do qual a pessoa pode ser despertada por um
estímulo sensorial ou outro (diferente do coma, em que a pessoa não pode despertar).
Tipos de sono – estágios percorridos durante a noite se alternando um com o outro:
1. Sono de ondas lentas: as ondas cerebrais são de baixa amplitude e frequência baixa;
sono profundo e restaurador.
Sono profundo após longo período sem dormir, excepcionalmente relaxante e
associado a diminuição do tônus vascular periférico, da pressão arterial, da freqüência
respiratória e da taxa metabólica basal.
Chamado sono sem sonhos, embora possam ocorrer inclusive pesadelos, no entanto
não são lembrados (não se consolidam na memória).
2. Sono com movimentos rápidos dos olhos (REM): os olhos se movimentam
rapidamente, mesmo com a pessoa dormindo; associado a sonhos vívidos, não sendo
restaurador.
Ocorre em episódios de 5 a 30 minutos a cada 90 minutos, aumentando na medida em
que a pessoa fica mais descansada (menos sonolenta).
Características importantes:
- Associado a muita atividade muscular corporal (durante os sonhos ativos).
- As pessoas nesse sono são mais suscetíveis ao despertar.
- Tônus muscular muito reduzido (inibição das áreas de controle da medula).
- Freqüências cardíaca e respiratória irregulares (característica dos sonhos).
- Movimentos musculares irregulares e oculares rápidos.
42
- Metabolismo encefálico aumentado; o EEG mostra padrão semelhante ao estado de
vigília (sono paradoxal).
O sono é causado por um processo inibitório ativo; a transecção do tronco ao nível médio
da ponte cria um cérebro cujo córtex nunca dorme, então parecem existir centros abaixo
dessa região necessários para causar sono pela inibição de outras partes do encéfalo.
A estimulação de algumas áreas do encéfalo pode produzir sono (quase natural):
1. Núcleos da rafe, na metade inferior da ponte e no bulbo: muitas das terminações
nervosas das fibras destes neurônios liberam serotonina (produz sono).
2. Núcleo do trato solitário: terminação do bulbo e da ponte, onde se projetam sinais
vindos das informações sensoriais viscerais que entram pelo vago e glossofaríngeo.
3. Diencéfalo: estimulação da parte rostral do hipotálamo (área supraquiasmática) e de
uma área ocasional nos núcleos talâmicos de projeção difusa.
Lesões em alguns desses locais causam elevado estado de insônia (estado de vigília
intensa), podendo provocar a morte do animal por exaustão.
O peptídeo muramil, que se acumula no líquido cefalorraquidiano, na urina e no sangue de
animais mantidos acordados, pode induzir o sono quase natural, quando injetado no
terceiro ventrículo de outro animal; o nonapeptídeo tem quase o mesmo efeito.
Drogas que mimetizam a ação da acetilcolina aumentam a ocorrência do sono REM.
Mecanismo sugerido para a causa do ciclo sono-vigília: após o cérebro permanecer ativo
por várias horas, devido a excitação do córtex e sistema nervoso periférico por núcleos
ativadores reticulares, os neurônios desse sistema tornam-se fatigados, desaparecendo o
ciclo de feedback positivo entre o núcleo reticular mesencefálico e o córtex, levando a
uma transição rápida da vigília ao sono.
O sono causa efeitos fisiológicos no próprio SN e em outros sistemas funcionais do corpo,
causando má formação no processo de pensamento, atividades comportamentais
anormais, irritação e psicose, sendo que o principal valor do sono é restaurar o equilíbrio
natural entre os centros neuronais.
Ondas cerebrais:
Existe atividade elétrica contínua no cérebro, determinada pelos níveis de excitação de
diferentes partes do SNC, resultantes de sono, vigília e doenças como epilepsia e psicose.
As ondulações nos potenciais elétricos registrados são chamadas ondas cerebrais e seu
caráter depende do grau de atividade nas respectivas partes do córtex cerebral.
Em pessoas de saúde normal, as ondas podem ser classificadas em:
Alfa: ondas rítmicas, encontradas nos EEG de adultos acordados e num estado de
calma e atividade cerebral em repouso.
Beta: substitui as ondas alfa quando a atenção da pessoa é direcionada para algum
tipo de atividade mental específica.
Teta: ocorrem normalmente em crianças e em adultos durante estresse emocional
(desapontamento e frustração), além de estar em estados cerebrais degenerativos.
Delta: ocorrem durante o sono profundo, na infância, e na doença cerebral orgânica
grave, podendo ocorrer estritamente no córtex, independente das regiões inferiores.
A freqüência média no ritmo do EEG aumenta progressivamente com maiores graus de
atividade cerebral, sendo que as ondas se tornam assincrônicas durante os períodos de
atividade mental, fazendo com que a voltagem caia consideravelmente, apesar do
aumento da atividade cortical.
O sono REM é frequentemente chamado sono dessincronizado, por não apresentar
sincronia no disparo de neurônios, apesar da atividade cerebral significativa.
Epilepsia:
Também chamada de estado convulsivo, é caracterizada por atividade excessiva
descontrolada de qualquer parte ou de todo o sistema nervoso central.
Uma pessoa predisposta à epilepsia tem ataques quando o nível basal de excitabilidade do
SNC se eleva acima de certo limiar crítico; pode ser classificada em 3 tipos:
1. Epilepsia tipo grande mal: caracterizada por descargas neuronais extremas em todas
as áreas do encéfalo, podendo causar convulsões tônicas por descargas transmitidas
pela medula espinhal, que terminam em alternação entre contrações musculares e
tônicas, chamada convulsão tônico-clônica; a pessoa geralmente morde ou engole a
43
língua, tendo dificuldade para respirar (pode levar à cianose), e sinais transmitidos às
vísceras causam micção e defecação; duram de segundos a 4 minutos e apresentam
depressão pós-convulsão; pode ser desencadeada por estimulantes neuronais
(pentilenotetrazol), hipoglicemia por insulina, passagem de corrente alternada
diretamente pelo cérebro, estímulo emocional forte, alcalose (pelo aumento da
frequência respiratória, drogas, febre, barulhos altos e luzes piscantes; envolve, além
da ativação de tálamo e córtex, porções subtalâmicas do tronco cerebral; a maioria
dos pacientes apresenta uma predisposição hereditária; o ataque é interrompido por
fadiga neuronal e inibição ativa por neurônios inibitórios.
2. Epilepsia tipo pequeno mal: envolve o sistema ativador cerebral talamocortical;
caracterizada por 3 a 30 segundos de inconsciência, durante os quais a pessoa
apresenta contrações bruscas dos músculos da cabeça (piscada de olhos), seguida de
retorno à consciência, sendo a sequência completa chamada síndrome de ausência;
surge na infância desaparecendo por volta dos 30 e pode iniciar um ataque tipo grande
mal; o padrão cerebral é do tipo espícula-onda.
3. Epilepsia focal: pode envolver qualquer parte do encéfalo, resultando, mais
frequentemente, de lesões orgânicas localizadas ou anormalidades funcionais como
tecido cicatricial no cérebro que envolve um tecido neuronal adjacente, um tumor que
comprime uma área do cérebro, uma área de tecido cerebral destruído e um
desarranjo congênito dos circuitos; tais lesões podem promover descargas rápidas nos
neurônios locais, gerando circuitos locais reverberantes que recrutam áreas adjacentes
do córtex na zona de descarga epiléptica.
- Epilepsia jacksoniana: quando a onda de excitação se dissemina pelo córtex motor,
causa uma marcha de contrações musculares do lado oposto do corpo, começando na
boca e indo para as pernas.
- Convulsão psicomotora: tipo de epilepsia focal que pode causar amnésia, ataque
anormal de raiva, ansiedade súbita, desconforto ou medo, momentos de fala incoerente
ou resmungos de frases estereotipadas; a pessoa pode não se lembrar ou estar
consciente não conseguindo se controlar.
A excisão cirúrgica de um foco epiléptico pode evitar convulsões.
Psicose e Demência:
Condições resultantes de uma função reduzida dos neurônios que liberam um
neurotransmissor específico, sendo usadas drogas que contra-atacam essas perdas.
A psicose de depressão mental pode se causada pela formação diminuída no cérebro de
norepinefrina, serotonina ou ambas, uma vez que drogas que bloqueiam a secreção
dessas substâncias (reserpina) frequentemente causam depressão.
A depressão mental pode ser tratada pela terapia eletroconvulsiva (eletrochoque), com a
passagem de corrente elétrica pelo encéfalo causando convulsões, que aumentam a
atividade da norepinefrina.
Algumas pessoas podem alternar entre depressão e mania (transtorno bipolar ou psicose
maníaco-depressiva), sendo tratadas com drogas que diminuem a formação ou a ação de
norepinefrina ou serotonina (compostos de lítio).
Esquizofrenia: apresenta-se em várias formas, embora o tipo mais comum seja observado
na pessoa que ouve vozes, tem ilusões de grandeza, medo intenso e outras sensações
irreais; muitos esquizofrênicos são paranóicos, podem desenvolver falas e pensamentos
incoerentes e podem ser retraídos; acredita-se que os lobos pré-frontais estão envolvidos,
já que a lesão destes gera mecanismos parecidos; pacientes tratados com L-Dopa podem
apresentar a doença, mostrando que a mesma pode ser causada pela dopamina, além
disso, muitas drogas usadas no tratamento da esquizofrenia (clorpromazina, haloperidol,
Captiotixeno) diminuem a secreção da dopamina nas terminações nervosas; o hipocampo
pode estar envolvido já que apresenta-se diminuído no esquizofrênico.
Doença de Alzheimer: definida como envelhecimento precoce do cérebro, começando na
vida adulta média e progredindo até a perda extrema da capacidade mental; inclui
características como deficiência da memória de forma amnésica (perda de neurônios do
sistema límbico que comanda o processo da memória), piora da linguagem, déficits
visuoespaciais; é uma doença neurodegenerativa progressiva e fatal, sendo uma forma de
44
demência mais comum nos idosos; quantidades aumentadas do peptídeo beta-amilóide
são encontradas nos encéfalos desses pacientes; existem evidências de que doença
cerebrovascular causada por hipertensão e aterosclerose pode ter um papel nessa doença,
constituindo, junto a diabetes e hiperlipidemia, fatores de risco comuns.
Cap. 60 – O Sistema Nervoso Autônomo e a Medula Adrenal
Sistema Nervoso Autônomo: porção do SNC que controla a maioria das funções viscerais
do organismo, como pressão arterial, motilidade e secreção gastrointestinal,
esvaziamento da bexiga, sudorese, temperatura corporal, etc.; algumas são controladas
parcialmente, outras inteiramente, de forma rápida e intensa.
É ativado por centros localizados na medula, tronco e hipotálamo, recebendo sinais,
também, do córtex límbico e operando através de reflexos viscerais (sinais sensoriais
subconscientes de um órgão visceral entram nos gânglios autônomos, no tronco cerebral
e hipotálamo, e retornam como respostas reflexas subconscientes para controlar a
atividade do órgão visceral.
Sinais autônomos aferentes são transmitidos aos órgãos por duas divisões, chamadas:
1. Sistema Nervoso Simpático:
Constituído por duas cadeias de gânglios simpáticos paravertebrais, interconectadas
com os nervos espinhas ao lado da coluna vertebral, gânglios pré-vertebrais e nervos
que se estendem dos gânglios aos diferentes órgãos internos.
As fibras nervosas simpáticas se originam na medula, com os nervos espinhais, entre
os seguimentos T1 e L2, projetando-se para a cadeia simpática e daí para os tecidos e
órgãos estimulados pelos nervos simpáticos.
Os nervos simpáticos são diferentes dos nervos motores esqueléticos (apenas um
neurônio), sendo que cada via simpática da medula ao tecido estimulado é composta
de dois neurônios (um pré-ganglionar e um pós-ganglionar).
As fibras pré-ganglionares, após o nervo deixar o canal espinhal, podem fazer sinapse
com neurônios simpáticos pós-ganglionares no gânglio que entra, dirigir-se para cima
ou para baixo da cadeia e fazer sinapse com outro gânglio ou percorrer distâncias
variáveis pela cadeia e, através de um dos nervos simpáticos, dirigir-se para fora da
cadeia, fazendo sinapse com um gânglio sináptico periférico.
O neurônio simpático pós-ganglionar origina-se nos gânglios da cadeia simpática e nos
simpático periféricos, sendo que as fibras seguem seu destino em direção aos órgãos.
Algumas fibras pós (tipo C) passam de volta da cadeia simpática para os nervos
espinhais, pelos ramos comunicantes cinzentos da medula, e se estendem ao corpo
pelos nervos esqueléticos, controlando vasos sanguíneos, glândulas sudoríparas e
músculos piloeretores.
As fibras simpáticas (que se originam na medula) do seguimento T1 projetam-se para
a cabeça, de T2 terminam no pescoço, de T3 a T6 para o tórax, de T7 a T11 para o
abdome e de T12, L1 e L2 para as pernas.
Fibras nervosas simpáticas pré projetam-se diretamente (sem fazer sinapse) da
medula para fazer sinapse nas medulas adrenais, terminando em células secretoras de
epinefrina e norepinefrina, que são verdadeiros neurônios pós-ganglionares.
2. Sistema Nervoso Parassimpático:
As fibras parassimpáticas deixam o SNC através dos nervos cranianos III, VII, IX e X,
além de fibras adicionais que deixam a parte mais inferior da medula através do
segundo e terceiro nervos espinhais sacrais (às vezes pelo primeiro e quarto).
75% dessas fibras estão no nervo vago (X par), suprindo coração, pulmões, esôfago,
estômago, intestino delgado, metade proximal do cólon, fígado, vesícula biliar,
pâncreas, rins e porções superiores dos ureteres.
As fibras III nervo vão para o esfíncter pupilar e músculo ciliar do olho, as do VII para
as glândulas lacrimais, nasais e submandibulares e as do IX para a glândula parótida.
As fibras sacrais se distribuem para o cólon descendente, reto, bexiga e porções
inferiores dos ureteres, além da genitália externa, causando ereção.
45
As fibras pré-ganglionares passam de forma ininterrupta ao órgão que deve ser
controlado, fazendo sinapse com os neurônios pós, na parede do órgão, que por sua
vez, através de fibras muito curtas inervam os tecidos do órgão.
Todos os neurônios pré-ganglionares são colinérgicos (secretam acetilcolina), tanto no
simpático quanto no parassimpático; quase todos os neurônios pós do parassimpático são
também colinérgicos, já os pós do simpático são adrenérgicos (secretam norepinefrina) –
com exceção das fibras pós simpáticas para as glândulas sudoríparas, músculos
piloeretores e alguns vasos sanguíneos, que são colinérgicas.
A acetilcolina é chamada transmissor parassimpático e a norepinefrina, simpático.
Antes que a acetilcolina, norepinefrina ou epinefrina (na medula adrenal) estimulem o
órgão efetor, elas se ligam primeiro a receptores específicos nas células efetoras, que são
proteínas da própria membrana, que possuem canais iônicos ou ativam (ou inativam) uma
enzima no interior da célula (segundos mensageiros).
A acetilcolina ativa principalmente dois tipos de receptores:
1. Muscarínicos: a muscarina é um veneno que ativa esses receptores, encontrados em
todas as células efetoras estimuladas pelos neurônios colinérgicos pós-ganglionares,
tanto do simpático quanto do parassimpático.
2. Nicotínicos: são ativados pela nicotina e encontrados nos gânglios autônomos nas
sinapses entre os neurônios pré e pós-ganglionares tanto no simpático quanto no
parassimpático.
Existem também dois tipos principais de receptores adrenérgicos: alfa e beta; a
norepinefrina excita principalmente receptores alfa, já a epinefrina excita ambos de fora
parecida; esses receptores não estão necessariamente associados a excitação e inibição.
1. Alfa: vasoconstrição, dilatação da íris, relaxamento intestinal, contração dos esfíncters
intestinais, pilomotora e do esfíncter vesical.
2. Beta: dividos em dois tipos
2.1) Beta 1: cardioaceleração, força aumentada do miocárdio e lipólise.
2.2) Beta 2: vasodilatação, relaxamento intestinal, uterino e da parede da bexiga,
broncodilatação, calorigênese e glicogenólise.
A estimulação simpática causa efeitos excitatórios em alguns órgãos e inibitórios em
outros, da mesma forma que a estimulação parassimpática, sendo que, algumas vezes,
quando a estimulação simpática excita um órgão, a parassimpática o inibe (agem
antagonicamente), no entanto a maioria dos órgãos é controlada por um ou outro.
A tabela 60.2 (pág. 754) lista os efeitos nas diferentes funções viscerais do organismo
causada pela estimulação simpática e parassimpática; algumas merecem destaque:
1. Olhos: têm duas funções controladas pelo SNA, a abertura das pupilas e o foco do
cristalino.
Simpático: contrai as fibras meridionais da íris provocando dilatação da pupila
(midríase).
Parassimpático: contrai o músculo circular da íris provocando a constrição da pupila
(miose); contrai o músculo ciliar, liberando a tensão dos ligamentos e permitindo que
o cristalino se torne mais convexo (focalização de objetos mais próximos).
2. Glândulas:
S: atua sobre as digestivas, produzindo secreção concentrada (muitas enzimas e
muco), no entanto, provoca vasoconstrição dos vasos que as irrigam, diminuindo, as
vezes, sua taxa de secreção; estimula as sudoríparas (fibras colinérgicas, com exceção
das adrenérgicas das palmas das mãos e solas dos pés), embora estas sejam
estimuladas pro centros do hipotálamo (considerados parassimpáticos); estimulam as
apócrinas das axilas (fibras adrenérgicas).
P: estimula fortemente as nasais, lacrimais, salivares e gastrointestinais
(principalmente da boca e do estômago), gerando abundante secreção aquosa.
3. Plexo nervoso intramural do sistema gastrointestinal:
S: uma forte estimulação inibe a peristalse e aumenta o tônus dos esfíncteres.
P: age sobre o plexo intramural (SN entérico), localizado nas paredes do intestino,
aumentando o grau de atividade total do trato pela promoção da peristalse e
relaxamento dos esfíncteres.
46
4. Coração:
S: aumenta a atividade total, tanto pelo aumento da freqüência quanto da força da
contração cardíaca (aumenta a eficácia, necessária ao exercício pesado).
P: diminui a freqüência e a força de contração (diminui o bombeamento do coração,
permitindo que ele descanse entre períodos de atividade exaustiva).
5. Vasos sanguíneos sistêmicos:
S: contringe os vasos das vísceras abdominais, pele e membros, sendo que, algumas
vezes, a sua função beta causa dilatação vascular (após uso de drogas que bloqueiam
os receptores alfa, dominantes).
P: atua apenas nos vasos da área ruborizante do rosto.
6. Pressão arterial:
S: aumenta a propulsão do sangue pelo coração e a resistência ao fluxo do sangue
pelos vasos sanguíneos periféricos, causando um aumento da pressão (a longo prazo).
P: diminui o bombeamento cardíaco, diminuindo levemente a pressão, a não ser que o
estímulo vagal seja muito forte, podendo até parar o coração.
A estimulação dos nervos simpáticos que vão às adrenais causa a liberação de grandes
quantidades de epinefrina e norepinefrina no sangue circulante, causando quase os
mesmos efeitos que a estimulação simpática direta, porém com efeitos muito mais
prolongados (são retirados mais lentamente do sangue).
A norepinefrina causa a constrição de quase todos os vasos sanguíneos do corpo,
atividade aumentada do coração, inibição do trato gastrointestinal, dilatação das pupilas.
A epinefrina causa quase os mesmos efeitos da norepinefrina, com algumas diferenças,
tendo um maior efeito na estimulação cardíaca, uma constrição fraca dos vasos
sanguíneos, aumentando muito menos a pressão arterial, mas, muito mais o débito
cardíaco, além de ter um efeito metabólico muito maior sobre os tecidos.
Os órgãos alvo são estimulados duas vezes: diretamente pelos nervos simpáticos e
indiretamente pelos hormônios da medula adrenal, sendo que os dois meios se apóiam
mutuamente e qualquer um pode substituir o outro; além disso, os hormônios da medula
podem estimular estruturas do corpo que não são inervadas por fibras simpáticas diretas.
O SN autônomo é estimulado com uma freqüência de estimulação muito mais baixa do
que a necessária para estimular o SN esquelético.
Os sistemas simpático e parassimpático são continuamente ativos e as taxas de atividades
basais são conhecidas como tônus, que permite a um único SN aumentar ou diminuir a
atividade de um órgão estimulado.
O tônus simpático normalmente mantém quase todas as artérias sistêmicas constritas,
sendo que o aumento do grau de estimulação pode contringí-las ainda mais, ou a
diminuição dele pode dilatá-las.
Quando o tônus simpático ou parassimpático é perdido (nervo cortado), um tônus
intrínseco, presente na maioria dos órgãos efetores, desenvolve-se rapidamente para
compensar a perda; o tônus simpático pode se adaptar em minutos (vasos sanguíneos),
já o parassimpático pode levar meses (coração).
Supersensibilidade de desnervação: a perda do tônus simpático e parassimpático leva a
uma multiplicação dos receptores nas membranas pós-sinápticas, tornando-se mais
sensíveis à norepinefrina e acetilcolina.
Muitas das funções viscerais são controladas por reflexos autônomos, entre eles:
Cardiovasculares: receptores de estiramento, chamados barorreceptores se localizam
na parede das artérias, especialmente a carótida interna e o arco da aorta; quando são
estirados por pressão alta, sinais são transmitidos ao tronco, onde inibem impulsos
simpáticos ao coração e aos vasos, excitando os parassimpáticos e normalizando a
pressão – reflexo barorreceptor.
Gastrointestinais: o cheiro de comida ou a presença desta na boca inicia sinais para os
núcleos vagais, glossofaríngeos e salivatórios do tronco, os quais transmitem sinais pelos
nervos parassimpáticos às glândulas secretoras da boca e estômago, causando secreção
de fluidos digestivos; quando o reto está cheio, impulsos sensoriais são transmitidos à
porção sacral da medula e um sinal de reflexo é transmitido de volta pelos
parassimpáticos sacrais até o cólon, provocando contrações, que causam defecação.
47
Outros: o esvaziamento da bexiga é controlado da mesma forma que o do reto, com o
relaxamento dos esfíncteres urinários; os reflexos sexuais são iniciados por estímulos
psíquicos vindos do encéfalo e estímulos dos órgãos sexuais, sendo que esses impulsos
convergem na medula espinhal sacral, resultando, no homem, primeiro na ereção
(parassimpático) e depois na ejaculação (simpático); além de muitas outras funções.
Descarga em massa: em muitas circunstâncias, quase todas as porções do SNS
descarregam simultaneamente como uma unidade completa, ocorrendo quando o
hipotálamo é ativado por medo, terror ou dor intensa (resposta de alarme).
Outras vezes a ativação ocorre em porções isoladas do SNS, como durante o processo de
regulação de calor (controlam a sudorese e o fluxo sanguíneo sem afetar outros órgãos),
reflexos locais, como o aquecimento de uma área restrita da pele, e os reflexos simpáticos
que controlam funções gastrointestinais, que operam por vias que não passam na medula.
As funções controladas pelo parassimpático são muito mais específicas, sendo que os
reflexos cardiovasculares só agem no coração e o reflexo de esvaziamento retal não afeta
outras partes do intestino de forma significativa; mesmo assim, pode haver uma
associação entre algumas funções (secreção salivar e gástrica).
Resposta de alarme ou estresse (SNS): a soma de alguns efeitos permite à pessoa
exercer uma atividade física com muito mais energia, através da estimulação em massa
do SNS, chamada, também, de reação de luta ou fuga; os efeitos são:
1. Aumento da pressão arterial.
2. Aumento do fluxo sanguíneo para músculos ativos e diminuição para órgãos não
necessários à atividade motora, como trato gastrointestinal e rins.
3. Aumento das taxas de metabolismo celular.
4. Aumento da concentração de glicose no sangue.
5. Aumento da força muscular.
6. Aumento da glicólise no fígado e no músculo.
7. Aumento da atividade mental.
8. Aumento da taxa de coagulação sanguínea.
Muitas áreas da formação reticular controlam funções autônomas diferentes; os fatores
mais importantes controlados pelo tronco são a pressão arterial e a freqüência cardíaca e
respiratória; os centros bulbares e pontinos regulam a respiração.
Os centros autônomos do tronco funcionam, até certo ponto, como estações de
retransmissão para controlar as atividades iniciadas em níveis superiores do encéfalo
(especialmente no hipotálamo).
Farmacologia do SNA:
Drogas que atuam em órgãos efetores adrenérgicos (simpatomiméticas):
Drogas que causam liberação de norepinefrina: efedrina, tiramina e anfetamina.
Drogas que bloqueiam a atividade adrenérgica: o bloqueio ocorre em diversos pontos:
1. Síntese e armazenamento nas terminações simpáticas – reserpina.
2. Liberação das terminações simpáticas – guanetidina.
3. Receptores simpáticos alfa – fenoxibenzamina e fentolamina.
4. Receptores simpáticos beta – propanolol (beta 1 e 2) e metoprolol (beta 1).
5. Impulsos nervosos da atividade simpática e parassimpática – hexametônio.
Drogas colinérgicas: pilocarpina e metacolina.
Drogas anticolinesterásicas: neostigmina, piridostigmina e ambenônio.
Drogas antimuscarínicas: atropina, homatropina e escopolamina.
Drogas que estimulam ou bloqueiam os neurônios simpáticos e parassimpáticos pósganglionares:
Drogas que estimulam os neurônios autônomos pós-ganglionares: nicotina (excita
tanto os simpáticos quanto os parassimpáticos) e drogas nicotínicas; a metacolina tem
ações nicotínicas e muscarínicas e a pilocarpina, apenas muscarínicas.
Drogas bloqueadoras ganglionares: íon tetraetil amônia, íon hexametônio e pentolínio.
-----------------------------------------------------------------
Barbra Rafaela de Melo Santos – XLI.
48
49