Universidade de São Paulo
Faculdade de Medicina de Ribeirão Preto
Programa de Pós-Graduação em Imunologia Básica e Aplicada
Autores: Gabriela Trentin Scortegagna e Vinícius Pinho dos Reis
Modulação da resposta imune: Mecanismos de Regulação e sua Aplicação Clínica
Ao observarmos o curso de uma resposta imunológica montada frente a um antígeno,
percebemos que diversos são os componentes imunológicos envolvidos em tal processo, desde o
início da resposta, pelo contato com o antígeno, até a contração da resposta mediante a eliminação
do agente estimulante. Apesar de, didaticamente, separarmos os componentes do sistema
imunológico, todos atuam mutuamente e em colaboração para o sucesso da eliminação do antígeno.
Como já sabemos, os mecanismos efetores envolvidos neste processo são variados e muito potentes
em sua ação, evidenciando a necessidade de mecanismos reguladores que garantam a ativação, o
direcionamento e a inibição correta de todo o processo imune.
Neste contexto, abordaremos os diversos mecanismos reguladores atuantes e apontaremos as
ferramentas terapêuticas que podem ser usadas na prática clínica. Os mecanismos reguladores, cuja
finalidade é manter a homeostase do organismo, serão abordados conforme o contexto que atuam
nas diferentes fases da resposta imune (Reconhecimento, Ativação, Efetora e Contração).
1. Regulação pelo Antígeno
A presença do antígeno é o estímulo inicial para se montar uma resposta imune, e à medida
que a resposta evolui, o antígeno vai sendo eliminado, finalizando a resposta imunológica montada,
assim, o antígeno por si só é um fator regulador importante. O antígeno ainda exerce a regulação
pela sua permanência, quantidade, natureza e via de entrada no organismo. Na fase de
reconhecimento, a quantidade do antígeno é importante para que os componentes imunológicos o
percebam e ativem os mecanismos efetores que irão eliminar este antígeno. Em termos gerais, altas
ou baixas doses do antígeno podem levar à tolerância, enquanto que uma imunidade eficaz é
desenvolvida na presença de doses ótimas de um determinado antígeno. Outro fator importante é a
natureza do antígeno (protéica, lipídica, etc), que influencia no seu processamento e
reconhecimento pelos receptores celulares do sistema imune. Além disso, a capacidade que o
antígeno possui em ativar as células apresentadoras de antígeno (APCs - antigen-presenting cell),
vai determinar se ele será apresentado por uma APC imatura, o que resultará em tolerância, ou
ativada, que levará a ativação da resposta imunológica. A via de entrada no organismo também é
fator importante na regulação exercida pelo antígeno. Geralmente, quando o contato é por via oral
ou intravenosa, o antígeno leva à tolerância, enquanto por via intramuscular ou subcutânea gera
imunidade.
Com base nessas características do antígeno, utilizamos as vacinas como ferramentas de
manipulação do sistema imune, que são desenvolvidas com a combinação desses fatores para
obtenção dos resultados desejados, seja imunidade ou tolerância. Por exemplo, a estratégia utilizada
na vacina antitetânica é a combinação do toxóide tetânico oriundo da bactéria patogênica, o uso de
hidróxido de alumínio como adjuvante, que ativa as APCs, e a aplicação intramuscular como via de
administração escolhida.
2. Regulação por Moléculas de superfície
Na fase de ativação, é importante que haja a sinalização via coestimuladores para que ocorra
a proliferação e diferenciação dos linfócitos, caso contrário, estas células entram em anergia
(tornam-se não funcionais). A coestimulação via CD28-B7 (imunidade celular) é um exemplo de
regulação por moléculas coestimuladoras e, terapeuticamente, pode-se transfectar a molécula B7 em
células tumorais para que haja ativação dos linfócitos específicos para o tumor, situação que
normalmente não ocorre pela falta do B7 nas células tumorais. A molécula CTLA-4 (Cytotoxic TLymphocyte Antigen 4) também interage com os receptores B7, porém é um regulador negativo que
inibe a proliferação de linfócitos ativados, auxiliando na contração da resposta imunológica. Alguns
polimorfismos (alterações nas sequências de bases nitrogenadas) do gene CTLA-4 estão associados
ao desenvolvimento de doenças autoimunes. Na clínica, uma molécula CTLA-4 recombinante
(CTLA-4 fusionada à porção Fc de Imunoglobulina) pode ser usada no tratamento de pacientes com
artrite reumatóide, com a finalidade de inibir os linfócitos ativados. Outra molécula inibidora é o
Receptor de Morte Programada-1 (PD-1, do inglês Programmed Death 1) expresso em células
ativadas (macrófagos e linfócitos) que leva à apoptose dessas células ao interagir com seus ligantes
PD-L1 e PD-L2, expresso em células dendríticas e macrófagos ativados.
Outra molécula inibidora muito interessante é o HLA-G, uma molécula de MCH classe I
não clássica, ou seja, não possui a função de apresentar antígenos. O HLA-G se apresenta na forma
solúvel ou como molécula de membrana celular. Ao interagirem com seus ligantes, KIR2DL4, ILT2
e ILT4, presentes em diversos tipos celulares, induzem a inibição da função da célula, ou seja,
diminuição da apresentação de antígenos pelas APCs, diminuição da proliferação alogênica de
linfócitos, inibição da atividade citotóxica de células T e linfócitos T CD8, mudança do padrão de
ciotocinas produzidas, e ainda, geração de células T reguladoras (Tregs).
Na interação célula T e B, a sinalização por CD40-CD40L é fundamental para a troca de
isotipo dos anticorpos. Indivíduos com mutação no gene CD40L desenvolvem a Síndrome da
Hiper-IgM ligada ao X, que é caracterizada por níveis séricos normais de IgD e elevados de IgM,
com ausência dos outros isotipos de imunoglobulinas e número normal de células B e T.
Na fase de contração, a sinalização Fas/Fas Ligand é importante para indução da apoptose
das células ativadas, mecanismo denominado Morte Celular Induzida por Ativação (AICD, do
inglês Activation-induced cell death). Além disso, esta mesma sinalização também é um dos
mecanimos de morte induzida por células T citotóxicas sobre células alvo. Mutações no gene FAS
geram a Síndrome autoimune linfoproliferativa (ALPS, do inglês Autoimmune Lymphoproliferative
Syndrome).
3. Regulação por Anticorpos
Na fase efetora da resposta, anticorpos circulantes formados contra o antígeno regulam a
produção de novos anticorpos contra o mesmo antígeno. Essa regulação pode ser por competição
pelo antígeno entre o anticorpo circulante e o BCR de um clone de linfócito específico para o
mesmo epítopo ou por um processo de regulação negativa de anticorpos. Assim, o anticorpo
circulante liga-se ao antígeno e, esse, se liga à célula B através do BCR. Ao mesmo tempo, o
anticorpo liga-se ao receptor FcyRII, que promove a transdução de sinais inibitórios, impedindo a
produção de mais anticorpos. Com base nesses mecanismos de regulação, intervenções terapêuticas
podem ser propostas com o uso de anticorpos neutralizantes que competem pelo antígeno ou
anticorpos bloqueadores que competem com os receptores celulares. A administração pós-parto de
anticorpos neutralizantes anti-Rh pode ser utilizada para prevenção da eritroblastose fetal. Já
baseado na regulação negativa de anticorpos temos o tratamento com imunoglobulinas intravenosa
(IIV) em altas doses que por ser uma terapia muito cara é utilizada somente em casos selecionados
de doenças inflamatórias, autoimunes ou infecções agudas. Assim, a IIV tem sido usada com
sucesso na púrpura trombocitopênica idiopática, doença na qual a grande produção de anticorpos
antiplaqueta pode ser inibida pela administração de altas doses da IIV.
Ainda dentre os mecanismos de regulação pelos anticorpos temos a teoria da rede idiotípica
imunológica, a qual postula que para cada clone de linfócito B produza um clone de anticorpo,
contendo um idiotipo, definido pela porção variável da imunoglobulina, ou seja, a porção que é
específica a um determinado epítopo (menor parte de um antígeno capaz de estimular uma resposta
imunológica). Assim, anticorpos anti-idiotipo reconhecem a porção específica de outros anticorpos
produzidos contra um determinado antígeno, e assim, sucessivamente. Na clínica, anticorpos
monoclonais anti-idiotipo têm sido utilizados com algum sucesso no tratamento de linfomas das
células B e leucemias de células T.
4. Regulação por Linfócitos e suas citocinas
Também temos a regulação exercida pelos linfócitos T e suas citocinas. Diversos perfis de
produção de citocinas têm sido descritos, cada qual identifica um grupo de células T que, além de
exercer diversas funções efetoras, regulam negativamente o desenvolvimento dos outros padrões de
células T. Por exemplo, o IFN-γ produzido pelo padrão Th1 inibe o desenvolvimento do padrão
Th2. Existem ainda as células T reguladoras (Treg), que através de suas citocinas, IL-10 e TGF-β,
inibem todos os padrões, principalmente os padrões pró-inflamatórios (Th1 e Th17), constituindo
assim um subtipo celular imunossupressor. Além da regulação via citocinas pelas Treg, essas
células atuam através do contato célula-célula, pelas interações CTLA-4, PD-1 e GITR
(glucocorticoid-induced TNFR family-related receptor) presentes nas Treg, com seus ligantes
presentes nas células alvo. As Treg também atuam sobre as APCs, inibindo sua função, ou seja, a
perda da expressão das moléculas coestimuladoras (CD40 e B7). Assim, as APCs continuam
apresentando os antígenos, porém não são capazes de ativar os linfócitos.
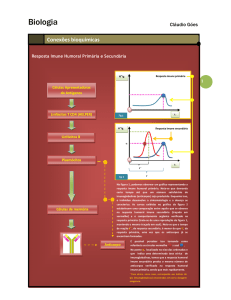
Figura Mecanismos de Regulação: Desde a entrada do antígeno, expressão de moléculas
coestimuladoras importantes para determinação da resposta montada, até o controle da resposta
efetora por células Treg e moléculas inibitórias.
5. Outros fatores
Além desses mecanismos, temos os fatores mais abrangentes que interferem no sistema
imunológico, como os fatores neuroendócrinos, idade, alimentação, etc. Os hormônios sexuais
atuam nas células do sistema imune, estimulando (estrógeno) ou reprimindo (andrógenos) asua
função. Já o cortisol e os glicocorticóides são potentes imunossupressores, pois estimulam citocinas
do padrão Th1, inibindo diversas funções do sistema imune. O estado nutricional é também um
fator regulador, por exemplo, a vitamina D participa da maturação das células dentríticas,
importantes APCs. O ácido retinóico, derivado da quebra da vitamina A, participa da geração de
células T reguladoras. Outros elementos, como o zinco e o ferro, também influenciam no sistema
imune, uma vez que deficiências nesses micronutrientes (como nas anemias) levam a respostas
imunes prejudicadas. Embora apresentem grande diversidade linfocitária, as respostas imunológicas
nos idosos tendem a ser mais lentas e menos vigorosas, deixando-os mais susceptíveis a infecções
principalmente do trato respiratório superior, face ao envelhecimento do sistema imune.
Referências Bibliográficas
ABBAS;LICHTMAN; PILAY; Imunologia Celular e Molecular, 6°ed., Editora Elsevier.
ROITT; Essential Immunology, 10°ed., Editora Elsevier.