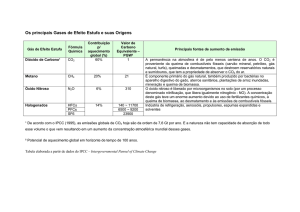
CONTESTAÇÃO DA QUESTÃO 34 DE QUÍMICA TIPO I
1ª ETAPA
Para a resolução do item 2 pode-se tomar dois parâmetros de comparação entre álcool e gasolina.
Primeiro: Calor de combustão.
∆H°
Substância
Fórmula
Etanol (álcool)
C2H5OH
–1368
Octano (gasolina)
C8H18
–5471
c
(kJ/mol)
ATKINS, P. Princípios de Química. Bookman, 2007 (adaptado)
Fazendo a proporção temos que na queima da gasolina são fornecidos 684kJ de energia por mol de CO2.
Fazendo a proporção temos que na queima do álcool são fornecidos 684kJ de energia por mol de CO2.
Portanto por esse parâmetro o item é falso.
No entanto o conteúdo calor de combustão não é pertinente ao programa da 1ª etapa do PAAES, o assunto é
abordado na segunda etapa.
Segundo: Considerar a queima de 1 mol de cada combustível.
Na queima de 1 mol de gasolina são liberados 8 mols de CO2.
Na queima 1 mol de álcool são liberados 2 mols de CO2.
Com base nesse parâmetro de comparação, o álcool libera quantidade menor de gás carbônico em relação à
gasolina.
Portanto por esse parâmetro o item é verdadeiro.
Ou o gabarito deverá ser alterado, ou a questão deverá ser anulada.
Equipe de professores de Química do Colégio Nacional.
ENSINO INFANTIL, FUNDAMENTAL, MÉDIO E PRÉ-VESTIBULARES
http: \\www.nacionalnet.com.br