PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
1
PATOLOGIA PULPAR
1- INTRODUÇÃO:
A principal causa das alterações pulpares é a cárie, e a resposta mais evidente é a dor. Na pulpite
deve-se considerar o envolvimento físico da polpa por tecidos duros, e as modificações estruturais da
polpa com a idade. É importante realçar que o estudo da inflamação pulpar é dificultado pelo seu
pequeno volume, cerca de 0,02ml para cada dente humano, e por estar envolvida por dentina.
Classicamente aceita-se que em um dente com cárie, a inflamação pulpar se inicia por resposta de
baixo grau e de natureza crônica, e a medida que a cárie avança, uma resposta aguda sobrepõe-se aos
elementos crônicos. O desenvolvimento da reação inflamatória na polpa precisa ser melhor estabelecido,
como a participação dos mastócitos, fibras nervosas e a influência de fatores sistêmicos, como a
imunosupressão. Experimentalmente poucos trabalhos descrevem a história natural da reação
inflamatória na polpa e periápice, sendo que a maioria dos estudos referem-se aos efeitos dos
procedimento terapêuticos e a biocompatibilidade de materiais.
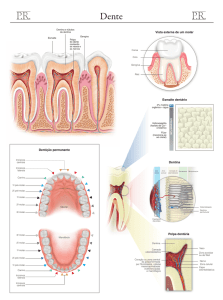
2- COMPLEXO POLPA-DENTINA:
A polpa é o tecido conjuntivo que ocupa a parte central do dente, cuja função principal é manter
a vitalidade da dentina, e conseqüentemente do dente. A polpa e a dentina formam um único complexo,
pois estão intimamente relacionados morfo e fisiologicamente.
2.1- Desenvolvimento
A polpa origina-se da papila dental, que passa a ser chamada de polpa a medida que a dentina é
formada. Após o início da formação da dentina, os ameloblastos começam a formar esmalte. Num dente
formado, o tecido envolvido por dentina é polpa e na região apical, a área envolvida por cemento é
considerada parte do periápice.
2.2- Zonas de Complexo Polpa-Dentina:
Dentina
Pré-dentina
Odontoblastos
Zona pobre em células (Zona de Weil)
Zona rica em células
Zona central da polpa
2.3- Dentina:
As alterações pulpares iniciam-se a partir de estímulos da dentina, e uma série de características
da dentina devem ser consideradas. A dentina é peculiar porque o prolongamento do odontoblasto
penetra no tecido duro, longe do corpo celular. A dentina é semelhante ao osso em composição, sendo
75% de material inorgânico e 20% orgânico.
Diâmetro do túbulos dentinários:
Próximo a polpa - 2-3 µm
junção amelo-dentinária - 0.5-0.9 µm
Na região próxima a junção amelo-dentinária não há prolongamento do odontoblasto, apenas fluído
dentinário.
Número de canalículos:
próximo a polpa - 45-65.000/mm
centro da dentina - 30-35.000/mm
próximo ao esmalte- 15-20.000/mm
(comparar com o raio de bicicleta)
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
2
Volume ocupado pelo túbulos:
4% na junção amelo-dentinária
28% na área próxima a polpa
Estes dados são importantes porque os canalículos são as regiões mais permeáveis da dentina,
por onde há penetração de substâncias lesivas e transmissão de impulsos dolorosos. Portanto deve-se
considerar que a dentina próxima a polpa é mais permeável, e que em dente “jovem” a dentina é mais
permeável e mais delgada.
2.4- Fluído Dentinário:
A pressão intrapulpar é de cerca de 30mmHg, que deve ser a pressão capilar. Esta pressão é
suficiente, por capilaridade, para fazer uma coluna de líquido de 7m de altura. Portanto há formação de
líquido da polpa para a junção amelo-dentinária. O líquido que permeia a dentina, em particular os
canalículos é chamado de fluído dentinário. Provavelmente este líquido pouco se movimenta. A
composição é semelhante ao líquido extracelular, com baixo teor de K, alto em Na, saturado em Ca e PO,
contendo proteínas plasmáticas.
Quando a polpa se inflama, mais líquido é pressionado para o interior dos canalículos, inclusive
fibrinogênio. Na dentina cariada o canalículo fica exposto, e a dentina sendo permeável permite o
deslocamento de líquido da polpa para a superfície. O deslocamento de líquido seria o responsável pela
geração de dor, mediada pelos odontoblastos ou diretamente pela fibras nervosas.
Deve-se ressaltar que em uma fratura de dentina o canalículo fica aberto, enquanto que num
preparo cavitário há formação da “smear layer”, que é uma camada de microcristais que cobrem a
superfície da dentina cortada, e que diminui a permeabilidade da dentina. Sugere-se também que após o
preparo cavitário há deposição de fibrinogênio nos canalículos, diminuindo a permeabilidade da dentina
em 10% por hora. Isto foi feito comparando-se cães normais e desfibrinados. Quando a cavidade é seca
com ar, seca-se o fluido dentinário. A polpa rapidamente forma mais fluido, e se o movimento for rápido
o corpo do odontoblasto pode ser aspirado para dentro do canalículo.
2.5- Mastócitos:
A morfologia do tecido conjuntivo pulpar permite supor que mastócitos estivessem presentes em
razoável quantidade. Por outro lado, considerando-se que os mastócitos são as principais fontes de
histamina, e que a polpa está envolvida por dentina, sua presença poderia ser mais prejudicial do que útil.
Os dados atuais não são claros. Vários autores descreveram ausência de mastócitos na polpa. Alguns
descreveram mastócitos apenas em polpas inflamadas. Atualmente considera-se que mastócitos estão
presente em algumas polpas normais 20% (?) e na maioria das inflamadas 70% (?).
Ainda não foi demonstrado mastócitos na polpa de outros animais, além do homem. Não há
também documentação em microscopia eletrônica.
IgE foi detectada na polpa inflamada, indicando a possível ocorrência de hipersensibilidade
imediata em associação com a presença de mastócitos. Após injúria térmica o teor de histamina na polpa
está aumentado de 4X depois de 30 minutos.
2.6- Alterações vasculares com a idade:
Em decorrência de sua peculiaridades, a polpa dental está sujeita a alterações com a idade. O
sistema vascular é grandemente afetado com a idade. Ocorre calcificação dos vasos, especialmente
daqueles da porção radicular. Em dentes de pessoas idosas, persistem somente os vasos de grande calibre
e assim mesmo apresentando calcificações em suas paredes. Ocorrendo diminuição do volume pulpar
com a idade, os vasos ficam localizados na porção central, enquanto que os vasos periféricos quase que
desaparecem. As arteríolas começam a apresentar hiperplasia da íntima, com diminuição da luz do vaso,
semelhante a arteroesclerose. O processo de calcificação inicia-se pala adventícia, chegando até a
íntima.
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
3
3- INERVAÇÃO DA POLPA E DA DENTINA:
3.1- Polpa:
Os nervos da polpa foram descritos por Raschkow em 1836. A polpa é ricamente inervada por
fibras mielinizadas e amielinizadas que penetram pelo forame apical, ramificando-se principalmente nas
áreas sub-odontoblástica, coronária e cornos pulpares. Os nervos são as últimas estruturas a aparecerem
na polpa, e não são vistos até que considerável quantidade de dentina seja formada. A inervação aumenta
quando o dente erupciona. A predominância de fibras amielinizadas ocorre na região próxima aos
odontoblastos. Geralmente as fibras nervosas acompanham os vasos sangüíneos. O primeiro molar
humano tem cerca de 400 axônios mielinizados e 1800 amelinizados entrando pelo ápice. O número
diminui com a idade.
As fibras mielinizadas medem de 1-4 µm de diâmetro e são estruturas especializadas na
transmissão dolorosa rápida, tendo baixo limiar. Devem participar da dor localizada e aguda. As fibras
amielinizadas são do tipo C e servem para transmissão de dor e função simpática. A condução é lenta, e
o limiar é alto. Devem participar da dor não localizada e de menor intensidade.
Os dentes decíduos têm aproximadamente o mesmo número de fibras nervosas que os
permanentes, mas o número diminui significantemente após o início da reabsorção. A dor, é difícil de ser
avaliada visto que os métodos são subjetivos, e as crianças reagem diferentemente do adulto.
3.2- Inervação da dentina:
A inervação da dentina e o mecanismo da transmissão da dor de dente sempre foram assuntos
muito controvertidos. Windle em 1934 fez um resumo dos trabalhos que discutiam a inervação da
dentina. O primeiro autor a descrever a possível presença de terminações nervosas na dentina foi Eale
em 1860. Cutler em 1867 comparou a dentina e polpa com o crânio e seus nervos.
Avery descreveu em microscopia eletrônica a presença de fibras mielizadas e amielinizadas na
região sub-odontoblástica, predominando as amielinizadas. Os canalículos da pré-dentina apresentam
fibras nervosas em quantidades variáveis. Em 1966 Frank demonstrou a presença de fibras nervosas na
dentina mais próxima a polpa.
3.3- Transmissão da Dor:
A qualquer estímulo a polpa reage com dor. As sensações de pressão são devidas ao periodonto.
O mecanismo de transmissão da dor no complexo polpa-dentina ainda é assunto de discussão. A
dificuldade é de se explicar como as fibrilas nervosas da polpa são estimuladas.
Teorias
-Hidrodinâmica: o rápido movimentos de fluidos no interior dos canalículos resulta em distorção de
terminações nervosas, iniciando um impulso e a sensação de dor. Atualmente é a teoria mais aceita.
- Odontoblastos como receptores: os prolongamento de Tomes transmitem os estímulos para o corpo
dos odontoblastos, e estes para as fibrilas nervosas do plexo sub-odontoblástico.
- Direta inervação: a presença de nervos, principalmente no terço interno da dentina, seria responsável
pela transmissão da dor.
4- MODIFICAÇÕES ESTRUTURAIS DO COMPLEXO PULPO DENTINÁRIO COM A
IDADE:
As principais modificações do órgão dental são:
- esclerose dentinária
- dentina de reparação
- espessura da dentina
- diâmetro dos canalículos
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
4
- volume da polpa
- fibrosamento
- calcificação - formação do periápice
As alterações da polpa com a idade são difíceis de serem separadas das modificações oriundas
dos mecanismos de defesa ou das patologias.
Em relação ao dente “velho”, o “jovem” tem as seguintes características:
- cavidade pulpar ampla
- espessura delgada da dentina
- dentina ainda a ser formada
- polpa rica em células e substâncias fundamental
- grande capacidade de reparação
- canalículos amplos
- rica inervação e vascularização
Por estas características é mais fácil trepanar um dente “jovem”. Se a polpa de um dente jovem
for retirada, a dentina que já é delgada, fica mais friável e mais susceptível a fratura.
4.1- Esclerose Dentinária:
A esclerose dentinária é a calcificação dos canalículos dentinários, com a dentina tornando-se
nesta região menos permeável, vítrea e sem vitalidade. A calcificação dos canalículos é contínua,
fazendo parte da fisiologia pulpo-dentinária. Este processo é acelerado frente a estímulos de baixa
intensidade, que não provocam necrose do prolongamento do odontoblasto. A esclerose da dentina é
freqüente na porção radicular de pessoas idosas.
4.2- Dentina de reparação:
A dentina de reparação é formada na superfície interna da dentina, quando há destruição,
geralmente por cárie, da dentina superficial, sem necrose dos odontoblastos. A dentina de reparação
acompanha os canalículos lesados, e a quantidade formada corresponde a que foi destruída. É menos
organizada e mais calcificada que a ortodentina, com canalículos tortuosos e em menor número. A
tendência é a dentina de reparação formar-se na mesma quantidade em que houve destruição da
ortodentina. Estima-se a dentina de reparação é formada numa velocidade de 1.5 µm/dia, e portanto em
100 dias forma-se 120 µm (0,12 mm).
5- POLPA E TRAUMA OCLUSAL:
O trauma oclusal pode causar alterações periodontais nos períodos iniciais, voltando a
normalidade posteriormente. Na polpa não causa alterações significativas, exceto formação de dentina
de reparação. Resultados de trauma causado por restauração alta de amálgama em molar antagonista de
rato mostrou que após 3-5 dias o periodonto apresentava áreas de hialinização e reabsorção óssea,
cementária e dentinária. A polpa estava normal. Após 28 dias o periodonto e a polpa estavam normais.
Houve restabelecimento da normalidade porque o dente se movimentou e houve desgaste do amálgama.
Foi alta a incidência de fratura do dente que tinha o amálgama.
6- POLPA E PREPARO DE CAVIDADES:
Se não feito com os devidos cuidados técnicos um preparo cavitário pode provocar alterações da
polpa. Os pontos a serem considerados são a espessura da dentina restante, a temperatura durante o
preparo e a pressão exercida.
Se houver acúmulo localizado de leucócitos, o processo é reversível. É importante que não haja
infecção da polpa. Quando há formação de microabscesso as chances de resolução do processo são
menores. A reversibilidade também é menor nos preparos cavitários de dentes cariados, onde há
alterações preexistentes.
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
5
7- ESPESSURA DA DENTINA RESTANTE (EDR):
O fator isolamento é o mais importante para determinar a resposta pulpar a um estímulo. A EDR
difere da profundidade do preparo da cavidade, visto que a espessura da dentina é variável de dente para
dente.
Geralmente 2 mm de dentina entre o assoalho da cavidade e a polpa oferece barreira adequada.
Nos dentes decíduos e anteriores este fator é crítico porque a espessura da dentina raramente excede
2,5mm. A medida que a espessura da dentina diminui as alterações da polpa aumentam.
Com a mesma EDR, as técnicas de alta velocidade produzem menos da metade das respostas
pulpares do que as baixas velocidades (baixas - 6-20.000 rpm; altas - 50-300.000 rpm). Além da
refrigeração deve-se considerar a menor pressão empregada nos equipamentos de alta rotação.
8- DESENVOLVIMENTO DA PULPITE:
A aplicação de produtos bacterianos sobre a dentina, 0.7-0.9mm da polpa, provocou após 32
horas intenso acúmulo de neutrófilos nas áreas abaixo dos canalículos dentinários expostos, formando
em alguns casos microabscessos. Após 10 dias predominam células mononucleares, e após 30 dias havia
dentina de reparação e ausência de células inflamatórias (Warfvinge e Bergenholtz, 1986). Se a distância
das bactérias até a polpa for de 1mm, geralmente não tem alteração pulpar. Se for de 0.5mm há formação
de microabscesso.
Vários experimentos como o descrito mostram que a polpa dental pode se recuperar de uma
inflamação aguda, desde que não haja grande número de microorganismos invadindo a polpa.
Em ratos convencionais e “germ-free” as alterações pulpares após exposição ao meio bucal são
diferentes. Nos “germ-free” há formação de pontes de dentina e ausência de inflamação, apesar de
necrose na superfície da área exposta. Algumas vezes ocorre necrose na polpa próxima a exposição ao
meio bucal, e isto é considerado como devido a impactação de alimentos. Nos convencionais após 2 dias
há infiltração de neutrófilos na camada superficial e início de necrose. Após 7 dias a necrose pulpar é
mais extensa, com inflamação periapical. Bactérias são encontradas apenas nos túbulos dentinários da
dentina coronária (Paterson 1987).
A capacidade de reparação da polpa é ilustrada nos casos de capeamento. O capeamento pulpar
era visto com pessimismo até a introdução do hidróxido de cálcio (Shroff 1959), mas dados mais
recentes indicam que o capeamento direto pode ter 80-90% de sucesso (Horsted et al. 1985). Quando a
exposição ocorre por cárie e num dente com dor, o prognóstico é menos favorável, sendo o grau de
inflamação e de contaminação os fatores que determinam o prognóstico. Idade também deve ser
considerada e Horsted et al. (1985) observaram resultados menos favoráveis em pacientes com 50-79
anos de idade. Os fatores principais a serem considerados são: idade do paciente, capacidade
imunológica do paciente e da polpa, estrutura da polpa, grau de contaminação, grau de inflamação.
8.1- Bactérias:
O trabalho clássico de Kakehashi e cols. (1965) mostrando em animais “germ-free” ausência de
inflamação e formação de pontes de dentina em polpas expostas ao meio bucal, fundamentou os
conceitos atuais da importância das bactérias e seus produtos na inflamação pulpar.
A coroa é a principal porta de entrada das bactérias, mas deve-se, considerar a possibilidade de
contaminação por via hematógena e através da bolsa periodontal.
Experimentos em humanos e animais durante os últimos 15 anos têm mostrado que os materiais
restauradores causam pouca ou nenhuma irritação na polpa, desde que bactérias não estejam presentes
nas margens das restaurações (Bergenholtz 1990). A quantidade e variedade de bactérias presentes num
canal contaminado é muito grande. Bystrom (1983) identificou 169 espécies, 88% anaeróbicas, e em
cada canal, de 1 a 11 espécies. O grupo predominante é dos estreptococos alfa-hemolíticos anaeróbios
facultativos (S. mitis, salivarius, mutans, sanguis). Outros isolados com freqüência são: enterococos (S.
faecalis), difteróides, estafilococos, lactobacilos, estreptococos anaeróbicos e espécies de Candida,
Neisseria e Veillonella. As espécies encontradas são numerosas, mas em um mesmo canal os tipos são
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
6
limitados, geralmente entre 3 a 6 espécies (Tronstad 1992). Em resumo a microbiota do canal é
caracterizada por combinações de poucos anaeróbios.
8.2- Dinâmica da Inflamação Pulpar:
Como em outros tecidos a inflamação pulpar é dinâmica passando de uma fase para outra na
dependência das condições locais.
8.3- Pólipo pulpar:
o pólipo pulpar é bom exemplo de inflamação crônica hiperplásica e da grande capacidade de
defesa de uma polpa jovem. Ocorre quase que exclusivamente em dentes jovens com ápice amplo, com
a polpa tendo abundante suprimento vascular e celularidade. A exposição da polpa permite a
epitelização do pólipo, com predominância de fenômenos proliferativos sobre os destrutivos.
9- IMUNIDADE:
9.1- Imunidade humoral:
Como a inflamação pulpar é causada por microorganismos e seus produtos, certamente que
reações imunológicas são importantes entretanto os dados da literatura ainda são escassos. A seqüência
de resposta imunológica na polpa ainda não é bem conhecida.
A presença de anticorpos na polpa inflamada foi inicialmente descrita por Honjo et al. (1970),
com predominância de IgG. De acordo com Pulver et al. (1977) a polpa normal não tem células
formadoras de anticorpos, e na inflamada mais de 60% das células produzem anticorpos, principalmente
IgG, seguido de IgA e IgE, e apenas 3 de 12 casos foram positivos para IgM. A ausência de Linfócitos B
na polpa normal foi confirmada por imunocitoquímicas por Jontell e cols. (1987).
9.2- Imunidade celular:
A polpa normal tem linfócitos T helper e citotóxico, macrófagos, mas não linfócitos B, isto foi
verificado por marcadores de membrana celular (Jontell e cols. 1987, 1988). Estes mesmos autores
também demonstraram presença de células dendríticas capazes de apresentarem antígenos na região
sub-odontoblástica, sugerindo que estas células na polpa teriam função semelhante à das células de
Langerhans na pele. Estes dados sugerem que linfócitos T participam da resposta inicial imunológica da
polpa.
Na polpa normal linfócitos T correspondem 1,0 a 2,0% do total de células, numa proporção
semelhante de CD4 e CD8 (Mangkornkan 1991). Células B não foram detectadas.
De acordo com Bergenholtz, Nagaoka e Jontell (1991) células que expressam antígenos classe II
aumentam em polpas inflamadas.
10- CORRELAÇÃO CLÍNICO-HISTOPATOLÓGICA:
Os trabalhos desde o inicio do século mostram que não há correlação entre os achados clínicos e
os aspectos microscópicos da polpa. Polpas microscopicamente consideradas normais podem apresentar
sintomatologia dolorosa, isto parcialmente explicado pela resposta de dor a um estímulo que atinja
apenas a dentina, promovendo movimentação de líquidos. Portanto o volume de líquido extravasado
pode ser mais relevante que a natureza das células inflamatórias presentes. A pressão normal do tecido
pulpar é de 6-10mmHg, e na inflamação chega a 16mm (Tonder e Kvinnsland, 1983). Em outros tecidos
este aumento seria insignificante, mas na polpa pode causar importantes modificações na circulação e
atividades nervosas.
Outras variáveis devem ser consideradas:
- variação na estrutura da polpa normal
- variação na inervação da polpa e dentina
- tempo de duração da cárie
- diferença de sensibilidade entre os indivíduos
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
7
- espessura de dentina
Em outros tecidos, se apenas o parâmetro dor for considerado, é pouco provável que se chegue a
correlação clínicas e microscópicas mais seguras do que acontece na polpa. As condições pulpares são
interpretadas indiretamente, considerando-se a idade do paciente, profundidade da cárie e
sintomatologia dolorosa.
11- EFEITOS SISTÊMICOS NAS PULPITES:
O fibrosamento da polpa dental reduz a sua capacidade de defesa, e as melhores respostas frente
a pulpotomias de dentes com polpa jovem. Além da idade, outros fatores sistêmicos podem ser
relevantes, mas ainda não demonstrados, como diabetes e imunosupressão. De acordo com Fawzie e cols.
(1985) quando há exposição pulpar, a capacidade de defesa da polpa de ratos irradiados com 400 rads
está diminuída.
12- SEPTICEMIA:
A incidência de bacteremia após a manipulação é considerada mais baixa que após extração e
tratamento periodontal, mas pacientes de risco, tratados com imunosupressores ou portadores de
válvulas artificiais, ou com história de febre reumática, devem ser medicados com antibióticos
previamente ao tratamento (Baumgartner, Heggers e Harrison 1977). A septicemia pode ser facilitada se
o ápice for amplo. Klotz et al. (1965) detectaram bacteremia em 4 de 19 casos de polpas de Macaca
mulatta (Rhesus) infectadas com S. faecalis e tratadas topicamente com prednisolona.
Bacteremia após tratamento endodôntico foi estimado em 20%, após tratamento periodontal em
70% e 100% após cirurgia (Heimdahl et al. 1990).
13- REABSORÇÃO:
Reabsorção interna de dentina está geralmente associada a causas desconhecidas, e não como
parte da progressão natural de inflamação pulpar. A dissolução da dentina intracanal, após a necrose da
polpa, pode ser considerada como processo similar a cárie dental que destrói a dentina coronária.
A reabsorção externa da dentina é mais evidente em casos de trauma e reimplantes dentários,
quando o processo pode ser contínuo e irreversível.
Nas lesões apicais, a reabsorção é principalmente observada no osso, sendo em menor grau a
destruição do cemento e da dentina. A dentina externa, quando reabsorvida é recoberta por material
cementóide.
Considera-se que tanto a reabsorção externa quanto a interna é mediada por células
multinucleadas, oriundas de monócitos ou macrófagos, num processo semelhante ao que ocorre no osso.
PATOLOGIA GERAL - DB-301, UNIDADE III FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
8
OBJETIVOS:
01. Qual as funções da dentina e da polpa e porque são consideradas como um único complexo?
02. Quais as zonas do complexo dentina-polpa?
03. Diferencie diâmetro dos túbulos, número de canalículos e volume tubular na dentina próxima à polpa
e próxima à junção amelo-dentinária.
04. Que é fluído dentinário?
05. Que é “Smear layer”?
06. Comente a presença de mastócitos na polpa.
07. Comente a inervação da polpa e da dentina.
08. Citar e explicar as 3 teorias principais sobre a transmissão da dor no complexo dentina-polpa.
09. Quais as modificações estruturais do órgão-dental com a idade?
10. Conceitue esclerose dentinária e dentina de reparação.
11. Quais as características estruturais de um dente “Jovem”?
12. Quais os efeitos do trauma oclusal e do preparo de cavidades na polpa?
13. Comente a importância da espessura de dentina restante.
14. Cite os fatores que regulam o sucesso do capeamento.
15. Qual a importância das bactérias no desenvolvimento da pulpite?
16. Que é pólipo pulpar?
17. Comente imunidade celular e humoral na inflamação pulpar.
18. Existe correlação clínico-histopatológica na polpa? Explique.
19. Comente septicemia após manipulação pulpar, comparando-a com tratamento periodontal e
cirúrgica.
20. Comente reabsorção interna e externa da dentina.
PATOLOGIA GERAL - DB-301, UNIDADE III, FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
9
PATOLOGIA PERIAPICAL
1- INTRODUÇÃO:
As lesões periapicais na maioria das vezes correspondem a reações inflamatórias decorrentes da
necrose pulpar e contaminação bacteriana do canal radicular. Aceita-se que na ausência de bactérias a
inflamação apical é de pouca intensidade. Como ocorre com inflamação de outros tecidos, uma vez
removida a causa através da obturação do canal radicular, a normalidade do periápice é restabelecida. As
inflamações periapicais freqüentemente são crônicas e assintomáticas. No exame radiográfico aparecem
como áreas radiolúcidas circunscritas, e associada a dente sem vitalidade. Mesmo que a coroa esteja
integra, na presença de imagem radiolúcida associada ao ápice dentário deve-se considerar como
primeira hipótese de diagnóstico uma inflamação periapical. Até 1950 prevalecia o conceito do
tratamento de canal baseado na medicação antibacteriana, ao invés da limpeza químico-mecânica. Os
canais eram mal preparados e conseqüentemente mal obturados. As vezes a reação inflamatória se
desenvolve na porção lateral da raiz, ou seja em canais acessórios ou laterais. O processo é semelhante
ao que ocorre no ápice. Nestes casos, a polpa está desvitalizada. Processos agudos ocorrem em crianças,
nos dentes com canal amplo, ou em adultos devido aumento da carga bacteriana no ápice. Fatores locais
são os que determinam a evolução das inflamações periapicais, havendo pouca influência de fatores
sistêmicos, como diabetes, idade, fatores hormonais e imunosupressão. Como os agentes etiológicos
principais são as bactérias e seus produtos, na inflamação periapical predominam os fenômenos
imunológicos.
Os diferentes tipos de lesões periapicais representam diferentes estágios da reação inflamatória,
em diferentes fases de desenvolvimento.
2- ESTRUTURA DO PERIÁPICE:
O periápice é formado pela porção terminal da raiz, e o ligamento periodontal e osso alveolar
correspondentes. O ápice dentário é formado principalmente por cemento, sendo que o conjuntivo
intracementário está em continuidade com a polpa.
O limite CDC (cemento-dentina-canal) é considerado o ponto de referência para a obturação do
canal, corresponde ao ponto onde termina o canal formado por dentina e começa o formado por cemento.
Tem 0,5 - 2,0 mm de comprimento e 0,1 - 0,22 mm de diâmetro. Entretanto como na prática este limite
não pode ser definido, considera-se que a obturação deve ser feita 1-2 mm do ápice radiográfico. Após a
obturação do canal 1 a 2 mm aquém do ápice, pode ocorrer o selamento do canal com cemento. Por outro
lado sabe-se que se o canal estiver amplo ou alargado há penetração de tecido conjuntivo no canal, com
formação de material cementóide e/ou osteóide.
Através do ligamento periodontal do periápice penetra o feixe vásculo-nervoso para o interior do
dente. Além do forame principal deve-se considerar os canais laterais, canais na furca e presença de um
4o canal na raiz M-V em molares superiores.
2.1- Restos Epiteliais de Mallassez:
Os R.E.M. foram descritos em 1885 por Mallassez e são remanescentes da bainha de Hertwig
encontrados no ligamento periodontal. Geralmente aparecem como grupos de 10 células poliédricas e
uniformes, com escasso citoplasma e núcleo grande. São envolvidos externamente por membrana basal.
Ficam a 20-40µm do cemento.
De 280 dentes permanentes examinados por Reeve e Wentz, todos tinham R.E. Malassez. No
adulto predominam nos terços cervical e médio. Em jovens são mais numerosos do que em adultos, com
freqüência maior no periápice. Em dentes de pessoas jovens, terminando a formação da raiz, grupos de
células epiteliais podem estar em degeneração, com vacuolização e núcleo escuro e picnótico, às vezes
com calcificação.
PATOLOGIA GERAL - DB-301, UNIDADE III, FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
10
3- BACTÉRIAS:
As bactérias responsáveis pela inflamação periapical são oriundas do canal radicular (ver polpa).
Considera-se que se as bactérias não estiverem presentes, a resposta inflamatória apical é pequena, não
causando reabsorção óssea e formação de granuloma. Sundquist (1976) detectou bactérias nas polpas
necróticas de dentes com coroas íntegras, apenas nos casos com áreas periapicais radiolúcidas.
É discutível a presença ou não de bactérias nos granulomas e cistos periapicais. Deve-se
considerar que as células inflamatórias se concentram no periápice para destruir as bactérias que
ultrapassam o forame apical. Bactérias quando presentes nas lesões crônicas, deve ser por tempo
limitado e em pequena quantidade.
William Hunter em 1910 afirmava que o dentista criava “dourados mausoléus sépticos”,
colocando peças protéticas de ouro sobre dentes despolpados e contaminados, fontes de focos de
infecção.
4- PERICEMENTITE:
A pericementite é uma inflamação aguda do periápice, caracterizada clinicamente por grande
sensibilidade do dente ao toque. Radiograficamente pode-se eventualmente observar alargamento do
espaço periodontal provavelmente devido a extrusão dentária. Microscopicamente corresponde a
discreto acúmulo de neutrófilos e exsudato inflamatório. A dor intensa é devida principalmente a
compressão das fibras nervosas, visto que é uma área que não permite expansão ou drenagem de fluído
plasmático.
A pericementite pode ser uma extensão da inflamação aguda da polpa, ou ser decorrente de
trauma, pontos prematuros de contato, movimentação ortodôntica, irritação química ou mecânica
durante o tratamento de canal. O processo é reversível quando a causa é eliminada.
5- GRANULOMA:
Após a necrose pulpar, as bactérias que estão dentro do canal radicular, alcançam o periápice
apenas através do forame apical. A via de entrada é relativamente pequena, e o estímulo lesivo é
constante e de baixa intensidade. Há conseqüentemente o desenvolvimento de um processo crônico, sem
sintomatologia dolorosa. Com o decorrer do tempo há reabsorção óssea e a lesão geralmente é detectada
no exame radiográfico, sendo chamado de granuloma.
Os granulomas apicais são portanto processos inflamatórios crônicos para combater e neutralizar
os agentes agressores do canal. O termo granuloma é usado porque a reabsorção óssea em torno do ápice
dentário permite a reação inflamatória ocupar um espaço circular ou oval, com a forma de um grânulo de
1-5 mm de diâmetro. O termo granuloma foi inicialmente aplicado na tuberculose, mas foi
posteriormente usado em outros processos inflamatórios específicos ou não, desde que circunscritos e
com a forma de um grão.
O granuloma periapical é uma inflamação crônica, com predominância de células
imunologicamente competentes, como os macrófagos, linfócitos e plasmócitos. Os LT predominam
sobre os LB. Os neutrófilos se localizam principalmente na área do forame apical. Contém também
vasos e fibroblastos. Corpúsculos de Russel são encontrados na maioria dos granulomas e cistos.
Correspondem a plasmócitos hialinizados facilmente identificados. Os granulomas muitas vezes têm
uma cápsula que se adere a raiz.
Após o tratamento de canal os granulomas regridem, com a área adquirindo aspectos
radiográficos normais após 12 meses.
6- CISTO PERIAPICAL:
Cisto é uma cavidade patológica revestida por epitélio. No periápice é feito o diagnóstico de cisto
quando a lesão apresenta epitélio oriundo dos restos epiteliais de Malassez. Como a formação da
cavidade cística é gradativa, o epitélio pode apresentar-se em diferentes graus de proliferação e
organização.
PATOLOGIA GERAL - DB-301, UNIDADE III, FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
11
A proliferação epitelial é estimulada pela reação inflamatória, que deve causar rompimento da
membrana basal que envolve as células epiteliais. Portanto o cisto periapical é oriundo de um
granuloma, embora nem todos os granulomas evoluam obrigatoriamente para cistos.
Radiograficamente não é possível distinguir os cistos dos granulomas, mas geralmente os cistos
são maiores e com limites ósseos mais delimitados. Microscopicamente a cavidade cística pode ou não
ter continuidade com o forame apical.
O tratamento dos cistos é semelhante ao dos granulomas. Aceita-se que a maioria dos cistos
regridem após o tratamento endodôntico, sendo pouco freqüente as cirurgias das lesões apicais. A célula
epitelial pode se comportar como antígeno, pois pode ser modificada pela reação inflamatória e
antígenos do canal.
7- REPARAÇÃO DAS LESÕES PERIAPICAIS:
Por muito tempo considerou-se que apenas os granulomas regrediam após o tratamento de canal,
e que os cistos precisavam de complementação cirúrgica. Esta idéia foi suportada em 1961 pela
Associação Americana de Endodontistas. Bhaskar (1966) rejeitou esta hipótese, pois de 2.308 lesões
examinadas, 42% eram cistos, 48% granulomas e 10% outras lesões não inflamatórias. Considerando
que em 90% dos casos há regressão, deve-se aceitar que cistos regridem. Saada (1987) verificou que
57% das lesões persistentes após o tratamento endodôntico eram granulomas.
EM RESUMO:
- O procedimento clínico é o tratamento de canal. Se a lesão persistir deve-se analisar a obturação
e refazer o tratamento. A remoção cirúrgica deve ser reservada para os casos de não sucesso pela
endodontia.
- As lesões que não regridem após tratamento endodôntico podem ser granulomas ou cistos.
- Há casos de cistos que não regridem mesmo quando a obturação do canal elimina as bactérias.
- As lesões residuais que persistem são sempre cistos.
7- ABSCESSO PERIAPICAL:
O abscesso periapical é diagnosticado clinicamente, apresentando-se com aumento de volume da
face e intensa dor. É comum em crianças, quando tem evolução rápida devido ao amplo forame apical.
Nestes casos não há imagem radiolúcida no periápice. Em adultos geralmente ocorre pela agudização do
granuloma ou cisto preexistente.
A via de drenagem do abscesso depende da posição da raiz envolvida. Pode ocorrer por via
vestibular, lingual, palatina ou cutânea. A fistula é recoberta por tecido de granulação, mas na região da
superfície da mucosa ou pele é revestida por epitélio. A fistula regride com o tratamento do abcesso.
O tratamento do abscesso deve ser feito por drenagem do material purulento, associado a
antibioticoterapia e tratamento de canal.
8- CICATRIZ PERIAPICAL:
Após o tratamento de canal, a área radiolúcida periapical pode aumentar ou diminuir, até o
restabelecimento da normalidade. Eventualmente a área diminui, mas não desaparece. Nestes casos
pode-se tratar de uma cicatriz fibrosa periapical. Ao invés da formação de tecido ósseo, a cavidade é em
parte preenchida por tecido fibroso, como numa cicatriz da pele. Calcula-se que 3% das radiolucências
periapicais correspondem a cicatrizes periapicais.
Alguns autores consideram que as cicatrizes se formam após curetagem do periápice, quando o
espaço destruído é maior.
9- CISTO RESIDUAL:
Pacientes desdentados podem apresentar aumento de volume localizado na mandíbula ou maxila,
que radiograficamente correspondem a áreas radiolúcidas. A remoção cirúrgica e exame histopatológico
confirmam o diagnóstico de cisto. Microscopicamente o cisto apresenta além do epitélio, densos feixes
PATOLOGIA GERAL - DB-301, UNIDADE III, FOP/UNICAMP
ÁREAS DE SEMIOLOGIA E PATOLOGIA
12
de colágeno e infiltrado inflamatório discreto. No cisto residual o epitélio é delgado, pois está envolvido
por tecido fibroso, com poucas células inflamatórias que estimulariam a proliferação epitelial. São
chamados de cisto residual porque permanecem e evoluíram mesmo após a extração do dente ao qual
estava associado. Achamos que é um bom exemplo para demonstrar que cistos periapicais nem sempre
regridem após a eliminação do agente etiológico.
OBJETIVOS:
01. Defina lesão periapical.
02. Comente a importância dos fatores locais e sistêmicos nas lesões periapicais.
03. Quais os componentes do periápice?
04. Que é CDC e qual sua importância?
05. Que são restos epiteliais de Malassez e qual seu aspecto microscópico?
06. Comente a origem e a presença de bactérias nas lesões periapicais.
07. Que é pericementite e quais suas possíveis origens?
08. Que são granulomas periapicais?
09. Que células predominam nos granulomas periapicais?
10. Conceitue cisto periapical e diferencie-o de um granuloma periapical.
11. Qual o tratamento de granulomas e cistos periapicais, e o que pode se esperar como resposta
evolutiva destas lesões após o tratamento?
12. Defina abscesso periapical, e explique seu tratamento.
13. Comente cicatriz periapical.
14. Que são cistos residuais?
15. Quais os achados microscópicos em cistos residuais?