As questões feitas pelos alunos estão separadas por tópicos:
DISTRIBUIÇÃO ELETRONICA
Qual será a distribuição eletrônica em subníveis do sódio (Na) depois de ganhar 2
elétrons?
Resolva a distribuição eletrônica dos seguintes elementos:
Na –
Si –
Fe2+ –
O2- –
O diagrama de Pauling simplifica a tarefa de distribuir os eletrons em um átomoneutro.
Nele existem 7 níveis e 4 subníveis. Qual é respectivamente o numero máximo de
elétrons pó nível e subnível.
a) 1, 2, 3, 4, 5, 6, 7 / 8, 9, 10, 11
b) 5, 10, 15, 20, 25, 30, 25 / 2, 6, 10, 14
c) 2, 8, 18, 32, 32, 18, 2 / 2, 6, 10, 14
d) 14, 10, 16, 2 / 2, 8, 32, 32, 8, 18, 2
Faça a distribuição eletrônica para o Sn.
O que acontece quando há menos elétrons na ultima camada? Por quê?
A distribuição eletrônica do átomo de ferro é 1s2 2s2 2p6 3s2 3p6 4s2 3d6, com esses
dados, quantos átomos ele tem na camada mais externa?
CLASSIFICAÇÃO PERIODICA DOS ELEMENTOS
São propriedades dos metais:
a) densidade baixa.
b) maleabilidade.
c) ponto de fusão e ebulição elevadas.
d) condutividade térmica e elétrica baixa.
Como são divididos os elementos na tabela periódica, cite as suas características:
O que indica o aumento do numero atômico quando passamos de uma “casa” para outra
ao longo dos 7 períodos?
O elemento que estiver na família A, tende a doar ou a receber elétrons?
Quando um átomo irá adquirir estabilidade?
Caracterize o elemento de numero atômico 56.
.
As dezoitos linhas verticais que aparecem na tabela são denominadas colunas, grupos
ou famílias, algumas dessas famílias t^m nomes especiais. Cite esses nomes.
Todas as alternativas são falsas, EXCETO:
a) Be, Mg, Ca, Sr, Ba, Ra são calcogênios
b) São metais alcalinos: Li, Na, K, Rb, Cs, Ra.
c) Ligações apolares: apresentam diferença de eletronegatividade diferente de zero.
d) Os elementos da coluna 8A são gases nobres.
e) Óxidos básicos são formados por ametais com nox altos.
Na tabela periódica existem elementos naturais e elementos artificiais. Explique o que
são elementos artificiais e naturais e dê dois exemplos.
Mendeleyev, um químico russo foi o criador da tabela periódica, e depois de algum
tempo e deduções ele chegou a algumas conclusões, como: muitas propriedades físicas
e químicas dos elementos variam periodicamente na seqüência de suas massas atômicas.
Essas são características de uma lei, qual será está?
Os nomes dos elementos químicos conhecidos desde a antiguidade foram dados
arbitariamente e variam de uma língua para outra. Cite alguns:
O que são átomos biatômicos?
De acordo com quais critérios os elementos são distribuídos na tabela periódica
moderna?
Os elementos lítio, sódio e os outros elementos da família 1ª são metais alcalinos ou
alcalino-terrosos?
Considerando os átomos Al e O, dê a classificação desses átomos e a formula da
sustância iônica formada.
PROPRIEDADES PERIODICAS E APERIODICAS
Como chama a energia liberada quando um elétron é adicionado a um átomo neutro no
estado gasoso?
Raio atômico, volume atômico, densidade absoluta são características de uma
propriedade _________.
Agora número de massa que sempre aumenta com o número atômico e calor específico
são características de uma propriedade _________.
Qual é o marco anunciado da lei da periodicidade.
Qual dos elementos abaixo apresenta maior potencial de ionização:
a) H - hidrogênio
b) He – hélio
c) F – flúor
d) Be – berílio
e) Li – lítio
LIGAÇÕES QUIMICAS
Como se chama a propriedade que os metais apresentam de se deixarem reduzir a
chapas e lâminas?
Quais são as características dos metais?
Quais são as diferenças entre os metais e os não-metais?
Com relação às propriedades dos metais, todas as alternativas estão corretas, EXCETO:
a) Condutividade térmica e elétrica – os metais possuem elétrons livres em suas ligações
metálicas, permitindo a passagem rápida de temperatura e calor
b) Resistência – os metais são bastante resistentes quando estão sendo tracionados com
força. Isso ocorre porque os átomos estão bem separados.
c) Ponto de fusão e ebulição – os metais fundem e fervem em temperaturas elevadas,
graças à ligação metálica ser muito forte.
Por que os compostos iônicos são sólidos?
Quais são as principais características dos metais?
Qual a comparação entre ligação iônica e covalente?
Dê exemplos de cátions monovalentes, bivalentes, trivalentes e tetravalentes.
Como podemos classificar as ligações covalentes, explique:
Complete as frases:
a) Um átomo adquire estabilidade quando possui ______, na camada eletrônica mais
externa ou _______ quando possui apenas a camada K.
b) Ligação iônica é a força que mantêm os __________ depois que um átomo cede
_______________ um, dois ou mais elétrons para outro elétrons para outro átomo.
c) Ligação covalente é a _______ entre ________ estabelecida por pares de elétrons.
d) Ligas metálicas são ________ de dois ou mais ________ podendo ainda incluir
semi-metais ou ________.
GEOMETRIA MOLECULAR
Explique o fenômeno da alotropia e dê dois exemplos.
Explique sobre a alotropia de carbono do enxofre e do fósforo.
Dê a geometria molecular de cada composto abaixo:
a) PCl4
b) H2, HCl e CO2
c) CH4
d) H2O
e) BF3
f) SF6
g) NH3
Qual é o tipo de estrutura molecular dos elementos CH4 e BeH2.
Desenhe exemplos de formas moleculares, trigonal, bipiramidal trigonal, tetraédrica e
linear.
As moléculas piramidais apresentam a formula:
a) AX3, são polares e formadas por elementos da coluna 5A.
b) Apresentam a mesma formula das tetraédricas, que, ao contrário destas, são apolares
e compostas somente de elementos da coluna 3A.
c) AX5, sendo polares e podendo também ser bipiramidais.
d) AX3, polares e compostas de elementos da coluna 3A.
ELETRONEGATIVIDADE
Coloque V ou F:
( ) O cloro não é mais eletronegativo que o hidrogênio.
( ) A eletronegatividade é também uma propriedade periódica
( ) O crescimento da eletronegatividade é da direita para esquerda e de baixo para cima.
OXI-REDUÇÃO
Quantos elétrons o carbono doa em uma ligação?
Qual o numero de oxidação dos seguintes elementos marcados
H3PO3
CaCO2
KMnO4
Calcule o nox dos elementos sublinhados:
a) Ca3(PO4)2
b) Cu(NO3)2
c) SO42Explique o que é e o que ocorre na oxi-redução
Quando um elemento sofre oxidação? E redução?
“Os fenômenos de oxidação e redução são fenômenos importantes na química e
freqüente no nosso dia-a-dia”. Com base na afirmação, dê um exemplo de oxidação e
exemplifique.
FORÇAS INTERMOLECULARES
Algumas substâncias apolares podem ser liquefeitas e solidificadas com facilidade. Esse
fenômeno deve-se a um dos tipos de ligação estudadas. Cite qual é este tipo de ligação e
explique-a
Como podemos determinar se um composto é iônico ou molecular, polar ou apolar?
Explique as ligações dipolo-dipolo e diga em que tipo de molécula ocorre.
O que ocorre quando há ligação de Van der Waals?
Complete a frase:
Substância polar tende a se dissolver em outra substância ______, e substância apolar
tende a se dissolver em outra substância ______.
GRAU DE IONIZAÇÃO
O que é função química?
Qual a diferença de dissociação e ionização?
Como descobrimos o grau de ionização de uma molécula?
O que é o potencial de ionização? Como esse potencial é expresso?
O grau de ionização varia. Das alternativas abaixo, qual está correta?
a) 0 e 1 (ou 0% ou 100%), o valor zero está bastante ionização e o valor aproxima de
um está pouco ionizada.
b) o grau de ionização varia de 0,08 ou 8% até 0,92 ou 92%.
c) quando o α tem valor próximo de zero, é chamado de eletrólito fraco e quando o α
tem valor aproxima de 1, é chamado de eletrólito forte.
d) O grau de ionização (α) é representado dessa forma, “o número de moléculas
dissociadas é dividida pelo número de moléculas ionizadas”.
Qual a finalidade de uma dissociação?
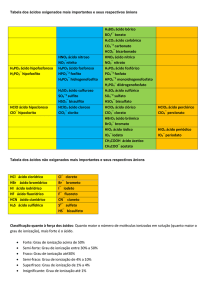
ÁCIDOS
Cite 3 ácidos e determine a sua utilização
Quais são as duas características dos ácidos
O que é necessário analisar para saber se uma substancia é ácida? Dê exemplo.
Quais são as principais propriedades dos ácidos?
Os ácidos são muitos usados em industrias químicas? Se for, para quê? E dê exemplo do
principal ácido usado em industria química?
Quais as características dos ácidos?
De acordo com quais critérios é dada a classificação dos ácidos?
O que é um hidrácido? E um oxiácido?
Faça a classificação dos ácidos de acordo com o número de hidrogênios ionizáveis.
BASES
Classifique as bases, tomando como exemplo os critérios já estudados:
a) KOH
b) Ba(OH)2
c) Fe(OH)3
e) Zn(OH)2
d) Al(OH)3
f) Ca(OH)2
Um composto que libera oxidrila em solução aquosa é:
a) base, como H2SO4
b) ácido, como H3PO4
c) anidrido, como CO
d) base, como NH4OH
e) ácido, como o Sn(OH)4
O hidróxido de amônio, que é muito usado em limpeza domestica, como fertilizante
agrícola e na produção de compostos orgânicos e como gás de refrigeração. Dessa
substância é incorreto afirmar que:
a) tem formula NH4OH.
b) é um composto iônico.
c) é usado na produção de sabões.
d) é uma molécula insolúvel em água.
As bases são formadas por metal, que constitui um radical positivo ligado
individualmente ao OH-, há uma única base não metal, qual é essa base?
O que é necessário para formarmos substâncias básicas e quais são suas propriedade
NaOH e Mg(OH)2 como já vimos, são bases. Em que no nosso dia-a-dia elas podem ser
úteis? Qual é forte e qual é fraca? Dê os nomes.
Quando uma base sofre dissociação iônica, o que essa base libera na água?
OXIDOS
Qual a formula do óxido periódico
a) H2IO2
b) HIO3
c) HIO4
d) HI
f) H3PO3
Dê a formula do composto de Al e O, classifique em ácido, base ou óxido e nomei-o.
A água oxigenada é um exemplo de:
a) Peróxido
b) Hidrácido
c) Base
d) Óxidos anfótero
Cite as possíveis classificações dos óxidos e dê pelo menos uma característica para cada
uma delas.
Quais são os óxidos que se comportam ora como básico, ora como ácido?
Descreva o comportamento dos óxidos anfóteros.
Dentre as alternativas abaixo, escolha a que enumera corretamente as características dos
óxidos anfóteros.
a) São insolúveis em água, geralmente são líquidos.
b) São, em geral, sólidos, iônicos, insolúveis na água.
c) São solúveis em água, formado apenas por semimetais.
d) São sólidos, solúveis em água.
Existe um tipo de óxido que não reage com a água, que é chamado de “óxido
indiferente”. Cite os mais comuns.
Classificamos os compostos em que o oxigênio apresenta nox = -1, como:
a) oxiácido, moderado, diácido
b) monobase, forte
c) oxiácido, forte, diácido
d) dibase, moderado
e) peróxido
Um estudante relatou ter obtido através da reação entre Na2O + H2O um ácido. O relato
do estudante é verdadeiro ou falso. Justifique.
OUTROS
Qual é a maneira, que também pode ser entendida, sobre a lei de Lovoisier?
(a) A soma das massas antes da reação é igual a subtração das massas após a reação.
(b) A soma das massas antes da reação é igual a soma das massas após a reação.
(c) A subtração das massas antes da reação é igual a subtração das massas após a
reação.
(d) A subtração das massas antes da reação é igual a soma das massas após a reação
Complete a 2ª coluna de acordo do a 1ª coluna:
(1) Fusão
( ) é a passagem do estado líquido para o gasoso.
(2) Vaporização
(3) Ebulição
( ) é a vaporização rápida, com agitação do líquido e
aparecimento de bolhas.
( ) é a passagem do estado sólido para o líquido
Enumere a 2ª coluna de acordo com a 1ª coluna:
(1) É um dos produto da queima do carvão ( ) NaOCl
(2) É utilizado na fabricação de sabões
( ) Na2CO3
(3) É utilizado para limpezas
( ) NaCl4
(4) Contém na água do mar
( ) H2O2
(5) É utilizado no branqueamento de cabelo ( ) CO2
Explique o que é uma reação de salificação e dê um exemplo e a reação.
Diga de onde se originam as substâncias inorgânicas e as substâncias orgânicas
Cite um composto que solubilizado em água, geram soluções aquosa.
O que acontece com um ácido e uma base quando essas duas substâncias se misturam?