Conjunto
Código
PF - 4º
Q14
Período Turma
T
A
Data
09/11/06
1. Na combustão de 20,0 mols de isoctano (C8H18), de acordo com a seguinte equação, há
a produção de x mols de CO2 e y mols de H2O Assim, x e y são, respectivamente:
C8H18(g) +
a) 4 e 4,5.
b) 8 e 9.
25
O2(g) 8 CO2(g) + 9 H2O(g)
2
c) 16 e 18.
d) 20 e 40.
e) 160 e 180.
2. Considere a reação entre sódio metálico e água representada pela equação:
Na(s) + H2O(aq) ½ H2(g) + NaOH(aq)
Numa reação realizada nas CNTP são utilizados 46 mg de sódio. O volume de hidrogênio
obtido é de aproximadamente:
(Dados: Na: 23 g/mol; volume molar nas CNTP = 22,4 L)
a) 2,2 mL.
b) 4,4 mL.
c) 22,4 mL.
d) 2,24 L.
e) 22,4 L.
3. Considere a reação entre hidróxido de potássio e ácido clorídrico representada pela
seguinte equação:
KOH(aq) + HCl(aq) H2O(l) + KCl(aq)
A massa de hidróxido de potássio necessária para a produção de 150 g de KCl é de
aproximadamente:
(Dados: KOH: 56 g/mol; KCl = 74,5 g/mol)
a) 2 g.
b) 56 g.
c) 22,4 g.
d) 113 g.
e) 224 g.
4. Na reação representada por CH4(g) + 4 Cl2(g) CCl4(l) + 4 HCl(g) há liberação de 108 kJ
de energia térmica por mol de HCl(g) formado. Nas mesmas condições, qual será a energia
térmica liberada na formação de 73 g de HCl(g)?
(Dados: massas atômicas: H = 1,0 u; Cl = 35,5 u)
a) 54 kJ.
b) 108 kJ.
c) 162 kJ.
d) 216 kJ.
e) 432 kJ.
5. Uma determinada quantidade de um composto contendo potássio, cromo e oxigênio foi
analisada e obteve-se os seguintes resultados: 1,98 g de potássio, 3,96 g de cromo e
4,06 g de oxigênio.A fórmula correta do composto é:
(Dados: massas atômicas: O = 16 u; K = 39 u; Cr = 52 u)
a) KCrO2.
b) KCrO3.
c) K2CrO4.
d) K2Cr2O7.
e)
K2Cr3O10.
6. A combustão da grafite é representada por:
C(grafite) + O2(g) CO2(g)
H = – 94 kcal/mol
A energia térmica requerida para dissociar 88 g de gás carbônico em carbono grafite e
oxigênio, em kcal, é de:
(Dados: CO2 = 44 g/mol)
a) 44.
b) 66.
c) 94.
d) 188.
e) – 94.
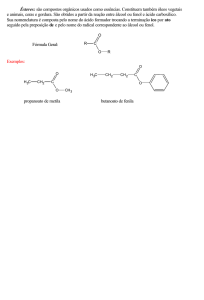
7.
As funções presentes na molécula do composto a seguir são:
H
CH 2
C
CH3
O
CH
OH
a)
b)
c)
d)
e)
8.
cetona e amina.
aldeído e álcool.
aldeído e ácido carboxílico.
fenol e álcool.
aldeído e cetona.
Os nomes oficiais dos compostos são, respectivamente:
OH
H3C
CH
HO
O
CH 2
OH
C
H
CH3
CH3
a)
b)
c)
d)
e)
1,2–dimetilfenol, 1,2,3–propanotriol e etanal.
3–metilfenol, 1,2,2–propanotriol e metanal.
3–metilfenol, 1,2–propanodiol e etanal.
álcool 3–metilbenzílico,1,2–propanodiol e etanal.
3–metilfenol, 2,1–propanodiol e etanal.
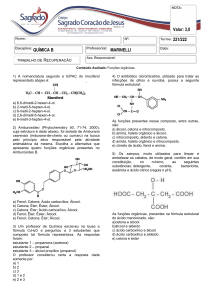
9. O óleo de amêndoas, muito usado em cosméticos e alimentos, é rico no seguinte
composto que lhe dá odor característico:
H
C
O
A função presente neste composto é:
a) álcool.
b) fenol.
c) cetona.
d) ácido carboxílico.
e) aldeído.
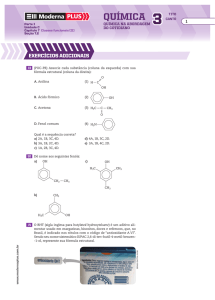
10. As funções orgânicas do composto a seguir são:
HO
CH
CH3
O
C
HO
H
CH 2
C
O
a)
b)
c)
d)
e)
álcool, aldeído e ácido carboxílico
álcool, ácido carboxílico e cetona.
fenol, ácido carboxílico, álcool .
fenol, éter e álcool.
álcool, amida e éster.