Química 1
aulas 1 e 2
COMENTÁRIOS – ATIVIDADES
1.
I.
II. Cálculo do calor necessário para 400g de H2O, a
uma temperatura de 55°C, passar para 0°C.
QL = MC = ΔT
QL = –400 . 55
QL = −22.000cal → calor liberado
PARA
SALA
De acordo com o equilíbrio:
SO2(g) + O2(g)
Como |QF| > |QL|, implica que a água líquida entrará
em equilíbrio térmico com o resto da massa de gelo
que sobrará. No equilíbrio teremos uma temperatura
de 0°C.
2 SO3(g)
Esse tipo de reação é bastante comum na atmosfera
das regiões onde há uma emissão de gases provenientes de queima de combustíveis fósseis, porém trata-se de um equilíbrio homogêneo.
II. No equilíbrio:
hemoglobina + oxigênio
III. Cálculo da massa de gelo que sobrará:
Q − QL 24.000 − 22.000
=
= 25g
M= F
L
80
Sobrarão 25g de gelo a 0°C.
Resposta correta: C
oxiemoglobina
Em locais de grande altitude, a pressão é menor,
implicando no deslocamento de equilíbrio no sentido inverso (maior número de mol), assim, a quantidade de oxigênio dissolvido no sangue diminui, causando as consequências citadas no enunciado.
COMENTÁRIOS – ATIVIDADES PROPOSTAS
1.
Resposta correta: B
2.
O diamante, a grafita e o fulereno são formas alotrópicas cristalinas. Existem também em maior quantidade as
formas amorfas. A forma mais rara e mais dura do diamante é a forma covalente, em que o carbono forma
uma estrutura tridimensional.
Resposta correta: C
3.
a) Falso – Desinfetantes e cosméticos produzidos a
partir do eucalipto são misturas de substâncias e,
portanto, não possuem ponto de fusão definido.
b) Falso – A celulose é um composto orgânico, sendo
classificado como um polímero formado pela união
de moléculas de β-glucose.
c) Falso – Os desinfetantes e os cosméticos não são
substâncias alotrópicas. Como exemplos de substâncias alotrópicas temos, carbono: (carbono grafite,
carbono diamenta, fulerenos); enxofre: ( rômbico,
monoclínico).
d) Verdadeiro – A madeira é um material orgânico,
como já comentado no item B.
Resposta correta: D
2.
a) Admitindo-se a existência de líquido nos frascos, a
temperatura máxima alcançada pelo sistema constituído pelo líquido X + frasco é 50°C (durante o processo
de ebulição). Esse frasco poderá ser tocado com a
mão, sem que houvesse risco de queimaduras.
No sistema constituído pelo líquido Y + frasco, a temperatura máxima alcançada é 100°C, quando atinge o
equilíbrio com a chapa elétrica de aquecimento. Neste
caso, poderá haver risco de queimaduras, se o frasco
em questão for tocado com a mão.
b) A adição de um soluto não-volátil eleva a temperatura de ebulição de um líquido. Portanto:
– o líquido X poderá atingir uma temperatura superior a 50°C, antes de entrar em ebulição.
– a temperatura máxima que o líquido Y atingirá
será 100°C, mesmo com a presença de soluto
não-volátil, porque é igual à temperatura de aquecimento da chapa.
3.
•
Resposta correta: D
4.
O ar dissolvido na água líquida não é solúvel na água
sólida, com isso, ocorre a formação de bolhas.
Resposta correta: E
5.
Mgelo = 300g
MH2O = 400g
Tgelo = 0°C
TH2O = 55°C
I. Sendo QF a quantidade de calor absorvido pelo gelo
para se fundir, temos:
a) Correta. O sistema mostra a mudança de estado
físico da água pura, portanto o ponto de fusão permanece constante até o derretimento total da água
sólida (0°C).
b) Correta. A massa da fase sólida diminuirá porque a
temperatura ambiente (25°C) é maior que 0°C.
c) Correta. A pressão de vapor da fase líquida permanecerá constante, pois a temperatura do sistema é
constante (0°C).
d) Errada. A relação quantidade de matéria por volume será diferente, pois o volume ocupado pela fase
líquida é menor em relação à fase sólida, para uma
mesma massa.
e) Correta. A massa do corpo diminuirá devido à evaporação da água, pois é um sistema aberto.
massa
calor de fusão de gelo
QF = M . L
•
QF = 300 . 80
QF = 24.000cal
Substâncias puras apresentam temperatura de fusão
e ebulição constantes. No caso, a substância 1 apresenta ponto de ebulição constante e igual a 100ºC
ou pode ser uma mistura azeotrópica (ponto de fusão constante e ponto de ebulição variável).
Os béqueres 2 e 3 não apresentam o mesmo soluto,
pois a temperatura de ebulição é diferente.
Logo, I e II são verdadeiras e III é falsa.
Resposta correta: B
3ª SÉRIE E EXTENSIVO OLÍMPICOS
|
VOLUME 1
|
QUÍMICA 1
1
4.
Mistura heterogênea é aquela que apresenta propriedades microscópicas diferentes, em pontos diferentes da
mistura.
Exemplo:
10. Analisando o gráfico, podemos observar que no ponto D
coexistem as fases líquida e de vapor.
Resposta correta: E
11.
Substância
X
Y
W
R
Resposta correta: C
5.
A densidade da água é (1,0g/cm3) e a densidade do álcool
(d = 0,78g/cm3). Como as gotículas de óleo ficaram na
região interfacial entre água e óleo, justifica-se assim o
fato de as gotículas de óleo ficarem suspensas na água.
Assim, temos: dH2O > dóleo > dálcool .
a 2°C
a 30°
líquido
gasoso
líquido
gasoso
sólido
sólido
gasoso
gasoso
T = líquido; a 100° = gasoso
R e W respectivamente.
Resposta correta: A
12.
Resposta correta: A
6.
Quando misturamos água com gasolina, o álcool presente na gasolina se solubiliza formando uma mistura de
álcool + água + gasolina.
Resposta correta: E
7.
O Ca3(PO4)2 é um antiumectante muito usado em bebidas. Sua função é diminuir a adesão da umidade por
parte das bebidas.
Como o tempo de mudança de fase em B é relativamente maior que em A, temos que a massa de B é maior que
a massa de A.
Resposta correta: C
Resposta correta: D
13. O tempo em que a temperatura permanece constante é
justamente o necessário para que todas as moléculas
vençam as forças intermoleculares.
8.
Resposta correta: D
14. Considerando a mesma massa de água, a quantidade de
energia liberada em I (processo endotérmico) é igual à
quantidade de energia absorvida em II (processo endotérmico).
Resposta correta: E
15.
Pela análise do gráfico, podemos observar que o líquido I,
durante a ebulição, permanece à temperatura constante,
caracterizando assim uma substância pura, e II, por não
possuir temperatura de ebulição constante, apresenta
uma curva que pode representar uma solução.
Resposta correta: A
9.
2
Como o barro é poroso, a água o atravessa e entra em
contato com o ar, evaporando. Como o processo de
evaporação da água é endotérmico, retirando calor da
cerâmica ou moringa, a água ficará resfriada.
Pela análise do gráfico, podemos observar o aquecimento de uma mistura eutética. Este sistema possui ponto
de ebulição variável.
Resposta correta: C
Resposta correta: E
3ª SÉRIE E EXTENSIVO OLÍMPICOS
|
VOLUME 1
|
QUÍMICA 1
16. I.
( F ) T2 corresponde ao máximo de temperatura
atingida quando submetida à pressão P2.
II. ( V )
III. ( V )
3.
Resposta correta: E
17. I. ( F ); II. ( F ); III. ( V ); IV. ( F)
Apoiado na visão substancialista do autor, temos os itens I, II e IV, sabendo que são quimicamente sem fundamento.
I. ( V )
II. ( F ) Levando em conta a reatividade dos metais,
temos a seguinte ordem: (o cobre é mais reativo que o ouro), logo, na reação com HNO3 o
ouro não reagirá.
O sólido X possui massa molecular 197g/mol.
III. ( V )
IV. ( F ) Cu(NO3)2 + Zn
→
Zn(NO3)2 + Cu
↓
↓
Resposta correta: D
18. O ferro possui ponto de fusão mais elevado que os
outros metais citados. Devido à dificuldade de atingir
temperaturas mais elevadas sua extração foi mais tardia.
NOX = 0
↑ NOX: oxidação
Resposta correta: B
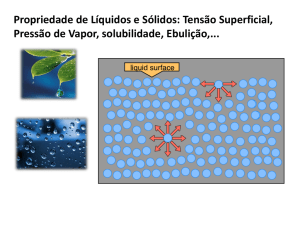
19. Analisando a figura, podemos observar que as “moléculas” estão próximas, porém, em estado relativamente
desorganizado.
Resposta correta: D
ag. redutor
Resposta correta: B
4.
20. De acordo com as características citadas no texto, temos, respectivamente:
W: grafite.
Y: Óxido de alumínio.
X: Ácido acético.
Z: Cobre.
5.
COMENTÁRIOS – ATIVIDADES
1.
PARA
SALA
I. (F) É utilizada na separação de líquidos imissíveis.
II. (V)
III. (F) A vidraria (B) é o condensador, um dos instrumentos usados na aparelhagem do sistema de
destilação.
IV. ( V )
Resposta correta: C
Resposta correta: E
aulas 3 e 4
NOX = +2
De acordo com o esquema, todas as alternativas estão
corretas.
Resposta correta: E
COMENTÁRIOS – ATIVIDADES PROPOSTAS
1.
O equipamento apresentado na figura é utilizado para
realizar a filtração a vácuo. Essa filtração utiliza uma
trompa de água para reduzir a pressão e aumentar a velocidade do processo de filtração.
Os equipamentos utilizados no processo são: funil de
Büchner, papel de filtro e kitassato.
A filtração é um processo utilizado para separar componentes de uma mistura heterogênea do tipo sólido mais líquido.
Resposta correta: D
2.
a) 80g
b) Temos 20g de fenolftaleína:
100mL
6,7g
350mL
x
x = 23,45g
O volume de etanol é suficiente para dissolver toda
a fenolftaleína.
O álcool é solúvel em água devido à sua parte polar
(–CH2–O–H), ocorrendo ponte de hidrogênio entre
as duas espécies.
A parte apolar do etanol (H3C–CH2–) é responsável
pela dissolução da fenolftaleína por meio de forças
de Van der Waals entre as duas espécies.
A adição de água (bastante polar) na solução de fenolftaleína em etanol deixa o meio mais polar, provocando a cristalização da fenolftaleína. Esta é insolúvel em solvente bastante polar.
3ª SÉRIE E EXTENSIVO OLÍMPICOS
Resposta correta: E
|
VOLUME 1
|
QUÍMICA 1
3
2.
O processo de destilação é um processo de purificação
de água em laboratório.
11. O gráfico que demonstra este comportamento é:
Resposta correta: E
3.
A sinfonação é um processo de separação que é executado com o auxílio da gravidade.
Pois à medida que aumentamos a temperatura, também
aumentamos a quantidade de compostos em ebulição.
Resposta correta: D
12. De acordo com o conceito de destilação.
Resposta correta: B
Resposta correta: C
4.
Uma extração do café em água, e posteriormente uma
filtração de possíveis resíduos sólidos.
13. A destilação é usada na separação de misturas homogêneas líquidas.
Resposta correta: C
Resposta correta: A
5.
A separação magnética é usada para separar metais de
não-metais.
14. Decantação: separa o petróleo da água.
Filtração: separa o petróleo das impurezas.
Resposta correta: A
Resposta correta: E
6.
De acordo com os conceitos de conservação e preservação do meio ambiente.
15. VG = 50mL
VH2O = 50mL
50mL de gasolina
12,5mL
Resposta correta: D
7.
VG pura = 12,5mL
As telas funcionam como um filtro para retirada de materiais em suspensão (filtração), e quando mantida em repouso
nos tanques, temos a caracterização de uma decantação.
100%
y
y = 25%
Resposta correta: B
Resposta correta: E
8.
Separação I: decantação.
Separação II: flotação.
Separação III: destilação fracionada.
Resposta correta: B
9.
O açúcar em solução pode ser separado por uma filtração (para retirada de precipitados) e posteriormente
uma destilação simples.
Resposta correta: E
16. Como o composto formado é básico (AA(OH)3), pode ser
neutralizado por um ácido.
Resposta correta: B
17. Se água + açúcar formam uma mistura heterogênea,
pode ser separada por filtração.
Resposta correta: A
18. No Erlenmeyer ficará o produto final, H2O destilada.
Resposta correta: A
10.
19. O etanol não é solúvel em álcool hidratado, logo, pode
ser separado por filtração simples.
Resposta correta: A
20. Podemos observar que o mercúrio é condensado e
coletado em um béquer. Logo, podemos concluir que o
mercúrio é mais volátil.
Resposta correta: D
4
Resposta correta: A
3ª SÉRIE E EXTENSIVO OLÍMPICOS
|
VOLUME 1
|
QUÍMICA 1
21. De acordo com os processos de separação adequados.
27.
Resposta correta: A
22. I.
II.
III.
IV.
V.
(V)
(F)
(F)
(F)
(F)
em nenhum dos casos, é possível separar a
parafina da sacarose (C12H22O11).
Resposta correta: V, F, F, F, F
23. Usando soluções com densidade 2,1g especificamente,
teremos o seguinte esquema de separação:
50mL de gasolina
+
5mL de água
100mL no
total
Logo, se temos 61mL de solução aquosa, teremos 39mL
de gasolina, e 11mL de álcool, assim:
50mL
100%
11mL
x = 22% de álcool
Resposta correta: B
28. De acordo com as características de cada método de
separação, podemos afirmar que se referem a decantação, filtração e destilação.
Resposta correta: D
29. O primeiro processo trata-se de uma extração, o segunde uma filtração simples e o terceiro de uma destilação
simples.
Resposta correta: A
24. I. ( F ) O N2 possui comportamento de gás real.
II. ( V )
III. ( F ) O N2 só poderá sofrer compressão a baixas
temperaturas.
Resposta correta: D
30. Provavelmente, o sólido X trata-se de uma mistura, pois
possui ponto de fusão variável.
Resposta correta: B
Resposta correta: A
25. I. ( V )
II. ( F ) A concentração das soluções é diferente, D é
mais concentrada que A.
III. ( V )
IV. ( V )
V. ( V )
Resposta correta: V, F, V, V, V
aula 5
COMENTÁRIOS – ATIVIDADES
1.
26.
PARA
SALA
Fe(HCO3)2
I. Analisando o ânion bicarbonato, temos:
FG HCO IJ
H K
+1 x −2
−
3
+1+x–6=–1
x=–1+6–1
x = +4
Aplicando no composto
x
FG
H
+1 +4 −2
Fe H C O3
IJ
K
2
x + 2 + 8 – 12 = 0
x = +2
O NOX do
Fe = +2
Fe2O3 . 6H2O
Resposta correta: E
3ª SÉRIE E EXTENSIVO OLÍMPICOS
|
VOLUME 1
|
QUÍMICA 1
5
II. A água é um ligante que está nos espaços vazios do
composto Fe2O3, não participando do cálculo do
NOX:
5.
−2
x
A embalagem adequada impede a oxidação das vitaminas C e D, que em contato com o ar, poderiam ser oxidadas.
Resposta correta: B
Logo: Fe2 O3
2x – 6 = 0
6.
x = +3
Atenção: A água faz apenas o papel de hidratação
no composto.
Como o nitrogênio e o enxofre são elementos com uma
eletronegatividade considerável, o ferro doa (“perde”)
elétrons para esses metais, gerando o estresse oxidativo.
Resposta correta: D
III. Outra forma prática:
7.
Fe(HCO3)2
O coeficiente corresponde ao NOX do metal +2.
Resposta correta: D
2.
Analisando a situação em termos de reatividade, podemos observar:
I. qP + pQq+ → Não ocorre.
Logo: pQq+ é menos oxidante do que qP. Qq+ < P
II. rP + pRr+ → Não ocorre.
Logo: pRr+ é menos oxidante que rP.
III. rS + sRr+ → sR + rSs+ (ocorre reação)
Logo: sRr+ é mais oxidante que S.
IV. sQ + qSs+ → qS + sQq+
Ss+ é mais oxidante que Q.
I. (F) Após o “H” os metais são mais nobres (menos
reativos). Logo, possui uma menor tendência à
oxidação.
II. (V)
III. (F) O zinco é mais nobre (menos reativo) que o cálcio.
IV. (V)
V. (F) O níquel é menos reativo (mais nobre) que o alumínio, logo ele seria reduzido.
Resposta correta: B
Rr+ < P
Rr+ > S
S>Q
Logo, temos ordem crescente de poder oxidante.
Qq+ < Ss+ < Rr+ < Pp+
Resposta correta: E
Redução
+5
3.
+2
Ag. oxidante
−1
−
−
+
−
Au( s) + NO3(
aq) + 4H(aq) + 4CA(aq) → AuCA4 + 2H2O( A ) + NO(g)
0
Oxidação
+3
Ag. redutor
x
1−
AuCA4 −1
x–4 =–1
x = +3
Resposta correta: A
Redução
(ag. oxidante)
4.
Recipiente 1:
Cu2+(aq) + Pb(s)
→
Pb2+ + Cu0
Oxidação
(ag. redutor)
Oxidação
(ag. redutor)
Recipiente 2:
Cu2+(aq) + Zn(s)
→
Zn2+(aq) + Cu0
Redução
(ag. oxidante)
O cobre é reduzido pelo zinco metálico.
Resposta correta: A
6
-291208
Rev.: Jéssica
3ª SÉRIE E EXTENSIVO OLÍMPICOS
|
VOLUME 1
|
QUÍMICA 1