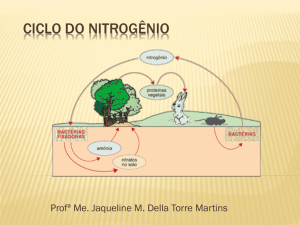
CICLO DO NITROGÊNIO
N
Felipe Ibañez de Santi Ferrara – Instituto de Ciências Biomédicas II,
Universidade de São Paulo.
A Importância do nitrogênio
Transformação de Compostos Nitrogenados
Ciclo do Nitrogênio
A Importância do nitrogênio
O nitrogênio é um elemento químico encontrado na tabela periódica com
massa atômica 14. Esse elemento é parte essencial de alguns compostos
estruturais dos seres vivos como aminoácidos e ácidos nucléicos, que são os
mais abundantes compostos nitrogenados. Porém grande parte de outros
compostos biológicos importantes contém algum átomo de nitrogênio. Como
exemplo podemos citar fitormônios, poliaminas, vitaminas, etc... Calcula-se que
as plantas e animais do planeta, juntos, contêm aproximadamente um trilhão e
quinhentos bilhões de toneladas de N.
Transformações
As transformações que o nitrogênio sofre em seu ciclo alteram o conteúdo
energético das moléculas. Esse aspecto é importante pois as moléculas
nitrogenadas podem fornecer energia para alguns seres vivos.
Assim podemos resumir os estados em que podem ser encontradas as
moléculas nitrogenadas em NOX , N2, NHX e Moléculas orgânicas.
Ciclo do Nitrogênio
Todos os compostos possuem um conteúdo energético. No caso dos
compostos nitrogenados, as moléculas com maior quantidade de átomos de
hidrogênio têm mais energia e as moléculas com mais átomos de oxigênio, menos
energia.
Essa energia é chamada de valência. Assim, a valência do nitrogênio
pode variar de +5 (NO3) até -3 (NH4), sendo os valores menores atribuídos
para as moléculas com maior capacidade de doar energia e os maiores para as
moléculas com maior capacidade de receber energia. Abaixo se encontram as
formas que o nitrogênio assume em seu ciclo:
NO3, NO2, NO, N2O, N2, NH3, NH4
O N2, o N2O e o NO, assim que formados voltam à atmosfera na forma
gasosa, enquanto os outros compostos ficam no solo e podem ser aproveitados
pelos organismos.
NH3
NH4
N2
NO2
NO3
Proteínas e
compostos
nitrogenados
O maior reservatório de nitrogênio do planeta é encontrado na forma de
N2 na atmosfera. Entretanto, apesar de estar ao alcance de praticamente todos
os organismos da superfície terrestre essa forma não pode ser utilizada pela
maioria destes organismos. Este gás é praticamente inerte devido à sua tripla
ligação:
N
N
Um pequeno grupo de microrganismos procariotos, que inclui bactérias e
arquéias é capaz de promover a fixação do nitrogênio, ou seja, a transformação
do N2 em NH3 assimilável. Isso se dá através de uma enzima chamada
nitrogenase que catalisa a reação à custa de grandes gastos de energia na forma
de ATP. Estima-se que os microrganismos sejam responsáveis por 200 milhões
de toneladas de nitrogênio fixado anualmente
A fixação de nitrogênio também pode ocorrer por meios abióticos através
descargas elétricas ou queimadas, ou ainda por interferência do homem. O
processo de fixação industrial do nitrogênio e’muito dispendioso e envolve
quantidades elevadas de combustíveis fósseis, para produzir um ambiente de
alta temperatura e pressão. Os produtos desse processo, (amônia e nitrato) são
utilizados como fertilizante na agricultura. Essa atividade gera 60 milhões de
toneladas de nitrogênio fixado por ano.
O destino da Amônia (NH3), é a incorporação. Esse composto quando
obtido no interior da célula é utilizado na formação de aminoácidos para a
formação de proteínas, ácidos nucléicos (DNA e RNA) e outros compostos
nitrogenados.
A amonificação, também chamada de mineralização, é o processo que
retorna o nitrogênio incorporado para a forma de amônia. Os organismos
liberam o nitrogênio de dentro de suas células na forma de amônia, um produto
comum de decomposição.
Alguns microrganismos possuem deaminases, que são enzimas que
removem os grupos amina de compostos orgânicos formando amônia.
A assimilação do nitrogênio acontece através da enzima nitrato redutase
assimilatória presente em microrganismos e plantas. Essa enzima transforma o
nitrato(NO3-) em NH3 que pode ser incorporado. Os animais não possuem essa
enzima, sendo assim incapazes de utilizar o nitrato como fonte de nitrogênio.
A nitrificação é outro dos processos envolvidos no ciclo do nitrogênio
realizado exclusivamente por microrganismos. Isso ocorre porque esses
microrganismos chamados de nitrificantes, além de utilizarem o NH3 como
fonte de nitrogênio para incorporação, podem usar as diferentes formas do
nitrogênio como fonte de energia. O resultado da nitrificação é a liberação de
um outro composto nitrogenado ao meio ambiente. Entretanto o composto
liberado terá sempre menos energia que o composto inicial seguindo a ordem:
NHX > NO2 > NO3
Barbosa, H. R. & Torres, B. B. 2000. Microbiologia Básica. Ed.
Atheneu, 196p.
Perry, J. J. & Staley, J. T. 1997. Microbiology: Dynamics and
Diversity. Saunders College Publishing, 911p.
Postgate, J. 1998. Nitrogen Fixation. 3rd Ed. Press Sindicate of
the University of Cambrige
A desnitrificação é uma reação que ocorre de maneira inversa a
nitrificação tendo como resultado um composto com conteúdo energético maior
que o inicial. Essa reação também é feita apenas por microrganismos,
denominados denitrificantes, que utilizam o NO3 da mesma forma que os
animais utilizam O2 na respiração. O resultado da utilização dessa substância
normalmente é a formação de NO2, N2O, NO ou N2 causando a perda do
nitrogênio fixado presente no solo para a atmosfera.